江苏省泰州市2020-2021年高二下学期4月期中考试模拟训练化学试题四 Word版含答案
文档属性
| 名称 | 江苏省泰州市2020-2021年高二下学期4月期中考试模拟训练化学试题四 Word版含答案 |  | |
| 格式 | docx | ||
| 文件大小 | 670.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-18 11:40:12 | ||
图片预览




文档简介
江苏省泰州市2020~2021年高二下学期期中考试模拟训四
一、单选题
1.按1:4比例在试管中收集甲烷和氯气的混合气体,用橡皮塞塞紧,光照一段时间后,倒扣于水中,拔开试管塞,在实验的过程中不可能观察到的现象是( )
A.试管中气体黄绿色变浅 B.试管中出现大量的白烟
C.试管壁上有油状液滴出现 D.试管内液面上升
2.设NA为阿伏加德罗常数的数值。下列说法正确的是
A.标准状况下,11.2LH2O中含有的氧原子数为0.5NA
B.14g由CO和N2组成的混合气体中含有的分子总数为0.5NA
C.1L0.5mol·L-1醋酸溶液中含有的氢离子数目为0.5NA
D.H2O2分解制取O2的反应中,每生成0.125molO2,转移的电子数为0.5NA
3.下列应用与反应原理设计不一致的是( )
A.热的纯碱溶液清洗油污:COfalse+H2Ofalse HCOfalse+OH-
B.明矾净水:Al3++3H2OfalseAl(OH)3+3H+
C.用TiCl4制备TiO2:TiCl4+(x+2)H2O(过量) falseTiO2?xH2O↓+4HCl
D.配制氯化亚锡溶液时加入氢氧化钠:SnCl2+H2OfalseSn(OH)Cl+HCl
4.下列物质各3g,在氧气中完全燃烧,于150℃时将产物通过足量的Na2O2固体后,固体增重大于3g的是( )
A.HCOOH B.CH3COOH C.C2H5OH D.C6H12O8
5.苯丙炔酸()广泛用于医药、香料等化工产品中。下列关于苯丙炔酸的说法正确的是
A.分子式为C9H7O2
B.与丙炔酸(CH≡C—COOH)互为同系物
C.是的单体
D.1 mol苯丙炔酸最多可与4mol氢气发生反应
6.下列说法正确的是(????)
A.相对分子质量相同而结构不同的物质是同分异构体
B.?的核磁共振氢谱中有6种峰
C.有机物中碳、氢原子个数比为1:4,则该有机物为false
D.具有相同官能团的物质是同一类有机物
7.关于炔烃的描述中正确的是( )
A.分子组成符合CnH2n-2通式的链烃一定是炔烃
B.炔烃既易发生加成反应,又易发生取代反应
C.炔烃既能使溴水退色,也能使酸性高锰酸钾溶液退色
D.炔烃分子里所有的碳原子都在同一条直线上
8.聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图所示:
(图中虚线表示氢键)
下列说法不正确的是
A.聚维酮的单体是
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质
D.聚维酮的单体能使酸性KMnO4溶液褪色
9.下列有关“实验操作”、“现象”及“实验结论”都正确的是
选项
实验操作
现象
实验结论
A
将湿润的有色布条放入充满氯气的集气瓶中
布条褪色
氯气具有漂白性
B
在 CO 还原 Fe3O4 得到的黑色固体中加入盐酸,固体溶解,再加入 KSCN 溶液
溶液不显血红色
黑色固体一定是 Fe
C
向 BaCl2 溶液中通入适量 CO2
产生白色沉淀
白色沉淀为 BaCO3
D
向包有 Na2O2粉末的脱脂棉中滴几滴水
脱脂棉剧烈燃烧
Na2O2 与水反应放热
A.A B.B C.C D.D
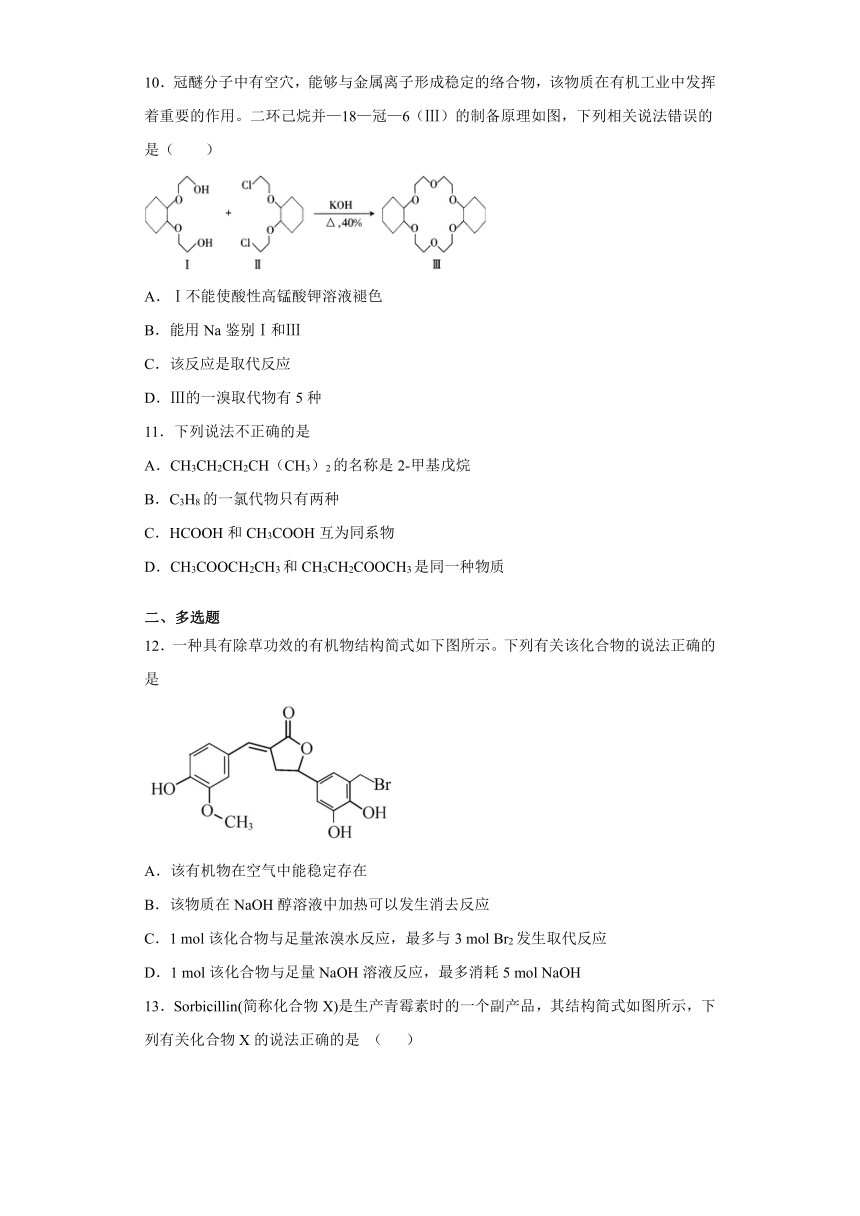
10.冠醚分子中有空穴,能够与金属离子形成稳定的络合物,该物质在有机工业中发挥着重要的作用。二环己烷并—18—冠—6(Ⅲ)的制备原理如图,下列相关说法错误的是( )
A.Ⅰ不能使酸性高锰酸钾溶液褪色
B.能用Na鉴别Ⅰ和Ⅲ
C.该反应是取代反应
D.Ⅲ的一溴取代物有5种
11.下列说法不正确的是
A.CH3CH2CH2CH(CH3)2的名称是2-甲基戊烷
B.C3H8的一氯代物只有两种
C.HCOOH和CH3COOH互为同系物
D.CH3COOCH2CH3和CH3CH2COOCH3是同一种物质
二、多选题
12.一种具有除草功效的有机物结构简式如下图所示。下列有关该化合物的说法正确的是
A.该有机物在空气中能稳定存在
B.该物质在NaOH醇溶液中加热可以发生消去反应
C.1 mol该化合物与足量浓溴水反应,最多与3 mol Br2发生取代反应
D.1 mol该化合物与足量NaOH溶液反应,最多消耗5 mol NaOH
13.Sorbicillin(简称化合物X)是生产青霉素时的一个副产品,其结构简式如图所示,下列有关化合物X的说法正确的是 ( )
A.分子中所有碳原子可能处于同一平面
B.1 mol化合物X可以与2molNa2CO3反应
C.1 mol化合物X可以与浓溴水发生取代反应,消耗3 mol Br2
D.化合物X与H2完全加成,每个产物分子中含有4个手性碳原子
三、实验题
14.乙酰水杨酸(阿司匹林)是目前常用药物之一。实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:
水杨酸
醋酸酐
乙酰水杨酸
熔点/℃
157~159
-72~-74
135~138
相对密度/(g·cm﹣3)
1.44
1.10
1.35
相对分子质量
138
102
180
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴加0.5 mL浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作。
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤。
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
④固体经纯化得白色的乙酰水杨酸晶体5.4 g。
回答下列问题:
(1)该合成反应中应采用_______加热。(填标号)
A.热水浴 B.酒精灯 C.煤气灯 D.电炉
(2)下列玻璃仪器中,①中需使用的有_______(填标号),不需使用的_______(填名称)。
(3)①中需使用冷水,目的是_______。
(4)②中饱和碳酸氢钠的作用是_______,以便过滤除去难溶杂质。
(5)④采用的纯化方法为_______。
四、原理综合题
15.克矽平是一种治疗矽肺病的药物,其合成路线如图(反应均在一定条件下进行):
(1)化合物Ⅰ的某些性质类似苯。例如,化合物Ⅰ可以在一定条件下与氢气发生反应生成,该反应类型为__________,反应化学方程式为__________。
(2)已知化合物Ⅰ生成化合物Ⅱ是原子利用率100%的反应,则所需另一种反应物的分子式__________。
(3)下列关于化合物Ⅱ和化合物Ⅲ的化学性质,说法正确的是(填字母)__________。
A.化合物Ⅱ可以与CH3COOH发生酯化反应
B.化合物Ⅲ不可以与金属钠生成氢气
C.化合物Ⅲ可以使溴的四氯化碳溶液褪色
D.化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
(4)下列化合物中,能发生类似于“Ⅲ→Ⅳ”反应的是(填字母)__________。
A.乙烷 B.乙烯 C.乙醇 D.苯
16.沙丁胺醇()是一种新型药物,常用于缓解哮喘等肺部疾病,其一种合成路线如下。
(1)沙丁胺醇的分子式为_____________,C中官能团的名称为_____________。
(2)①的反应类型为____________,⑥的反应类型为____________。
(3)B的结构简式为_____________。
(4)A在酸性条件下发生缩聚反应的化学方程式为__________________________。
(5)符合下列条件的B的同分异构体有________种(不考虑立体异构),其中任意一种的结构简式为_____________。
a.苯环上有两个取代基; b.能与NaHC03反应生成CO2。
(6)写出以苯酚、甲醛和乙酸酐()为原料制备高分子的合成路线:____________________________________________________(无机试剂任选)
五、有机推断题
17.已知:下列反应是有机合成的重要成环反应。
化合物A可由化合物C合成,其流程为:
(1)A+B→W的反应类型是______________,物质H的名称是_________________。
(2)由C得到D需要经过两步反应,其反应过程中需要的试剂依次是___________。
(3)写出D→E的化学方程式______________________________________________。
(4)物质X是G的同分异构体,请写出符合下列条件的X的结构简式________________。(任写一种)
①苯环上有三个取代基 ②1 mol X与足量银氨溶液反应能生成4 molAg
18.(1)烷烃分子可看成由—CH3、—CH2—、和等结合而成的。试写出同时满足下列条件的烷烃的结构简式:_______,此烷烃可由烯烃加成得到,则该烯烃可能有_____种。
① 分子中同时存在上述 4 种基团;
② 分子中所含碳原子数最少;
③ 该烷烃的一氯代物同分异构体的数目最少。
(2)已知:烯烃通过臭氧氧化并经锌和水处理得到醛或酮,例如:
false(R1、R2、R3 表示烃基)
现有 1 mol 某烃 A 通过臭氧氧化并经锌和水处理后只得到和各 1 mol。
则可推出:A 分子中有 _________个双键,A 的分子式是 ________。
(3)有机物 A 是未成熟葡萄中含有的一种物质,由C、H、O 三种元素组成,A 在气态时的密度是相同条件下氢气密度的 38 倍。在一定条件下A 既可以与乙醇反应生成酯又可以与乙酸反应生成酯。已知 0.1mol A 完全燃烧时生成 0.2mol CO2 和 0.2mol H2O;1mol A 可与2mol Na 或 1mol NaOH 反应。试写出A与浓硫酸共热生成六元环状酯化合物的反应方程式:_______。
19.丁苯酞(J)作为药物被广泛使用在临床,主要应用于缺血性疾病,合成J的一种路线如图所示:
已知:①;
②J是一种酯,分子中除苯环外还含有一个五元环。
请回答下列问题:
(1)化合物B中最多有_______个原子共平面;
(2)已知化合物C可发生银镜反应,请写出C的结构简式_______;
(3)E的核磁共振氢谱只有一组,则D的结构简式为_______,由D→E的反应类型为_______;
(4)请写出H→J反应的化学方程式:_______;
(5)同时满足下列条件的G的同分异构体有_______种。
①能与FeCl3溶液发生显色反应
②核磁共振氢谱有四组峰,且峰面积之比为6∶6∶2∶1
(6)根据题给信息,以乙醛和苯为原料经过三步合成某化工原料,请写出合成路线_______(其他无机试剂任选)。
参考答案
1.B
【解析】甲烷和氯气发生取代反应,生成CH3Cl、CH2Cl2、CHCl3、CCl4和HCl,CH3Cl是气体,CH2Cl2、CHCl3、CCl4是不溶于水的液体,HCl极易溶于水,因此观察到黄绿色变浅,试管壁上有油状液体产生,液面上升,故选项B正确。
2.B
【解析】
A、标准状况下,H2O不是气体,选项A错误;B、CO和N2的分子量都为28,所以混合气体的平均分子量为28,n总=false=false=0.5 mol,N=n NA=0.5NA,选项B正确;C、醋酸是弱酸,不完全电离,1L0.5mol·L-1醋酸溶液中含有的氢离子数目小于0.5NA,选项C错误;D、分解H2O2制O2,2H2O2=2H2O+O2↑,过氧化氢分解氧元素化合价从-1价变化为-2价和0价,每生成0.125mol O2转移0.25NA个电子,选项D错误。答案选B。
3.D
【详解】
A. 热的纯碱溶液存在水解平衡:COfalse+H2Ofalse HCOfalse+OH-,水解过程是吸热的过程,升高温度,可以促进盐的水解,所以热的纯碱溶液清洗油污,属于盐的水解原理的应用,故A不符合;
B. 铝离子水解生成氢氧化铝胶体:Al3++3H2OfalseAl(OH)3+3H+,氢氧化铝胶体能吸附水中悬物并使之沉降,故明矾净水属于盐的水解原理的应用,故B不符合;
C. TiCl4水解可以得到TiO2?xH2O,加热失去结晶水即可得到二氧化钛,故用TiCl4制备TiO2:TiCl4+(x+2)H2O(过量) falseTiO2?xH2O↓+4HCl,属于盐的水解原理的应用,故C不符合;
D. SnCl2溶液水解反应为:SnCl2+H2OfalseSn(OH)Cl+HCl,故溶液呈酸性,可以加盐酸来抑制其水解,配制氯化亚锡溶液时加入氢氧化钠会促使平衡正向移动,不能制得氯化亚锡溶液,不属于盐的水解原理的应用,故D符合;
答案选D。
4.C
【分析】
ag有机物能改写成(CO)m(H2)n的有机物在氧气中充分燃烧,生成的产物通入足量过氧化钠中,增加的质量就为ag。过氧化钠会吸收CO2中CO,吸收水中的H2。
【详解】
A选项,HCOOH能改写成(CO)(H2)n,增加的质量等于3g,故A不符合题意;
B选项,CH3COOH能改写成(CO)2(H2)2,增加的质量等于3g,故B不符合题意;
C选项,C2H5OH能改写成(CO)(H2)3C,C燃烧变为CO2,过氧化钠会吸收CO2中CO,因此增加的质量大于3g,故C符合题意;
D选项,C6H12O8能改写成(CO)6(H2)6O2,O2不会被过氧化钠吸收,因此增加的质量等于3g,故D不符合题意。
综上所述,答案为C。
5.C
【分析】
有机物含有碳碳三键,可发生加成、加聚和氧化反应,含有羧基,具有酸性,可发生中和、酯化等反应,以此解答该题。
【详解】
A.由结构简式可知分子式为C9H6O2,故A错误;
B.含有苯环,与CH≡C?COOH结构不同,不是同系物,故B错误;
C.可发生加聚反应生成,为的单体,故C正确;
D.能与氢气反应的为苯环和碳碳三键,则1?mol苯丙炔酸最多可与5mol氢气发生反应,故D错误;
答案选C。
【点睛】
同系物的判断需要注意三点:一是看结构是否相似,结构不同不是同系物;二是看类别是否相同,有机物类别不同不是同系物;三是看组成,是否相差一个或多个“CH2”原子团,不符合该原子团结构的不是同系物。
6.B
【详解】
A.相对分子质量相同而结构不同的物质,可能组成不同,如硫酸与磷酸,不互为同分异构体,故A错误;
B.中环上含4种H,侧链含2种H,则核磁共振氢谱中有6种峰,故B正确;
C.有机物中碳、氢原子个数比为1:4,还可能含O元素,则有机物可能为false(甲醇),故C错误;
D.具有相同官能团的物质,如苯酚、苯甲醇,均含false,为不同类有机物,故D错误;
答案选B。
【点睛】
本题考查有机物的结构与性质,把握官能团与性质、有机物类别、结构对称性为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的易错点。
7.C
【解析】A、分子组成符合CnH2n-2的链烃,可能含有2个C=C双键,为二烯烃,或1个C≡C三键,为炔烃,故A错误;B、炔烃易发生加成反应难发生取代反应,故B错误;C、炔烃既能使溴水褪色,也可以使高锰酸钾酸性溶液褪色,故C正确;D、多碳原子的炔烃中碳原子不一定在一条直线上,如1-丁炔中的4个碳原子不在同一直线上,故D错误。故选C。
8.B
【详解】
A.由聚维酮碘的分子结构知,聚维酮由加聚反应制得,其单体为,故A正确;
B.由聚维酮碘的分子结构知,聚维酮分子中左侧链节由2个单体构成,因此,聚维酮分子由2m+n个单体聚合而成,故B项错误;
C.由题干信息“聚维酮碘的水溶液”知,聚维酮碘能溶于水,故C项正确;
D.由聚维酮碘的分子结构知,聚维酮由加聚反应制得,其单体为,该单体分子中含有碳碳双键,能使酸性KMnO4溶液褪色,故D项正确;故答案:B。
9.D
【详解】
A.氯气本身不具有漂白性,布条褪色是因为氯气和水反应生成了具有漂白性的次氯酸,A项错误;
B.得到的黑色固体可能为Fe3O4和Fe的混合物,加入盐酸,固体溶解中生成铁离子,铁离子具有强氧化性,会与Fe反应,加入 KSCN 溶液,溶液不显血红色,不能说明黑色固体一定是 Fe,B项错误;
C.碳酸的酸性弱于盐酸,所以二氧化碳和氯化钡溶液不反应,C项错误;
D.向包有Na2O2粉末的脱脂棉滴几滴水,脱脂棉剧烈燃烧,说明该反应放出热量使温度达到脱脂棉的着火点,剧烈燃烧说明氧气浓度较大,该反应产生氧气,D项正确;
答案选D。
10.A
【详解】
A.Ⅰ含有羟基,且与羟基相连的碳原子上有氢原子,可被酸性高锰酸钾氧化,高锰酸钾溶液褪色,故A错误;
B.Ⅰ含有羟基,可与钠反应生成氢气,而Ⅲ与钠不反应,可鉴别,故B正确;
C.反应中-OH中的H被替代,为取代反应,故C正确;
D.Ⅲ结构对称,含有如图所示5种H,则一氯代物有5种,故D正确;
故选:A。
11.D
【详解】
A.根据烷烃命名原则,CH3CH2CH2CH(CH3)2的名称是2-甲基戊烷,故A正确;
B.因为C3H8是丙烷有2种不同类型的H原子,所以一氯代物有2种,故B正确;
C.结构相似、在分子组成上相差一个或若干个-CH2原子团的有机物间互称同系物,甲酸(HCOOH)和乙酸(CH3COOH)的官能团的个数、种类都相同,相差一个-CH2原子团,故两者是同系物,故C正确;
D.CH3COOCH2CH3和CH3CH2COOCH3为分子式相同,结构不同的同分异构体,不是同一种物质,故D错误;
故答案:D。
【点睛】
根据烷烃命名原则:①长-----选最长碳链为主链;②多-----遇等长碳链时,支链最多为主链;③近-----离支链最近一端编号;④小-----支链编号之和最小。
12.CD
【分析】
由图可知该有机物含有的官能团为碳碳双键、醚键、酚羟基、溴原子和酯基,有机物表现酚、烯烃、卤代烃及酯的性质。
【详解】
A.该有机物中含有酚羟基,该有机物露置在在空气中酚羟基易被氧化,故A错误;
B.该物质含有溴原子,但溴原子所连碳的邻位碳上没有H原子,不能发生消去反应,故B错误;
C.酚-OH的邻对位与溴水发生取代,碳碳双键与溴水发生加成反应,则1 mol该化合物与足量浓溴水反应,最多消耗4 mol Br2,其中取代反应消耗3mol,加成反应消耗1mol,故C正确;
D.酚羟基、溴原子、酯基均与NaOH溶液反应,1 mol该化合物与足量NaOH溶液反应,最多消耗5 mol NaOH,故D正确;
故选:CD。
13.AB
【解析】
A.分子中存在的苯环、羰基及碳碳双键均为平面结构,则所有碳原子可能处于同一平面,故A正确;B.酚羧基能与Na2CO3反应生成NaHCO3,且分子中有2个酚羟基,则1mol化合物X可以与2 molNa2CO3反应,故B正确;C.1mol化合物X最多可以3molBr2反应,其中2mol是加成,1mol发生取代,故C错误;D.化合物X中苯环、碳碳双键及羰基均能与H2完全加成反应,每个产物分子中含有3个手性碳原子,故D错误;答案为AB。
14.A BD 分液漏斗、容量瓶 充分析出乙酰水杨酸固体(结晶) 生成可溶的乙酰水杨酸钠 重结晶
【详解】
(1)因为反应温度在70℃,低于水的沸点,且需维温度不变,故采用热水浴的方法加热,故答案为:A。
(2)操作①需将反应物倒入冷水,需要用烧杯量取和存放冷水,过滤的操作中还需要漏斗,分液漏斗主要用于分离互不相容的液体混合物,容量瓶用于配制一定浓度的溶液,这两个仪器用不到,故答案为B、D;分液漏斗、容量瓶。
(3)反应时温度较高,加入冷水可以降低反应后的混合物的温度,使其冷却结晶,即析出固体得到乙酰水杨酸产物,故答案为:充分析出乙酰水杨酸固体(结晶)。
(4)乙酰水杨酸难溶于水,为了除去其中的杂质,加入饱和碳酸氢钠可以与乙酰水杨酸反应,生成可以溶于水的乙酰水杨酸钠,除去粗产品表面附着的有机物,达到再次洗涤的目的,故答案为:生成可溶的乙酰水杨酸钠。
(5)每次结晶过程中会有少量杂质一起析出,可以通过多次结晶的方法进行纯化,也就是重结晶,故答案为:重结晶。
15.加成反应 +3H2false CH2O A、B、C B
【详解】
(1)化合物I的结构简式为,由某些性质类似苯可知, 在一定条件下与氢气发生反应生成,反应的化学方程式为+3H2
false,故答案为:加成反应;+3H2false;
(2)由化合物Ⅰ生成化合物Ⅱ是原子利用率100%的反应可知,与甲醛发生加成反应生成,甲醛的分子式为CH2O,故答案为:CH2O;
(3)A.因化合物Ⅱ分子中含有羟基,在浓硫酸作用下,可以和CH3COOH共热发生酯化反应,故正确;
B.化合物Ⅲ不含羟基、羧基等,不可以与金属钠生成氢气,故正确;
C.化合物Ⅲ的分子中含有碳碳双键,能与溴的四氯化碳溶液发生加成反应,使溴的四氯化碳溶液褪色,故正确;
D.化合物Ⅲ的分子中含有碳碳双键,能与酸性高锰酸钾溶液发生氧化反应,使酸性高锰酸钾溶液褪色,故错误;
ABC正确,故答案为:A、B、C;
(4)化合物Ⅲ含有碳碳双键,一定条件下,能发生加聚反应反应生成化合物Ⅳ,乙烯含有碳碳双键,与化合物Ⅲ性质相似,也能发生加聚反应生成聚乙烯,B正确,故答案为:B。
16.C13H21NO3 酯基、羰基(或酮基) 加成反应 取代反应 18种 、、、、、,再分别有邻位和间位,任写一种即可
【详解】
①与甲醛加成生成A、,②A中醇中羟基与HCl发生取代反应生成B、,③B与乙酸钠发生取代反应生成,④再发生取代反应生成C、,⑤C与溴发生取代反应生成、⑥发生取代反应生成D、 。
(1)沙丁胺醇的分子式为C13H21NO3 ,C中官能团的名称为酯基、羰基(或酮基)。(2)①的反应类型为加成反应,⑥的反应类型为取代反应。(3)B的结构简式为。(4)A在酸性条件下发生缩聚反应的化学方程式为。(5)符合下列条件的B的同分异构体有18种 种(不考虑立体异构),其中任意一种的结构简式为 、、、、、,再分别有邻位和间位,任写一种即可。(6)写出以苯酚、甲醛和乙酸酐()为原料制备高分子的合成路线:
17.(1)加成反应 甲醇
(2)溴水(氯气)、氢氧化钠水溶液
(3)
(4)(合理即给分)
【解析】
试题分析:(1)B与A发生1,4加成成环,从组成分析得出G经过与甲醇酯化可以得到A;(2)C到D由碳碳双键衍变为两个羟基,故先加成溴单质再水解可得,反应条件为溴水、氢氧化钠水溶液;(3)D经过催化氧化,羟基转化为醛基,
(4)由②知物质X含有2个醛基,故其共有2个醛基和1个甲基,有不同的位置变化。如等。
考点:考查有机物的相互转化的关系,涉及反应类型、方程式的书写、同分异构体等有关问题。
18. 2 2 C8H12 2HO-CH2-COOH+2H2O
【分析】
(1)如果某烷烃分子中同时存在这4种基团,最少-CH2-、和各含有一个,剩下的为甲基,根据烷烃通式确定碳原子个数并确定结构简式,然后根据氢原子种类等于一氯代物同分异构体的数目分析解答;
(2)分子中碳碳双键氧化生成羰基,每个碳碳双键生成2个羰基;碳碳双键断裂形成C=O双键,产物中碳原子、氢原子总数与原烯烃中相等;结合产物的结构和数目分析判断;
(3)A由C、H、O三种元素组成,A在气态时的密度是相同条件下氢气密度的38倍,则A的相对分子质量为76,在一定条件下A既可以与乙醇反应生成酯又可以与乙酸反应生成酯,说明A中含有羧基和羟基,在根据0.1mol A完全燃烧时生成0.2mol CO2和0.2mol H2O确定分子中C、H的个数,结合相对分子质量计算O的个数,结合分子式写出结构简式,然后写出在浓硫酸作用下,两分子A相互反应生成六元环状物质的化学方程式。
【详解】
(1)如果某烷烃分子中同时存在—CH3、—CH2—、和4种基团,则最少含有-CH2-、和各一个,剩下的为甲基,设甲基的个数是x,由烷烃的通式知2(x+3)+2=2+1+3x,解得:x=5,所以最少应含有的碳原子数是8,该烷烃的结构简式有3种,分别为:、、,其一氯代物的种类分别为:5种、5种、4种,所以一氯代物同分异构体的数目最少的烷烃的结构简式:,此烷烃可由烯烃加成得到,则该烯烃中碳碳双键可能的位置有2种(),故答案为:;2;
(2)分子中碳碳双键氧化生成羰基,每个碳碳双键生成2个羰基;碳碳双键断裂形成C=O双键,产物中碳原子、氢原子总数与原烯烃相等,由产物和的结构可知,A分子中碳原子数目为8,分子中含有2个碳碳双键,由于2种产物各1mol,因此分子中还存在1个环,不饱和度为3,故A的分子式为C8H12,故答案为:2;C8H12;
(3)A由C、H、O三种元素组成,A在气态时的密度是相同条件下氢气密度的38倍,则A的相对分子质量为76,在一定条件下A既可以与乙醇反应生成酯又可以与乙酸反应生成酯,说明A中含有羧基和羟基,已知0.1mol A完全燃烧时生成0.2mol CO2和0.2mol H2O,则分子中N(C)=false=2,N(H)=false=4,所以N(O)=false=3,所以A的分子式为:C2H4O3;A中含有羧基和羟基,则A的结构简式为HO-CH2-COOH,因此A在浓硫酸作用下,两分子A相互反应生成六元环状酯的化学方程式为2HO-CH2-COOH+2H2O,故答案为:2HO-CH2-COOH+2H2O。
【点睛】
本题的易错点和难点为(2),要注意确定分子结构中存在一个环。
19.13 加成反应 false+H2O 3 falsefalsefalse
【分析】
根据G的结构逆推可知甲苯与Br2在Fe作催化剂条件下发生苯环上甲基邻位C原子上的取代反应产生B,B为,B与H2在MnO2及加热条件下反应产生C,化合物C可发生银镜反应,则C为;D分子式是C4H8,D与HBr反应产生E,E的核磁共振氢谱只有一组峰,说明D是烯烃,与HBr发生加成反应,可知D结构简式是,E是;E与Mg,乙醚反应产生F,F为,C与F反应产生G,G与Mg、乙醚、CO2作用下反应产生H,J是一种酯,分子中除苯环外还含有一个五元环,H在一定条件下发生反应产生J,J为,据此分析解答。
【详解】
(1)化合物B为,苯环是平面结构,甲基是四面体结构,甲基中最大有1个氢原子在苯环所处平面内,因此B中最多有13个原子共平面,故答案为:13;
(2)根据上述分析,C的结构简式为,故答案为:;
(3)E核磁共振氢谱只有一组峰,说明分子中只有1种H原子,则D结构简式是,E是,D与HBr发生加成反应产生E,故答案为:;加成反应;
(4) J是一种酯,分子中除苯环外还含有一个五元环,H()在一定条件下发生反应产生J,J为,反应的化学方程式为false+H2O, 故答案为:false+H2O;
(5)G的结构简式是,其分子式是C11H15OBr,G的同分异构体符合条件:①能与FeCl3溶液发生显色反应,说明分子中含有酚羟基,②核磁共振氢谱有四组峰,且峰面积之比为6∶6∶2∶1,说明物质分子中含有四种H原子,这四种H原子的个数比为6∶6∶2∶1,符合条件的有、、,共3种,故答案为:3;
(6)与Br2在Fe作催化剂条件下发生取代反应产生,与Mg、乙醚发生反应产生,与CH3CHO在水溶液中发生反应产生,故乙醛和苯为原料经过三步合成的流程图为:falsefalsefalse,故答案为:falsefalsefalse。
一、单选题
1.按1:4比例在试管中收集甲烷和氯气的混合气体,用橡皮塞塞紧,光照一段时间后,倒扣于水中,拔开试管塞,在实验的过程中不可能观察到的现象是( )
A.试管中气体黄绿色变浅 B.试管中出现大量的白烟
C.试管壁上有油状液滴出现 D.试管内液面上升
2.设NA为阿伏加德罗常数的数值。下列说法正确的是
A.标准状况下,11.2LH2O中含有的氧原子数为0.5NA
B.14g由CO和N2组成的混合气体中含有的分子总数为0.5NA
C.1L0.5mol·L-1醋酸溶液中含有的氢离子数目为0.5NA
D.H2O2分解制取O2的反应中,每生成0.125molO2,转移的电子数为0.5NA
3.下列应用与反应原理设计不一致的是( )
A.热的纯碱溶液清洗油污:COfalse+H2Ofalse HCOfalse+OH-
B.明矾净水:Al3++3H2OfalseAl(OH)3+3H+
C.用TiCl4制备TiO2:TiCl4+(x+2)H2O(过量) falseTiO2?xH2O↓+4HCl
D.配制氯化亚锡溶液时加入氢氧化钠:SnCl2+H2OfalseSn(OH)Cl+HCl
4.下列物质各3g,在氧气中完全燃烧,于150℃时将产物通过足量的Na2O2固体后,固体增重大于3g的是( )
A.HCOOH B.CH3COOH C.C2H5OH D.C6H12O8
5.苯丙炔酸()广泛用于医药、香料等化工产品中。下列关于苯丙炔酸的说法正确的是
A.分子式为C9H7O2
B.与丙炔酸(CH≡C—COOH)互为同系物
C.是的单体
D.1 mol苯丙炔酸最多可与4mol氢气发生反应
6.下列说法正确的是(????)
A.相对分子质量相同而结构不同的物质是同分异构体
B.?的核磁共振氢谱中有6种峰
C.有机物中碳、氢原子个数比为1:4,则该有机物为false
D.具有相同官能团的物质是同一类有机物
7.关于炔烃的描述中正确的是( )
A.分子组成符合CnH2n-2通式的链烃一定是炔烃
B.炔烃既易发生加成反应,又易发生取代反应
C.炔烃既能使溴水退色,也能使酸性高锰酸钾溶液退色
D.炔烃分子里所有的碳原子都在同一条直线上
8.聚维酮碘的水溶液是一种常用的碘伏类缓释消毒剂,聚维酮通过氢键与HI3形成聚维酮碘,其结构表示如图所示:
(图中虚线表示氢键)
下列说法不正确的是
A.聚维酮的单体是
B.聚维酮分子由(m+n)个单体聚合而成
C.聚维酮碘是一种水溶性物质
D.聚维酮的单体能使酸性KMnO4溶液褪色
9.下列有关“实验操作”、“现象”及“实验结论”都正确的是
选项
实验操作
现象
实验结论
A
将湿润的有色布条放入充满氯气的集气瓶中
布条褪色
氯气具有漂白性
B
在 CO 还原 Fe3O4 得到的黑色固体中加入盐酸,固体溶解,再加入 KSCN 溶液
溶液不显血红色
黑色固体一定是 Fe
C
向 BaCl2 溶液中通入适量 CO2
产生白色沉淀
白色沉淀为 BaCO3
D
向包有 Na2O2粉末的脱脂棉中滴几滴水
脱脂棉剧烈燃烧
Na2O2 与水反应放热
A.A B.B C.C D.D
10.冠醚分子中有空穴,能够与金属离子形成稳定的络合物,该物质在有机工业中发挥着重要的作用。二环己烷并—18—冠—6(Ⅲ)的制备原理如图,下列相关说法错误的是( )
A.Ⅰ不能使酸性高锰酸钾溶液褪色
B.能用Na鉴别Ⅰ和Ⅲ
C.该反应是取代反应
D.Ⅲ的一溴取代物有5种
11.下列说法不正确的是
A.CH3CH2CH2CH(CH3)2的名称是2-甲基戊烷
B.C3H8的一氯代物只有两种
C.HCOOH和CH3COOH互为同系物
D.CH3COOCH2CH3和CH3CH2COOCH3是同一种物质
二、多选题
12.一种具有除草功效的有机物结构简式如下图所示。下列有关该化合物的说法正确的是
A.该有机物在空气中能稳定存在
B.该物质在NaOH醇溶液中加热可以发生消去反应
C.1 mol该化合物与足量浓溴水反应,最多与3 mol Br2发生取代反应
D.1 mol该化合物与足量NaOH溶液反应,最多消耗5 mol NaOH
13.Sorbicillin(简称化合物X)是生产青霉素时的一个副产品,其结构简式如图所示,下列有关化合物X的说法正确的是 ( )
A.分子中所有碳原子可能处于同一平面
B.1 mol化合物X可以与2molNa2CO3反应
C.1 mol化合物X可以与浓溴水发生取代反应,消耗3 mol Br2
D.化合物X与H2完全加成,每个产物分子中含有4个手性碳原子
三、实验题
14.乙酰水杨酸(阿司匹林)是目前常用药物之一。实验室通过水杨酸进行乙酰化制备阿司匹林的一种方法如下:
水杨酸
醋酸酐
乙酰水杨酸
熔点/℃
157~159
-72~-74
135~138
相对密度/(g·cm﹣3)
1.44
1.10
1.35
相对分子质量
138
102
180
实验过程:在100 mL锥形瓶中加入水杨酸6.9 g及醋酸酐10 mL,充分摇动使固体完全溶解。缓慢滴加0.5 mL浓硫酸后加热,维持瓶内温度在70 ℃左右,充分反应。稍冷后进行如下操作。
①在不断搅拌下将反应后的混合物倒入100 mL冷水中,析出固体,过滤。
②所得结晶粗品加入50 mL饱和碳酸氢钠溶液,溶解、过滤。
③滤液用浓盐酸酸化后冷却、过滤得固体。
④固体经纯化得白色的乙酰水杨酸晶体5.4 g。
回答下列问题:
(1)该合成反应中应采用_______加热。(填标号)
A.热水浴 B.酒精灯 C.煤气灯 D.电炉
(2)下列玻璃仪器中,①中需使用的有_______(填标号),不需使用的_______(填名称)。
(3)①中需使用冷水,目的是_______。
(4)②中饱和碳酸氢钠的作用是_______,以便过滤除去难溶杂质。
(5)④采用的纯化方法为_______。
四、原理综合题
15.克矽平是一种治疗矽肺病的药物,其合成路线如图(反应均在一定条件下进行):
(1)化合物Ⅰ的某些性质类似苯。例如,化合物Ⅰ可以在一定条件下与氢气发生反应生成,该反应类型为__________,反应化学方程式为__________。
(2)已知化合物Ⅰ生成化合物Ⅱ是原子利用率100%的反应,则所需另一种反应物的分子式__________。
(3)下列关于化合物Ⅱ和化合物Ⅲ的化学性质,说法正确的是(填字母)__________。
A.化合物Ⅱ可以与CH3COOH发生酯化反应
B.化合物Ⅲ不可以与金属钠生成氢气
C.化合物Ⅲ可以使溴的四氯化碳溶液褪色
D.化合物Ⅲ不可以使酸性高锰酸钾溶液褪色
(4)下列化合物中,能发生类似于“Ⅲ→Ⅳ”反应的是(填字母)__________。
A.乙烷 B.乙烯 C.乙醇 D.苯
16.沙丁胺醇()是一种新型药物,常用于缓解哮喘等肺部疾病,其一种合成路线如下。
(1)沙丁胺醇的分子式为_____________,C中官能团的名称为_____________。
(2)①的反应类型为____________,⑥的反应类型为____________。
(3)B的结构简式为_____________。
(4)A在酸性条件下发生缩聚反应的化学方程式为__________________________。
(5)符合下列条件的B的同分异构体有________种(不考虑立体异构),其中任意一种的结构简式为_____________。
a.苯环上有两个取代基; b.能与NaHC03反应生成CO2。
(6)写出以苯酚、甲醛和乙酸酐()为原料制备高分子的合成路线:____________________________________________________(无机试剂任选)
五、有机推断题
17.已知:下列反应是有机合成的重要成环反应。
化合物A可由化合物C合成,其流程为:
(1)A+B→W的反应类型是______________,物质H的名称是_________________。
(2)由C得到D需要经过两步反应,其反应过程中需要的试剂依次是___________。
(3)写出D→E的化学方程式______________________________________________。
(4)物质X是G的同分异构体,请写出符合下列条件的X的结构简式________________。(任写一种)
①苯环上有三个取代基 ②1 mol X与足量银氨溶液反应能生成4 molAg
18.(1)烷烃分子可看成由—CH3、—CH2—、和等结合而成的。试写出同时满足下列条件的烷烃的结构简式:_______,此烷烃可由烯烃加成得到,则该烯烃可能有_____种。
① 分子中同时存在上述 4 种基团;
② 分子中所含碳原子数最少;
③ 该烷烃的一氯代物同分异构体的数目最少。
(2)已知:烯烃通过臭氧氧化并经锌和水处理得到醛或酮,例如:
false(R1、R2、R3 表示烃基)
现有 1 mol 某烃 A 通过臭氧氧化并经锌和水处理后只得到和各 1 mol。
则可推出:A 分子中有 _________个双键,A 的分子式是 ________。
(3)有机物 A 是未成熟葡萄中含有的一种物质,由C、H、O 三种元素组成,A 在气态时的密度是相同条件下氢气密度的 38 倍。在一定条件下A 既可以与乙醇反应生成酯又可以与乙酸反应生成酯。已知 0.1mol A 完全燃烧时生成 0.2mol CO2 和 0.2mol H2O;1mol A 可与2mol Na 或 1mol NaOH 反应。试写出A与浓硫酸共热生成六元环状酯化合物的反应方程式:_______。
19.丁苯酞(J)作为药物被广泛使用在临床,主要应用于缺血性疾病,合成J的一种路线如图所示:
已知:①;
②J是一种酯,分子中除苯环外还含有一个五元环。
请回答下列问题:
(1)化合物B中最多有_______个原子共平面;
(2)已知化合物C可发生银镜反应,请写出C的结构简式_______;
(3)E的核磁共振氢谱只有一组,则D的结构简式为_______,由D→E的反应类型为_______;
(4)请写出H→J反应的化学方程式:_______;
(5)同时满足下列条件的G的同分异构体有_______种。
①能与FeCl3溶液发生显色反应
②核磁共振氢谱有四组峰,且峰面积之比为6∶6∶2∶1
(6)根据题给信息,以乙醛和苯为原料经过三步合成某化工原料,请写出合成路线_______(其他无机试剂任选)。
参考答案
1.B
【解析】甲烷和氯气发生取代反应,生成CH3Cl、CH2Cl2、CHCl3、CCl4和HCl,CH3Cl是气体,CH2Cl2、CHCl3、CCl4是不溶于水的液体,HCl极易溶于水,因此观察到黄绿色变浅,试管壁上有油状液体产生,液面上升,故选项B正确。
2.B
【解析】
A、标准状况下,H2O不是气体,选项A错误;B、CO和N2的分子量都为28,所以混合气体的平均分子量为28,n总=false=false=0.5 mol,N=n NA=0.5NA,选项B正确;C、醋酸是弱酸,不完全电离,1L0.5mol·L-1醋酸溶液中含有的氢离子数目小于0.5NA,选项C错误;D、分解H2O2制O2,2H2O2=2H2O+O2↑,过氧化氢分解氧元素化合价从-1价变化为-2价和0价,每生成0.125mol O2转移0.25NA个电子,选项D错误。答案选B。
3.D
【详解】
A. 热的纯碱溶液存在水解平衡:COfalse+H2Ofalse HCOfalse+OH-,水解过程是吸热的过程,升高温度,可以促进盐的水解,所以热的纯碱溶液清洗油污,属于盐的水解原理的应用,故A不符合;
B. 铝离子水解生成氢氧化铝胶体:Al3++3H2OfalseAl(OH)3+3H+,氢氧化铝胶体能吸附水中悬物并使之沉降,故明矾净水属于盐的水解原理的应用,故B不符合;
C. TiCl4水解可以得到TiO2?xH2O,加热失去结晶水即可得到二氧化钛,故用TiCl4制备TiO2:TiCl4+(x+2)H2O(过量) falseTiO2?xH2O↓+4HCl,属于盐的水解原理的应用,故C不符合;
D. SnCl2溶液水解反应为:SnCl2+H2OfalseSn(OH)Cl+HCl,故溶液呈酸性,可以加盐酸来抑制其水解,配制氯化亚锡溶液时加入氢氧化钠会促使平衡正向移动,不能制得氯化亚锡溶液,不属于盐的水解原理的应用,故D符合;
答案选D。
4.C
【分析】
ag有机物能改写成(CO)m(H2)n的有机物在氧气中充分燃烧,生成的产物通入足量过氧化钠中,增加的质量就为ag。过氧化钠会吸收CO2中CO,吸收水中的H2。
【详解】
A选项,HCOOH能改写成(CO)(H2)n,增加的质量等于3g,故A不符合题意;
B选项,CH3COOH能改写成(CO)2(H2)2,增加的质量等于3g,故B不符合题意;
C选项,C2H5OH能改写成(CO)(H2)3C,C燃烧变为CO2,过氧化钠会吸收CO2中CO,因此增加的质量大于3g,故C符合题意;
D选项,C6H12O8能改写成(CO)6(H2)6O2,O2不会被过氧化钠吸收,因此增加的质量等于3g,故D不符合题意。
综上所述,答案为C。
5.C
【分析】
有机物含有碳碳三键,可发生加成、加聚和氧化反应,含有羧基,具有酸性,可发生中和、酯化等反应,以此解答该题。
【详解】
A.由结构简式可知分子式为C9H6O2,故A错误;
B.含有苯环,与CH≡C?COOH结构不同,不是同系物,故B错误;
C.可发生加聚反应生成,为的单体,故C正确;
D.能与氢气反应的为苯环和碳碳三键,则1?mol苯丙炔酸最多可与5mol氢气发生反应,故D错误;
答案选C。
【点睛】
同系物的判断需要注意三点:一是看结构是否相似,结构不同不是同系物;二是看类别是否相同,有机物类别不同不是同系物;三是看组成,是否相差一个或多个“CH2”原子团,不符合该原子团结构的不是同系物。
6.B
【详解】
A.相对分子质量相同而结构不同的物质,可能组成不同,如硫酸与磷酸,不互为同分异构体,故A错误;
B.中环上含4种H,侧链含2种H,则核磁共振氢谱中有6种峰,故B正确;
C.有机物中碳、氢原子个数比为1:4,还可能含O元素,则有机物可能为false(甲醇),故C错误;
D.具有相同官能团的物质,如苯酚、苯甲醇,均含false,为不同类有机物,故D错误;
答案选B。
【点睛】
本题考查有机物的结构与性质,把握官能团与性质、有机物类别、结构对称性为解答的关键,侧重分析与应用能力的考查,注意选项D为解答的易错点。
7.C
【解析】A、分子组成符合CnH2n-2的链烃,可能含有2个C=C双键,为二烯烃,或1个C≡C三键,为炔烃,故A错误;B、炔烃易发生加成反应难发生取代反应,故B错误;C、炔烃既能使溴水褪色,也可以使高锰酸钾酸性溶液褪色,故C正确;D、多碳原子的炔烃中碳原子不一定在一条直线上,如1-丁炔中的4个碳原子不在同一直线上,故D错误。故选C。
8.B
【详解】
A.由聚维酮碘的分子结构知,聚维酮由加聚反应制得,其单体为,故A正确;
B.由聚维酮碘的分子结构知,聚维酮分子中左侧链节由2个单体构成,因此,聚维酮分子由2m+n个单体聚合而成,故B项错误;
C.由题干信息“聚维酮碘的水溶液”知,聚维酮碘能溶于水,故C项正确;
D.由聚维酮碘的分子结构知,聚维酮由加聚反应制得,其单体为,该单体分子中含有碳碳双键,能使酸性KMnO4溶液褪色,故D项正确;故答案:B。
9.D
【详解】
A.氯气本身不具有漂白性,布条褪色是因为氯气和水反应生成了具有漂白性的次氯酸,A项错误;
B.得到的黑色固体可能为Fe3O4和Fe的混合物,加入盐酸,固体溶解中生成铁离子,铁离子具有强氧化性,会与Fe反应,加入 KSCN 溶液,溶液不显血红色,不能说明黑色固体一定是 Fe,B项错误;
C.碳酸的酸性弱于盐酸,所以二氧化碳和氯化钡溶液不反应,C项错误;
D.向包有Na2O2粉末的脱脂棉滴几滴水,脱脂棉剧烈燃烧,说明该反应放出热量使温度达到脱脂棉的着火点,剧烈燃烧说明氧气浓度较大,该反应产生氧气,D项正确;
答案选D。
10.A
【详解】
A.Ⅰ含有羟基,且与羟基相连的碳原子上有氢原子,可被酸性高锰酸钾氧化,高锰酸钾溶液褪色,故A错误;
B.Ⅰ含有羟基,可与钠反应生成氢气,而Ⅲ与钠不反应,可鉴别,故B正确;
C.反应中-OH中的H被替代,为取代反应,故C正确;
D.Ⅲ结构对称,含有如图所示5种H,则一氯代物有5种,故D正确;
故选:A。
11.D
【详解】
A.根据烷烃命名原则,CH3CH2CH2CH(CH3)2的名称是2-甲基戊烷,故A正确;
B.因为C3H8是丙烷有2种不同类型的H原子,所以一氯代物有2种,故B正确;
C.结构相似、在分子组成上相差一个或若干个-CH2原子团的有机物间互称同系物,甲酸(HCOOH)和乙酸(CH3COOH)的官能团的个数、种类都相同,相差一个-CH2原子团,故两者是同系物,故C正确;
D.CH3COOCH2CH3和CH3CH2COOCH3为分子式相同,结构不同的同分异构体,不是同一种物质,故D错误;
故答案:D。
【点睛】
根据烷烃命名原则:①长-----选最长碳链为主链;②多-----遇等长碳链时,支链最多为主链;③近-----离支链最近一端编号;④小-----支链编号之和最小。
12.CD
【分析】
由图可知该有机物含有的官能团为碳碳双键、醚键、酚羟基、溴原子和酯基,有机物表现酚、烯烃、卤代烃及酯的性质。
【详解】
A.该有机物中含有酚羟基,该有机物露置在在空气中酚羟基易被氧化,故A错误;
B.该物质含有溴原子,但溴原子所连碳的邻位碳上没有H原子,不能发生消去反应,故B错误;
C.酚-OH的邻对位与溴水发生取代,碳碳双键与溴水发生加成反应,则1 mol该化合物与足量浓溴水反应,最多消耗4 mol Br2,其中取代反应消耗3mol,加成反应消耗1mol,故C正确;
D.酚羟基、溴原子、酯基均与NaOH溶液反应,1 mol该化合物与足量NaOH溶液反应,最多消耗5 mol NaOH,故D正确;
故选:CD。
13.AB
【解析】
A.分子中存在的苯环、羰基及碳碳双键均为平面结构,则所有碳原子可能处于同一平面,故A正确;B.酚羧基能与Na2CO3反应生成NaHCO3,且分子中有2个酚羟基,则1mol化合物X可以与2 molNa2CO3反应,故B正确;C.1mol化合物X最多可以3molBr2反应,其中2mol是加成,1mol发生取代,故C错误;D.化合物X中苯环、碳碳双键及羰基均能与H2完全加成反应,每个产物分子中含有3个手性碳原子,故D错误;答案为AB。
14.A BD 分液漏斗、容量瓶 充分析出乙酰水杨酸固体(结晶) 生成可溶的乙酰水杨酸钠 重结晶
【详解】
(1)因为反应温度在70℃,低于水的沸点,且需维温度不变,故采用热水浴的方法加热,故答案为:A。
(2)操作①需将反应物倒入冷水,需要用烧杯量取和存放冷水,过滤的操作中还需要漏斗,分液漏斗主要用于分离互不相容的液体混合物,容量瓶用于配制一定浓度的溶液,这两个仪器用不到,故答案为B、D;分液漏斗、容量瓶。
(3)反应时温度较高,加入冷水可以降低反应后的混合物的温度,使其冷却结晶,即析出固体得到乙酰水杨酸产物,故答案为:充分析出乙酰水杨酸固体(结晶)。
(4)乙酰水杨酸难溶于水,为了除去其中的杂质,加入饱和碳酸氢钠可以与乙酰水杨酸反应,生成可以溶于水的乙酰水杨酸钠,除去粗产品表面附着的有机物,达到再次洗涤的目的,故答案为:生成可溶的乙酰水杨酸钠。
(5)每次结晶过程中会有少量杂质一起析出,可以通过多次结晶的方法进行纯化,也就是重结晶,故答案为:重结晶。
15.加成反应 +3H2false CH2O A、B、C B
【详解】
(1)化合物I的结构简式为,由某些性质类似苯可知, 在一定条件下与氢气发生反应生成,反应的化学方程式为+3H2
false,故答案为:加成反应;+3H2false;
(2)由化合物Ⅰ生成化合物Ⅱ是原子利用率100%的反应可知,与甲醛发生加成反应生成,甲醛的分子式为CH2O,故答案为:CH2O;
(3)A.因化合物Ⅱ分子中含有羟基,在浓硫酸作用下,可以和CH3COOH共热发生酯化反应,故正确;
B.化合物Ⅲ不含羟基、羧基等,不可以与金属钠生成氢气,故正确;
C.化合物Ⅲ的分子中含有碳碳双键,能与溴的四氯化碳溶液发生加成反应,使溴的四氯化碳溶液褪色,故正确;
D.化合物Ⅲ的分子中含有碳碳双键,能与酸性高锰酸钾溶液发生氧化反应,使酸性高锰酸钾溶液褪色,故错误;
ABC正确,故答案为:A、B、C;
(4)化合物Ⅲ含有碳碳双键,一定条件下,能发生加聚反应反应生成化合物Ⅳ,乙烯含有碳碳双键,与化合物Ⅲ性质相似,也能发生加聚反应生成聚乙烯,B正确,故答案为:B。
16.C13H21NO3 酯基、羰基(或酮基) 加成反应 取代反应 18种 、、、、、,再分别有邻位和间位,任写一种即可
【详解】
①与甲醛加成生成A、,②A中醇中羟基与HCl发生取代反应生成B、,③B与乙酸钠发生取代反应生成,④再发生取代反应生成C、,⑤C与溴发生取代反应生成、⑥发生取代反应生成D、 。
(1)沙丁胺醇的分子式为C13H21NO3 ,C中官能团的名称为酯基、羰基(或酮基)。(2)①的反应类型为加成反应,⑥的反应类型为取代反应。(3)B的结构简式为。(4)A在酸性条件下发生缩聚反应的化学方程式为。(5)符合下列条件的B的同分异构体有18种 种(不考虑立体异构),其中任意一种的结构简式为 、、、、、,再分别有邻位和间位,任写一种即可。(6)写出以苯酚、甲醛和乙酸酐()为原料制备高分子的合成路线:
17.(1)加成反应 甲醇
(2)溴水(氯气)、氢氧化钠水溶液
(3)
(4)(合理即给分)
【解析】
试题分析:(1)B与A发生1,4加成成环,从组成分析得出G经过与甲醇酯化可以得到A;(2)C到D由碳碳双键衍变为两个羟基,故先加成溴单质再水解可得,反应条件为溴水、氢氧化钠水溶液;(3)D经过催化氧化,羟基转化为醛基,
(4)由②知物质X含有2个醛基,故其共有2个醛基和1个甲基,有不同的位置变化。如等。
考点:考查有机物的相互转化的关系,涉及反应类型、方程式的书写、同分异构体等有关问题。
18. 2 2 C8H12 2HO-CH2-COOH+2H2O
【分析】
(1)如果某烷烃分子中同时存在这4种基团,最少-CH2-、和各含有一个,剩下的为甲基,根据烷烃通式确定碳原子个数并确定结构简式,然后根据氢原子种类等于一氯代物同分异构体的数目分析解答;
(2)分子中碳碳双键氧化生成羰基,每个碳碳双键生成2个羰基;碳碳双键断裂形成C=O双键,产物中碳原子、氢原子总数与原烯烃中相等;结合产物的结构和数目分析判断;
(3)A由C、H、O三种元素组成,A在气态时的密度是相同条件下氢气密度的38倍,则A的相对分子质量为76,在一定条件下A既可以与乙醇反应生成酯又可以与乙酸反应生成酯,说明A中含有羧基和羟基,在根据0.1mol A完全燃烧时生成0.2mol CO2和0.2mol H2O确定分子中C、H的个数,结合相对分子质量计算O的个数,结合分子式写出结构简式,然后写出在浓硫酸作用下,两分子A相互反应生成六元环状物质的化学方程式。
【详解】
(1)如果某烷烃分子中同时存在—CH3、—CH2—、和4种基团,则最少含有-CH2-、和各一个,剩下的为甲基,设甲基的个数是x,由烷烃的通式知2(x+3)+2=2+1+3x,解得:x=5,所以最少应含有的碳原子数是8,该烷烃的结构简式有3种,分别为:、、,其一氯代物的种类分别为:5种、5种、4种,所以一氯代物同分异构体的数目最少的烷烃的结构简式:,此烷烃可由烯烃加成得到,则该烯烃中碳碳双键可能的位置有2种(),故答案为:;2;
(2)分子中碳碳双键氧化生成羰基,每个碳碳双键生成2个羰基;碳碳双键断裂形成C=O双键,产物中碳原子、氢原子总数与原烯烃相等,由产物和的结构可知,A分子中碳原子数目为8,分子中含有2个碳碳双键,由于2种产物各1mol,因此分子中还存在1个环,不饱和度为3,故A的分子式为C8H12,故答案为:2;C8H12;
(3)A由C、H、O三种元素组成,A在气态时的密度是相同条件下氢气密度的38倍,则A的相对分子质量为76,在一定条件下A既可以与乙醇反应生成酯又可以与乙酸反应生成酯,说明A中含有羧基和羟基,已知0.1mol A完全燃烧时生成0.2mol CO2和0.2mol H2O,则分子中N(C)=false=2,N(H)=false=4,所以N(O)=false=3,所以A的分子式为:C2H4O3;A中含有羧基和羟基,则A的结构简式为HO-CH2-COOH,因此A在浓硫酸作用下,两分子A相互反应生成六元环状酯的化学方程式为2HO-CH2-COOH+2H2O,故答案为:2HO-CH2-COOH+2H2O。
【点睛】
本题的易错点和难点为(2),要注意确定分子结构中存在一个环。
19.13 加成反应 false+H2O 3 falsefalsefalse
【分析】
根据G的结构逆推可知甲苯与Br2在Fe作催化剂条件下发生苯环上甲基邻位C原子上的取代反应产生B,B为,B与H2在MnO2及加热条件下反应产生C,化合物C可发生银镜反应,则C为;D分子式是C4H8,D与HBr反应产生E,E的核磁共振氢谱只有一组峰,说明D是烯烃,与HBr发生加成反应,可知D结构简式是,E是;E与Mg,乙醚反应产生F,F为,C与F反应产生G,G与Mg、乙醚、CO2作用下反应产生H,J是一种酯,分子中除苯环外还含有一个五元环,H在一定条件下发生反应产生J,J为,据此分析解答。
【详解】
(1)化合物B为,苯环是平面结构,甲基是四面体结构,甲基中最大有1个氢原子在苯环所处平面内,因此B中最多有13个原子共平面,故答案为:13;
(2)根据上述分析,C的结构简式为,故答案为:;
(3)E核磁共振氢谱只有一组峰,说明分子中只有1种H原子,则D结构简式是,E是,D与HBr发生加成反应产生E,故答案为:;加成反应;
(4) J是一种酯,分子中除苯环外还含有一个五元环,H()在一定条件下发生反应产生J,J为,反应的化学方程式为false+H2O, 故答案为:false+H2O;
(5)G的结构简式是,其分子式是C11H15OBr,G的同分异构体符合条件:①能与FeCl3溶液发生显色反应,说明分子中含有酚羟基,②核磁共振氢谱有四组峰,且峰面积之比为6∶6∶2∶1,说明物质分子中含有四种H原子,这四种H原子的个数比为6∶6∶2∶1,符合条件的有、、,共3种,故答案为:3;
(6)与Br2在Fe作催化剂条件下发生取代反应产生,与Mg、乙醚发生反应产生,与CH3CHO在水溶液中发生反应产生,故乙醛和苯为原料经过三步合成的流程图为:falsefalsefalse,故答案为:falsefalsefalse。
同课章节目录
