氮的氧化物
图片预览







文档简介
(共24张PPT)
氮的氧化物
南京市第十二中学 刘建国
氮的各种氧化物(NOx)
氧化物
化合价
N2O
NO
N2O3
NO2
N2O4
N2O5
+1
+2
+3
+4
+4
+5
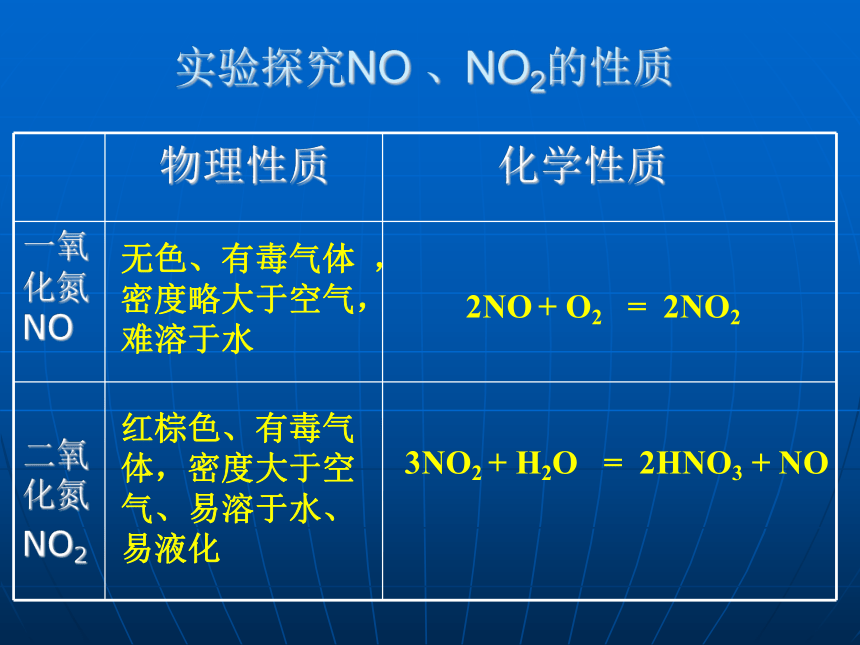
实验探究NO 、NO2的性质
物理性质 化学性质
一氧化氮 NO
二氧化氮
NO2
无色、有毒气体 ,密度略大于空气,难溶于水
红棕色、有毒气体,密度大于空气、易溶于水、易液化
2NO + O2 = 2NO2
3NO2 + H2O = 2HNO3 + NO
思考
1、我们怎样才能使二氧化氮尽可能的被水吸收呢?
2NO + O2 = 2NO2
3NO2 + H2O = 2HNO3 + NO
理论上:4 NO2 + 2H2O + O2 = 4HNO3
2、对工业上生产硝酸有什么启示?
在工业生产硝酸时,使用稍过量的空气,经过多次循环氧化吸收,可充分利用原料,并减少NO的排放。
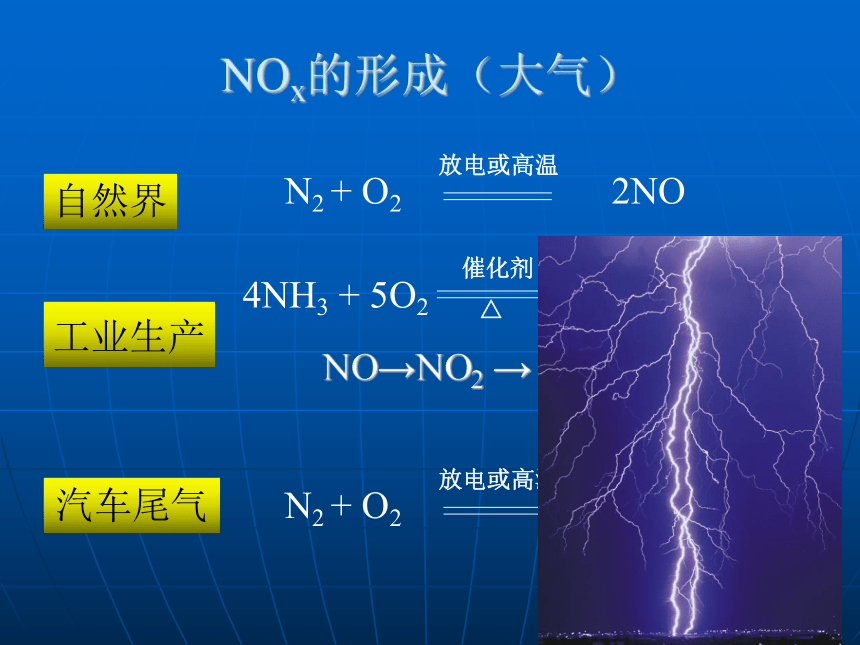
NOx的形成(大气)
自然界
工业生产
汽车尾气
N2 + O2 2NO
放电或高温
4NH3 + 5O2 4NO + 6H2O
催化剂
△
NO→NO2 → HNO3
N2 + O2 2NO
放电或高温
课堂练习
在新疆与青海交界处有一山谷,人称魔鬼谷,经常电闪雷鸣,狂风暴雨,把人畜击毙。然而谷内却是牧草茂盛,四季常青。请解释原因。
__________________________________
雷雨发庄稼
氮的氧化物对我们生活的影响
有利的方面
有害的方面
有利的方面
自然界中
工业中
生命科学中
N2 NO NO2 HNO3 氮肥(可溶性硝酸盐)
O2
闪电
O2
H2O
土壤
NH3 → NO→NO2 → HNO3 进行各种化工生产
如NO——信使分子
Robert F. Furchgott
Louis J. Ignarro
Ferid Murad
由于他们发现了NO可以作为心血管系统的传导分子,而获得1998年的诺贝尔生理医学奖。
NO在人体的生理过程中的作用
计算机模拟的NO分子的图像
硝化甘油
— 心脏病内服药
患有动脉硬化的病人,因血块堵住了动脉的血管,血肌供氧量的减少,引起胸部的疼痛,有时甚至导致心肌梗塞。服用硝化甘油,就是提供了NO,扩大了心肌血管,增大了血流量。
有害的方面
大气中NOx对人体的直接伤害
大气中NOx引起的二次污染
1、酸雨
2、光化学烟雾
3、臭氧层破坏
二氧化氮的毒性比一氧化氮大,它有特殊的刺激性臭味,对呼吸道和肺部有严重的刺激作用,能引起支气管哮喘、肺水肿等疾病。二氧化氮对心、肝、肾造血系统也能造成损害。
思考:一氧化碳使人中毒的生物原理是什么?
一氧化氮和一氧化碳一样,也能和血液中的血红蛋白结合,而且结合能力比一氧化碳强得多。一氧化氮和血红蛋白结合后,能造成血液缺氧而引起中枢神经麻痹。因此当一氧化氮浓度较大时,对人体的危害也是很大的。
酸雨的形成:
石油、煤、金属矿物、汽车尾气
CO2 SO2
NOx
雨水. 霜. 雹. 露 等
由于溶解了二氧化碳的缘故,正常雨水的PH值在5.6左右,然而,当空气中大量N和S的氧化物随雨水降落下来就会使得雨水的PH值小于5.6而形成酸雨。
正常雨水的PH值在5.6左右,酸雨的PH值小于5.6
光化学烟雾
1943年,美国洛杉矶市发生了世界上最早的光化学烟雾事件,此后,在北美、日 本、澳大利亚和欧洲部分地区也先后出现这种烟雾。经过反复的调查研究,直到1958年才发现,这一事件是由于洛杉矶市拥有的250万辆汽车排气污染造成的,这些汽车每天消耗约1600 t汽油,向大气排放1000多吨碳氢化合物和400多吨氮氧化物,这些气体受阳光作用,酿成了危害人类的光化学烟雾事件。
光化学烟雾
汽车尾气和工厂废气里含大量氮氧化物和碳氢化合物,这些气体在阳光和紫外线作用下,会发生光热化学反应,产生光化学烟雾。它的毒性很大,对人体有强烈的刺激作用,严重时会使人出现呼吸困难,视力衰退,手足抽搐等症状。
当汽车尾气产生的NO2在日光照射下,即开始光化学烟雾的循环,不断产生O3。
这个循环包括了下列3个化学反应,请补充化学方程式②
写出以上3个化学反应的净结果:________
① NO2 NO + O
② _____________________
③ O + O2 == O3
光
如何降低以上的污染呢?
减少机动车的使用
改进能源结构(清洁燃料或使用电力)
将汽车尾气中的NOx转化为无污染的物质。
清洁燃料、电力在汽车工业中的应用
氢动力概念车
将汽车尾气中的NOx转化为无污染的物质
环境保护一直是当今社会的热,目前城市中的汽车拥有量在不断增多,而在汽车的排气管上安装“催化转化器”(用铂、钯合金作催化剂),它可以减少污染。其作用是让CO、NO反应生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧。
写出CO与NO反应的化学方程式: ,
该反应作氧化剂的物质是_________。
将工业废气中的NOx转化为无害的物质
一氧化氮是大气污染物之一。目前,有一种治理方法是在400℃左右.有催化剂存在的情况下,用氨将一氧化氮转化为空气中含量最大的气体,同时生成一种常见的五色液体。请写出该反应的化学方程式,并分析该反应的电子转移情况。
_____________________________
1、某试管内盛有NO2气体12体积,把它倒立于盛水的水槽中,剩余____气体,试管内的气体为_____体积;试管内的溶液为_______溶液。
如要使试管内充满水,则应通入02___体积。
4
NO
HNO3
3
课堂练习
2、有气体:H2 O2 NO NO2 CO2
(1)、若洗气瓶是干燥的,由A口进气,可收集的气体有:
(2)、若瓶中充满水,可收集的气体有:
A B
O2 NO2 CO2
H2 O2 NO
课堂练习
课堂练习
3、下列反应中属于氧化还原反应,但水既不作氧化剂,又不作还原剂的是 A.2F2+2H2O=4HF+O2 B.3NO2+H2O=NO+2HNO3 C.2Na2O2+2H2O=4NaOH+O2↑ D.2Na+2H2O=2NaOH+H2↑ E.2H2O=2H2↑+O2↑ F.SO2+H2O=H2SO3
氮的氧化物
南京市第十二中学 刘建国
氮的各种氧化物(NOx)
氧化物
化合价
N2O
NO
N2O3
NO2
N2O4
N2O5
+1
+2
+3
+4
+4
+5
实验探究NO 、NO2的性质
物理性质 化学性质
一氧化氮 NO
二氧化氮
NO2
无色、有毒气体 ,密度略大于空气,难溶于水
红棕色、有毒气体,密度大于空气、易溶于水、易液化
2NO + O2 = 2NO2
3NO2 + H2O = 2HNO3 + NO
思考
1、我们怎样才能使二氧化氮尽可能的被水吸收呢?
2NO + O2 = 2NO2
3NO2 + H2O = 2HNO3 + NO
理论上:4 NO2 + 2H2O + O2 = 4HNO3
2、对工业上生产硝酸有什么启示?
在工业生产硝酸时,使用稍过量的空气,经过多次循环氧化吸收,可充分利用原料,并减少NO的排放。
NOx的形成(大气)
自然界
工业生产
汽车尾气
N2 + O2 2NO
放电或高温
4NH3 + 5O2 4NO + 6H2O
催化剂
△
NO→NO2 → HNO3
N2 + O2 2NO
放电或高温
课堂练习
在新疆与青海交界处有一山谷,人称魔鬼谷,经常电闪雷鸣,狂风暴雨,把人畜击毙。然而谷内却是牧草茂盛,四季常青。请解释原因。
__________________________________
雷雨发庄稼
氮的氧化物对我们生活的影响
有利的方面
有害的方面
有利的方面
自然界中
工业中
生命科学中
N2 NO NO2 HNO3 氮肥(可溶性硝酸盐)
O2
闪电
O2
H2O
土壤
NH3 → NO→NO2 → HNO3 进行各种化工生产
如NO——信使分子
Robert F. Furchgott
Louis J. Ignarro
Ferid Murad
由于他们发现了NO可以作为心血管系统的传导分子,而获得1998年的诺贝尔生理医学奖。
NO在人体的生理过程中的作用
计算机模拟的NO分子的图像
硝化甘油
— 心脏病内服药
患有动脉硬化的病人,因血块堵住了动脉的血管,血肌供氧量的减少,引起胸部的疼痛,有时甚至导致心肌梗塞。服用硝化甘油,就是提供了NO,扩大了心肌血管,增大了血流量。
有害的方面
大气中NOx对人体的直接伤害
大气中NOx引起的二次污染
1、酸雨
2、光化学烟雾
3、臭氧层破坏
二氧化氮的毒性比一氧化氮大,它有特殊的刺激性臭味,对呼吸道和肺部有严重的刺激作用,能引起支气管哮喘、肺水肿等疾病。二氧化氮对心、肝、肾造血系统也能造成损害。
思考:一氧化碳使人中毒的生物原理是什么?
一氧化氮和一氧化碳一样,也能和血液中的血红蛋白结合,而且结合能力比一氧化碳强得多。一氧化氮和血红蛋白结合后,能造成血液缺氧而引起中枢神经麻痹。因此当一氧化氮浓度较大时,对人体的危害也是很大的。
酸雨的形成:
石油、煤、金属矿物、汽车尾气
CO2 SO2
NOx
雨水. 霜. 雹. 露 等
由于溶解了二氧化碳的缘故,正常雨水的PH值在5.6左右,然而,当空气中大量N和S的氧化物随雨水降落下来就会使得雨水的PH值小于5.6而形成酸雨。
正常雨水的PH值在5.6左右,酸雨的PH值小于5.6
光化学烟雾
1943年,美国洛杉矶市发生了世界上最早的光化学烟雾事件,此后,在北美、日 本、澳大利亚和欧洲部分地区也先后出现这种烟雾。经过反复的调查研究,直到1958年才发现,这一事件是由于洛杉矶市拥有的250万辆汽车排气污染造成的,这些汽车每天消耗约1600 t汽油,向大气排放1000多吨碳氢化合物和400多吨氮氧化物,这些气体受阳光作用,酿成了危害人类的光化学烟雾事件。
光化学烟雾
汽车尾气和工厂废气里含大量氮氧化物和碳氢化合物,这些气体在阳光和紫外线作用下,会发生光热化学反应,产生光化学烟雾。它的毒性很大,对人体有强烈的刺激作用,严重时会使人出现呼吸困难,视力衰退,手足抽搐等症状。
当汽车尾气产生的NO2在日光照射下,即开始光化学烟雾的循环,不断产生O3。
这个循环包括了下列3个化学反应,请补充化学方程式②
写出以上3个化学反应的净结果:________
① NO2 NO + O
② _____________________
③ O + O2 == O3
光
如何降低以上的污染呢?
减少机动车的使用
改进能源结构(清洁燃料或使用电力)
将汽车尾气中的NOx转化为无污染的物质。
清洁燃料、电力在汽车工业中的应用
氢动力概念车
将汽车尾气中的NOx转化为无污染的物质
环境保护一直是当今社会的热,目前城市中的汽车拥有量在不断增多,而在汽车的排气管上安装“催化转化器”(用铂、钯合金作催化剂),它可以减少污染。其作用是让CO、NO反应生成可参与大气生态环境循环的无毒气体,并促使烃类充分燃烧。
写出CO与NO反应的化学方程式: ,
该反应作氧化剂的物质是_________。
将工业废气中的NOx转化为无害的物质
一氧化氮是大气污染物之一。目前,有一种治理方法是在400℃左右.有催化剂存在的情况下,用氨将一氧化氮转化为空气中含量最大的气体,同时生成一种常见的五色液体。请写出该反应的化学方程式,并分析该反应的电子转移情况。
_____________________________
1、某试管内盛有NO2气体12体积,把它倒立于盛水的水槽中,剩余____气体,试管内的气体为_____体积;试管内的溶液为_______溶液。
如要使试管内充满水,则应通入02___体积。
4
NO
HNO3
3
课堂练习
2、有气体:H2 O2 NO NO2 CO2
(1)、若洗气瓶是干燥的,由A口进气,可收集的气体有:
(2)、若瓶中充满水,可收集的气体有:
A B
O2 NO2 CO2
H2 O2 NO
课堂练习
课堂练习
3、下列反应中属于氧化还原反应,但水既不作氧化剂,又不作还原剂的是 A.2F2+2H2O=4HF+O2 B.3NO2+H2O=NO+2HNO3 C.2Na2O2+2H2O=4NaOH+O2↑ D.2Na+2H2O=2NaOH+H2↑ E.2H2O=2H2↑+O2↑ F.SO2+H2O=H2SO3
