3.1 物质的转化 同步练习(含解析)
文档属性
| 名称 | 3.1 物质的转化 同步练习(含解析) |

|
|
| 格式 | docx | ||
| 文件大小 | 84.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-04-26 00:00:00 | ||
图片预览


文档简介
3.1物质的转化
一、单选题
1.下列物质的转化,不能一步实现的是( )
A.?Cu→Cu(OH)2 ??????????????B.?Ba(NO3)2→BaSO4??????????????C.?Zn→ZnCl2 ??????????????D.?Ca(OH)2→NaOH
2.常温下,某反应M+N →盐+水,其中M、N的类别不可能是(?? )
A.?酸、碱????????????????????????B.?单质、氧化物????????????????????????C.?氧化物、酸????????????????????????D.?氧化物、碱
3.下列物质的转化在给定条件下均能实现的是(?? )
A.?Fe Fe2O3 FeCl3??????????????????????????????????B.?SO2 H2SO3 H2SO4
C.?Na2CO3 NaNO3 KNO3?????????????????D.?CaCl2溶液 CaCO3 Ca(OH)2
4.甲、乙、丙、丁是初中科学中常见的四种物质,它们有如下关系:①甲+乙→H2O;②乙+丁→CO2;③丙+乙→CO2+H2O。则丙物质可能是(?? )
A.?甲烷?????????????????????????????????????B.?氢气?????????????????????????????????????C.?氧气?????????????????????????????????????D.?盐酸
5.下列关于碳和碳的氧化物知识网络图(图中“→”表示转化关系,“—”表示相互能反应),说法正确的是(?? )
A.?“C→CO2”的反应碳元素的化合价未发生改变?????????B.?“CO →CO2”的反应类型为置换反应
C.?“CO2→CaCO3”的反应可用于检验二氧化碳?????????D.?“CO2→H2CO3”的反应可用酚酞试剂验证
6.下列各组转化中,一定条件下均能一步实现的组合是(?? )
A.?只有②??????????????????????????????????B.?②③??????????????????????????????????C.?①③??????????????????????????????????D.?①②③
7.甲、乙、丙、丁四种物质的转化关系如图所示。下列说法正确的是(? ?)
A.?若丙、丁为盐和水,则甲、乙一定是酸、碱??????????B.?若丙为气体,则甲、乙中一定有单质
C.?若丁为水,则该反应一定是复分解反应???????????????D.?若只有甲、丁是单质,则该反应一定是置换反应
二、实验探究题
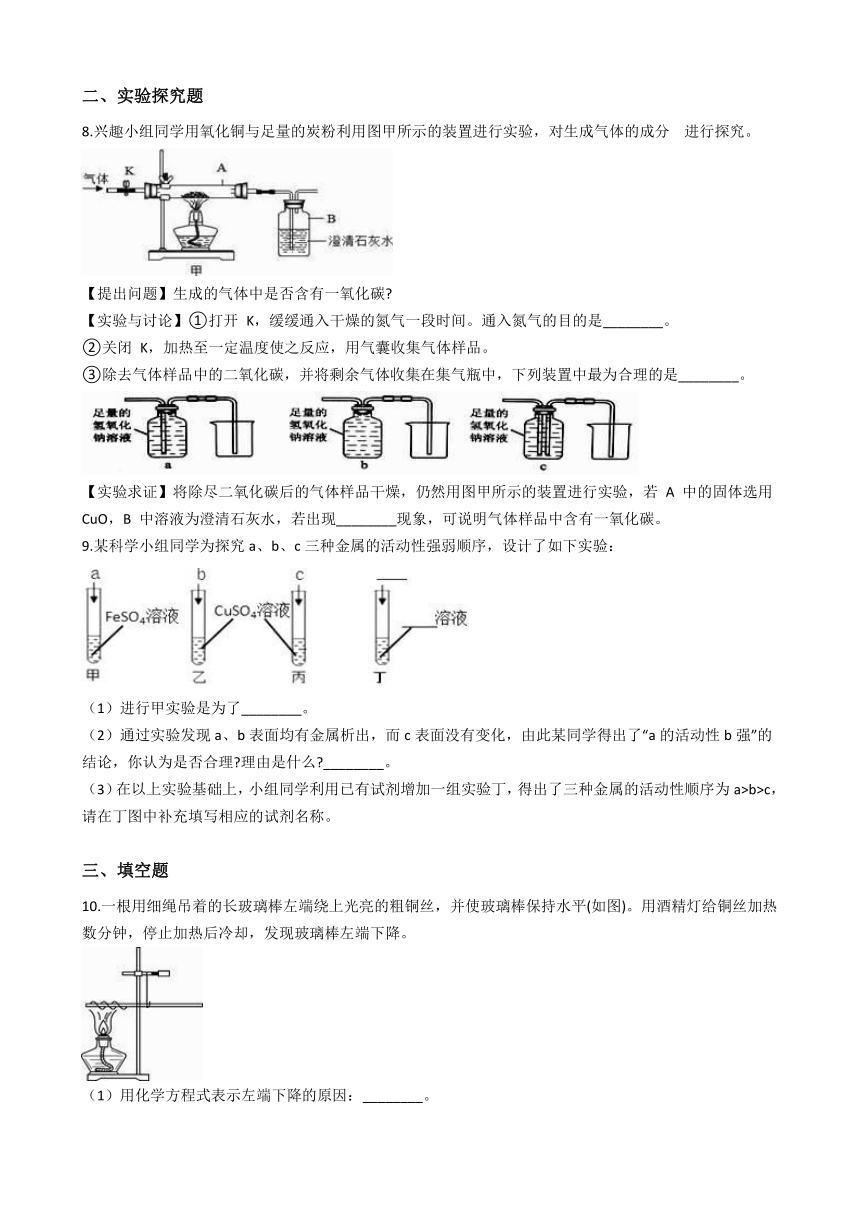
8.兴趣小组同学用氧化铜与足量的炭粉利用图甲所示的装置进行实验,对生成气体的成分?? 进行探究。
【提出问题】生成的气体中是否含有一氧化碳?
【实验与讨论】①打开 K,缓缓通入干燥的氮气一段时间。通入氮气的目的是________。
②关闭 K,加热至一定温度使之反应,用气囊收集气体样品。
③除去气体样品中的二氧化碳,并将剩余气体收集在集气瓶中,下列装置中最为合理的是________。
【实验求证】将除尽二氧化碳后的气体样品干燥,仍然用图甲所示的装置进行实验,若 A 中的固体选用 CuO,B 中溶液为澄清石灰水,若出现________现象,可说明气体样品中含有一氧化碳。
9.某科学小组同学为探究a、b、c三种金属的活动性强弱顺序,设计了如下实验:
(1)进行甲实验是为了________。
(2)通过实验发现a、b表面均有金属析出,而c表面没有变化,由此某同学得出了“a的活动性b强”的结论,你认为是否合理?理由是什么?________。
(3)在以上实验基础上,小组同学利用已有试剂增加一组实验丁,得出了三种金属的活动性顺序为a>b>c,请在丁图中补充填写相应的试剂名称。
三、填空题
10.一根用细绳吊着的长玻璃棒左端绕上光亮的粗铜丝,并使玻璃棒保持水平(如图)。用酒精灯给铜丝加热数分钟,停止加热后冷却,发现玻璃棒左端下降。
(1)用化学方程式表示左端下降的原因:________。
(2)将玻璃棒连同细绳取下,铜丝端浸入稀硫酸,充分反应后取出,洗涤、干燥再重新吊起(细绳系在玻璃棒的位置不变),玻璃棒________(填“能”或“不能”)再次保持水平。
11.把铁粉和硫粉以适当的质量比均匀混合,堆放在石棉网上,然后用烧红的玻璃棒的一端接触混合物。这时部分混合物迅速变成红热状态,移开玻璃棒后,反应继续剧烈进行,混合物全部呈红热状态,冷却后得到黑色的固体化合物——硫化亚铁。
(1)这一变化的化学方程式是________。
(2)铁跟硫反应时是吸收热量还是放出热量?________。
(3)用什么实验可以证实反应中铁已从游离态变成化合态________。
(4)从理论上计算,为使铁粉和硫粉都能全部反应,两者最佳质量比应是________。
答案解析部分
一、单选题
1.【答案】 A
【解析】【分析】根据题中所涉及 物质的化学性质分析。
【解答】A.铜不能直接转化成氢氧化铜,符合题意;
B.硝酸钡与硫酸钠可直接生成硫酸钡,不符合题意;
C.锌与盐酸反应可生成氯化锌,不符合题意;
D.氢氧化钙与碳酸钠反应可生成氢氧化钠,不符合题意;
故答案为:A。
2.【答案】 B
【解析】【分析】根据单质与氧化物反应不能生成盐和水分析。
【解答】反应后生成盐和水,所以一定不是单质和氧化物的反应;
故答案为:B。
3.【答案】 B
【解析】【分析】根据各化合物的性质及相互反应关系分析。
【解答】A.铁与氧气点燃生成四氧化三铁,不是三氧化二铁,不符合题意;
B.二氧化硫与水化合生成亚硫酸,亚硫酸与氧气反应生成硫酸,符合题意;
C.硝酸钠与氯化钾不反应,不符合题意;
D.氯化钙与二氧化碳不反应,不符合题意;
故答案为:B。
4.【答案】 A
【解析】【分析】根据物质与氧气的反应进行分析,可利用反应前后元素种类不变结合物质的性质选择。
【解答】甲乙能生成水,乙丁能生成二氧化碳,丙和乙能生成二氧化碳和水,则说明乙为氧气,甲为氢气,乙为碳或一氧化碳,丙可以为甲烷;
故答案为:A。
5.【答案】 C
【解析】【分析】根据碳、一氧化碳、二氧化碳的性质及相互转化进行分析。
【解答】A.“C→CO2”的反应碳元素的化合价从0价变为+4价,不符合题意;
B.“CO →CO2”的反应类型不属于置换反应,不符合题意;
C.“CO2→CaCO3”可利用二氧化碳与氢氧化钙反应,该反应可用于检验二氧化碳,符合题意;
D.碳酸不能使酚酞变色,“CO2→H2CO3”的反应不能用酚酞试剂验证,不符合题意;
故答案为:C。
6.【答案】 D
【解析】【分析】一步反应实现即原物质只发生一个反应即可转化为目标物质,根据所涉及物质的性质,分析能否只通过一个反应而实现即可。
【解答】(1)水能与三氧化硫发生反应生成硫酸,硫酸又能与金属铁等发生置换而得到氢气,氢气与氧气反应则可得到水,因此①转化关系中的三种物质均可实现一步转化;(2)碳酸钙在高温下分解可一步转化为氧化钙,氧化钙再与盐酸反应又可一步转化为氯化钙,氯化钙与碳酸钠可一步转化为碳酸钙,因此②转化关系中的三种物质均可实现一步转化;(3)③硫酸镁与氯化钡反应生成氯化镁,氯化镁可与氢氧化钠反应生成氢氧化镁,氢氧化镁与硫酸反应生成碳酸钠,因此③转化中的三种物质都能实现一步的转化。所以①②③一定条件下均能一步实现,D符合题意。
故答案为:D
7.【答案】 D
【解析】【分析】由物质转化关系图可知,甲与乙反应生成了丙和丁,此反应中有两种反应物,得到两种生成物。根据学习中已掌握的物质间的反应,通过找出特列可以判断选项。
【解答】A、若丙、丁为盐和水,则甲、乙一定是酸、碱,CuO和HCl反应也能生成盐和水,A错误;
B、若丙为气体,则甲、乙中一定有单质,CaCO3和HCl反应也能生成CO2气体,B错误;
C、若丁为水,则该反应一定是复分解反应, CuO和H2的反应中也生成了水,但不是复分解反应,C错误;
D、若只有甲、丁是单质,则该反应一定是置换反应,因只有甲、丁是单质,所以乙、丙不是单质,所以此反应中反应物是一种单质和一种化合物,生成物中是另一种单质和另一种化合物,符合置换反应的概念,D正确。
故选D
二、实验探究题
8.【答案】 将装置中的空气排净,防止加热爆炸;c;黑色固体变为红色粉末,澄清石灰水变浑浊
【解析】【分析】该题主要考查学生对氢气还原氧化铜实验的掌握,及二氧化碳的相关性质应用;
【解答】(1)氮气比较稳定,通常用作化学反应的保护气,而通入氮气主要是可以将装置内的空气排净,防止一氧化碳纯度不足发生爆炸;故答案为:将装置中的空气排净,防止加热爆炸;
(2)除去二氧化碳,要将二氧化碳通入氢氧化钠溶液中,而为了充分吸收导管要通入集气瓶底部;而一氧化碳的密度比液体密度小,会浮在集气瓶上方,所以要将导管伸入集气瓶底部防止一氧化碳气体逸出;故答案为:c;
(3)CuO+CO=Cu+CO2? 如果剩余气体是一氧化碳则会与CuO反应生成铜单质和二氧化碳; 而二氧化碳通入澄清石灰水会变混浊;故答案为:黑色固体变为红色粉末,澄清石灰水变浑浊;
故答案为:(1)将装置中的空气排净,防止加热爆炸;2)c;(3)黑色固体变为红色粉末,澄清石灰水变浑浊。
9.【答案】 (1)比较a金属与Fe的金属活动性强弱
(2)不合理,因为甲实验只能得出活动性a比Fe强,乙实验只得出活动性b比Cu强,a、b之间无法比较(甲、乙试管中的溶液不同,无法比较)
(3)
【解析】【分析】(1)金属活动性顺序特点有,排在前面的金属能将排在后面的金属从该金属的盐溶液中置换出来。所以由甲实验中所用的盐溶液可以得出实验的目的;
(2)由于甲、乙实验中所用的盐溶液是不同的,实验中只能说明活动性a与Fe的关系,说明活动性b与Cu的关系,无法说明a与b的活动性关系;
(3)由乙和丙实验可以确定b与c的活动性关系。由实验结论三种金属的活动性顺序为a>b>c,需要确定出a>b的关系,需要将a与b放到同一种盐溶液中进行比较。
【解答】(1)进行甲实验是为了比较a金属与Fe的金属活动性强弱。
(2)研究金属活动性顺序应该让同种金属放到不同溶液中,或不同金属放到同种溶液中进行比较。题中设计的实验不合理,因为甲实验只能得出活动性a比Fe强,乙实验只得出活动性b比Cu强,a、b之间无法比较(甲、乙试管中的溶液不同,无法比较);
(3)由乙和丙实验可以确定b的活动性比c强。要比较a、b的金属活动性顺序,由题中实验使用的溶液FeSO4和CuSO4 , Fe的活动性比Cu强可知,a放入CuSO4中一定能置换出铜,所以丁图中要使用的试剂,优先选择FeSO4。
故答案为:(1)比较a金属与Fe的金属活动性强弱;(2)不合理,因为甲实验只能得出活动性a比Fe强,乙实验只得出活动性b比Cu强,a、b之间无法比较(甲、乙试管中的溶液不同,无法比较);(3)FeSO4
三、填空题
10.【答案】 (1)2Cu+O2 2CuO
(2)不能
【解析】【分析】根据铜与氧气的质量总和等于生成的氧化铜的质量分析;根据氧化铜能与硫酸反应生成硫酸铜和水分析。
【解答】(1)左端下降是因为铜与空气中氧气反应生成氧化铜,氧化铜的质量等于铜与氧气质量之和;(2)铜丝表面的氧化铜能与硫酸反应生成硫酸铜和水,所以剩余的铜的质量减少,玻璃棒不能保持水平。
11.【答案】 (1)Fe+S FeS
(2)放出热量
(3)用磁铁吸引,若没有物质被吸引则铁已从游离态变成化合态
(4)7∶4
【解析】【分析】根据题中所给信息分析,确定反应物生成物及反应条件,从而写也反应方程式,利用方程式确定各物质间的质量关系。
【解答】(1)由题中所给信息可知,该反应为铁与硫加热条件下生成硫化亚铁的反应;(2)由题意可知,铁与硫用烧红的玻璃棒接触后反应部分混合物迅速变成红热状态,,移开玻璃棒后,反应继续剧烈进行,混合物全部呈红热状态,由此说明该反应为放热反应;(3)铁有铁磁性,能被磁铁吸引,所以可用磁铁吸引,若不能被吸引则说明铁从游离态变成了化合态;(4)由方程式可知铁与硫参加反应的质量比为56:32=7:4.
一、单选题
1.下列物质的转化,不能一步实现的是( )
A.?Cu→Cu(OH)2 ??????????????B.?Ba(NO3)2→BaSO4??????????????C.?Zn→ZnCl2 ??????????????D.?Ca(OH)2→NaOH
2.常温下,某反应M+N →盐+水,其中M、N的类别不可能是(?? )
A.?酸、碱????????????????????????B.?单质、氧化物????????????????????????C.?氧化物、酸????????????????????????D.?氧化物、碱
3.下列物质的转化在给定条件下均能实现的是(?? )
A.?Fe Fe2O3 FeCl3??????????????????????????????????B.?SO2 H2SO3 H2SO4
C.?Na2CO3 NaNO3 KNO3?????????????????D.?CaCl2溶液 CaCO3 Ca(OH)2
4.甲、乙、丙、丁是初中科学中常见的四种物质,它们有如下关系:①甲+乙→H2O;②乙+丁→CO2;③丙+乙→CO2+H2O。则丙物质可能是(?? )
A.?甲烷?????????????????????????????????????B.?氢气?????????????????????????????????????C.?氧气?????????????????????????????????????D.?盐酸
5.下列关于碳和碳的氧化物知识网络图(图中“→”表示转化关系,“—”表示相互能反应),说法正确的是(?? )
A.?“C→CO2”的反应碳元素的化合价未发生改变?????????B.?“CO →CO2”的反应类型为置换反应
C.?“CO2→CaCO3”的反应可用于检验二氧化碳?????????D.?“CO2→H2CO3”的反应可用酚酞试剂验证
6.下列各组转化中,一定条件下均能一步实现的组合是(?? )
A.?只有②??????????????????????????????????B.?②③??????????????????????????????????C.?①③??????????????????????????????????D.?①②③
7.甲、乙、丙、丁四种物质的转化关系如图所示。下列说法正确的是(? ?)
A.?若丙、丁为盐和水,则甲、乙一定是酸、碱??????????B.?若丙为气体,则甲、乙中一定有单质
C.?若丁为水,则该反应一定是复分解反应???????????????D.?若只有甲、丁是单质,则该反应一定是置换反应
二、实验探究题
8.兴趣小组同学用氧化铜与足量的炭粉利用图甲所示的装置进行实验,对生成气体的成分?? 进行探究。
【提出问题】生成的气体中是否含有一氧化碳?
【实验与讨论】①打开 K,缓缓通入干燥的氮气一段时间。通入氮气的目的是________。
②关闭 K,加热至一定温度使之反应,用气囊收集气体样品。
③除去气体样品中的二氧化碳,并将剩余气体收集在集气瓶中,下列装置中最为合理的是________。
【实验求证】将除尽二氧化碳后的气体样品干燥,仍然用图甲所示的装置进行实验,若 A 中的固体选用 CuO,B 中溶液为澄清石灰水,若出现________现象,可说明气体样品中含有一氧化碳。
9.某科学小组同学为探究a、b、c三种金属的活动性强弱顺序,设计了如下实验:
(1)进行甲实验是为了________。
(2)通过实验发现a、b表面均有金属析出,而c表面没有变化,由此某同学得出了“a的活动性b强”的结论,你认为是否合理?理由是什么?________。
(3)在以上实验基础上,小组同学利用已有试剂增加一组实验丁,得出了三种金属的活动性顺序为a>b>c,请在丁图中补充填写相应的试剂名称。
三、填空题
10.一根用细绳吊着的长玻璃棒左端绕上光亮的粗铜丝,并使玻璃棒保持水平(如图)。用酒精灯给铜丝加热数分钟,停止加热后冷却,发现玻璃棒左端下降。
(1)用化学方程式表示左端下降的原因:________。
(2)将玻璃棒连同细绳取下,铜丝端浸入稀硫酸,充分反应后取出,洗涤、干燥再重新吊起(细绳系在玻璃棒的位置不变),玻璃棒________(填“能”或“不能”)再次保持水平。
11.把铁粉和硫粉以适当的质量比均匀混合,堆放在石棉网上,然后用烧红的玻璃棒的一端接触混合物。这时部分混合物迅速变成红热状态,移开玻璃棒后,反应继续剧烈进行,混合物全部呈红热状态,冷却后得到黑色的固体化合物——硫化亚铁。
(1)这一变化的化学方程式是________。
(2)铁跟硫反应时是吸收热量还是放出热量?________。
(3)用什么实验可以证实反应中铁已从游离态变成化合态________。
(4)从理论上计算,为使铁粉和硫粉都能全部反应,两者最佳质量比应是________。
答案解析部分
一、单选题
1.【答案】 A
【解析】【分析】根据题中所涉及 物质的化学性质分析。
【解答】A.铜不能直接转化成氢氧化铜,符合题意;
B.硝酸钡与硫酸钠可直接生成硫酸钡,不符合题意;
C.锌与盐酸反应可生成氯化锌,不符合题意;
D.氢氧化钙与碳酸钠反应可生成氢氧化钠,不符合题意;
故答案为:A。
2.【答案】 B
【解析】【分析】根据单质与氧化物反应不能生成盐和水分析。
【解答】反应后生成盐和水,所以一定不是单质和氧化物的反应;
故答案为:B。
3.【答案】 B
【解析】【分析】根据各化合物的性质及相互反应关系分析。
【解答】A.铁与氧气点燃生成四氧化三铁,不是三氧化二铁,不符合题意;
B.二氧化硫与水化合生成亚硫酸,亚硫酸与氧气反应生成硫酸,符合题意;
C.硝酸钠与氯化钾不反应,不符合题意;
D.氯化钙与二氧化碳不反应,不符合题意;
故答案为:B。
4.【答案】 A
【解析】【分析】根据物质与氧气的反应进行分析,可利用反应前后元素种类不变结合物质的性质选择。
【解答】甲乙能生成水,乙丁能生成二氧化碳,丙和乙能生成二氧化碳和水,则说明乙为氧气,甲为氢气,乙为碳或一氧化碳,丙可以为甲烷;
故答案为:A。
5.【答案】 C
【解析】【分析】根据碳、一氧化碳、二氧化碳的性质及相互转化进行分析。
【解答】A.“C→CO2”的反应碳元素的化合价从0价变为+4价,不符合题意;
B.“CO →CO2”的反应类型不属于置换反应,不符合题意;
C.“CO2→CaCO3”可利用二氧化碳与氢氧化钙反应,该反应可用于检验二氧化碳,符合题意;
D.碳酸不能使酚酞变色,“CO2→H2CO3”的反应不能用酚酞试剂验证,不符合题意;
故答案为:C。
6.【答案】 D
【解析】【分析】一步反应实现即原物质只发生一个反应即可转化为目标物质,根据所涉及物质的性质,分析能否只通过一个反应而实现即可。
【解答】(1)水能与三氧化硫发生反应生成硫酸,硫酸又能与金属铁等发生置换而得到氢气,氢气与氧气反应则可得到水,因此①转化关系中的三种物质均可实现一步转化;(2)碳酸钙在高温下分解可一步转化为氧化钙,氧化钙再与盐酸反应又可一步转化为氯化钙,氯化钙与碳酸钠可一步转化为碳酸钙,因此②转化关系中的三种物质均可实现一步转化;(3)③硫酸镁与氯化钡反应生成氯化镁,氯化镁可与氢氧化钠反应生成氢氧化镁,氢氧化镁与硫酸反应生成碳酸钠,因此③转化中的三种物质都能实现一步的转化。所以①②③一定条件下均能一步实现,D符合题意。
故答案为:D
7.【答案】 D
【解析】【分析】由物质转化关系图可知,甲与乙反应生成了丙和丁,此反应中有两种反应物,得到两种生成物。根据学习中已掌握的物质间的反应,通过找出特列可以判断选项。
【解答】A、若丙、丁为盐和水,则甲、乙一定是酸、碱,CuO和HCl反应也能生成盐和水,A错误;
B、若丙为气体,则甲、乙中一定有单质,CaCO3和HCl反应也能生成CO2气体,B错误;
C、若丁为水,则该反应一定是复分解反应, CuO和H2的反应中也生成了水,但不是复分解反应,C错误;
D、若只有甲、丁是单质,则该反应一定是置换反应,因只有甲、丁是单质,所以乙、丙不是单质,所以此反应中反应物是一种单质和一种化合物,生成物中是另一种单质和另一种化合物,符合置换反应的概念,D正确。
故选D
二、实验探究题
8.【答案】 将装置中的空气排净,防止加热爆炸;c;黑色固体变为红色粉末,澄清石灰水变浑浊
【解析】【分析】该题主要考查学生对氢气还原氧化铜实验的掌握,及二氧化碳的相关性质应用;
【解答】(1)氮气比较稳定,通常用作化学反应的保护气,而通入氮气主要是可以将装置内的空气排净,防止一氧化碳纯度不足发生爆炸;故答案为:将装置中的空气排净,防止加热爆炸;
(2)除去二氧化碳,要将二氧化碳通入氢氧化钠溶液中,而为了充分吸收导管要通入集气瓶底部;而一氧化碳的密度比液体密度小,会浮在集气瓶上方,所以要将导管伸入集气瓶底部防止一氧化碳气体逸出;故答案为:c;
(3)CuO+CO=Cu+CO2? 如果剩余气体是一氧化碳则会与CuO反应生成铜单质和二氧化碳; 而二氧化碳通入澄清石灰水会变混浊;故答案为:黑色固体变为红色粉末,澄清石灰水变浑浊;
故答案为:(1)将装置中的空气排净,防止加热爆炸;2)c;(3)黑色固体变为红色粉末,澄清石灰水变浑浊。
9.【答案】 (1)比较a金属与Fe的金属活动性强弱
(2)不合理,因为甲实验只能得出活动性a比Fe强,乙实验只得出活动性b比Cu强,a、b之间无法比较(甲、乙试管中的溶液不同,无法比较)
(3)
【解析】【分析】(1)金属活动性顺序特点有,排在前面的金属能将排在后面的金属从该金属的盐溶液中置换出来。所以由甲实验中所用的盐溶液可以得出实验的目的;
(2)由于甲、乙实验中所用的盐溶液是不同的,实验中只能说明活动性a与Fe的关系,说明活动性b与Cu的关系,无法说明a与b的活动性关系;
(3)由乙和丙实验可以确定b与c的活动性关系。由实验结论三种金属的活动性顺序为a>b>c,需要确定出a>b的关系,需要将a与b放到同一种盐溶液中进行比较。
【解答】(1)进行甲实验是为了比较a金属与Fe的金属活动性强弱。
(2)研究金属活动性顺序应该让同种金属放到不同溶液中,或不同金属放到同种溶液中进行比较。题中设计的实验不合理,因为甲实验只能得出活动性a比Fe强,乙实验只得出活动性b比Cu强,a、b之间无法比较(甲、乙试管中的溶液不同,无法比较);
(3)由乙和丙实验可以确定b的活动性比c强。要比较a、b的金属活动性顺序,由题中实验使用的溶液FeSO4和CuSO4 , Fe的活动性比Cu强可知,a放入CuSO4中一定能置换出铜,所以丁图中要使用的试剂,优先选择FeSO4。
故答案为:(1)比较a金属与Fe的金属活动性强弱;(2)不合理,因为甲实验只能得出活动性a比Fe强,乙实验只得出活动性b比Cu强,a、b之间无法比较(甲、乙试管中的溶液不同,无法比较);(3)FeSO4
三、填空题
10.【答案】 (1)2Cu+O2 2CuO
(2)不能
【解析】【分析】根据铜与氧气的质量总和等于生成的氧化铜的质量分析;根据氧化铜能与硫酸反应生成硫酸铜和水分析。
【解答】(1)左端下降是因为铜与空气中氧气反应生成氧化铜,氧化铜的质量等于铜与氧气质量之和;(2)铜丝表面的氧化铜能与硫酸反应生成硫酸铜和水,所以剩余的铜的质量减少,玻璃棒不能保持水平。
11.【答案】 (1)Fe+S FeS
(2)放出热量
(3)用磁铁吸引,若没有物质被吸引则铁已从游离态变成化合态
(4)7∶4
【解析】【分析】根据题中所给信息分析,确定反应物生成物及反应条件,从而写也反应方程式,利用方程式确定各物质间的质量关系。
【解答】(1)由题中所给信息可知,该反应为铁与硫加热条件下生成硫化亚铁的反应;(2)由题意可知,铁与硫用烧红的玻璃棒接触后反应部分混合物迅速变成红热状态,,移开玻璃棒后,反应继续剧烈进行,混合物全部呈红热状态,由此说明该反应为放热反应;(3)铁有铁磁性,能被磁铁吸引,所以可用磁铁吸引,若不能被吸引则说明铁从游离态变成了化合态;(4)由方程式可知铁与硫参加反应的质量比为56:32=7:4.
同课章节目录
- 第一章 宇宙的起源与演化
- 1 我们的宇宙
- 2 热大爆炸宇宙模型
- 3 恒星的一生
- 4 星际航行和空间技术
- 第二章 地球的演化和生物圈的形成
- 1 地球的演化
- 2 生命起源
- 3 生物进化
- 4 生态平衡
- 第三章 物质的转化和元素的循环
- 1 物质的转化
- 2 自然界中的碳循环和氧循环
- 3 自然界中的氮循环
- 第四章 健康与保健
- 1 健康、亚健康和疾病
- 2 运动与健康
- 3 免疫与健康
- 4 营养与健康
- 5 卫生与健康
- 6 环境与健康
- 第五章 生物的遗传和变异
- 1 生物的遗传
- 2 生物的变异
- 第六章 能源与社会
- 1 能源和能源的分类
- 2 太阳能的利用
- 3 核能的开发与放射性防护
- 4 新能源与可持续发展
- 第七章 科学与社会发展
- 1 科学就是力量
- 2 科学推动技术发展
- 3 科学技术推动经济增长
- 4 科学技术与可持续发展
