糖类
图片预览








文档简介
(共23张PPT)
第 二 节
糖 类
一、糖类具有怎样的特征?
绿色植物光合反应的产物
由C、H、O元素组成
常用通式Cn(H2O)m来表示
二、糖类如何分类?
单糖(不能水解成更简单的糖)
二糖(1mol水解产生2mol单糖)
多糖(1mol水解产生多摩单糖)
-葡萄糖、果糖
-麦芽糖、蔗糖
-淀粉、纤维素
[阅读课本]思考下列问题:
一、葡萄糖与果糖
根据下列信息推出葡萄糖的分子组成
葡萄糖的相对分子质量为180,其中
含碳40%,氢6.7%,其余是氧。求分子
式。
葡萄糖分子式:C6H12O6
1、葡萄糖
白色晶体、有甜味、能溶于水
(1)物理性质
根据下列信息推出葡萄糖的分子结构:
1、在一定条件下,1mol葡萄糖与1molH2反应,还原成己六醇
2、 葡萄糖能发生酯化反应生成五乙酸葡萄糖(提示:同一个C原子上连接2个羟基不稳定)
3、 葡萄糖分子被氧化,碳链并不断裂,而是生含6个C原子的葡萄糖酸
说明分子中有双键,也说明是直链化合物
说明葡萄糖分子中有5个—OH,且分别连在5个C原子上
说明葡萄糖分子中含有一个—CHO
科学推理:
分子式:C6H12O6
(2)结构
结构简式:
CH2 CH CH CH CH CHO
OH
OH
OH
OH
OH
预测:葡萄糖的化学性质
1、葡萄糖
(3)化学性质:
银镜反应
与新制Cu(OH)2反应
与H2加成
② 羟基的性质:
③ 人体内氧化反应-人体能量主要来源:
C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l)
①醛基的性质:
(4)用途
制药、制镜、制糖果
酯化
葡萄糖的性质
CH2OH(CHOH)4CHO + H2
CH2OH(CHOH)4CH2OH
催化剂
CH2OH(CHOH)4CHO+2 Ag(NH3)2OH
2Ag +CH2OH(CHOH)4COOH+4NH3 +H2O
CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+Cu2O +2H2O
2、果糖:
分子式:C6H12O6
结构简式:
CH2OHCHOHCHOHCHOHCOCH2OH
多羟基酮,是葡萄糖的同分异构体。
在碱性条件下,果糖分子中羰基受多个羟基的影响有很强的还原性,所以果糖能被银氨溶液和新制氢氧化铜氧化。
在酸性条件下,果糖不被溴水氧化,可用溴水区分葡萄糖和果糖。
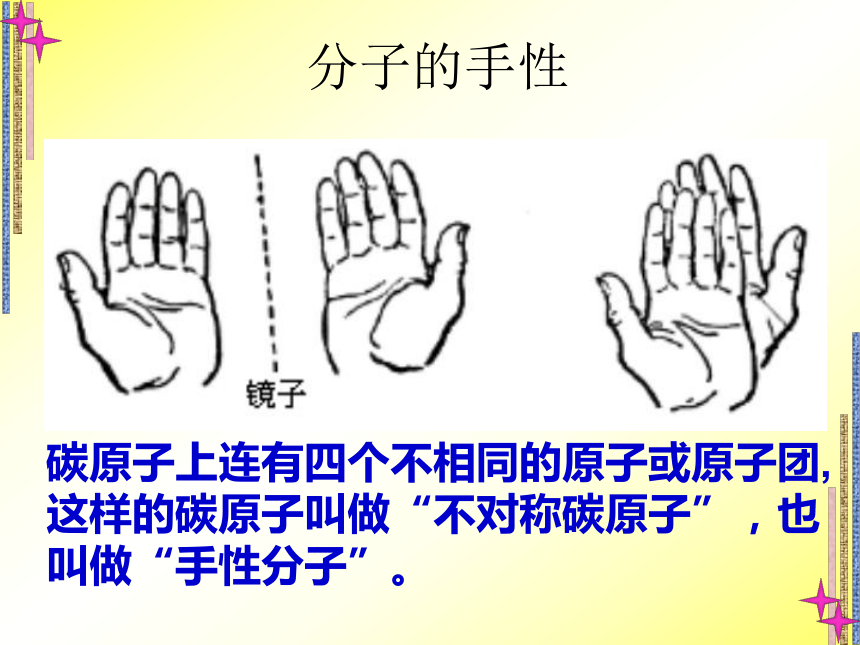
分子的手性
碳原子上连有四个不相同的原子或原子团,这样的碳原子叫做“不对称碳原子”,也叫做“手性分子”。
二、蔗糖 麦芽糖:
演示对比实验:
银氨溶液
银氨溶液
热水浴
热水浴
无现象
产生
银镜
热水浴
热水浴
20%蔗
糖溶液
20%麦芽糖溶液
无还原性
有还原性
蔗糖:
麦芽糖:
化学性质:
同分异构
演示对比实验:
热水浴
20%蔗
糖溶液
银氨溶液
热水浴
无现象
蔗糖 +
稀硫酸
热水浴
NaOH
中和酸
银氨溶液
热水浴
产生
银镜
C6H12O6 + C6H12O6
(葡萄糖) (果糖)
催化剂
C12H22O11 + H2O
(蔗糖)
二、蔗糖 麦芽糖:
二、蔗糖 麦芽糖:
●蔗糖与麦芽糖的比较:
蔗糖 C12H22O11
同分异构 非还原性糖
(无-CHO) 水解成一分子葡萄糖,一分子果糖 二糖
麦芽糖 还原性糖
(有-CHO) 水解成二分子葡萄糖 二糖
C12H22O11 + H2O 2 C6H12O6
(麦芽糖) (葡萄糖)
催化剂
三.淀粉与纤维素
1.淀粉
存在:存在于植物的种子和块根里。
结构:含有几百到几千个单糖单元(C6H10O5)。每个结构单元式量:162。相对分子质量从几万到几十万;属于天然有机高分子化合物
物质性质:白色、无气味、无味道的粉末状物质,不溶于冷水,在热水中产生糊化作用(即食物由生变熟的过程)
淀粉的化学性质
①通常淀粉不显还原性
②遇碘变蓝色
③淀粉在催化剂(如酸)存在和加热下可以逐步水解,生成一系列比淀粉分子小的化合物,最终生成还原性糖:葡萄糖。
(C6H10O5)n + n H2O n C6H12O6
淀粉 葡萄糖
催化剂
思考:解释为什么在吃馒头或米饭时,多加咀嚼就会感到有甜味?
答:淀粉在人体内进行水解。人在咀嚼馒头时,淀粉受唾液所含淀粉酶(一种蛋白质)的催化作用,开始水解,生成了一部分葡萄糖。
(淀粉在小肠里,在胰脏分泌出的淀粉酶的作用下,继续进行水解。生成的葡萄糖经过肠壁的吸收,进入血液,供人体组织的营养需要。)
淀粉的用途
(1)淀粉是食物的重要成分,是人体的重要能源;
(2)可用于制葡萄糖和酒精等;
(3)淀粉在淀粉酶的作用下,先转化为麦芽糖,再转化为葡萄糖,在酒化酶的作用下,转化为乙醇:
C6H12O6 2C2H5OH +2 CO2
催化剂
三.淀粉和纤维素
2.纤维素
存在:纤维素存在于一切植物中。是构成植物细胞壁的基础物质。
结构:分子中含有约几千个单糖单元(C6H10O5)n ;n为几千;属于天然高分子化合物;纤维素结构与淀粉不同,所以性质有差异。
纤维素的化学性质
不显还原性
可发生水解,但比淀粉水解困难
(C6H10H5)n + nH2O nC6H12O6(葡萄糖)
酯化反应
催化剂
△
纤维素的酯化反应
(C6H7O2)
O—NO2
O—NO2
O—NO2
n
(C6H7O2)
OH
OH
OH
n
3n HNO3
浓硫酸
3nH2O
+
+
纤维素硝酸酯
(硝酸纤维)
思考:如何设计实验检验纤维素水解已经开始?
答案:
取少量反应液,滴加几滴硫酸铜溶液,再加入过量的NaOH溶液,中和作催化剂的硫酸,一直加到出现Cu(OH)2沉淀,最后,加热煮沸,观察现象。如果出现红色沉淀,表明已经开始水解。
5.纤维素的用途
1、棉麻纤维大量用于纺织工业
2、木材、稻草、麦秸、蔗渣等用于造纸
3、制造纤维素硝酸酯(硝酸纤维)。根据含N量分为火棉(含N量较高,用于制造无烟火药)、胶棉(含N量较低,用于制赛璐璐和油漆)
4、制造纤维素乙酸酯(醋酸纤维),不易着火,用于制胶片
5、制造粘胶纤维(NaOH、CS2处理后所得,其中的长纤维称人造丝,短纤维称人造棉)
6、食物中的纤维素有利于人的消化。
糖的概念
具有多羟基醛或多羟基酮结构,以及能够水解生成它们的一类有机化合物叫做糖类,旧称碳水化合物,通式为Cm(H2O)n
分类及相互转化
低聚糖
单糖
多糖
水解
缩合
水解
缩聚
水解
缩合
(2~10)
( >10)
练一练:
1、下列物质具有相同的最简式的组是( )
A、乙醛 葡萄糖 B、乙酸 乙醛
C、乙醇 葡萄糖 D、甲酸甲酯 葡萄糖
2、葡萄糖所不具有的性质是( )
A、和H2发生加成反应
B、和银氨溶液发生氧化反应
C、和酸发生酯化反应
D、和NaOH溶液反应
D
D
第 二 节
糖 类
一、糖类具有怎样的特征?
绿色植物光合反应的产物
由C、H、O元素组成
常用通式Cn(H2O)m来表示
二、糖类如何分类?
单糖(不能水解成更简单的糖)
二糖(1mol水解产生2mol单糖)
多糖(1mol水解产生多摩单糖)
-葡萄糖、果糖
-麦芽糖、蔗糖
-淀粉、纤维素
[阅读课本]思考下列问题:
一、葡萄糖与果糖
根据下列信息推出葡萄糖的分子组成
葡萄糖的相对分子质量为180,其中
含碳40%,氢6.7%,其余是氧。求分子
式。
葡萄糖分子式:C6H12O6
1、葡萄糖
白色晶体、有甜味、能溶于水
(1)物理性质
根据下列信息推出葡萄糖的分子结构:
1、在一定条件下,1mol葡萄糖与1molH2反应,还原成己六醇
2、 葡萄糖能发生酯化反应生成五乙酸葡萄糖(提示:同一个C原子上连接2个羟基不稳定)
3、 葡萄糖分子被氧化,碳链并不断裂,而是生含6个C原子的葡萄糖酸
说明分子中有双键,也说明是直链化合物
说明葡萄糖分子中有5个—OH,且分别连在5个C原子上
说明葡萄糖分子中含有一个—CHO
科学推理:
分子式:C6H12O6
(2)结构
结构简式:
CH2 CH CH CH CH CHO
OH
OH
OH
OH
OH
预测:葡萄糖的化学性质
1、葡萄糖
(3)化学性质:
银镜反应
与新制Cu(OH)2反应
与H2加成
② 羟基的性质:
③ 人体内氧化反应-人体能量主要来源:
C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l)
①醛基的性质:
(4)用途
制药、制镜、制糖果
酯化
葡萄糖的性质
CH2OH(CHOH)4CHO + H2
CH2OH(CHOH)4CH2OH
催化剂
CH2OH(CHOH)4CHO+2 Ag(NH3)2OH
2Ag +CH2OH(CHOH)4COOH+4NH3 +H2O
CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+Cu2O +2H2O
2、果糖:
分子式:C6H12O6
结构简式:
CH2OHCHOHCHOHCHOHCOCH2OH
多羟基酮,是葡萄糖的同分异构体。
在碱性条件下,果糖分子中羰基受多个羟基的影响有很强的还原性,所以果糖能被银氨溶液和新制氢氧化铜氧化。
在酸性条件下,果糖不被溴水氧化,可用溴水区分葡萄糖和果糖。
分子的手性
碳原子上连有四个不相同的原子或原子团,这样的碳原子叫做“不对称碳原子”,也叫做“手性分子”。
二、蔗糖 麦芽糖:
演示对比实验:
银氨溶液
银氨溶液
热水浴
热水浴
无现象
产生
银镜
热水浴
热水浴
20%蔗
糖溶液
20%麦芽糖溶液
无还原性
有还原性
蔗糖:
麦芽糖:
化学性质:
同分异构
演示对比实验:
热水浴
20%蔗
糖溶液
银氨溶液
热水浴
无现象
蔗糖 +
稀硫酸
热水浴
NaOH
中和酸
银氨溶液
热水浴
产生
银镜
C6H12O6 + C6H12O6
(葡萄糖) (果糖)
催化剂
C12H22O11 + H2O
(蔗糖)
二、蔗糖 麦芽糖:
二、蔗糖 麦芽糖:
●蔗糖与麦芽糖的比较:
蔗糖 C12H22O11
同分异构 非还原性糖
(无-CHO) 水解成一分子葡萄糖,一分子果糖 二糖
麦芽糖 还原性糖
(有-CHO) 水解成二分子葡萄糖 二糖
C12H22O11 + H2O 2 C6H12O6
(麦芽糖) (葡萄糖)
催化剂
三.淀粉与纤维素
1.淀粉
存在:存在于植物的种子和块根里。
结构:含有几百到几千个单糖单元(C6H10O5)。每个结构单元式量:162。相对分子质量从几万到几十万;属于天然有机高分子化合物
物质性质:白色、无气味、无味道的粉末状物质,不溶于冷水,在热水中产生糊化作用(即食物由生变熟的过程)
淀粉的化学性质
①通常淀粉不显还原性
②遇碘变蓝色
③淀粉在催化剂(如酸)存在和加热下可以逐步水解,生成一系列比淀粉分子小的化合物,最终生成还原性糖:葡萄糖。
(C6H10O5)n + n H2O n C6H12O6
淀粉 葡萄糖
催化剂
思考:解释为什么在吃馒头或米饭时,多加咀嚼就会感到有甜味?
答:淀粉在人体内进行水解。人在咀嚼馒头时,淀粉受唾液所含淀粉酶(一种蛋白质)的催化作用,开始水解,生成了一部分葡萄糖。
(淀粉在小肠里,在胰脏分泌出的淀粉酶的作用下,继续进行水解。生成的葡萄糖经过肠壁的吸收,进入血液,供人体组织的营养需要。)
淀粉的用途
(1)淀粉是食物的重要成分,是人体的重要能源;
(2)可用于制葡萄糖和酒精等;
(3)淀粉在淀粉酶的作用下,先转化为麦芽糖,再转化为葡萄糖,在酒化酶的作用下,转化为乙醇:
C6H12O6 2C2H5OH +2 CO2
催化剂
三.淀粉和纤维素
2.纤维素
存在:纤维素存在于一切植物中。是构成植物细胞壁的基础物质。
结构:分子中含有约几千个单糖单元(C6H10O5)n ;n为几千;属于天然高分子化合物;纤维素结构与淀粉不同,所以性质有差异。
纤维素的化学性质
不显还原性
可发生水解,但比淀粉水解困难
(C6H10H5)n + nH2O nC6H12O6(葡萄糖)
酯化反应
催化剂
△
纤维素的酯化反应
(C6H7O2)
O—NO2
O—NO2
O—NO2
n
(C6H7O2)
OH
OH
OH
n
3n HNO3
浓硫酸
3nH2O
+
+
纤维素硝酸酯
(硝酸纤维)
思考:如何设计实验检验纤维素水解已经开始?
答案:
取少量反应液,滴加几滴硫酸铜溶液,再加入过量的NaOH溶液,中和作催化剂的硫酸,一直加到出现Cu(OH)2沉淀,最后,加热煮沸,观察现象。如果出现红色沉淀,表明已经开始水解。
5.纤维素的用途
1、棉麻纤维大量用于纺织工业
2、木材、稻草、麦秸、蔗渣等用于造纸
3、制造纤维素硝酸酯(硝酸纤维)。根据含N量分为火棉(含N量较高,用于制造无烟火药)、胶棉(含N量较低,用于制赛璐璐和油漆)
4、制造纤维素乙酸酯(醋酸纤维),不易着火,用于制胶片
5、制造粘胶纤维(NaOH、CS2处理后所得,其中的长纤维称人造丝,短纤维称人造棉)
6、食物中的纤维素有利于人的消化。
糖的概念
具有多羟基醛或多羟基酮结构,以及能够水解生成它们的一类有机化合物叫做糖类,旧称碳水化合物,通式为Cm(H2O)n
分类及相互转化
低聚糖
单糖
多糖
水解
缩合
水解
缩聚
水解
缩合
(2~10)
( >10)
练一练:
1、下列物质具有相同的最简式的组是( )
A、乙醛 葡萄糖 B、乙酸 乙醛
C、乙醇 葡萄糖 D、甲酸甲酯 葡萄糖
2、葡萄糖所不具有的性质是( )
A、和H2发生加成反应
B、和银氨溶液发生氧化反应
C、和酸发生酯化反应
D、和NaOH溶液反应
D
D
