2020-2021学年高中化学新人教版选择性必修1 第二章第二节 化学平衡(第2课时) 课件(29张)
文档属性
| 名称 | 2020-2021学年高中化学新人教版选择性必修1 第二章第二节 化学平衡(第2课时) 课件(29张) |  | |
| 格式 | pptx | ||
| 文件大小 | 2.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-04-28 16:16:00 | ||
图片预览











文档简介
人教(2019)版 选择性必修一
第二章 化学反应速率与化学平衡
第二节 化学平衡
第2课时 化学平衡常数及转化率
第二章 化学反应速率与化学平衡
第二节 化学平衡
第2课时 化学平衡常数及转化率
1.知道化学平衡常数的含义。
2.能书写平衡常数表达式,能进行化学平衡常数、转化率的简单计算。
3.通过化学平衡常数对化学平衡进行“定量”计算和判断化学平衡进行的程度及平衡移动方向。
课程目标
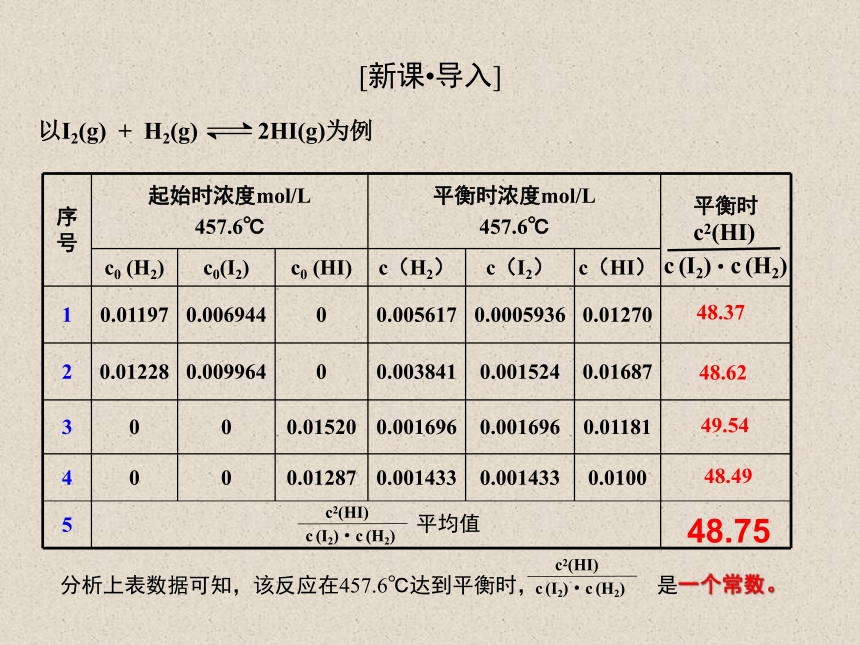
[新课?导入]
以I2(g) + H2(g) 2HI(g)为例
序号
起始时浓度mol/L
457.6℃
平衡时浓度mol/L
457.6℃
平衡时
c0 (H2)
c0(I2)
c0 (HI)
c(H2)
c(I2)
c(HI)
1
0.01197
0.006944
0
0.005617
0.0005936
0.01270
2
0.01228
0.009964
0
0.003841
0.001524
0.01687
3
0
0
0.01520
0.001696
0.001696
0.01181
4
0
0
0.01287
0.001433
0.001433
0.0100
5
c (I2)·c (H2)
c2(HI)
48.37
48.62
49.54
48.49
c (I2)·c (H2)
c2(HI)
平均值
48.75
分析上表数据可知,该反应在457.6℃达到平衡时, 是一个常数。
c (I2)·c (H2)
c2(HI)
一、化学平衡常数
[基础?初探]
(1)概念:对于一般的可逆反应,如 ,在任意时
刻的 称为浓度商,常用Q表示。
(2)使用范围:任意时刻的可逆反应(固体或液体纯物质一般不列入浓度商)
(3)表示方法:
1、浓度商
[基础?初探]
(2)使用范围:平衡时的可逆反应(固体或液体纯物质一般不列入平衡常数)
(3)表示方法:
(4)单位:K的单位为 , ,一般省略不写。
2、平衡常数
化学平衡
生成物浓度幂之积
反应物浓度幂之积
例如: ,
若写成 ,则 ;
若写成 ,则 ;
若写成 ,则 。
?名师点拨
书写时要注意以下三点:
(1)物质的浓度是指平衡时的物质的量浓度。
(2)反应物或生成物中有固体或纯液体存在时,由于其浓度可看作“1”而不代入表达式。
(3)化学平衡常数是指某一具体反应的平衡常数。若反应方向改变、化学计量数等倍扩大或缩小,化学平衡常数都会相应改变。
[课堂?专练]
[课堂?专练]
[基础?初探]
(5)影响因素:
①平衡常数K只受 影响。随温度的变化而变化,与反应物或生成物的浓度无关,也与反应是从正向开始还是从逆向开始无关。
②对于正反应是 的可逆反应, 温度,平衡右移,K值变 ;降低温度,平衡左移,K值变小。
对于正反应是 的可逆反应, 温度,平衡左移,K值变 ;降低温度,平衡右移,K值变大。
温度
吸热反应
升高
大
放热反应
升高
小
[课堂?专练]
×
×
×
×
[课堂?专练]
[课堂?专练]
[基础?初探]
(6)意义
K值越大→平衡体系中生成物所占的比例 →正向反应进行的程度 →反应进行得越 →反应物的转化率 :反之,就越不完全,转化率就越小。当 时,该反应进行得就基本完全了。当 时,认为该反应很难进行。
越大
越大
完全
越大
K>105
K<105
(7)应用
①判断反应进行的程度
K值越大,说明平衡体系中生成物所占的比例越大,正向反应进行的程度越大,即该反应进行得越完全,反应物转化率越大;反之,就越不完全,转化率就越小。
②若升高温度,K值增大,则正反应为吸热反应;若升高温度,K值减小,则正反应为放热反应。
③判断平衡移动方向
利用平衡常数可从定量的角度解释恒温下浓度、压强对化学平衡移动的影响。
当Q=K时,反应处于 状态,v正=v逆;
当Qv逆;
当Q>K时,反应向 方向进行,v正[基础?初探]
平衡
正反应
逆反应
④用于计算平衡浓度、物质的量分数、转化率等
[课堂?专练]
[课堂?专练]
[课堂?专练]
[课堂?专练]
二、平衡转化率
[基础?初探]
1、概念
平衡转化率是指平衡时 了的某反应物的量与 该反应物的量之比,用来表示反应限度。
2、表达式
已转化
起始时
[课堂?专练]
[课堂?专练]
[课堂?专练]
[课堂?专练]
[课堂?专练]
[课堂?专练]
[拓展?延伸]
压强平衡常数(Kp)
对于有气体参与的反应,用某气体(B)的平衡压强(pB)代替物质的量浓度(cB)也可表示平衡常数。如反应:
Thank you for watching !
本部分内容讲解结束
https://www.21cnjy.com/help/help_extract.php
第二章 化学反应速率与化学平衡
第二节 化学平衡
第2课时 化学平衡常数及转化率
第二章 化学反应速率与化学平衡
第二节 化学平衡
第2课时 化学平衡常数及转化率
1.知道化学平衡常数的含义。
2.能书写平衡常数表达式,能进行化学平衡常数、转化率的简单计算。
3.通过化学平衡常数对化学平衡进行“定量”计算和判断化学平衡进行的程度及平衡移动方向。
课程目标
[新课?导入]
以I2(g) + H2(g) 2HI(g)为例
序号
起始时浓度mol/L
457.6℃
平衡时浓度mol/L
457.6℃
平衡时
c0 (H2)
c0(I2)
c0 (HI)
c(H2)
c(I2)
c(HI)
1
0.01197
0.006944
0
0.005617
0.0005936
0.01270
2
0.01228
0.009964
0
0.003841
0.001524
0.01687
3
0
0
0.01520
0.001696
0.001696
0.01181
4
0
0
0.01287
0.001433
0.001433
0.0100
5
c (I2)·c (H2)
c2(HI)
48.37
48.62
49.54
48.49
c (I2)·c (H2)
c2(HI)
平均值
48.75
分析上表数据可知,该反应在457.6℃达到平衡时, 是一个常数。
c (I2)·c (H2)
c2(HI)
一、化学平衡常数
[基础?初探]
(1)概念:对于一般的可逆反应,如 ,在任意时
刻的 称为浓度商,常用Q表示。
(2)使用范围:任意时刻的可逆反应(固体或液体纯物质一般不列入浓度商)
(3)表示方法:
1、浓度商
[基础?初探]
(2)使用范围:平衡时的可逆反应(固体或液体纯物质一般不列入平衡常数)
(3)表示方法:
(4)单位:K的单位为 , ,一般省略不写。
2、平衡常数
化学平衡
生成物浓度幂之积
反应物浓度幂之积
例如: ,
若写成 ,则 ;
若写成 ,则 ;
若写成 ,则 。
?名师点拨
书写时要注意以下三点:
(1)物质的浓度是指平衡时的物质的量浓度。
(2)反应物或生成物中有固体或纯液体存在时,由于其浓度可看作“1”而不代入表达式。
(3)化学平衡常数是指某一具体反应的平衡常数。若反应方向改变、化学计量数等倍扩大或缩小,化学平衡常数都会相应改变。
[课堂?专练]
[课堂?专练]
[基础?初探]
(5)影响因素:
①平衡常数K只受 影响。随温度的变化而变化,与反应物或生成物的浓度无关,也与反应是从正向开始还是从逆向开始无关。
②对于正反应是 的可逆反应, 温度,平衡右移,K值变 ;降低温度,平衡左移,K值变小。
对于正反应是 的可逆反应, 温度,平衡左移,K值变 ;降低温度,平衡右移,K值变大。
温度
吸热反应
升高
大
放热反应
升高
小
[课堂?专练]
×
×
×
×
[课堂?专练]
[课堂?专练]
[基础?初探]
(6)意义
K值越大→平衡体系中生成物所占的比例 →正向反应进行的程度 →反应进行得越 →反应物的转化率 :反之,就越不完全,转化率就越小。当 时,该反应进行得就基本完全了。当 时,认为该反应很难进行。
越大
越大
完全
越大
K>105
K<105
(7)应用
①判断反应进行的程度
K值越大,说明平衡体系中生成物所占的比例越大,正向反应进行的程度越大,即该反应进行得越完全,反应物转化率越大;反之,就越不完全,转化率就越小。
②若升高温度,K值增大,则正反应为吸热反应;若升高温度,K值减小,则正反应为放热反应。
③判断平衡移动方向
利用平衡常数可从定量的角度解释恒温下浓度、压强对化学平衡移动的影响。
当Q=K时,反应处于 状态,v正=v逆;
当Q
当Q>K时,反应向 方向进行,v正
平衡
正反应
逆反应
④用于计算平衡浓度、物质的量分数、转化率等
[课堂?专练]
[课堂?专练]
[课堂?专练]
[课堂?专练]
二、平衡转化率
[基础?初探]
1、概念
平衡转化率是指平衡时 了的某反应物的量与 该反应物的量之比,用来表示反应限度。
2、表达式
已转化
起始时
[课堂?专练]
[课堂?专练]
[课堂?专练]
[课堂?专练]
[课堂?专练]
[课堂?专练]
[拓展?延伸]
压强平衡常数(Kp)
对于有气体参与的反应,用某气体(B)的平衡压强(pB)代替物质的量浓度(cB)也可表示平衡常数。如反应:
Thank you for watching !
本部分内容讲解结束
https://www.21cnjy.com/help/help_extract.php
