人教版(五四学制)化学九年级全册 第二单元 课题1 溶液的形成 第一课时课件(共17张PPT)
文档属性
| 名称 | 人教版(五四学制)化学九年级全册 第二单元 课题1 溶液的形成 第一课时课件(共17张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 561.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-02 00:00:00 | ||
图片预览






文档简介
溶液的形成
1.了解溶液的概念,认识溶液的本质特征。
2.知道物质在溶解过程中通常伴随着热量变化。
3.知道一些常见的乳化现象。
教学目标
1.建立溶液的概念,并认识溶液、溶质、溶剂之间的关系。
2.乳化现象及其应用。
3.溶解过程的吸热和放热现象及其理解。
教学重点和难点
什么是溶液,溶液的形成
在日常生活中,把一些糖或盐放入适量水中,充分溶解,过一会儿,放进水中的糖或盐就不见了,我们就得到了澄清的糖水或盐水。糖水、盐水以及在医疗上用的生理盐水、眼药水都是溶液,那么纯水是溶液吗?
教材(P27)一种或几种物质分散到另一种物质里,形成 的、 的混合物叫做溶液。
溶液的形成
均一
稳定
均一性:
稳定性:
只要外界条件不改变(如温度、水分不蒸发等)时,就不会发生下沉、上浮等变化(不分离)。
指溶液各处完全一样(指密度、浓度、组成、性质等)。
1、溶液一定是均一、稳定的,但均一、稳定的液体不一定是溶液,如水、酒精。
2、溶液是澄清、透明的,但不一定是无色的;
如: 溶液是 色的;
硫酸铜
3、一种溶液中只有一种溶剂,但不一定只有一种溶质,可以有多种溶质。
蓝
注意:
溶质
溶剂
溶液是由 和 组成的
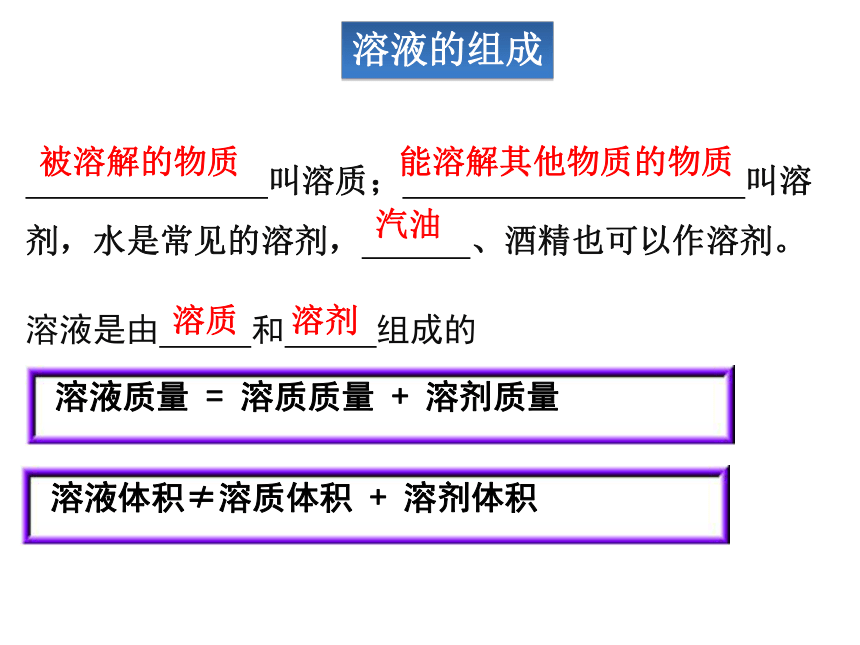
溶液的组成
溶液质量 = 溶质质量 + 溶剂质量
溶液体积≠溶质体积 + 溶剂体积
叫溶质; 叫溶剂,水是常见的溶剂, 、酒精也可以作溶剂。
被溶解的物质
能溶解其他物质的物质
汽油
探究实验:碘和高锰酸钾的溶解性比较
(实验9-2)
分析:由(1)(2)可知,同种溶质在不同种溶剂中的溶解能力不相同;由(1)(3)可知,不同溶质在同种溶剂中的溶解能力也不相同。
物质的溶解能力(溶解性)与溶质和溶剂的种类有关。
探究实验:乙醇能溶解在水中
(实验9-3)
溶剂
溶质
振荡前现象
振荡后现象
静置后现象
结论
水
乙醇
溶解
分层
溶解
水和乙醇能互溶
溶质可以是固体、 体或 体;
气
液
溶液的命名
(溶质)的(溶剂)溶液
溶剂是水的时候可以省略不说
溶剂的确定
①水为溶剂
②液体为溶剂
③量多为溶剂
分别指出下列各溶液里的溶质和溶剂:
溶液
溶质
溶剂
高锰酸钾溶液
碘酒
硫酸铜溶液
石灰水
质量分数为
75%的酒精溶液
碘
酒精
硫酸铜
水
氢氧化钙
水
酒精
水
高锰酸钾
水
溶液的应用
溶解时的吸热或放热现象
通过以上探究实验可以看出:有的物质溶于水会吸热(如硝酸铵);有的物质溶于水会放出热量(如氢氧化钠);有的物质溶于水,溶液的温度基本不变(如氯化钠)。
2.乳化现象:洗涤剂将大油滴分散成小油滴,均匀地分散在水中的现象叫乳化现象。
洗涤剂所起的作用叫乳化作用。
乳化现象
试管内加
入的物质
现象
用水冲洗后的
试管是否干净
振荡前
振荡后
静置后
水和植物油
溶液
分层
得到乳状
浑浊液体
溶液
分层
不干净
水和植物油
及洗涤剂
溶液
分层
得到乳状
浑浊液体
溶液不
分层
干净
课堂小结
1.一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物就是溶液。能溶解其他物质的物质叫做溶剂;被溶解的物质叫做溶质。溶液有广泛的用途。
2.溶质在溶解过程中,有的放出热量,有的吸收热量。
3.小液滴分散到液体里形成的混合物叫做乳浊液。
1、将下列物质分别放入水中,不能形成溶液的是( )
A.食用油 B. 酒精 C. 食盐 D.蔗糖
2、下列关于溶液特征的叙述中不正确的是( )
A.溶液都是澄清、透明、无色的
B.当外界条件不变时,溶液长期放置溶质不会从溶液里分离出来
C.一种溶液中各部分的浓稀和性质都是一致的。
D. 溶液是均一、稳定的混合物
3、某同学喝一杯糖开水,第一口与第二口“甜度”相同,这说明溶液是( )
A.混合物 B.澄精的 C.均一的 D.稳定的
课堂练习
A
A
C
4、某一杯食盐水, 若上部的密度为1.1g/cm3,则下部的密度是( )
A.大于1.1g/cm3 B. 等于1.1g/cm3
C.小于1.1g/cm3 D.无法判断
5、病人在医院接受静脉注射或滴注时,常用到生理盐水即氯化钠注射液,请回答:
(1)该注射液里的溶质是 _______:
(2)常温下,一瓶合格的氯化钠注射液密封放置一
段时间后,是否会出现浑浊现象?为什么?
氯化钠
不会,因为外界条件没有发生变化,溶液具有均一、稳定性。
B
6、某液体若是溶液,必须具备的条件是( )
A.某一固体物质溶解到另一种溶液里
B.至少有两种物质存在,并形成均一、稳定的体系
C.长时间敞口放置,不会有固体物质析出
D.以上均不是
7、把少量的白磷溶于二硫化碳中制成溶液,其中____ 是溶质,_________ 是溶剂.这种溶液叫做_______的__________溶液。碘酒中,___是溶剂,酒精溶液中,酒精是______。
8、用汽油或加了洗涤剂的水都能除去衣服上的油污。试分析二者的原理是否相同。
B
白磷
二硫化碳
白磷
二硫化碳
酒精
溶质
1.了解溶液的概念,认识溶液的本质特征。
2.知道物质在溶解过程中通常伴随着热量变化。
3.知道一些常见的乳化现象。
教学目标
1.建立溶液的概念,并认识溶液、溶质、溶剂之间的关系。
2.乳化现象及其应用。
3.溶解过程的吸热和放热现象及其理解。
教学重点和难点
什么是溶液,溶液的形成
在日常生活中,把一些糖或盐放入适量水中,充分溶解,过一会儿,放进水中的糖或盐就不见了,我们就得到了澄清的糖水或盐水。糖水、盐水以及在医疗上用的生理盐水、眼药水都是溶液,那么纯水是溶液吗?
教材(P27)一种或几种物质分散到另一种物质里,形成 的、 的混合物叫做溶液。
溶液的形成
均一
稳定
均一性:
稳定性:
只要外界条件不改变(如温度、水分不蒸发等)时,就不会发生下沉、上浮等变化(不分离)。
指溶液各处完全一样(指密度、浓度、组成、性质等)。
1、溶液一定是均一、稳定的,但均一、稳定的液体不一定是溶液,如水、酒精。
2、溶液是澄清、透明的,但不一定是无色的;
如: 溶液是 色的;
硫酸铜
3、一种溶液中只有一种溶剂,但不一定只有一种溶质,可以有多种溶质。
蓝
注意:
溶质
溶剂
溶液是由 和 组成的
溶液的组成
溶液质量 = 溶质质量 + 溶剂质量
溶液体积≠溶质体积 + 溶剂体积
叫溶质; 叫溶剂,水是常见的溶剂, 、酒精也可以作溶剂。
被溶解的物质
能溶解其他物质的物质
汽油
探究实验:碘和高锰酸钾的溶解性比较
(实验9-2)
分析:由(1)(2)可知,同种溶质在不同种溶剂中的溶解能力不相同;由(1)(3)可知,不同溶质在同种溶剂中的溶解能力也不相同。
物质的溶解能力(溶解性)与溶质和溶剂的种类有关。
探究实验:乙醇能溶解在水中
(实验9-3)
溶剂
溶质
振荡前现象
振荡后现象
静置后现象
结论
水
乙醇
溶解
分层
溶解
水和乙醇能互溶
溶质可以是固体、 体或 体;
气
液
溶液的命名
(溶质)的(溶剂)溶液
溶剂是水的时候可以省略不说
溶剂的确定
①水为溶剂
②液体为溶剂
③量多为溶剂
分别指出下列各溶液里的溶质和溶剂:
溶液
溶质
溶剂
高锰酸钾溶液
碘酒
硫酸铜溶液
石灰水
质量分数为
75%的酒精溶液
碘
酒精
硫酸铜
水
氢氧化钙
水
酒精
水
高锰酸钾
水
溶液的应用
溶解时的吸热或放热现象
通过以上探究实验可以看出:有的物质溶于水会吸热(如硝酸铵);有的物质溶于水会放出热量(如氢氧化钠);有的物质溶于水,溶液的温度基本不变(如氯化钠)。
2.乳化现象:洗涤剂将大油滴分散成小油滴,均匀地分散在水中的现象叫乳化现象。
洗涤剂所起的作用叫乳化作用。
乳化现象
试管内加
入的物质
现象
用水冲洗后的
试管是否干净
振荡前
振荡后
静置后
水和植物油
溶液
分层
得到乳状
浑浊液体
溶液
分层
不干净
水和植物油
及洗涤剂
溶液
分层
得到乳状
浑浊液体
溶液不
分层
干净
课堂小结
1.一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物就是溶液。能溶解其他物质的物质叫做溶剂;被溶解的物质叫做溶质。溶液有广泛的用途。
2.溶质在溶解过程中,有的放出热量,有的吸收热量。
3.小液滴分散到液体里形成的混合物叫做乳浊液。
1、将下列物质分别放入水中,不能形成溶液的是( )
A.食用油 B. 酒精 C. 食盐 D.蔗糖
2、下列关于溶液特征的叙述中不正确的是( )
A.溶液都是澄清、透明、无色的
B.当外界条件不变时,溶液长期放置溶质不会从溶液里分离出来
C.一种溶液中各部分的浓稀和性质都是一致的。
D. 溶液是均一、稳定的混合物
3、某同学喝一杯糖开水,第一口与第二口“甜度”相同,这说明溶液是( )
A.混合物 B.澄精的 C.均一的 D.稳定的
课堂练习
A
A
C
4、某一杯食盐水, 若上部的密度为1.1g/cm3,则下部的密度是( )
A.大于1.1g/cm3 B. 等于1.1g/cm3
C.小于1.1g/cm3 D.无法判断
5、病人在医院接受静脉注射或滴注时,常用到生理盐水即氯化钠注射液,请回答:
(1)该注射液里的溶质是 _______:
(2)常温下,一瓶合格的氯化钠注射液密封放置一
段时间后,是否会出现浑浊现象?为什么?
氯化钠
不会,因为外界条件没有发生变化,溶液具有均一、稳定性。
B
6、某液体若是溶液,必须具备的条件是( )
A.某一固体物质溶解到另一种溶液里
B.至少有两种物质存在,并形成均一、稳定的体系
C.长时间敞口放置,不会有固体物质析出
D.以上均不是
7、把少量的白磷溶于二硫化碳中制成溶液,其中____ 是溶质,_________ 是溶剂.这种溶液叫做_______的__________溶液。碘酒中,___是溶剂,酒精溶液中,酒精是______。
8、用汽油或加了洗涤剂的水都能除去衣服上的油污。试分析二者的原理是否相同。
B
白磷
二硫化碳
白磷
二硫化碳
酒精
溶质
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
