6.2.3 盐和肥料——常见盐的化学性质 教学设计
文档属性
| 名称 | 6.2.3 盐和肥料——常见盐的化学性质 教学设计 |

|
|
| 格式 | docx | ||
| 文件大小 | 24.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-06 00:00:00 | ||
图片预览

文档简介
《常见盐的化学性质》教学设计
一、教材分析
本节课是上教版教材第二学期第六章第二节第三课时内容,在教学基本要求中常见盐的性质属于B级学,虽然只要求知道氯化钠和硝酸银、碳酸钠与盐酸、硫酸、氢氧化钙的反应,但是因为这些知识点还要应用到物质的检验和鉴别上,因此学要求较高。在第五章酸和碱的学习中已经略有涉及酸与盐溶液、碱与盐溶液的反应,因此本节课想通过最常见盐的化学性质引出物质的简单检验和鉴别。此外,本课通过提出问题,初步引导学生根据探究目的涉及并优化实验方案;通过讨论,进一步改进实验设想,培养学生科学探究的化学学科核心素养。
二、学情分析
学生对酸和碱已经有一定的认识,食盐和纯碱又是生活中最常见的盐,也了解了一些盐的化学性质,与生活中实际联系起来,学习热情比较高。此外,进过一学期的学习,学生也逐步形成了一定的化学学习思维,有一定的观察、操作、理解及分析能力。但是,对于物质的检验和鉴别还没有系统化地归纳过。
另外,本节课的教学对象是九(1)班的学生,整个班级的整体水平还不错,但仍有个别基础较薄弱的学生。因此,本节课采用对分课堂的教学模式,在学生分组时充分考虑不同学生的学习程度,在课堂提问和评价时的要求也有所不同。
三、教学目标
1、知道氯化钠与硝酸银、碳酸钠与盐酸、硫酸、氢氧化钙的反应,并描述现象和书写化学方程式。
2、知道食盐和纯碱常用的化学性质。
3、知道物质的性质决定了物质的用途,物质的用途又反映了物质的性质。
4、通过内化、讨论等方式设计并优化实验方案,完成氯化钠和碳酸钠的检验和鉴别。
四、教学重、难点
重点:氯化钠和碳酸钠的化学性质
难点:氯化钠和碳酸钠的检验和鉴别
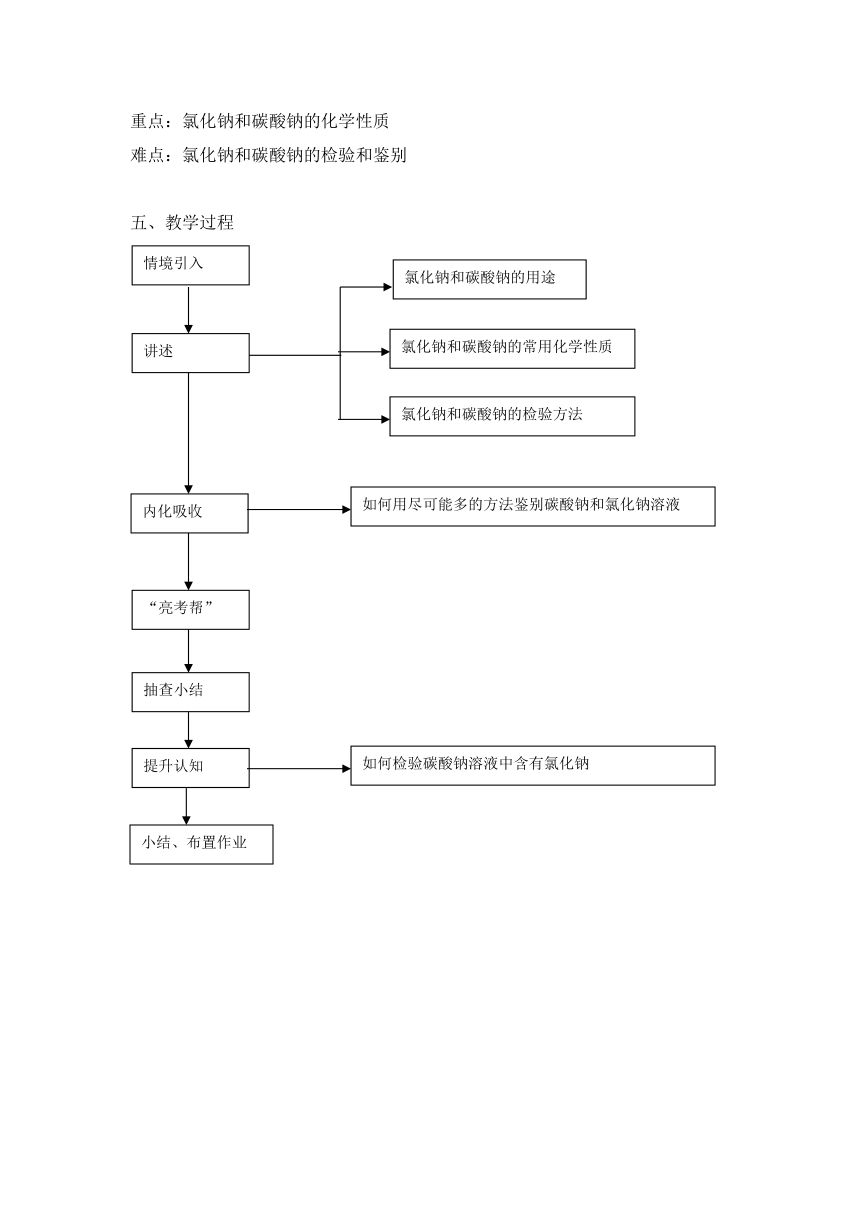
五、教学过程
“亮考帮”
抽查小结
提升认知
内化吸收
如何用尽可能多的方法鉴别碳酸钠和氯化钠溶液
小结、布置作业
情境引入
讲述
氯化钠和碳酸钠的用途
氯化钠和碳酸钠的检验方法
氯化钠和碳酸钠的常用化学性质
如何检验碳酸钠溶液中含有氯化钠
教学环节
教师活动
学生活动
设计意图
情境引入
常见盐的用途
【展示】生活中常用的盐
【展示】氯化钠的用途、碳酸钠的用途
从生活中的实物出发认识化学物质
常见盐的化学性质
【提问】公安人员破案时,常将一种无色溶液喷雾在作案人员用过的器皿或接触过白纸的表面上,以此来获得罪犯的指纹。这是为什么吗?
【演示实验】取一滴管NaCl溶液于试管中,滴入2滴AgNO3溶液再滴加少量稀硝酸。
【讲述】实验室通过这个方法检验含有盐酸根的酸或盐溶液。
【提问】以前做馒头时会加入一些纯碱水来消除酸味儿,蒸出的馒头还会松、软、白。你知道这是为什么吗?
【讲述】做馒头发酵用的酵母发酵时会产生酸味,纯碱能与酸反应并产生气泡,以盐酸为例。
【讲述】含有碳酸根的盐都可以用盐酸和石灰水来检验。
【演示实验】碳酸钠和盐酸反应并将生成的气体通入石灰水。
【讲述】工业上生产烧碱的方法有苛化法、电解法和离子交换膜法三种。用纯碱溶液和石灰乳来制烧碱就属于苛化法。
【演示实验】石灰水和碳酸钠反应。
【讲述】回忆一下碳酸盐的溶解性,如果溶液中反应得到了碳酸钡、碳酸钙等物质,也能看到有白色沉淀。因此碳酸钠还可以与氯化钙、氯化钡等溶液反应。
【演示实验】碳酸钠溶液与氯化钡、氯化钙的反应。
巩固物质的性质决定了物质的用途,物质的用途反映了物质的性质的化学学科核心素养。
鉴别碳酸钠和氯化钠
【提问】如何用尽可能多的方法鉴别碳酸钠和氯化钠。
方法有:
1、酚酞、石蕊、pH
2、稀盐酸、稀硫酸
3、石灰水、氢氧化钡溶液
4、氯化钙、氯化钡、硝酸钙、硝酸钡溶液
……
内化、讨论
【内化】独立完成实验设计
【讨论】分组讨论方法
【抽查】请同学介绍设计过程并完成演示实验
【提问】鉴别方案优选的原则是什么?
学生独立完成设计
分组讨论
回答问题并实验
现象明显、操作简单
巩固常见盐的化学性质
提升认知
【提问】如何检验碳酸钠溶液中含有氯化钠呢?刚才鉴别的方法是否可行。
【小结】检验混合物质时要考虑试剂用量和排除干扰。
方法为:
取样,加入足量硝酸钙或硝酸钡溶液,产生白色沉淀,取上层清液加入硝酸银溶液和稀硝酸,产生白色沉淀为含氯化钠。
突破混合物质检验的难点。
布置作业
详见课后作业。
六、板书
一、教材分析
本节课是上教版教材第二学期第六章第二节第三课时内容,在教学基本要求中常见盐的性质属于B级学,虽然只要求知道氯化钠和硝酸银、碳酸钠与盐酸、硫酸、氢氧化钙的反应,但是因为这些知识点还要应用到物质的检验和鉴别上,因此学要求较高。在第五章酸和碱的学习中已经略有涉及酸与盐溶液、碱与盐溶液的反应,因此本节课想通过最常见盐的化学性质引出物质的简单检验和鉴别。此外,本课通过提出问题,初步引导学生根据探究目的涉及并优化实验方案;通过讨论,进一步改进实验设想,培养学生科学探究的化学学科核心素养。
二、学情分析
学生对酸和碱已经有一定的认识,食盐和纯碱又是生活中最常见的盐,也了解了一些盐的化学性质,与生活中实际联系起来,学习热情比较高。此外,进过一学期的学习,学生也逐步形成了一定的化学学习思维,有一定的观察、操作、理解及分析能力。但是,对于物质的检验和鉴别还没有系统化地归纳过。
另外,本节课的教学对象是九(1)班的学生,整个班级的整体水平还不错,但仍有个别基础较薄弱的学生。因此,本节课采用对分课堂的教学模式,在学生分组时充分考虑不同学生的学习程度,在课堂提问和评价时的要求也有所不同。
三、教学目标
1、知道氯化钠与硝酸银、碳酸钠与盐酸、硫酸、氢氧化钙的反应,并描述现象和书写化学方程式。
2、知道食盐和纯碱常用的化学性质。
3、知道物质的性质决定了物质的用途,物质的用途又反映了物质的性质。
4、通过内化、讨论等方式设计并优化实验方案,完成氯化钠和碳酸钠的检验和鉴别。
四、教学重、难点
重点:氯化钠和碳酸钠的化学性质
难点:氯化钠和碳酸钠的检验和鉴别
五、教学过程
“亮考帮”
抽查小结
提升认知
内化吸收
如何用尽可能多的方法鉴别碳酸钠和氯化钠溶液
小结、布置作业
情境引入
讲述
氯化钠和碳酸钠的用途
氯化钠和碳酸钠的检验方法
氯化钠和碳酸钠的常用化学性质
如何检验碳酸钠溶液中含有氯化钠
教学环节
教师活动
学生活动
设计意图
情境引入
常见盐的用途
【展示】生活中常用的盐
【展示】氯化钠的用途、碳酸钠的用途
从生活中的实物出发认识化学物质
常见盐的化学性质
【提问】公安人员破案时,常将一种无色溶液喷雾在作案人员用过的器皿或接触过白纸的表面上,以此来获得罪犯的指纹。这是为什么吗?
【演示实验】取一滴管NaCl溶液于试管中,滴入2滴AgNO3溶液再滴加少量稀硝酸。
【讲述】实验室通过这个方法检验含有盐酸根的酸或盐溶液。
【提问】以前做馒头时会加入一些纯碱水来消除酸味儿,蒸出的馒头还会松、软、白。你知道这是为什么吗?
【讲述】做馒头发酵用的酵母发酵时会产生酸味,纯碱能与酸反应并产生气泡,以盐酸为例。
【讲述】含有碳酸根的盐都可以用盐酸和石灰水来检验。
【演示实验】碳酸钠和盐酸反应并将生成的气体通入石灰水。
【讲述】工业上生产烧碱的方法有苛化法、电解法和离子交换膜法三种。用纯碱溶液和石灰乳来制烧碱就属于苛化法。
【演示实验】石灰水和碳酸钠反应。
【讲述】回忆一下碳酸盐的溶解性,如果溶液中反应得到了碳酸钡、碳酸钙等物质,也能看到有白色沉淀。因此碳酸钠还可以与氯化钙、氯化钡等溶液反应。
【演示实验】碳酸钠溶液与氯化钡、氯化钙的反应。
巩固物质的性质决定了物质的用途,物质的用途反映了物质的性质的化学学科核心素养。
鉴别碳酸钠和氯化钠
【提问】如何用尽可能多的方法鉴别碳酸钠和氯化钠。
方法有:
1、酚酞、石蕊、pH
2、稀盐酸、稀硫酸
3、石灰水、氢氧化钡溶液
4、氯化钙、氯化钡、硝酸钙、硝酸钡溶液
……
内化、讨论
【内化】独立完成实验设计
【讨论】分组讨论方法
【抽查】请同学介绍设计过程并完成演示实验
【提问】鉴别方案优选的原则是什么?
学生独立完成设计
分组讨论
回答问题并实验
现象明显、操作简单
巩固常见盐的化学性质
提升认知
【提问】如何检验碳酸钠溶液中含有氯化钠呢?刚才鉴别的方法是否可行。
【小结】检验混合物质时要考虑试剂用量和排除干扰。
方法为:
取样,加入足量硝酸钙或硝酸钡溶液,产生白色沉淀,取上层清液加入硝酸银溶液和稀硝酸,产生白色沉淀为含氯化钠。
突破混合物质检验的难点。
布置作业
详见课后作业。
六、板书
