2021年中考化学复习重难点考点—化学计算题专题突破(WORD版含答案与解析)
文档属性
| 名称 | 2021年中考化学复习重难点考点—化学计算题专题突破(WORD版含答案与解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 691.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-08 00:00:00 | ||
图片预览


文档简介
重、难点考点—化学计算题专题突破
考点剖析:
此题型在中考中主要考查化学方程式的计算,化学方程式的计算题应注意的问题:
1:正确书写题目中相关的化学方程式。
2:对题目中所给的数据,表格及图像进行正确的分析,确定已知量和未知量。
3:根据题意写出相关的化学方程式式,并正确设出未知量。
4:在化学方程式式中列出相关物质的相对分子质量并把已知和未知的数据写到相关物质的下面。
5:正确列出比例式,并正确求解。
6:对所求出的数据或化学量进行作答。
典例剖析:
例1:
(2020年河北中考)某小组用粗锌测定某稀硫酸中溶质的质量分数。取一定质量的稀硫酸于烧杯中,称量稀硫酸和烧杯的总质量;然后,向其中分两次加入粗锌(杂质不参加反应),实验过程和数据如图所示。请计算:
(1)生成氢气的总质量为
g。
(2)稀硫酸中溶质的质量分数。
例2:(2020年广元中考)某兴趣小组同学将100g氢氧化钠溶液分五次加入到139.6g硫酸铜溶液中,测得实验数据如下表所示:
?
第一次
第二次
第三次
第四次
第五次
氢氧化钠溶液的质量/g
20
20
20
20
20
沉淀质量/g
4.9
9.8
m
19.6
19.6
(1)表格中m的值为多少。
(2)计算恰好完全反应时所得溶液中溶质的质量分数。(写出计算过程)
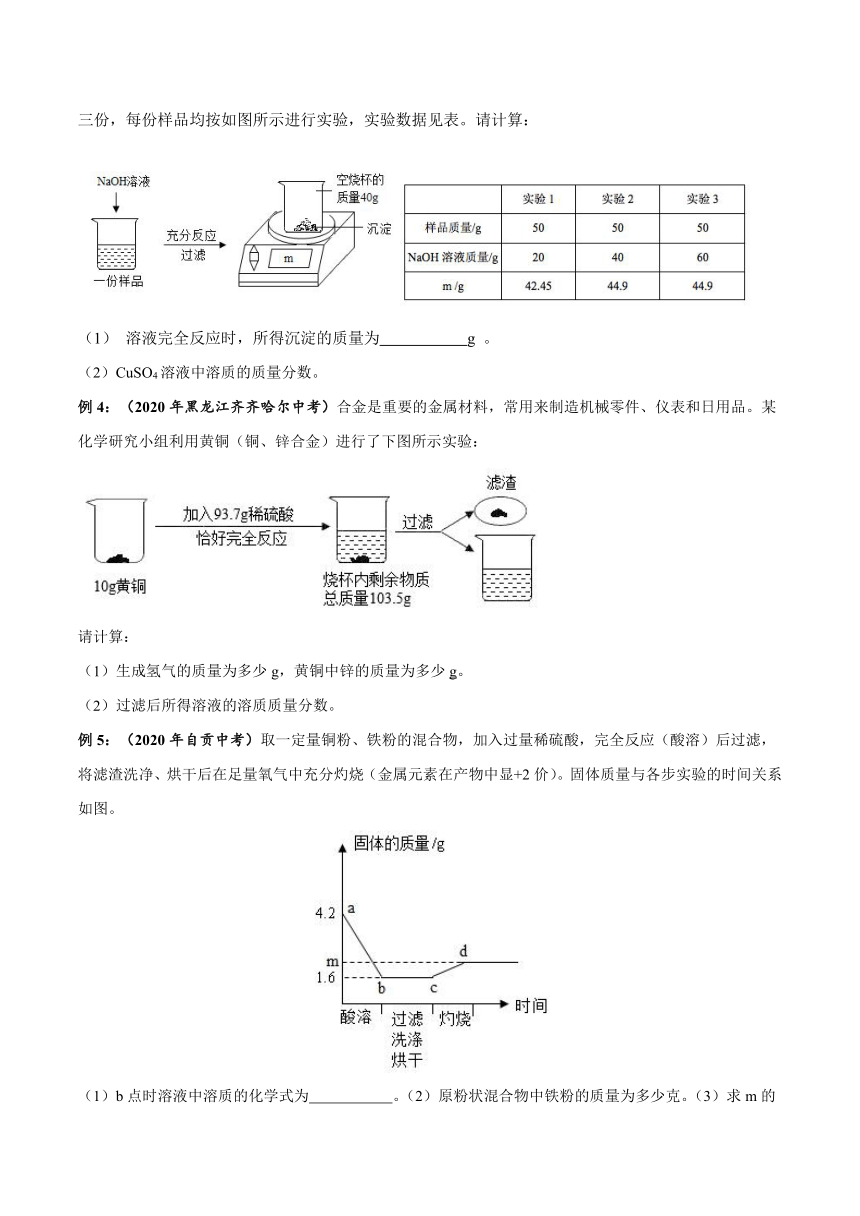
例3:(2019河北中考试题)为测定某
CuSO4溶液中溶质的质量分数,取150gCuSO4溶液,平均分为三份,每份样品均按如图所示进行实验,实验数据见表。请计算:
(1)
溶液完全反应时,所得沉淀的质量为
g
。
(2)CuSO4溶液中溶质的质量分数。
例4:(2020年黑龙江齐齐哈尔中考)合金是重要的金属材料,常用来制造机械零件、仪表和日用品。某化学研究小组利用黄铜(铜、锌合金)进行了下图所示实验:
请计算:
(1)生成氢气的质量为多少g,黄铜中锌的质量为多少g。
(2)过滤后所得溶液的溶质质量分数。
例5:(2020年自贡中考)取一定量铜粉、铁粉的混合物,加入过量稀硫酸,完全反应(酸溶)后过滤,将滤渣洗净、烘干后在足量氧气中充分灼烧(金属元素在产物中显+2价)。固体质量与各步实验的时间关系如图。
(1)b点时溶液中溶质的化学式为
。(2)原粉状混合物中铁粉的质量为多少克。(3)求m的值。(写出计算过程)
例6:(2018?枣庄)往100g硫酸和硫酸铜的混合液中,逐滴加入8%的氢氧化钠溶液直至过量,根据实验事实绘制了如图所示曲线,分析并计算:
(1)a→b段表示氢氧化钠与混合物中的
发生反应。
(2)求反应前混合液中硫酸铜的质量分数。(写出计算过程)
例7:(2019天水中考)某化学兴趣小组的同学取氢氧化钠和碳酸钠的混合溶液50g装入烧杯中,每次滴加50g稀盐酸充分反应。测得部分数据及图象如下:
次数
1
2
3
4
5
加入稀盐酸的质量/g
50
50
50
50
50
烧杯中物质的质量/g
100
150
197.8
245.6
295.6
请根据有关信息计算:
(1)a的数值为
。
(2)求稀盐酸中溶质的质量分数。(写出计算过程)
(3)求恰好完全反应后所得溶液中溶质的质量。(写出计算过程)
例8:(2020湖南长沙)为了测定某小苏打样品中碳酸氢钠的质量分数,小兰同学进行了如下实验:向盛有10g样品的烧杯中加入稀硫酸,恰好完全反应时,加入稀硫酸的质量为90g,反应后烧杯内物质的总质量为95.6g。(杂质不溶于水也不与酸发生反应)已知反应的化学方程式如下:2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O(1)该反应生成二氧化碳的质量为
g。
(2)求该样品中碳酸氢钠的质量分数(写出计算过程)。
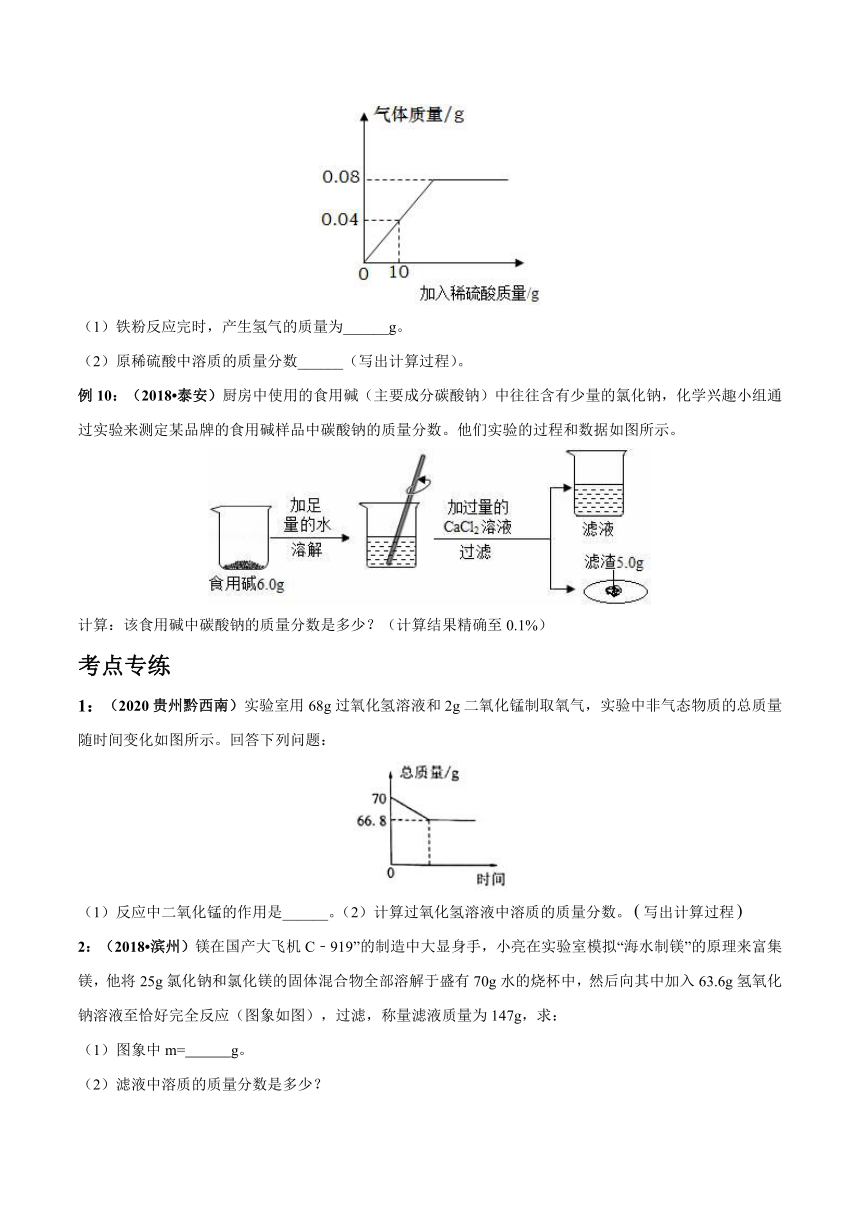
例9:(2020甘肃庆阳)向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。请根据关系图分析并计算:
(1)铁粉反应完时,产生氢气的质量为______g。
(2)原稀硫酸中溶质的质量分数______(写出计算过程)。
例10:(2018?泰安)厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如图所示。
计算:该食用碱中碳酸钠的质量分数是多少?(计算结果精确至0.1%)
考点专练
1:(2020贵州黔西南)实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验中非气态物质的总质量随时间变化如图所示。回答下列问题:
(1)反应中二氧化锰的作用是______。(2)计算过氧化氢溶液中溶质的质量分数。写出计算过程
2:(2018?滨州)镁在国产大飞机C﹣919”的制造中大显身手,小亮在实验室模拟“海水制镁”的原理来富集镁,他将25g氯化钠和氯化镁的固体混合物全部溶解于盛有70g水的烧杯中,然后向其中加入63.6g氢氧化钠溶液至恰好完全反应(图象如图),过滤,称量滤液质量为147g,求:
(1)图象中m=
g。
(2)滤液中溶质的质量分数是多少?
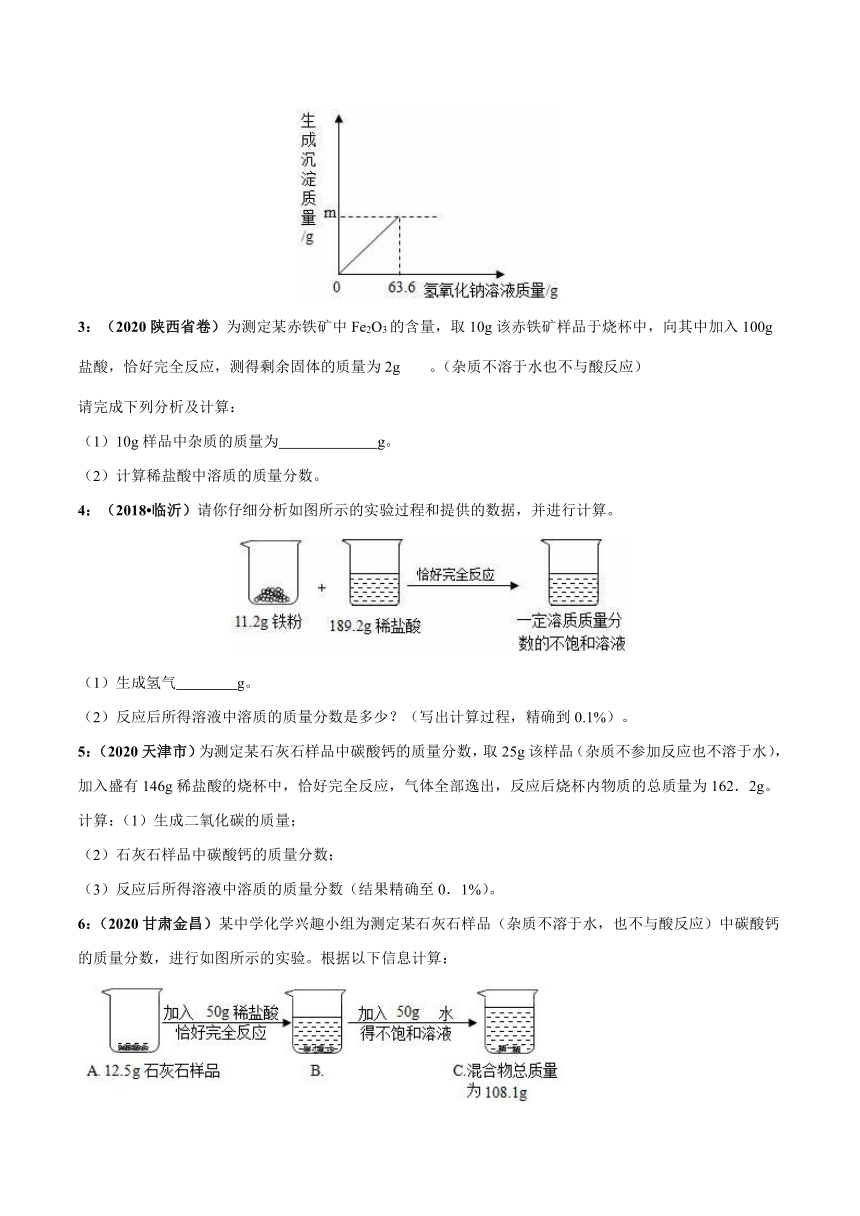
3:(2020陕西省卷)为测定某赤铁矿中Fe2O3的含量,取10g该赤铁矿样品于烧杯中,向其中加入100g盐酸,恰好完全反应,测得剩余固体的质量为2g。(杂质不溶于水也不与酸反应)
请完成下列分析及计算:
(1)10g样品中杂质的质量为
g。
(2)计算稀盐酸中溶质的质量分数。
4:(2018?临沂)请你仔细分析如图所示的实验过程和提供的数据,并进行计算。
(1)生成氢气
g。
(2)反应后所得溶液中溶质的质量分数是多少?(写出计算过程,精确到0.1%)。
5:(2020天津市)为测定某石灰石样品中碳酸钙的质量分数,取25g该样品(杂质不参加反应也不溶于水),加入盛有146g稀盐酸的烧杯中,恰好完全反应,气体全部逸出,反应后烧杯内物质的总质量为162.2g。计算:(1)生成二氧化碳的质量;
(2)石灰石样品中碳酸钙的质量分数;
(3)反应后所得溶液中溶质的质量分数(结果精确至0.1%)。
6:(2020甘肃金昌)某中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。根据以下信息计算:
(1)生成二氧化碳的质量为 g;
(2)样品中碳酸钙的质量分数是多少?
(3)C烧杯中溶液的溶质的质量分数是多少?
7:(2020广西北部湾)常温下,向盛有100.0gKOH溶液的烧杯中逐滴加入120.0g质量分数为7.3%的稀盐酸,用pH计(精确测定溶液pH的仪器)测定反应过程中溶液的pH,所得数据如下:
加入稀盐酸的质量/g
60.0
80.0
100.0
120.0
烧杯中溶液的pH
13.7
13.3
7.0
0.7
(1)恰好完全反应时,消耗稀盐酸的质量为______________g。
(2)求该KOH溶液中溶质的质量分数(结果精确到0.1%)。
8:(2018四川乐山中考)将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2mL水中(ρ水=1g/cm3),向所得溶液中滴加质量分数为14.2%的NaSO4溶液,至恰好完全反应。下图是所加NaSO4溶液质量与生成沉淀质量的关系图,计算:
(1)生成沉淀的质量是__________?
(2)所得溶液中溶质的质量分数为____________?
9:(2020甘肃天水)将氯化钠和氯化镁的固体混合物30g放入烧杯中,加入245.6g水使其完全溶解,再加入一定质量分数的氢氧化钠溶液,反应过程中滴加氢氧化钠溶液的质量与生成沉淀的质量关系如图所示。请计算;
(1)m的值为
;
(2)恰好完全反应时,消耗氢氧化钠的质量
克;
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数(写出具体计算过程)。
10:(2020辽宁抚顺)取6.5g锌粒放入烧杯中,向其中加入稀硫酸至恰好完全反应,共用去稀硫酸的质量为50g。请计算:稀硫酸中溶质的质量分数。
11:(2020年贵州遵义中考)欲测定一瓶标签破损的稀硫酸的溶质质量分数,现取30g稀硫酸样品于烧杯中,将15%的NaOH溶液逐滴加入烧杯中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示:
回答下列问题:
(1)a点溶液中的溶质是_____
(填化学式)。
(2)计算该稀硫酸的溶质质量分数。(
写出计算过程,结果精确到0.1%)
12:(2020年乐山中考)实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末,烧杯中现有100g碳酸钠溶液,将140g氯化钙溶液分四次加入,充分反应,注:发生反应的化学方程式为,四次测量所得数据如表所示:
次数
累计加入氯化钙溶液的质量/g
烧杯中溶液的总质量/g
一
40
135
二
80
170
三
120
205
四
140
225
(1)恰好完全反应时,生成沉淀的总质量为
g。
(2)第四次测量时,所得溶液中的溶质有
(填化学式)。
(3)计算氯化钙溶液的溶质质量分数(写出计算过程,计算结果保留到0.1%)
13:(2020年江西中考)“二氧化碳的实验室制取与性质”实验活动产生的废液中含稀盐酸,需先测定其溶质质量分数后进行处理。(杂质不参加反应)
(1)实验时需配制50g5%的氢氧化钠溶液,若用氢氧化钠固体和水来配制,则需称量氢氧化钠固体的质量为_____g。
(2)取20g废液样品于烧杯中,向其中逐滴加入5%的氢氧化钠溶液,恰好完全反应时共消耗氢氧化钠溶液16g。计算废液中盐酸的溶质质量分数。(写出计算过程)
(3)恰好完全反应时烧杯中的溶液所含粒子数目关系:Na+_____Cl-。(填“>”、“=”或“<”)
14:(2020年黑龙江牡丹江中考)为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:
(1)这种贝壳中碳酸钙的质量分数是__________
(2)25g贝壳与稀盐酸恰好完全反应时,生成二氧化碳的质量为多少?(写出计算步骤)
(3)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。
15:(2020辽宁辽阳)称取5g含杂质的氢氧化钙固体样品放入烧杯中,向烧杯中加入50g溶质的质量分数为7.3%的稀盐酸(假设杂质不与稀盐酸反应),二者恰好完全反应。请计算:固体样品中氢氧化钙的质量分数。
答案与解析
典例剖析:
例1:
(2020年河北中考)某小组用粗锌测定某稀硫酸中溶质的质量分数。取一定质量的稀硫酸于烧杯中,称量稀硫酸和烧杯的总质量;然后,向其中分两次加入粗锌(杂质不参加反应),实验过程和数据如图所示。请计算:
(1)生成氢气的总质量为
g。
(2)稀硫酸中溶质的质量分数。
【答案】(1)0.2g;(2)9.8%
【解析】(1)由图可知,先加入8g粗锌,反应后,天平显示的质量是213.4g,再加入2g粗锌,天平显示的质量是215.4g,故第一次加入8g粗锌,已经完全反应。生成氢气的总质量为:205.6g+8g-213.4g=0.2g;
(2)解:设稀硫酸中溶质的质量分数为x
加入稀硫酸的质量为:205.6g-105.6g=100g;
x=9.8%
答:稀硫酸中溶质的质量分数为9.8%。
例2:(2020年广元中考)某兴趣小组同学将100g氢氧化钠溶液分五次加入到139.6g硫酸铜溶液中,测得实验数据如下表所示:
?
第一次
第二次
第三次
第四次
第五次
氢氧化钠溶液的质量/g
20
20
20
20
20
沉淀质量/g
4.9
9.8
m
19.6
19.6
(1)表格中m的值为多少。
(2)计算恰好完全反应时所得溶液中溶质的质量分数。(写出计算过程)
【答案】(1)14.7g;(2)14.2%
【解析】(1)由表中数据可知,第一次加入20g氢氧化钠溶液,产生4.9g沉淀,第二次加入20g氢氧化钠溶液,共产生9.8g沉淀,第四次加入20g氢氧化钠溶液,共产生19.6g沉淀,由此可得出,每加入20g氢氧化钠溶液,产生4.9g沉淀,故m=4.9g×3=14.7g;
(2)由表中数据可知,当加入80g氢氧化钠溶液时,氢氧化钠与硫酸铜恰好完全反应,这时生成氢氧化铜沉淀的质量为19.6g。设恰好完全反应时,生成硫酸钠的质量为x。
x=28.4g
恰好完全反应时所得溶液中溶质的质量分数为:
答:恰好完全反应时所得溶液中溶质的质量分数为14.2%。
例3:(2019河北中考试题)为测定某
CuSO4溶液中溶质的质量分数,取150gCuSO4溶液,平均分为三份,每份样品均按如图所示进行实验,实验数据见表。请计算:
(1)
溶液完全反应时,所得沉淀的质量为
g
。
(2)CuSO4溶液中溶质的质量分数。
【答案】(1)4.9
(2)16%。
【解析】(1)由表可知,实验2和实验3中生成沉淀的质量相同,说明硫酸铜已经完全反应,所以当
完全反应时,沉淀的质量为44.9g—40g=4.9g
。
(2)设硫酸铜的质量为x
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
160
98
X
4.9g
则160g/x=98/4.9g可解得:x=8g,则CuSO4溶液中溶质的质量分数为:(8g/50g)×100%=16%.
答:CuSO4溶液中溶质的质量分数为16%。
例4:(2020年黑龙江齐齐哈尔中考)合金是重要的金属材料,常用来制造机械零件、仪表和日用品。某化学研究小组利用黄铜(铜、锌合金)进行了下图所示实验:
请计算:
(1)生成氢气的质量为多少g,黄铜中锌的质量为多少g。
(2)过滤后所得溶液的溶质质量分数。
【答案】0.2;6.5;16.1%
【解析】(1)根据质量守恒定律,加入稀硫酸恰好完全反应后,烧杯内物质总质量减少质量即为生成氢气的质量,故生成氢气的质量为10g+93.7g-103.5g=0.2g;设黄铜中锌的质量为x,则
解得x=6.5g;故黄铜中锌的质量为6.5g。
(2)样品中锌与加入的稀硫酸恰好完全反应,设生成硫酸锌的质量为y,则
解得y=16.1g;根据质量守恒定律,所得溶液质量为6.5g+93.7g-0.2g=100g,故过滤后所得溶液的溶质质量分数为。
例5:(2020年自贡中考)取一定量铜粉、铁粉的混合物,加入过量稀硫酸,完全反应(酸溶)后过滤,将滤渣洗净、烘干后在足量氧气中充分灼烧(金属元素在产物中显+2价)。固体质量与各步实验的时间关系如图。
(1)b点时溶液中溶质的化学式为
。(2)原粉状混合物中铁粉的质量为多少克。(3)求m的值。(写出计算过程)
【答案】(1)H2SO4、FeSO4;(2)2.6g;(3)2.0g
【解析】(1)铁和稀硫酸反应生成硫酸亚铁和氢气,铜不和稀硫酸反应,b点时铁恰好和稀硫酸反应,硫酸过量,溶液中溶质为硫酸和硫酸亚铁,化学式为:H2SO4、FeSO4;
(2)铜不和稀硫酸反应,剩余1.6g固体为铜,则原粉状混合物中铁粉的质量为:4.2g-1.6g=2.6g;
(3)滤渣是铜,洗涤、烘干、灼烧后生成氧化铜,m为生成氧化铜的质量;
,,解得:m=2.0g。
例6:(2018?枣庄)往100g硫酸和硫酸铜的混合液中,逐滴加入8%的氢氧化钠溶液直至过量,根据实验事实绘制了如图所示曲线,分析并计算:
(1)a→b段表示氢氧化钠与混合物中的
发生反应。
(2)求反应前混合液中硫酸铜的质量分数。(写出计算过程)
【答案】(1)硫酸
(2)16%。
【解析】(1)根据溶质的变化可以看出,ab段是硫酸和氢氧化钠的反应,所以a→b段表示氢氧化钠与混合物中的硫酸发生反应。(2)根据图,可以看出与硫酸铜反应的氢氧化钠溶液的质量为150g﹣50g=100g。
设反应前混合液中硫酸铜的质量分数为x。
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
80
160
8%×100g
100gx
=
x=16%
答:(1)a→b段表示氢氧化钠与混合物中的
硫酸发生反应。(2)反应前混合液中硫酸铜的质量分数为16%。
例7:(2019天水中考)某化学兴趣小组的同学取氢氧化钠和碳酸钠的混合溶液50g装入烧杯中,每次滴加50g稀盐酸充分反应。测得部分数据及图象如下:
次数
1
2
3
4
5
加入稀盐酸的质量/g
50
50
50
50
50
烧杯中物质的质量/g
100
150
197.8
245.6
295.6
请根据有关信息计算:
(1)a的数值为
。
(2)求稀盐酸中溶质的质量分数。(写出计算过程)
(3)求恰好完全反应后所得溶液中溶质的质量。(写出计算过程)
【答案】(1)4.4;(2)7.3%;
(3)23.4g。
【解析】根据质量守恒定律可得,生成的二氧化碳的质量为50g+250g295.6g=4.4g
且根据图可知,加入100g盐酸时才有二氧化碳生成,且加入第三个50g盐酸时生成的二氧化碳为2.2g,第
四个50g盐酸生成的二氧化碳的质量为2.2g,之后质量不再变化,说明碳酸钠已经完全反应。
即与碳酸钠反应的稀盐酸的质量为100g
。设稀盐酸中溶质的质量分数为x,生成的氯化钠的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
73
117
44
100gx
y
4.4g
可得比例:73/100x=44/4.4g可解得:x=7.3%;同理可得比例:117/y=44/4.4g,可解得y=11.7g.根据氯元素守恒确定与氢氧化钠反应生成的氯化钠的质量与100g稀盐酸和碳酸钠反应生成的氯化钠的质量相等,所以氢氧化钠对应的氯化钠的质量也为11.7g
,所以氯化钠的总质量为11.7g+11.7g=23.4g
【点评】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程
要完整。
例8:(2020湖南长沙)为了测定某小苏打样品中碳酸氢钠的质量分数,小兰同学进行了如下实验:向盛有10g样品的烧杯中加入稀硫酸,恰好完全反应时,加入稀硫酸的质量为90g,反应后烧杯内物质的总质量为95.6g。(杂质不溶于水也不与酸发生反应)已知反应的化学方程式如下:2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O(1)该反应生成二氧化碳的质量为
g。
(2)求该样品中碳酸氢钠的质量分数(写出计算过程)。
【答案】(1)4.4;(2)84%
【解析】(1)该反应生成二氧化碳的质量为:10g+90g﹣95.6g=4.4g。故填:4.4。(2)设碳酸氢钠质量为x,
2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O,
168
88
x
4.4g
=,
x=8.4g,
该样品中碳酸氢钠的质量分数是:×100%=84%,
答:该样品中碳酸氢钠的质量分数是84%。
例9:(2020甘肃庆阳)向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。请根据关系图分析并计算:
(1)铁粉反应完时,产生氢气的质量为______g。
(2)原稀硫酸中溶质的质量分数______(写出计算过程)。
【答案】(1)0.08
;(2)19.6%
【解析】(1)由图可知铁粉反应完时,产生氢气的质量为
0.08g。(2)设原稀硫酸中溶质的质量分数为x
由图可知10g硫酸对应0.04g氢气生成
答:原稀硫酸中溶质的质量分数为19.6%。
例10:(2018?泰安)厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如图所示。
计算:该食用碱中碳酸钠的质量分数是多少?(计算结果精确至0.1%)
【答案】88.3%
【解析】生成碳酸钙沉淀的质量为5.0g,设该食用碱中碳酸钠的质量分数为x
CaCl2+Na2CO3═CaCO3↓+2NaCl
106
100
6.0gx
5.0g
=
可解得:x≈88.3%
答:该食用碱中碳酸钠的质量分数为88.3%。
考点专练
1:(2020贵州黔西南)实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验中非气态物质的总质量随时间变化如图所示。回答下列问题:
(1)反应中二氧化锰的作用是______。(2)计算过氧化氢溶液中溶质的质量分数。写出计算过程
【答案】(1)催化作用;(2)10%
【解析】(1)过氧化氢在二氧化锰催化作用下生成水和氧气,故反应中二氧化锰的作用是催化作用。(2)根据质量守恒定律,反应前后反应物的总质量等于生成物的总质量,减少的是生成沉淀或气体的质量,故反应产生氧气的质量是。
设产生3.2g氧气需要的质量为x
故过氧化氢溶液的溶质质量分数为。答:过氧化氢溶液的质量分数是。
2:(2018?滨州)镁在国产大飞机C﹣919”的制造中大显身手,小亮在实验室模拟“海水制镁”的原理来富集镁,他将25g氯化钠和氯化镁的固体混合物全部溶解于盛有70g水的烧杯中,然后向其中加入63.6g氢氧化钠溶液至恰好完全反应(图象如图),过滤,称量滤液质量为147g,求:
(1)图象中m=
g。
(2)滤液中溶质的质量分数是多少?
【答案】(1)11.6
(2)20%。
【解析】(1)图象中m=25g+70g+63.6g﹣147g=11.6g。
(2)设氯化镁质量为x,反应生成氯化钠质量为y,
MgCl2+2NaOH=2NaCl+Mg(OH)2↓,
95
117
58
x
y
11.6g
=
=,可解得:x=19g,y=23.4g,滤液中溶质的质量分数是:×100%=20%,答:滤液中溶质的质量分数是20%。
3:(2020陕西省卷)为测定某赤铁矿中Fe2O3的含量,取10g该赤铁矿样品于烧杯中,向其中加入100g盐酸,恰好完全反应,测得剩余固体的质量为2g。(杂质不溶于水也不与酸反应)
请完成下列分析及计算:
(1)10g样品中杂质的质量为
g。
(2)计算稀盐酸中溶质的质量分数。
【答案】(1)2;(2)10.95%
【解析】(1)根据题意,赤铁矿石中的杂质既不溶于水也不与盐酸反应,剩余固体(即杂质)的质量为2g,氧化铁的质量是10g-2g=8g;(2)根据氧化铁与盐酸反应的化学方程式,由反应消耗氧化铁的质量计算出参加反应的HCl的质量,进而计算出盐酸的溶质质量分数。设100g稀盐酸中溶质的质量为x。
x=10.95g
稀盐酸中溶质的质量分数=(其它合理的解法均照上述标准给分)
答:稀盐酸中溶质的质量分数10.95%。
4:(2018?临沂)请你仔细分析如图所示的实验过程和提供的数据,并进行计算。
(1)生成氢气
g。
(2)反应后所得溶液中溶质的质量分数是多少?(写出计算过程,精确到0.1%)。
【答案】(1)0.4
(2)12.7%。
【解析】(1)设消耗11.2g铁生成的氯化亚铁的质量为x,生成的氢气的质量为y。
Fe+2HCl═FeCl2+H2↑,
56
127
2
11.2g
x
y
可解得:x=25.4g,y=0.4g
,反应后所得溶液中溶质的质量分数是×100%=12.7%,
答:(1)生成氢气0.4g,(2)反应后所得溶液中溶质的质量分数是12.7%。
5:(2020天津市)为测定某石灰石样品中碳酸钙的质量分数,取25g该样品(杂质不参加反应也不溶于水),加入盛有146g稀盐酸的烧杯中,恰好完全反应,气体全部逸出,反应后烧杯内物质的总质量为162.2g。计算:(1)生成二氧化碳的质量;
(2)石灰石样品中碳酸钙的质量分数;
(3)反应后所得溶液中溶质的质量分数(结果精确至0.1%)。
【答案】(1)8.8g
;(2)80%;(3)14.1%
【解析】(1)由质量守恒定律可知,反应物的总质量等于生成物的总质量,减少的是生成沉淀或气体的质量,故生成的二氧化碳的质量为。
(2)设原样品中碳酸钙的质量为x,生成氯化钙的质量为y
故石灰石样品中碳酸钙的质量分数
(3)反应后所得溶液的质量为
故反应后所得溶液中溶质的质量分数为答:生成二氧化碳的质量为8.8g;石灰石样品中碳酸钙的质量分数为80%;反应后所得溶液中溶质的质量分数为14.1%。
6:(2020甘肃金昌)某中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。根据以下信息计算:
(1)生成二氧化碳的质量为 g;
(2)样品中碳酸钙的质量分数是多少?
(3)C烧杯中溶液的溶质的质量分数是多少?
【答案】(1)4.4;(2)80.0%
;(3)10.5%
【解析】(1)生成的二氧化碳的质量:12.5g+50g+50g﹣108.1g=4.4g;
(2)设碳酸钙的质量为x,生成氯化钙的质量为y,
,x=10g
,y=11.1
样品中碳酸钙的质量分数为:×100%=80.0%;
(3)C烧杯中溶液中溶质的质量分数为:×100%≈10.5%。
7:(2020广西北部湾)常温下,向盛有100.0gKOH溶液的烧杯中逐滴加入120.0g质量分数为7.3%的稀盐酸,用pH计(精确测定溶液pH的仪器)测定反应过程中溶液的pH,所得数据如下:
加入稀盐酸的质量/g
60.0
80.0
100.0
120.0
烧杯中溶液的pH
13.7
13.3
7.0
0.7
(1)恰好完全反应时,消耗稀盐酸的质量为______________g。
(2)求该KOH溶液中溶质的质量分数(结果精确到0.1%)。
【答案】(1)100.0;(2)11.2%
【解析】(1)pH=7,表示恰好完全反应,此时消耗稀盐酸的质量为100.0g,故填:100.0。(2)解:恰好完全反应时,消耗的稀盐酸中溶质的质量设反应消耗KOH的质量为x
该KOH溶液中溶质的质量分数为:
答:该KOH溶液中溶质的质量分数为11.2%。
8:(2018四川乐山中考)将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2mL水中(ρ水=1g/cm3),向所得溶液中滴加质量分数为14.2%的NaSO4溶液,至恰好完全反应。下图是所加NaSO4溶液质量与生成沉淀质量的关系图,计算:
(1)生成沉淀的质量是__________?
(2)所得溶液中溶质的质量分数为____________?
【答案】
(1).
23.3g
(2).
10%
【解析】解:(1)由图可知,生成BaSO4沉淀的质量为23.3g(2)设BaCl2的质量为x,生成NaCl的质量为y
BaCl2+Na2SO4=BaSO4↓+2NaCl
208
233
117
x=20.8g,y=11.7g
,溶液的总质量=29.1g+94.2g+100g-23.3g=200g
溶质的总质量=11.7g+(29.1g-20.8g)
=20g
NaCl%=×100%=10%
答:生成沉淀23.3g,所得NaCl溶液的质量分数为10%。
9:(2020甘肃天水)将氯化钠和氯化镁的固体混合物30g放入烧杯中,加入245.6g水使其完全溶解,再加入一定质量分数的氢氧化钠溶液,反应过程中滴加氢氧化钠溶液的质量与生成沉淀的质量关系如图所示。请计算;
(1)m的值为
;
(2)恰好完全反应时,消耗氢氧化钠的质量
克;
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数(写出具体计算过程)。
【答案】(1)8.7g;(2)16g;(3)10%
【解析】(1)由图中信息可知,20g氢氧化钠溶液完全反应生成2.9g沉淀,加入氢氧化钠溶液60g以后仍然产生沉淀,说明加入60g氢氧化钠溶液时,氢氧化钠完全反应,生成氢氧化镁质量是2.9g
×3=8.7g。(2)当加入的氢氧化钠溶液质量为80克时,为恰好完全反应。设氯化镁的质量为x,氢氧化钠的质量为y,生成的氯化钠的质量为z
故恰好完全反应时,消耗氢氧化钠的质量16克。(3)溶液中氯化钠质量为,溶液质量为,故恰好完全反应时,所得不饱和溶液中溶质的质量分数为
。
答:恰好完全反应时,消耗氢氧化钠的质量16克;所得不饱和溶液中溶质的质量分数为10.0%。
10:(2020辽宁抚顺)取6.5g锌粒放入烧杯中,向其中加入稀硫酸至恰好完全反应,共用去稀硫酸的质量为50g。请计算:稀硫酸中溶质的质量分数。
【答案】19.6%
【解析】解:设稀硫酸中溶质的质量为x。
答:该稀硫酸中溶质的质量分数为19.6%。
11:(2020年贵州遵义中考)欲测定一瓶标签破损的稀硫酸的溶质质量分数,现取30g稀硫酸样品于烧杯中,将15%的NaOH溶液逐滴加入烧杯中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示:
回答下列问题:
(1)a点溶液中的溶质是_____
(填化学式)。
(2)计算该稀硫酸的溶质质量分数。(
写出计算过程,结果精确到0.1%)
【答案】(1)、
(2)4.9%
【解析】(1)当滴加NaOH溶液至a点时,由于溶液此时pH小于7,显酸性,也就是硫酸有剩余,此时的溶质为剩余的硫酸和生成的硫酸钠,所以溶液中的溶质的化学式为和;
(2)当pH值为7时,此时消耗的氢氧化钠溶液的质量为8g,则消耗NaOH溶液中的NaOH质量为8g×15%=1.2g,设消耗氢氧化钠1.2g时消耗的稀硫酸的溶质的质量为x,则
x=1.47g;该稀硫酸的溶质质量分数为;答:该稀硫酸的溶质质量分数为4.9%。
12:(2020年乐山中考)实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末,烧杯中现有100g碳酸钠溶液,将140g氯化钙溶液分四次加入,充分反应,注:发生反应的化学方程式为,四次测量所得数据如表所示:
次数
累计加入氯化钙溶液的质量/g
烧杯中溶液的总质量/g
一
40
135
二
80
170
三
120
205
四
140
225
(1)恰好完全反应时,生成沉淀的总质量为
g。
(2)第四次测量时,所得溶液中的溶质有
(填化学式)。
(3)计算氯化钙溶液的溶质质量分数(写出计算过程,计算结果保留到0.1%)
【答案】(1)15;(2)NaCl和CaCl2;(3)13.9%
【解析】(1)碳酸钠和氯化钙反应生成碳酸钙和氯化钠,减少的质量的即为反应生成的碳酸钙沉淀的质量,第一次测量总质量减少的质量为,第二次测量总质量减少的质量为,第三次测量总质量减少的质量为,第四次测量总质量减少的质量为,故恰好完全反应时,生成沉淀的总质量为15g。
(2)碳酸钠和氯化钙反应生成碳酸钙和氯化钠,第四次测量时,氯化钙过量,所得溶液中的溶质有生成的氯化钠和过量的氯化钙,化学式为NaCl和CaCl2。(3)设80g氯化钙溶液的溶质质量为x
氯化钙溶液的溶质质量分数为
答:(1)恰好完全反应时,生成沉淀的总质量为15g;(2)第四次测量时,所得溶液中的溶质有NaCl和CaCl2;(3)氯化钙溶液的溶质质量分数为13.9%。
13:(2020年江西中考)“二氧化碳的实验室制取与性质”实验活动产生的废液中含稀盐酸,需先测定其溶质质量分数后进行处理。(杂质不参加反应)
(1)实验时需配制50g5%的氢氧化钠溶液,若用氢氧化钠固体和水来配制,则需称量氢氧化钠固体的质量为_____g。
(2)取20g废液样品于烧杯中,向其中逐滴加入5%的氢氧化钠溶液,恰好完全反应时共消耗氢氧化钠溶液16g。计算废液中盐酸的溶质质量分数。(写出计算过程)
(3)恰好完全反应时烧杯中的溶液所含粒子数目关系:Na+_____Cl-。(填“>”、“=”或“<”)
【答案】(1)2.5;(2)3.65%(过程见解析);(3)<
【解析】(1)氢氧化钠质量:50g×5%=2.5g,故填:2.5。
(2)设:盐酸溶质质量分数为x。
答:废液中盐酸的溶质质量分数3.65%。(3)实验室用稀盐酸和石灰石或大理石制取二氧化碳,废液中还有氯化钙,故氯离子数目大于钠离子数目,故填:<。
14:(2020年黑龙江牡丹江中考)为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:
(1)这种贝壳中碳酸钙的质量分数是__________
(2)25g贝壳与稀盐酸恰好完全反应时,生成二氧化碳的质量为多少?(写出计算步骤)
(3)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。
【答案】(1)80%(2)8.8g(详见解析)(3)不能,因为碳酸钙和稀硫酸反应生成微溶的硫酸钙,硫酸钙覆盖在碳酸钙的表面阻碍碳酸钙与稀硫酸的接触,导致不能继续反应,使反应慢慢停止
【解析】由图可以看固体减少了20g即碳酸钙的质量为20g,根据碳酸钙的质量和对应的化学方程式求算氯化钙和二氧化碳的质量,进而求算对应的质量分数。
(1)由图可以看出固体减少了20g,即碳酸钙的质量为20g,所以贝壳中碳酸钙的质量分数为;
(2)设恰好反应时,产生二氧化碳的质量为x
x=8.8g
(3)本实验不可以用稀硫酸代替稀盐酸完成实验,因为碳酸钙和稀硫酸反应生成微溶的硫酸钙,硫酸钙覆盖在碳酸钙的表面阻碍碳酸钙与稀硫酸的接触,导致不能继续反应,使反应慢慢停止。
15:(2020辽宁辽阳)称取5g含杂质的氢氧化钙固体样品放入烧杯中,向烧杯中加入50g溶质的质量分数为7.3%的稀盐酸(假设杂质不与稀盐酸反应),二者恰好完全反应。请计算:固体样品中氢氧化钙的质量分数。
【答案】74%
【解析】参加反应的盐酸的质量:,设氢氧化钙的质量为x。
x=3.7g
样品中氢氧化钙的质量分数:
答:固体样品中氢氧化钙的质量分数为74%。
考点剖析:
此题型在中考中主要考查化学方程式的计算,化学方程式的计算题应注意的问题:
1:正确书写题目中相关的化学方程式。
2:对题目中所给的数据,表格及图像进行正确的分析,确定已知量和未知量。
3:根据题意写出相关的化学方程式式,并正确设出未知量。
4:在化学方程式式中列出相关物质的相对分子质量并把已知和未知的数据写到相关物质的下面。
5:正确列出比例式,并正确求解。
6:对所求出的数据或化学量进行作答。
典例剖析:
例1:
(2020年河北中考)某小组用粗锌测定某稀硫酸中溶质的质量分数。取一定质量的稀硫酸于烧杯中,称量稀硫酸和烧杯的总质量;然后,向其中分两次加入粗锌(杂质不参加反应),实验过程和数据如图所示。请计算:
(1)生成氢气的总质量为
g。
(2)稀硫酸中溶质的质量分数。
例2:(2020年广元中考)某兴趣小组同学将100g氢氧化钠溶液分五次加入到139.6g硫酸铜溶液中,测得实验数据如下表所示:
?
第一次
第二次
第三次
第四次
第五次
氢氧化钠溶液的质量/g
20
20
20
20
20
沉淀质量/g
4.9
9.8
m
19.6
19.6
(1)表格中m的值为多少。
(2)计算恰好完全反应时所得溶液中溶质的质量分数。(写出计算过程)
例3:(2019河北中考试题)为测定某
CuSO4溶液中溶质的质量分数,取150gCuSO4溶液,平均分为三份,每份样品均按如图所示进行实验,实验数据见表。请计算:
(1)
溶液完全反应时,所得沉淀的质量为
g
。
(2)CuSO4溶液中溶质的质量分数。
例4:(2020年黑龙江齐齐哈尔中考)合金是重要的金属材料,常用来制造机械零件、仪表和日用品。某化学研究小组利用黄铜(铜、锌合金)进行了下图所示实验:
请计算:
(1)生成氢气的质量为多少g,黄铜中锌的质量为多少g。
(2)过滤后所得溶液的溶质质量分数。
例5:(2020年自贡中考)取一定量铜粉、铁粉的混合物,加入过量稀硫酸,完全反应(酸溶)后过滤,将滤渣洗净、烘干后在足量氧气中充分灼烧(金属元素在产物中显+2价)。固体质量与各步实验的时间关系如图。
(1)b点时溶液中溶质的化学式为
。(2)原粉状混合物中铁粉的质量为多少克。(3)求m的值。(写出计算过程)
例6:(2018?枣庄)往100g硫酸和硫酸铜的混合液中,逐滴加入8%的氢氧化钠溶液直至过量,根据实验事实绘制了如图所示曲线,分析并计算:
(1)a→b段表示氢氧化钠与混合物中的
发生反应。
(2)求反应前混合液中硫酸铜的质量分数。(写出计算过程)
例7:(2019天水中考)某化学兴趣小组的同学取氢氧化钠和碳酸钠的混合溶液50g装入烧杯中,每次滴加50g稀盐酸充分反应。测得部分数据及图象如下:
次数
1
2
3
4
5
加入稀盐酸的质量/g
50
50
50
50
50
烧杯中物质的质量/g
100
150
197.8
245.6
295.6
请根据有关信息计算:
(1)a的数值为
。
(2)求稀盐酸中溶质的质量分数。(写出计算过程)
(3)求恰好完全反应后所得溶液中溶质的质量。(写出计算过程)
例8:(2020湖南长沙)为了测定某小苏打样品中碳酸氢钠的质量分数,小兰同学进行了如下实验:向盛有10g样品的烧杯中加入稀硫酸,恰好完全反应时,加入稀硫酸的质量为90g,反应后烧杯内物质的总质量为95.6g。(杂质不溶于水也不与酸发生反应)已知反应的化学方程式如下:2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O(1)该反应生成二氧化碳的质量为
g。
(2)求该样品中碳酸氢钠的质量分数(写出计算过程)。
例9:(2020甘肃庆阳)向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。请根据关系图分析并计算:
(1)铁粉反应完时,产生氢气的质量为______g。
(2)原稀硫酸中溶质的质量分数______(写出计算过程)。
例10:(2018?泰安)厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如图所示。
计算:该食用碱中碳酸钠的质量分数是多少?(计算结果精确至0.1%)
考点专练
1:(2020贵州黔西南)实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验中非气态物质的总质量随时间变化如图所示。回答下列问题:
(1)反应中二氧化锰的作用是______。(2)计算过氧化氢溶液中溶质的质量分数。写出计算过程
2:(2018?滨州)镁在国产大飞机C﹣919”的制造中大显身手,小亮在实验室模拟“海水制镁”的原理来富集镁,他将25g氯化钠和氯化镁的固体混合物全部溶解于盛有70g水的烧杯中,然后向其中加入63.6g氢氧化钠溶液至恰好完全反应(图象如图),过滤,称量滤液质量为147g,求:
(1)图象中m=
g。
(2)滤液中溶质的质量分数是多少?
3:(2020陕西省卷)为测定某赤铁矿中Fe2O3的含量,取10g该赤铁矿样品于烧杯中,向其中加入100g盐酸,恰好完全反应,测得剩余固体的质量为2g。(杂质不溶于水也不与酸反应)
请完成下列分析及计算:
(1)10g样品中杂质的质量为
g。
(2)计算稀盐酸中溶质的质量分数。
4:(2018?临沂)请你仔细分析如图所示的实验过程和提供的数据,并进行计算。
(1)生成氢气
g。
(2)反应后所得溶液中溶质的质量分数是多少?(写出计算过程,精确到0.1%)。
5:(2020天津市)为测定某石灰石样品中碳酸钙的质量分数,取25g该样品(杂质不参加反应也不溶于水),加入盛有146g稀盐酸的烧杯中,恰好完全反应,气体全部逸出,反应后烧杯内物质的总质量为162.2g。计算:(1)生成二氧化碳的质量;
(2)石灰石样品中碳酸钙的质量分数;
(3)反应后所得溶液中溶质的质量分数(结果精确至0.1%)。
6:(2020甘肃金昌)某中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。根据以下信息计算:
(1)生成二氧化碳的质量为 g;
(2)样品中碳酸钙的质量分数是多少?
(3)C烧杯中溶液的溶质的质量分数是多少?
7:(2020广西北部湾)常温下,向盛有100.0gKOH溶液的烧杯中逐滴加入120.0g质量分数为7.3%的稀盐酸,用pH计(精确测定溶液pH的仪器)测定反应过程中溶液的pH,所得数据如下:
加入稀盐酸的质量/g
60.0
80.0
100.0
120.0
烧杯中溶液的pH
13.7
13.3
7.0
0.7
(1)恰好完全反应时,消耗稀盐酸的质量为______________g。
(2)求该KOH溶液中溶质的质量分数(结果精确到0.1%)。
8:(2018四川乐山中考)将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2mL水中(ρ水=1g/cm3),向所得溶液中滴加质量分数为14.2%的NaSO4溶液,至恰好完全反应。下图是所加NaSO4溶液质量与生成沉淀质量的关系图,计算:
(1)生成沉淀的质量是__________?
(2)所得溶液中溶质的质量分数为____________?
9:(2020甘肃天水)将氯化钠和氯化镁的固体混合物30g放入烧杯中,加入245.6g水使其完全溶解,再加入一定质量分数的氢氧化钠溶液,反应过程中滴加氢氧化钠溶液的质量与生成沉淀的质量关系如图所示。请计算;
(1)m的值为
;
(2)恰好完全反应时,消耗氢氧化钠的质量
克;
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数(写出具体计算过程)。
10:(2020辽宁抚顺)取6.5g锌粒放入烧杯中,向其中加入稀硫酸至恰好完全反应,共用去稀硫酸的质量为50g。请计算:稀硫酸中溶质的质量分数。
11:(2020年贵州遵义中考)欲测定一瓶标签破损的稀硫酸的溶质质量分数,现取30g稀硫酸样品于烧杯中,将15%的NaOH溶液逐滴加入烧杯中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示:
回答下列问题:
(1)a点溶液中的溶质是_____
(填化学式)。
(2)计算该稀硫酸的溶质质量分数。(
写出计算过程,结果精确到0.1%)
12:(2020年乐山中考)实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末,烧杯中现有100g碳酸钠溶液,将140g氯化钙溶液分四次加入,充分反应,注:发生反应的化学方程式为,四次测量所得数据如表所示:
次数
累计加入氯化钙溶液的质量/g
烧杯中溶液的总质量/g
一
40
135
二
80
170
三
120
205
四
140
225
(1)恰好完全反应时,生成沉淀的总质量为
g。
(2)第四次测量时,所得溶液中的溶质有
(填化学式)。
(3)计算氯化钙溶液的溶质质量分数(写出计算过程,计算结果保留到0.1%)
13:(2020年江西中考)“二氧化碳的实验室制取与性质”实验活动产生的废液中含稀盐酸,需先测定其溶质质量分数后进行处理。(杂质不参加反应)
(1)实验时需配制50g5%的氢氧化钠溶液,若用氢氧化钠固体和水来配制,则需称量氢氧化钠固体的质量为_____g。
(2)取20g废液样品于烧杯中,向其中逐滴加入5%的氢氧化钠溶液,恰好完全反应时共消耗氢氧化钠溶液16g。计算废液中盐酸的溶质质量分数。(写出计算过程)
(3)恰好完全反应时烧杯中的溶液所含粒子数目关系:Na+_____Cl-。(填“>”、“=”或“<”)
14:(2020年黑龙江牡丹江中考)为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:
(1)这种贝壳中碳酸钙的质量分数是__________
(2)25g贝壳与稀盐酸恰好完全反应时,生成二氧化碳的质量为多少?(写出计算步骤)
(3)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。
15:(2020辽宁辽阳)称取5g含杂质的氢氧化钙固体样品放入烧杯中,向烧杯中加入50g溶质的质量分数为7.3%的稀盐酸(假设杂质不与稀盐酸反应),二者恰好完全反应。请计算:固体样品中氢氧化钙的质量分数。
答案与解析
典例剖析:
例1:
(2020年河北中考)某小组用粗锌测定某稀硫酸中溶质的质量分数。取一定质量的稀硫酸于烧杯中,称量稀硫酸和烧杯的总质量;然后,向其中分两次加入粗锌(杂质不参加反应),实验过程和数据如图所示。请计算:
(1)生成氢气的总质量为
g。
(2)稀硫酸中溶质的质量分数。
【答案】(1)0.2g;(2)9.8%
【解析】(1)由图可知,先加入8g粗锌,反应后,天平显示的质量是213.4g,再加入2g粗锌,天平显示的质量是215.4g,故第一次加入8g粗锌,已经完全反应。生成氢气的总质量为:205.6g+8g-213.4g=0.2g;
(2)解:设稀硫酸中溶质的质量分数为x
加入稀硫酸的质量为:205.6g-105.6g=100g;
x=9.8%
答:稀硫酸中溶质的质量分数为9.8%。
例2:(2020年广元中考)某兴趣小组同学将100g氢氧化钠溶液分五次加入到139.6g硫酸铜溶液中,测得实验数据如下表所示:
?
第一次
第二次
第三次
第四次
第五次
氢氧化钠溶液的质量/g
20
20
20
20
20
沉淀质量/g
4.9
9.8
m
19.6
19.6
(1)表格中m的值为多少。
(2)计算恰好完全反应时所得溶液中溶质的质量分数。(写出计算过程)
【答案】(1)14.7g;(2)14.2%
【解析】(1)由表中数据可知,第一次加入20g氢氧化钠溶液,产生4.9g沉淀,第二次加入20g氢氧化钠溶液,共产生9.8g沉淀,第四次加入20g氢氧化钠溶液,共产生19.6g沉淀,由此可得出,每加入20g氢氧化钠溶液,产生4.9g沉淀,故m=4.9g×3=14.7g;
(2)由表中数据可知,当加入80g氢氧化钠溶液时,氢氧化钠与硫酸铜恰好完全反应,这时生成氢氧化铜沉淀的质量为19.6g。设恰好完全反应时,生成硫酸钠的质量为x。
x=28.4g
恰好完全反应时所得溶液中溶质的质量分数为:
答:恰好完全反应时所得溶液中溶质的质量分数为14.2%。
例3:(2019河北中考试题)为测定某
CuSO4溶液中溶质的质量分数,取150gCuSO4溶液,平均分为三份,每份样品均按如图所示进行实验,实验数据见表。请计算:
(1)
溶液完全反应时,所得沉淀的质量为
g
。
(2)CuSO4溶液中溶质的质量分数。
【答案】(1)4.9
(2)16%。
【解析】(1)由表可知,实验2和实验3中生成沉淀的质量相同,说明硫酸铜已经完全反应,所以当
完全反应时,沉淀的质量为44.9g—40g=4.9g
。
(2)设硫酸铜的质量为x
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
160
98
X
4.9g
则160g/x=98/4.9g可解得:x=8g,则CuSO4溶液中溶质的质量分数为:(8g/50g)×100%=16%.
答:CuSO4溶液中溶质的质量分数为16%。
例4:(2020年黑龙江齐齐哈尔中考)合金是重要的金属材料,常用来制造机械零件、仪表和日用品。某化学研究小组利用黄铜(铜、锌合金)进行了下图所示实验:
请计算:
(1)生成氢气的质量为多少g,黄铜中锌的质量为多少g。
(2)过滤后所得溶液的溶质质量分数。
【答案】0.2;6.5;16.1%
【解析】(1)根据质量守恒定律,加入稀硫酸恰好完全反应后,烧杯内物质总质量减少质量即为生成氢气的质量,故生成氢气的质量为10g+93.7g-103.5g=0.2g;设黄铜中锌的质量为x,则
解得x=6.5g;故黄铜中锌的质量为6.5g。
(2)样品中锌与加入的稀硫酸恰好完全反应,设生成硫酸锌的质量为y,则
解得y=16.1g;根据质量守恒定律,所得溶液质量为6.5g+93.7g-0.2g=100g,故过滤后所得溶液的溶质质量分数为。
例5:(2020年自贡中考)取一定量铜粉、铁粉的混合物,加入过量稀硫酸,完全反应(酸溶)后过滤,将滤渣洗净、烘干后在足量氧气中充分灼烧(金属元素在产物中显+2价)。固体质量与各步实验的时间关系如图。
(1)b点时溶液中溶质的化学式为
。(2)原粉状混合物中铁粉的质量为多少克。(3)求m的值。(写出计算过程)
【答案】(1)H2SO4、FeSO4;(2)2.6g;(3)2.0g
【解析】(1)铁和稀硫酸反应生成硫酸亚铁和氢气,铜不和稀硫酸反应,b点时铁恰好和稀硫酸反应,硫酸过量,溶液中溶质为硫酸和硫酸亚铁,化学式为:H2SO4、FeSO4;
(2)铜不和稀硫酸反应,剩余1.6g固体为铜,则原粉状混合物中铁粉的质量为:4.2g-1.6g=2.6g;
(3)滤渣是铜,洗涤、烘干、灼烧后生成氧化铜,m为生成氧化铜的质量;
,,解得:m=2.0g。
例6:(2018?枣庄)往100g硫酸和硫酸铜的混合液中,逐滴加入8%的氢氧化钠溶液直至过量,根据实验事实绘制了如图所示曲线,分析并计算:
(1)a→b段表示氢氧化钠与混合物中的
发生反应。
(2)求反应前混合液中硫酸铜的质量分数。(写出计算过程)
【答案】(1)硫酸
(2)16%。
【解析】(1)根据溶质的变化可以看出,ab段是硫酸和氢氧化钠的反应,所以a→b段表示氢氧化钠与混合物中的硫酸发生反应。(2)根据图,可以看出与硫酸铜反应的氢氧化钠溶液的质量为150g﹣50g=100g。
设反应前混合液中硫酸铜的质量分数为x。
2NaOH+CuSO4=Na2SO4+Cu(OH)2↓
80
160
8%×100g
100gx
=
x=16%
答:(1)a→b段表示氢氧化钠与混合物中的
硫酸发生反应。(2)反应前混合液中硫酸铜的质量分数为16%。
例7:(2019天水中考)某化学兴趣小组的同学取氢氧化钠和碳酸钠的混合溶液50g装入烧杯中,每次滴加50g稀盐酸充分反应。测得部分数据及图象如下:
次数
1
2
3
4
5
加入稀盐酸的质量/g
50
50
50
50
50
烧杯中物质的质量/g
100
150
197.8
245.6
295.6
请根据有关信息计算:
(1)a的数值为
。
(2)求稀盐酸中溶质的质量分数。(写出计算过程)
(3)求恰好完全反应后所得溶液中溶质的质量。(写出计算过程)
【答案】(1)4.4;(2)7.3%;
(3)23.4g。
【解析】根据质量守恒定律可得,生成的二氧化碳的质量为50g+250g295.6g=4.4g
且根据图可知,加入100g盐酸时才有二氧化碳生成,且加入第三个50g盐酸时生成的二氧化碳为2.2g,第
四个50g盐酸生成的二氧化碳的质量为2.2g,之后质量不再变化,说明碳酸钠已经完全反应。
即与碳酸钠反应的稀盐酸的质量为100g
。设稀盐酸中溶质的质量分数为x,生成的氯化钠的质量为y
Na2CO3+2HCl═2NaCl+H2O+CO2↑
73
117
44
100gx
y
4.4g
可得比例:73/100x=44/4.4g可解得:x=7.3%;同理可得比例:117/y=44/4.4g,可解得y=11.7g.根据氯元素守恒确定与氢氧化钠反应生成的氯化钠的质量与100g稀盐酸和碳酸钠反应生成的氯化钠的质量相等,所以氢氧化钠对应的氯化钠的质量也为11.7g
,所以氯化钠的总质量为11.7g+11.7g=23.4g
【点评】根据化学方程式计算时,第一要正确书写化学方程式,第二要使用正确的数据,第三计算过程
要完整。
例8:(2020湖南长沙)为了测定某小苏打样品中碳酸氢钠的质量分数,小兰同学进行了如下实验:向盛有10g样品的烧杯中加入稀硫酸,恰好完全反应时,加入稀硫酸的质量为90g,反应后烧杯内物质的总质量为95.6g。(杂质不溶于水也不与酸发生反应)已知反应的化学方程式如下:2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O(1)该反应生成二氧化碳的质量为
g。
(2)求该样品中碳酸氢钠的质量分数(写出计算过程)。
【答案】(1)4.4;(2)84%
【解析】(1)该反应生成二氧化碳的质量为:10g+90g﹣95.6g=4.4g。故填:4.4。(2)设碳酸氢钠质量为x,
2NaHCO3+H2SO4═Na2SO4+2CO2↑+2H2O,
168
88
x
4.4g
=,
x=8.4g,
该样品中碳酸氢钠的质量分数是:×100%=84%,
答:该样品中碳酸氢钠的质量分数是84%。
例9:(2020甘肃庆阳)向盛有一定质量铁粉的烧杯中逐滴加入稀硫酸充分反应,产生气体质量与所加稀硫酸质量的关系如图所示。请根据关系图分析并计算:
(1)铁粉反应完时,产生氢气的质量为______g。
(2)原稀硫酸中溶质的质量分数______(写出计算过程)。
【答案】(1)0.08
;(2)19.6%
【解析】(1)由图可知铁粉反应完时,产生氢气的质量为
0.08g。(2)设原稀硫酸中溶质的质量分数为x
由图可知10g硫酸对应0.04g氢气生成
答:原稀硫酸中溶质的质量分数为19.6%。
例10:(2018?泰安)厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如图所示。
计算:该食用碱中碳酸钠的质量分数是多少?(计算结果精确至0.1%)
【答案】88.3%
【解析】生成碳酸钙沉淀的质量为5.0g,设该食用碱中碳酸钠的质量分数为x
CaCl2+Na2CO3═CaCO3↓+2NaCl
106
100
6.0gx
5.0g
=
可解得:x≈88.3%
答:该食用碱中碳酸钠的质量分数为88.3%。
考点专练
1:(2020贵州黔西南)实验室用68g过氧化氢溶液和2g二氧化锰制取氧气,实验中非气态物质的总质量随时间变化如图所示。回答下列问题:
(1)反应中二氧化锰的作用是______。(2)计算过氧化氢溶液中溶质的质量分数。写出计算过程
【答案】(1)催化作用;(2)10%
【解析】(1)过氧化氢在二氧化锰催化作用下生成水和氧气,故反应中二氧化锰的作用是催化作用。(2)根据质量守恒定律,反应前后反应物的总质量等于生成物的总质量,减少的是生成沉淀或气体的质量,故反应产生氧气的质量是。
设产生3.2g氧气需要的质量为x
故过氧化氢溶液的溶质质量分数为。答:过氧化氢溶液的质量分数是。
2:(2018?滨州)镁在国产大飞机C﹣919”的制造中大显身手,小亮在实验室模拟“海水制镁”的原理来富集镁,他将25g氯化钠和氯化镁的固体混合物全部溶解于盛有70g水的烧杯中,然后向其中加入63.6g氢氧化钠溶液至恰好完全反应(图象如图),过滤,称量滤液质量为147g,求:
(1)图象中m=
g。
(2)滤液中溶质的质量分数是多少?
【答案】(1)11.6
(2)20%。
【解析】(1)图象中m=25g+70g+63.6g﹣147g=11.6g。
(2)设氯化镁质量为x,反应生成氯化钠质量为y,
MgCl2+2NaOH=2NaCl+Mg(OH)2↓,
95
117
58
x
y
11.6g
=
=,可解得:x=19g,y=23.4g,滤液中溶质的质量分数是:×100%=20%,答:滤液中溶质的质量分数是20%。
3:(2020陕西省卷)为测定某赤铁矿中Fe2O3的含量,取10g该赤铁矿样品于烧杯中,向其中加入100g盐酸,恰好完全反应,测得剩余固体的质量为2g。(杂质不溶于水也不与酸反应)
请完成下列分析及计算:
(1)10g样品中杂质的质量为
g。
(2)计算稀盐酸中溶质的质量分数。
【答案】(1)2;(2)10.95%
【解析】(1)根据题意,赤铁矿石中的杂质既不溶于水也不与盐酸反应,剩余固体(即杂质)的质量为2g,氧化铁的质量是10g-2g=8g;(2)根据氧化铁与盐酸反应的化学方程式,由反应消耗氧化铁的质量计算出参加反应的HCl的质量,进而计算出盐酸的溶质质量分数。设100g稀盐酸中溶质的质量为x。
x=10.95g
稀盐酸中溶质的质量分数=(其它合理的解法均照上述标准给分)
答:稀盐酸中溶质的质量分数10.95%。
4:(2018?临沂)请你仔细分析如图所示的实验过程和提供的数据,并进行计算。
(1)生成氢气
g。
(2)反应后所得溶液中溶质的质量分数是多少?(写出计算过程,精确到0.1%)。
【答案】(1)0.4
(2)12.7%。
【解析】(1)设消耗11.2g铁生成的氯化亚铁的质量为x,生成的氢气的质量为y。
Fe+2HCl═FeCl2+H2↑,
56
127
2
11.2g
x
y
可解得:x=25.4g,y=0.4g
,反应后所得溶液中溶质的质量分数是×100%=12.7%,
答:(1)生成氢气0.4g,(2)反应后所得溶液中溶质的质量分数是12.7%。
5:(2020天津市)为测定某石灰石样品中碳酸钙的质量分数,取25g该样品(杂质不参加反应也不溶于水),加入盛有146g稀盐酸的烧杯中,恰好完全反应,气体全部逸出,反应后烧杯内物质的总质量为162.2g。计算:(1)生成二氧化碳的质量;
(2)石灰石样品中碳酸钙的质量分数;
(3)反应后所得溶液中溶质的质量分数(结果精确至0.1%)。
【答案】(1)8.8g
;(2)80%;(3)14.1%
【解析】(1)由质量守恒定律可知,反应物的总质量等于生成物的总质量,减少的是生成沉淀或气体的质量,故生成的二氧化碳的质量为。
(2)设原样品中碳酸钙的质量为x,生成氯化钙的质量为y
故石灰石样品中碳酸钙的质量分数
(3)反应后所得溶液的质量为
故反应后所得溶液中溶质的质量分数为答:生成二氧化碳的质量为8.8g;石灰石样品中碳酸钙的质量分数为80%;反应后所得溶液中溶质的质量分数为14.1%。
6:(2020甘肃金昌)某中学化学兴趣小组为测定某石灰石样品(杂质不溶于水,也不与酸反应)中碳酸钙的质量分数,进行如图所示的实验。根据以下信息计算:
(1)生成二氧化碳的质量为 g;
(2)样品中碳酸钙的质量分数是多少?
(3)C烧杯中溶液的溶质的质量分数是多少?
【答案】(1)4.4;(2)80.0%
;(3)10.5%
【解析】(1)生成的二氧化碳的质量:12.5g+50g+50g﹣108.1g=4.4g;
(2)设碳酸钙的质量为x,生成氯化钙的质量为y,
,x=10g
,y=11.1
样品中碳酸钙的质量分数为:×100%=80.0%;
(3)C烧杯中溶液中溶质的质量分数为:×100%≈10.5%。
7:(2020广西北部湾)常温下,向盛有100.0gKOH溶液的烧杯中逐滴加入120.0g质量分数为7.3%的稀盐酸,用pH计(精确测定溶液pH的仪器)测定反应过程中溶液的pH,所得数据如下:
加入稀盐酸的质量/g
60.0
80.0
100.0
120.0
烧杯中溶液的pH
13.7
13.3
7.0
0.7
(1)恰好完全反应时,消耗稀盐酸的质量为______________g。
(2)求该KOH溶液中溶质的质量分数(结果精确到0.1%)。
【答案】(1)100.0;(2)11.2%
【解析】(1)pH=7,表示恰好完全反应,此时消耗稀盐酸的质量为100.0g,故填:100.0。(2)解:恰好完全反应时,消耗的稀盐酸中溶质的质量设反应消耗KOH的质量为x
该KOH溶液中溶质的质量分数为:
答:该KOH溶液中溶质的质量分数为11.2%。
8:(2018四川乐山中考)将29.1g由NaCl和BaCl2组成的固体混合物溶解于94.2mL水中(ρ水=1g/cm3),向所得溶液中滴加质量分数为14.2%的NaSO4溶液,至恰好完全反应。下图是所加NaSO4溶液质量与生成沉淀质量的关系图,计算:
(1)生成沉淀的质量是__________?
(2)所得溶液中溶质的质量分数为____________?
【答案】
(1).
23.3g
(2).
10%
【解析】解:(1)由图可知,生成BaSO4沉淀的质量为23.3g(2)设BaCl2的质量为x,生成NaCl的质量为y
BaCl2+Na2SO4=BaSO4↓+2NaCl
208
233
117
x=20.8g,y=11.7g
,溶液的总质量=29.1g+94.2g+100g-23.3g=200g
溶质的总质量=11.7g+(29.1g-20.8g)
=20g
NaCl%=×100%=10%
答:生成沉淀23.3g,所得NaCl溶液的质量分数为10%。
9:(2020甘肃天水)将氯化钠和氯化镁的固体混合物30g放入烧杯中,加入245.6g水使其完全溶解,再加入一定质量分数的氢氧化钠溶液,反应过程中滴加氢氧化钠溶液的质量与生成沉淀的质量关系如图所示。请计算;
(1)m的值为
;
(2)恰好完全反应时,消耗氢氧化钠的质量
克;
(3)恰好完全反应时,所得不饱和溶液中溶质的质量分数(写出具体计算过程)。
【答案】(1)8.7g;(2)16g;(3)10%
【解析】(1)由图中信息可知,20g氢氧化钠溶液完全反应生成2.9g沉淀,加入氢氧化钠溶液60g以后仍然产生沉淀,说明加入60g氢氧化钠溶液时,氢氧化钠完全反应,生成氢氧化镁质量是2.9g
×3=8.7g。(2)当加入的氢氧化钠溶液质量为80克时,为恰好完全反应。设氯化镁的质量为x,氢氧化钠的质量为y,生成的氯化钠的质量为z
故恰好完全反应时,消耗氢氧化钠的质量16克。(3)溶液中氯化钠质量为,溶液质量为,故恰好完全反应时,所得不饱和溶液中溶质的质量分数为
。
答:恰好完全反应时,消耗氢氧化钠的质量16克;所得不饱和溶液中溶质的质量分数为10.0%。
10:(2020辽宁抚顺)取6.5g锌粒放入烧杯中,向其中加入稀硫酸至恰好完全反应,共用去稀硫酸的质量为50g。请计算:稀硫酸中溶质的质量分数。
【答案】19.6%
【解析】解:设稀硫酸中溶质的质量为x。
答:该稀硫酸中溶质的质量分数为19.6%。
11:(2020年贵州遵义中考)欲测定一瓶标签破损的稀硫酸的溶质质量分数,现取30g稀硫酸样品于烧杯中,将15%的NaOH溶液逐滴加入烧杯中,边加边搅拌,随着NaOH溶液的不断加入,溶液pH的变化如图所示:
回答下列问题:
(1)a点溶液中的溶质是_____
(填化学式)。
(2)计算该稀硫酸的溶质质量分数。(
写出计算过程,结果精确到0.1%)
【答案】(1)、
(2)4.9%
【解析】(1)当滴加NaOH溶液至a点时,由于溶液此时pH小于7,显酸性,也就是硫酸有剩余,此时的溶质为剩余的硫酸和生成的硫酸钠,所以溶液中的溶质的化学式为和;
(2)当pH值为7时,此时消耗的氢氧化钠溶液的质量为8g,则消耗NaOH溶液中的NaOH质量为8g×15%=1.2g,设消耗氢氧化钠1.2g时消耗的稀硫酸的溶质的质量为x,则
x=1.47g;该稀硫酸的溶质质量分数为;答:该稀硫酸的溶质质量分数为4.9%。
12:(2020年乐山中考)实验室用碳酸钠溶液与氯化钙溶液反应制取高纯度碳酸钙粉末,烧杯中现有100g碳酸钠溶液,将140g氯化钙溶液分四次加入,充分反应,注:发生反应的化学方程式为,四次测量所得数据如表所示:
次数
累计加入氯化钙溶液的质量/g
烧杯中溶液的总质量/g
一
40
135
二
80
170
三
120
205
四
140
225
(1)恰好完全反应时,生成沉淀的总质量为
g。
(2)第四次测量时,所得溶液中的溶质有
(填化学式)。
(3)计算氯化钙溶液的溶质质量分数(写出计算过程,计算结果保留到0.1%)
【答案】(1)15;(2)NaCl和CaCl2;(3)13.9%
【解析】(1)碳酸钠和氯化钙反应生成碳酸钙和氯化钠,减少的质量的即为反应生成的碳酸钙沉淀的质量,第一次测量总质量减少的质量为,第二次测量总质量减少的质量为,第三次测量总质量减少的质量为,第四次测量总质量减少的质量为,故恰好完全反应时,生成沉淀的总质量为15g。
(2)碳酸钠和氯化钙反应生成碳酸钙和氯化钠,第四次测量时,氯化钙过量,所得溶液中的溶质有生成的氯化钠和过量的氯化钙,化学式为NaCl和CaCl2。(3)设80g氯化钙溶液的溶质质量为x
氯化钙溶液的溶质质量分数为
答:(1)恰好完全反应时,生成沉淀的总质量为15g;(2)第四次测量时,所得溶液中的溶质有NaCl和CaCl2;(3)氯化钙溶液的溶质质量分数为13.9%。
13:(2020年江西中考)“二氧化碳的实验室制取与性质”实验活动产生的废液中含稀盐酸,需先测定其溶质质量分数后进行处理。(杂质不参加反应)
(1)实验时需配制50g5%的氢氧化钠溶液,若用氢氧化钠固体和水来配制,则需称量氢氧化钠固体的质量为_____g。
(2)取20g废液样品于烧杯中,向其中逐滴加入5%的氢氧化钠溶液,恰好完全反应时共消耗氢氧化钠溶液16g。计算废液中盐酸的溶质质量分数。(写出计算过程)
(3)恰好完全反应时烧杯中的溶液所含粒子数目关系:Na+_____Cl-。(填“>”、“=”或“<”)
【答案】(1)2.5;(2)3.65%(过程见解析);(3)<
【解析】(1)氢氧化钠质量:50g×5%=2.5g,故填:2.5。
(2)设:盐酸溶质质量分数为x。
答:废液中盐酸的溶质质量分数3.65%。(3)实验室用稀盐酸和石灰石或大理石制取二氧化碳,废液中还有氯化钙,故氯离子数目大于钠离子数目,故填:<。
14:(2020年黑龙江牡丹江中考)为测定某种贝壳中碳酸钙的含量,取25g贝壳,逐渐加入稀盐酸,充分反应后,测得剩余固体质量与加入稀盐酸的质量关系如图所示(已知杂质不参与反应,也不溶于水)请计算:
(1)这种贝壳中碳酸钙的质量分数是__________
(2)25g贝壳与稀盐酸恰好完全反应时,生成二氧化碳的质量为多少?(写出计算步骤)
(3)本实验是否可以用稀硫酸代替稀盐酸完成实验,并说明理由_____。
【答案】(1)80%(2)8.8g(详见解析)(3)不能,因为碳酸钙和稀硫酸反应生成微溶的硫酸钙,硫酸钙覆盖在碳酸钙的表面阻碍碳酸钙与稀硫酸的接触,导致不能继续反应,使反应慢慢停止
【解析】由图可以看固体减少了20g即碳酸钙的质量为20g,根据碳酸钙的质量和对应的化学方程式求算氯化钙和二氧化碳的质量,进而求算对应的质量分数。
(1)由图可以看出固体减少了20g,即碳酸钙的质量为20g,所以贝壳中碳酸钙的质量分数为;
(2)设恰好反应时,产生二氧化碳的质量为x
x=8.8g
(3)本实验不可以用稀硫酸代替稀盐酸完成实验,因为碳酸钙和稀硫酸反应生成微溶的硫酸钙,硫酸钙覆盖在碳酸钙的表面阻碍碳酸钙与稀硫酸的接触,导致不能继续反应,使反应慢慢停止。
15:(2020辽宁辽阳)称取5g含杂质的氢氧化钙固体样品放入烧杯中,向烧杯中加入50g溶质的质量分数为7.3%的稀盐酸(假设杂质不与稀盐酸反应),二者恰好完全反应。请计算:固体样品中氢氧化钙的质量分数。
【答案】74%
【解析】参加反应的盐酸的质量:,设氢氧化钙的质量为x。
x=3.7g
样品中氢氧化钙的质量分数:
答:固体样品中氢氧化钙的质量分数为74%。
同课章节目录
