新人教版高中化学必修第二册第七章第三节第1课时《乙醇》(22张ppt)
文档属性
| 名称 | 新人教版高中化学必修第二册第七章第三节第1课时《乙醇》(22张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 4.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-10 09:04:38 | ||
图片预览


文档简介
(共24张PPT)
第三节 乙醇与乙酸
第1课时
乙 醇
人教版(2019)高中化学必修第二册第七章
烃的衍生物:烃分子中的氢原子被其它原子或原子团所取代而衍变生成的一系列新的有机物。
官能团:决定有机化合物的化学特性的原子或原子团。
如:卤素原子( —X)硝基( — NO2)羟基( — OH)等都是官能团,烯烃中的碳碳双键也是官能团。
自学导入:
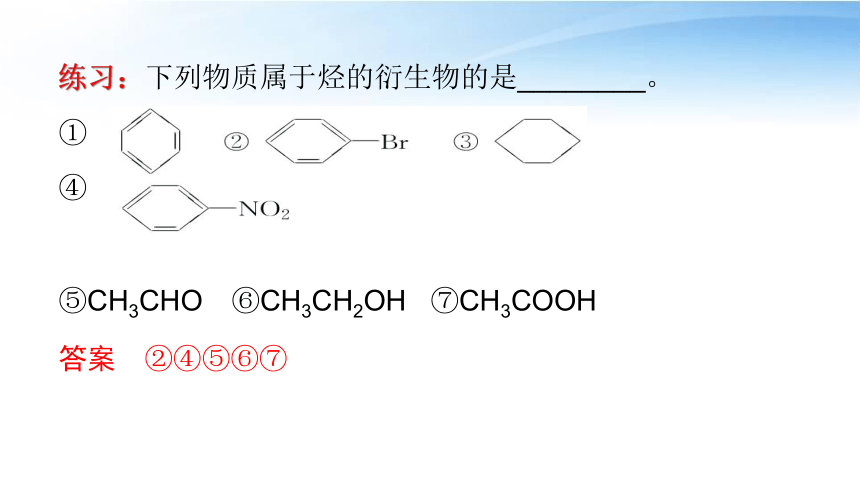
练习:下列物质属于烃的衍生物的是________。
①
④
⑤CH3CHO ⑥CH3CH2OH ⑦CH3COOH
答案 ②④⑤⑥⑦
一、乙醇的物理性质
颜 色:
气 味:
状 态:
挥发性:
熔沸点:
密 度:
溶解性:
无色透明
特殊香味
液 体
小
易挥发
低
能与水以任意比互溶,能溶解多种
有机物和无机物。
汽油、苯
I2等
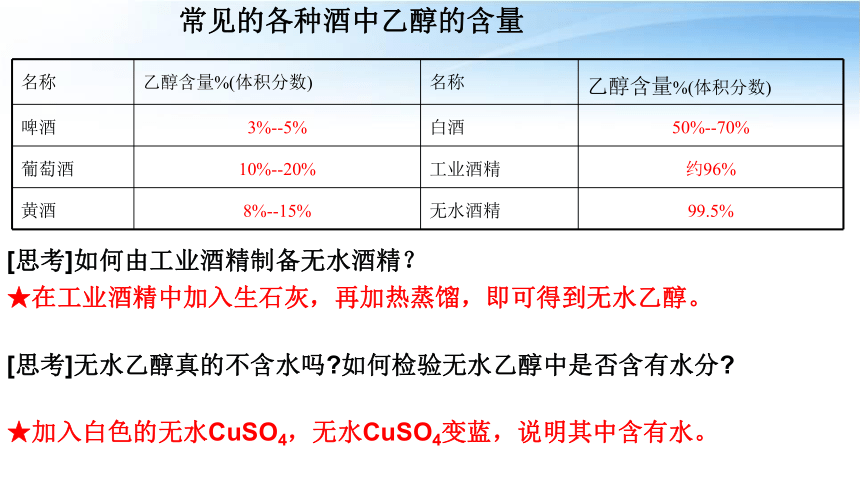
名称 乙醇含量%(体积分数) 名称 乙醇含量%(体积分数)
啤酒 3%--5% 白酒 50%--70%
葡萄酒 10%--20% 工业酒精 约96%
黄酒 8%--15% 无水酒精 99.5%
常见的各种酒中乙醇的含量
[思考]无水乙醇真的不含水吗 如何检验无水乙醇中是否含有水分
[思考]如何由工业酒精制备无水酒精?
★在工业酒精中加入生石灰,再加热蒸馏,即可得到无水乙醇。
★加入白色的无水CuSO4,无水CuSO4变蓝,说明其中含有水。
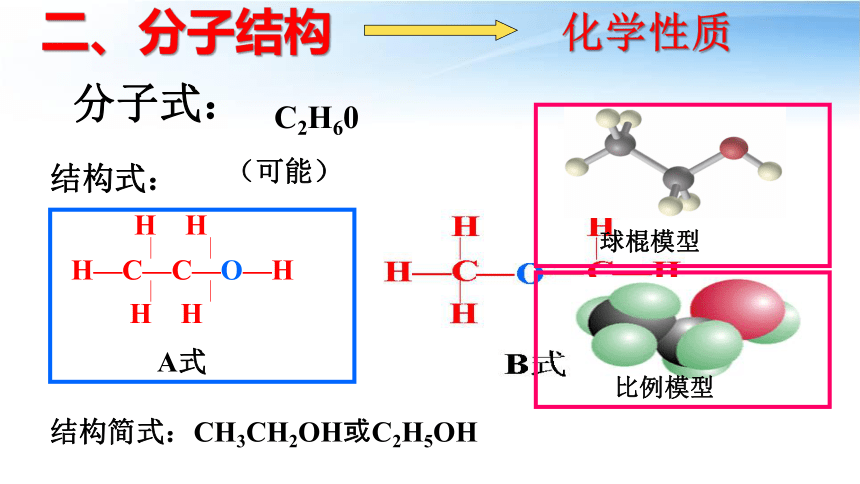
分子式:
结构式:
H—C—C—O—H
H H
H H
A式
C2H60
二、分子结构
化学性质
(可能)
结构简式:CH3CH2OH或C2H5OH
球棍模型
比例模型
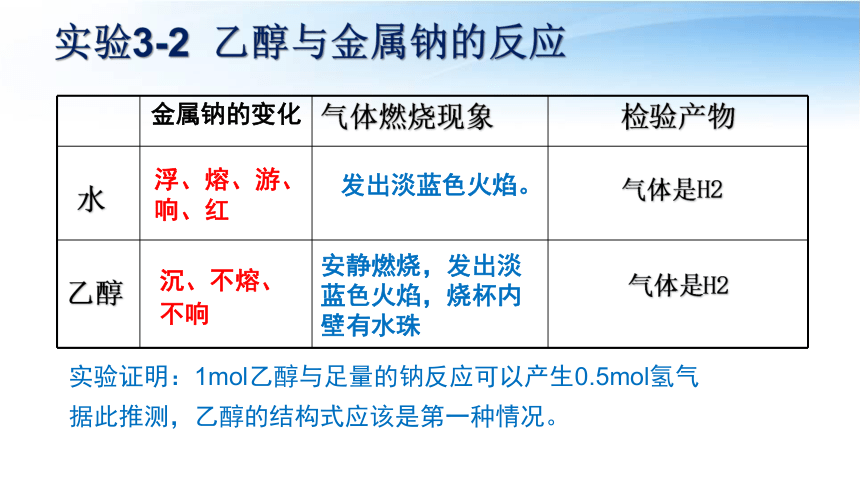
实验3-2 乙醇与金属钠的反应
金属钠的变化 气体燃烧现象 检验产物
水
乙醇
浮、熔、游、响、红
沉、不熔、不响
发出淡蓝色火焰。
安静燃烧,发出淡蓝色火焰,烧杯内壁有水珠
气体是H2
气体是H2
实验证明:1mol乙醇与足量的钠反应可以产生0.5mol氢气
据此推测,乙醇的结构式应该是第一种情况。
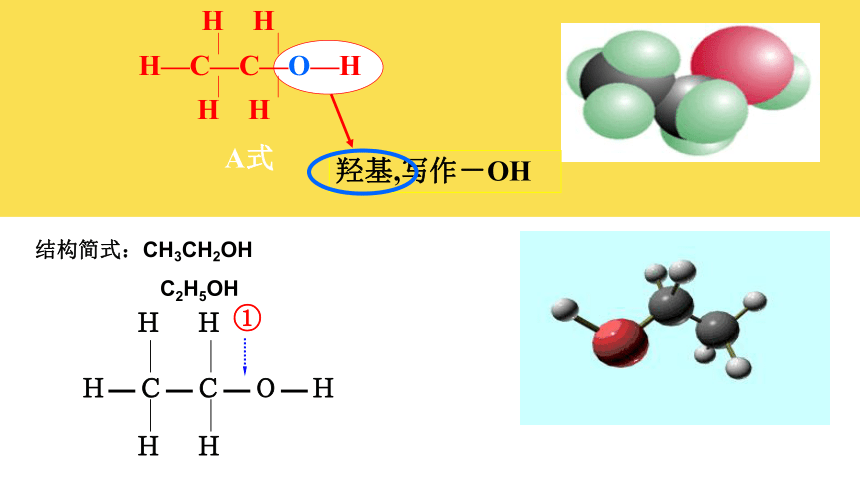
H—C—C—O—H
H H
H H
A式
羟基,写作-OH
结构简式:CH3CH2OH
C2H5OH
H―C―C―O―H
H
H
H
H
①
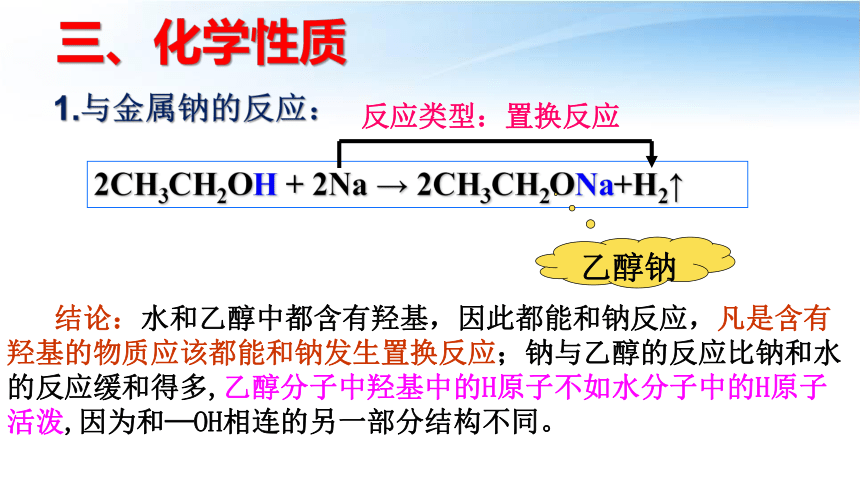
三、化学性质
2CH3CH2OH + 2Na → 2CH3CH2ONa+H2↑
1.与金属钠的反应:
乙醇钠
反应类型:置换反应
结论:水和乙醇中都含有羟基,因此都能和钠反应,凡是含有羟基的物质应该都能和钠发生置换反应;钠与乙醇的反应比钠和水的反应缓和得多,乙醇分子中羟基中的H原子不如水分子中的H原子活泼,因为和—OH相连的另一部分结构不同。
钠与乙醇和与水的反应的对比
水与钠反应 乙醇与钠反应
钠的变化 钠粒浮于水面,熔成闪亮的小球,并快速地四处游动,很快消失 钠粒开始沉于试管底部,未熔化,最终慢慢消失
声的现象 有“嘶嘶”声响 无声响
气体检验 点燃,发出淡蓝色的火焰 点燃,发出淡蓝色的火焰
2.氧化反应:
①可燃性:
C2H5OH+3O2 2CO2+3H2O
点燃
现象:发出淡蓝色火焰,并放出大量的热
〖实验现象〗 a. 铜丝红色→黑色→红色反复变化
b. 在试管口可以闻到刺激性气味 。
黑色→红色
?
H O-H
│ │
H-C-C-H
│ │
H H
Cu O
+
Cu
+
H2O
△
+
H O
│
H-C-C-H
│
H
乙醛(刺激性气味)
红色→黑色
醛基 -CHO
两个氢脱去与O结合成H2O
2Cu + O2 2CuO
?
[活动·探究](实验3-3演示)
乙醛无色、有刺激性气味液体,密度比水小,易挥发,易燃烧,与水、乙醇等互溶。
乙醇催化氧化的实质
催化剂
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu或Ag
乙醇的催化氧化,写出乙醇催化氧化的化学方程式
工业上利用此原理生产乙醛
与-OH相连的碳原子必须有H才能被氧化。
〖说明〗整个过程中,Cu丝在反应前后质量和性质都没变化,起催化剂作用,故称它为乙醇的催化氧化.
②催化氧化:
2CH3CHO+O2 2CH3COOH
催化剂
拓展练习:醇的催化氧化产物书写和条件
结论:α—C上有2个H原子的醇被氧化成醛
α—C上有1个H原子的醇被氧化成酮
α—C上没有H原子的醇不能被氧化
世界卫生组织的事故调查显示,大约50%-60%的交通事故与酒后驾驶有关。
交警判断驾驶员是否酒后驾车的方法 ?
酸性高锰
酸钾溶液
乙 醇
酸性重铬
酸钾溶液
乙 醇
身边的化学 ——酒后驾车的检查原理
CH3CH2OH CH3COOH
酸性高锰酸钾溶液
酸性重铬酸钾溶液
K2Cr2O7 Cr2(SO4)3
重铬酸钾(橙色) 硫酸铬 (绿色)
乙醇
(五)乙醇工业制法
1、发酵法
以含糖类很丰富的农产品为原料经过发酵,再进行分馏可制得乙醇。
如:
2、乙烯水化法
以乙烯为原料,以H2SO4或H3PO4作催化剂,在加热、加压下与水反应生成乙醇
(四)乙醇用途
乙醇是重要有机溶剂,还可作燃料,制饮料,作有机化工原料。
医疗上用75%酒精作消毒杀菌剂。
②
①
⑤
③
④
H―C―C―O―H
H
H
H
H
反应 断键位置
与金属钠反应
Cu或Ag催化氧化
① ③
①
乙醇的化学性质主要由官能团 ( -OH ) 羟基决定,羟基比较活泼,重点掌握乙醇的结构,与钠的反应、催化氧化反应。
课堂小结
一、乙醇的物理性质
二、乙醇的结构
三、乙醇的化学性质
反应中乙醇断键位置?
作业布置:阅读课本,完成课后习题。
同学们再见!
https://www.21cnjy.com/help/help_extract.php
第三节 乙醇与乙酸
第1课时
乙 醇
人教版(2019)高中化学必修第二册第七章
烃的衍生物:烃分子中的氢原子被其它原子或原子团所取代而衍变生成的一系列新的有机物。
官能团:决定有机化合物的化学特性的原子或原子团。
如:卤素原子( —X)硝基( — NO2)羟基( — OH)等都是官能团,烯烃中的碳碳双键也是官能团。
自学导入:
练习:下列物质属于烃的衍生物的是________。
①
④
⑤CH3CHO ⑥CH3CH2OH ⑦CH3COOH
答案 ②④⑤⑥⑦
一、乙醇的物理性质
颜 色:
气 味:
状 态:
挥发性:
熔沸点:
密 度:
溶解性:
无色透明
特殊香味
液 体
小
易挥发
低
能与水以任意比互溶,能溶解多种
有机物和无机物。
汽油、苯
I2等
名称 乙醇含量%(体积分数) 名称 乙醇含量%(体积分数)
啤酒 3%--5% 白酒 50%--70%
葡萄酒 10%--20% 工业酒精 约96%
黄酒 8%--15% 无水酒精 99.5%
常见的各种酒中乙醇的含量
[思考]无水乙醇真的不含水吗 如何检验无水乙醇中是否含有水分
[思考]如何由工业酒精制备无水酒精?
★在工业酒精中加入生石灰,再加热蒸馏,即可得到无水乙醇。
★加入白色的无水CuSO4,无水CuSO4变蓝,说明其中含有水。
分子式:
结构式:
H—C—C—O—H
H H
H H
A式
C2H60
二、分子结构
化学性质
(可能)
结构简式:CH3CH2OH或C2H5OH
球棍模型
比例模型
实验3-2 乙醇与金属钠的反应
金属钠的变化 气体燃烧现象 检验产物
水
乙醇
浮、熔、游、响、红
沉、不熔、不响
发出淡蓝色火焰。
安静燃烧,发出淡蓝色火焰,烧杯内壁有水珠
气体是H2
气体是H2
实验证明:1mol乙醇与足量的钠反应可以产生0.5mol氢气
据此推测,乙醇的结构式应该是第一种情况。
H—C—C—O—H
H H
H H
A式
羟基,写作-OH
结构简式:CH3CH2OH
C2H5OH
H―C―C―O―H
H
H
H
H
①
三、化学性质
2CH3CH2OH + 2Na → 2CH3CH2ONa+H2↑
1.与金属钠的反应:
乙醇钠
反应类型:置换反应
结论:水和乙醇中都含有羟基,因此都能和钠反应,凡是含有羟基的物质应该都能和钠发生置换反应;钠与乙醇的反应比钠和水的反应缓和得多,乙醇分子中羟基中的H原子不如水分子中的H原子活泼,因为和—OH相连的另一部分结构不同。
钠与乙醇和与水的反应的对比
水与钠反应 乙醇与钠反应
钠的变化 钠粒浮于水面,熔成闪亮的小球,并快速地四处游动,很快消失 钠粒开始沉于试管底部,未熔化,最终慢慢消失
声的现象 有“嘶嘶”声响 无声响
气体检验 点燃,发出淡蓝色的火焰 点燃,发出淡蓝色的火焰
2.氧化反应:
①可燃性:
C2H5OH+3O2 2CO2+3H2O
点燃
现象:发出淡蓝色火焰,并放出大量的热
〖实验现象〗 a. 铜丝红色→黑色→红色反复变化
b. 在试管口可以闻到刺激性气味 。
黑色→红色
?
H O-H
│ │
H-C-C-H
│ │
H H
Cu O
+
Cu
+
H2O
△
+
H O
│
H-C-C-H
│
H
乙醛(刺激性气味)
红色→黑色
醛基 -CHO
两个氢脱去与O结合成H2O
2Cu + O2 2CuO
?
[活动·探究](实验3-3演示)
乙醛无色、有刺激性气味液体,密度比水小,易挥发,易燃烧,与水、乙醇等互溶。
乙醇催化氧化的实质
催化剂
2CH3CH2OH+O2 2CH3CHO+2H2O
Cu或Ag
乙醇的催化氧化,写出乙醇催化氧化的化学方程式
工业上利用此原理生产乙醛
与-OH相连的碳原子必须有H才能被氧化。
〖说明〗整个过程中,Cu丝在反应前后质量和性质都没变化,起催化剂作用,故称它为乙醇的催化氧化.
②催化氧化:
2CH3CHO+O2 2CH3COOH
催化剂
拓展练习:醇的催化氧化产物书写和条件
结论:α—C上有2个H原子的醇被氧化成醛
α—C上有1个H原子的醇被氧化成酮
α—C上没有H原子的醇不能被氧化
世界卫生组织的事故调查显示,大约50%-60%的交通事故与酒后驾驶有关。
交警判断驾驶员是否酒后驾车的方法 ?
酸性高锰
酸钾溶液
乙 醇
酸性重铬
酸钾溶液
乙 醇
身边的化学 ——酒后驾车的检查原理
CH3CH2OH CH3COOH
酸性高锰酸钾溶液
酸性重铬酸钾溶液
K2Cr2O7 Cr2(SO4)3
重铬酸钾(橙色) 硫酸铬 (绿色)
乙醇
(五)乙醇工业制法
1、发酵法
以含糖类很丰富的农产品为原料经过发酵,再进行分馏可制得乙醇。
如:
2、乙烯水化法
以乙烯为原料,以H2SO4或H3PO4作催化剂,在加热、加压下与水反应生成乙醇
(四)乙醇用途
乙醇是重要有机溶剂,还可作燃料,制饮料,作有机化工原料。
医疗上用75%酒精作消毒杀菌剂。
②
①
⑤
③
④
H―C―C―O―H
H
H
H
H
反应 断键位置
与金属钠反应
Cu或Ag催化氧化
① ③
①
乙醇的化学性质主要由官能团 ( -OH ) 羟基决定,羟基比较活泼,重点掌握乙醇的结构,与钠的反应、催化氧化反应。
课堂小结
一、乙醇的物理性质
二、乙醇的结构
三、乙醇的化学性质
反应中乙醇断键位置?
作业布置:阅读课本,完成课后习题。
同学们再见!
https://www.21cnjy.com/help/help_extract.php
同课章节目录
- 第五章 化工生产中的重要非金属元素
- 第一节 硫及其化合物
- 第二节 氮及其化合物
- 第三节 无机非金属材料
- 实验活动4 用化学沉淀法去除粗盐中的杂质离子
- 实验活动5 不同价态含硫物质的转化
- 第六章 化学反应与能量
- 第一节 化学反应与能量变化
- 第二节 化学反应的速率与限度
- 实验活动6 化学能转化成电能
- 实验活动7 化学反应速率的影响因素
- 第七章 有机化合物
- 第一节 认识有机化合物
- 第二节 乙烯与有机高分子材料
- 第三节 乙醇与乙酸
- 第四节 基本营养物质
- 实验活动8 搭建球棍模型认识有机化合物分子结构的特点
- 实验活动9 乙醇、乙酸的主要性质
- 第八章 化学与可持续发展
- 第一节 自然资源的开发利用
- 第二节 化学品的合理使用
- 第三节 环境保护与绿色化学
