高中化学苏教版(2019)选择性必修3专题1有机化学的发展及研究思路巩固练习 含答案
文档属性
| 名称 | 高中化学苏教版(2019)选择性必修3专题1有机化学的发展及研究思路巩固练习 含答案 |
|
|
| 格式 | zip | ||
| 文件大小 | 560.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-10 00:00:00 | ||
图片预览




文档简介
2020-2021学年度第一学期高二化学苏教版(2019)选择性必修3专题1有机化学的发展及研究思路巩固练习
一、单选题
1.下列有机化学方程式中属于加成反应的是(
)
A.CH4+Cl2CH3Cl+HCl
B.CH4+2O2CO2+H2O
C.CH2=CH2+HBr→CH3CH2Br
D.+Br2+HBr
2.打破无机物和有机物界限的化学家是(
)
A.维勒
B.李比希
C.科里
D.范特霍夫
3.一定条件下能发生水解反应的有机物是(
)
A.乙醇
B.乙酸
C.油脂
D.葡萄糖
4.某有机物A用质谱仪测定如图①,核磁共振氢谱示意图如图②,则A的结构简式可能为(
)
A.CH3CH2OH
B.CH3CHO
C.HCOOH
D.CH3CH2CH2COOH
5.下列混合物能用分液法分离的是(
)
A.乙醇与乙酸
B.苯和溴苯
C.葡萄糖与果糖混合液
D.乙酸乙酯和Na2CO3溶液
6.下列物质进行核磁共振得到的核磁共振氢谱中,信号峰有4个的是(
)
A.
B.CH3CH2OCH2CH3
C.CH3CH(CH3)2
D.CH4
7.为测定某有机物的结构,用核磁共振仪处理后得到如图所示的核磁共振氢谱,则该有机物可能是(
)
A.C2H5OH
B.
C.CH3CH2CH2COOH
D.
8.某有机物完全燃烧生成CO2和H2O,将12g该有机物完全燃烧,产物通过浓硫酸,浓硫酸增重14.4g,再通过碱石灰,又增重26.4g。则该有机物的分子式为(
)
A.C4H10
B.C2H6O
C.C3H8O
D.C2H4O2
9.下列物质的核磁共振氢谱图中,吸收峰最少的是(
)
A.
B.
C.
D.
10.如图是某有机物分子的比例(填充),该有机物的分子式是(
)
A.C2H6
B.C6H6
C.C2H6O
D.C2H6O2
11.头孢克肟是第三代头孢菌素抗生素,其分子式为C16H15N5O7S2。下列有关说法不正确的是(
)
A.头孢克肟的相对分子质量是453
B.只有具备用药常识,才能避免抗生素药物的滥用
C.头孢克肟中含有的5种元素均是非金属元素
D.“OTC”药物是指处方药
12.1mol某烃在氧气中充分燃烧,需要消耗氧气179.2L(标准状况下)。它在光照的条件下与氯气反应能生成3种不同的一氯取代物。该烃的结构简式是(
)
A.
B.CH3—CH2—CH2—CH2—CH3
C.
D.
13.下列反应中,属于加成反应的是(
)
A.CH4+Cl2CH3C1+
HCI
B.2CH3CH2OH+O2
2CH3CHO+
2H2O
C.CH2=CH2+Br2
CH2Br-CH2Br
D.+HO-NO2+H2O
14.将有机物完全燃烧,生成CO2和H2O。将12g该有机物完全燃烧后的产物通过浓H2SO4,浓H2SO4增重14.4g,再通过碱石灰,碱石灰增重26.4g。该有机物分子式为(
)
A.C3H8O2
B.C2H6O
C.C3H8O
D.С3Н4O2
15.下列实验操作正确且能达到对应实验目的的是( )
A.石油的分馏
B.煤的干馏
C.除去乙烷中的乙烯
D.提纯乙酸乙酯
二、填空题
16.(1)化合物A只含C、H、N三种元素,氮的质量分数为19.7%,相对分子质量不超过100,则A的分子式为______,若A分子中含五元环结构,试用键线式表示A的结构______。
(2)无机橡胶的制取是用氯代三聚磷腈(结构类似苯)开环聚合而成,反应如下:
N(Cl2PN)3
①写出氯代三聚磷腈的结构式______
②无机橡胶中的P-Cl键对水很敏感,用有机基团取代Cl后在耐水、耐热、抗燃等性能方面会有很大改善,请写出无机橡胶与CF3-CH2-ONa反应的化学反应方程式:______。
17.某研究性学习小组为了解有机物A的性质,对A的结构进行了如下实验。
实验一:通过质谱分析仪分析得知有机物A的相对分子质量为90。
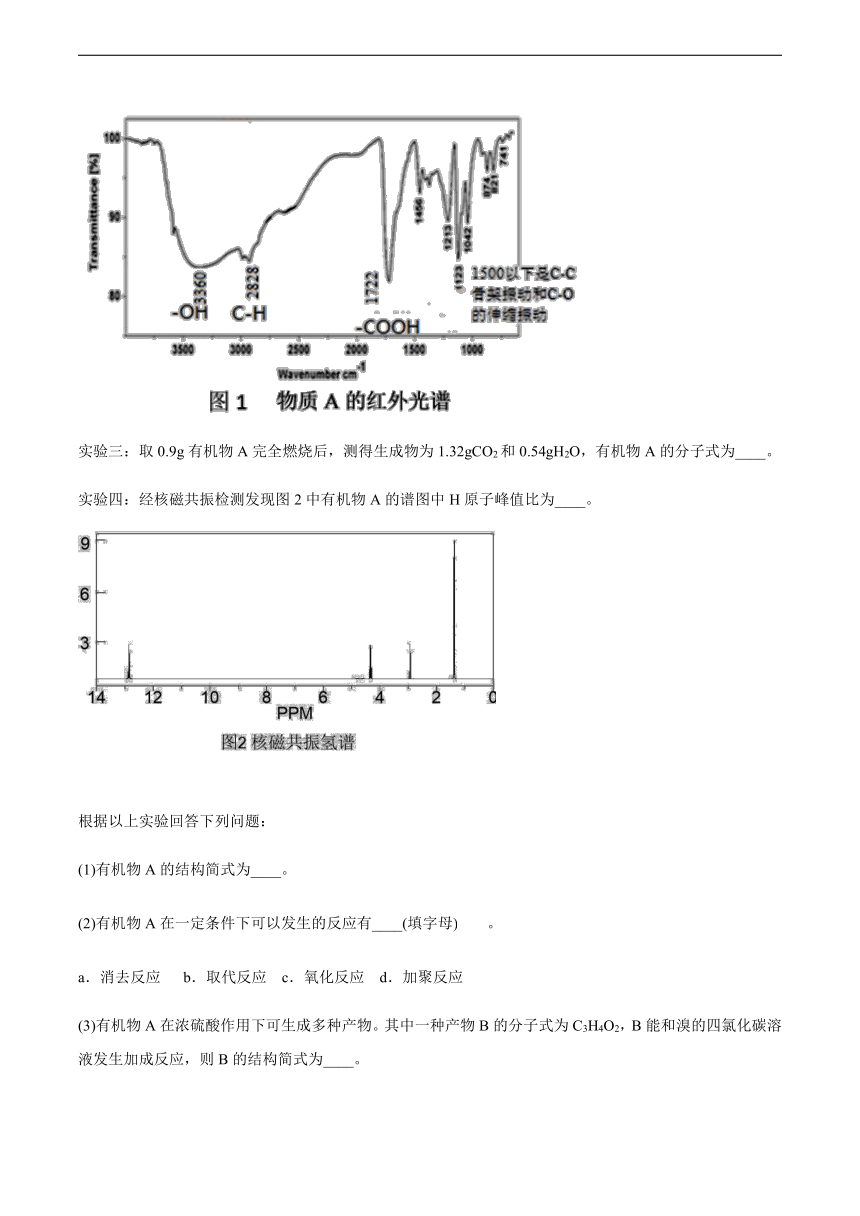
实验二:红外光谱分析:图1中不同吸收峰峰谷代表不同基团,图中有机物A中含氧官能团名称为____和____。
实验三:取0.9g有机物A完全燃烧后,测得生成物为1.32gCO2和0.54gH2O,有机物A的分子式为____。
实验四:经核磁共振检测发现图2中有机物A的谱图中H原子峰值比为____。
根据以上实验回答下列问题:
(1)有机物A的结构简式为____。
(2)有机物A在一定条件下可以发生的反应有____(填字母)。
a.消去反应
b.取代反应
c.氧化反应
d.加聚反应
(3)有机物A在浓硫酸作用下可生成多种产物。其中一种产物B的分子式为C3H4O2,B能和溴的四氯化碳溶液发生加成反应,则B的结构简式为____。
18.某研究性学习小组为确定一种从煤中提取的液态烃X的结构,对其进行探究。
步骤一:这种碳氢化合物蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和固体氢氧化钠的吸收管完全吸收。
2.12g有机物X的蒸气氧化产生7.04g二氧化碳和1.80g水;
步骤二:通过仪器分析得知X的相对分子质量为106;
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2∶3
(如图Ⅰ)
步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ,试回答:
(1)步骤二中的仪器分析方法称为
___________。
(2)X的分子式为___________;
(3)X的结构简式为___________;名称为:___________
。
19.0.2mol某烃A在氧气中充分燃烧后,生成化合物CO2、H2O各0.8mol。
(1)烃A的分子式为____________________。
(2)若取一定量的A完全燃烧后,生成CO2、H2O各2mol,则有___________g烃A参加了反应。
(3)若烃A不能使溴水褪色,则A的结构简式可能为____________________。(任写一种)
(4)若烃A能使溴水褪色,在催化剂作用下与H2加成,其加成产物分子中含有3个甲基,则A的结构简式为____________,A发生加聚反应的化学方程式为_____________。
20.为测定某有机化合物A的结构,进行如下实验:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4
g
H2O和8.8
g
CO2,消耗氧气6.72
L(标准状况下),则该物质的实验式是________。
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为__________,该物质的分子式是________。
(3)核磁共振氢谱能对有机物分子中不同化学环境的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:甲基氯甲基醚(ClCH2OCH3)有两种氢原子如图②。经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为__________。
三、综合题
21.苯甲酸广泛存在于自然界,常用于合成杀菌剂和香料等。KMnO4具有强氧化性,其氧化甲苯可生成苯甲酸钾和MnO2。已知:甲苯不溶于水;苯甲酸是一元弱酸,微溶于冷水,易溶于热水,100
℃升华。实验室制备苯甲酸的步骤如下:
步骤a:向图中所示装置中加入KMnO4、H2O和甲苯,搅拌,加热至反应完全。
步骤b:冷却片刻后,加适量饱和NaHSO3溶液,充分反应。
步骤c:趁热过滤,将滤液在冰水浴中冷却。
步骤d:加浓盐酸至苯甲酸晶体完全析出。
步骤e:过滤,洗涤,干燥。
(1)水从图中仪器A的____(填“M”或“N”)端通入,仪器A的作用是____。
(2)步骤a中反应完全的现象是____。
(3)为提高苯甲酸的产率,可以洗涤步骤c中过滤所得滤渣,并将洗涤所得液体与滤液合并。
①滤渣的主要成分是____。
②洗涤滤渣适宜选用____(填字母)。
a.冷水
b.热水
c.NaOH溶液
d.盐酸
(4)步骤d中浓盐酸的作用是____(用离子方程式表示)。
(5)步骤e中,干燥时温度过高,苯甲酸的产率会降低,其主要原因是____。
22.常温下,青蒿素是一种无色针状晶体,易溶于有机溶剂,难溶于水,熔点约为156.5℃,易受湿、热的影响而分解。某实验小组对青蒿素的提取和组成进行了探究。
Ⅰ.提取流程:
(1)“破碎”的目的是________________。
(2)
操作a和操作b的名称分别是____________、____________。
Ⅱ.燃烧法测定最简式:
实验室用如图所示装置测定青蒿素(烃的含氧衍生物)中氧元素的质量分数。
(3)
A装置是提供实验所需的O2,B装置中浓硫酸的作用是_______________;C中CuO的作用是______________________。
(4)
燃烧m
g青蒿素,图中D(装无水CaCl2)、E的质量分别增重a
g、b
g,则青蒿素中氧元素的质量分数可表示为_________(只写计算式,用含有m、a、b的符号来表示,可不化简)。
(5)该装置也可以用来测其他有机物的最简式。
准确称取9.0
g某烃的含氧衍生物X的样品,经充分燃烧后,D管质量增加9.0g,E管质量增加17.6
g,则该有机物的实验式是_______,能不能确定分子式
___________(能确定写出分子式,不能确定填“否”)
23.某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90,有C-O键、C=O键、C-H键、O-H键,核磁共振氢谱图有四种类型的氢原子,峰面积之比为3:1:1:1。取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g。试求:
(1)该有机物的分子式____
(2)该有机物的结构简式_____
24.某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352g,置于铂舟并放入燃烧管中,不断通入氧气流.用酒精喷灯持续加热样品,将生成物先后通过浓硫酸和碱石灰,两者分别增重0.144g和0.528g,生成物完全被吸收.试回答以下问题:
(1)维生素C中碳的质量分数是______,氢的质量分数______
(2)维生素中是否含有氧元素?为什么?(试通过计算说明)______________
参考答案
1.C2.A3.C4.A5.D6.A7.A8.C9.A10.B11.D12.B13.C14.C15.C
16.C4H9N
+6nCF3CH2ONa+6
nNaCl
17.羟基
羧基
C3H6O3
3:1:1:1
abc
CH2=CHCOOH
18.质谱法
X的分子式为C8H10
对二甲苯(或者
1,4-二甲苯)
19.C4H8
28
n→
20.C2H6O
46
C2H6O
CH3CH2OH
21.M
冷凝回流,防止甲苯的挥发而降低产品产率
回流液无油珠
MnO2
b
C6H5COO-+H+→C6H5COOH
苯甲酸升华而损失
22.增大青蒿与乙醚的接触面积,提高青蒿素的浸取率
过滤
蒸馏
吸收水蒸气,干燥氧气
使有机物完全氧化或使有机物完全燃烧生成CO2
×100%
C2H5O
C4H10O2
23.C3H6O3
CH2(OH)CH2COOH
24.40.9%
4.5%
含有维生素中一定含有氧元素,因为C、H元素的质量之和小于维生素的质量
一、单选题
1.下列有机化学方程式中属于加成反应的是(
)
A.CH4+Cl2CH3Cl+HCl
B.CH4+2O2CO2+H2O
C.CH2=CH2+HBr→CH3CH2Br
D.+Br2+HBr
2.打破无机物和有机物界限的化学家是(
)
A.维勒
B.李比希
C.科里
D.范特霍夫
3.一定条件下能发生水解反应的有机物是(
)
A.乙醇
B.乙酸
C.油脂
D.葡萄糖
4.某有机物A用质谱仪测定如图①,核磁共振氢谱示意图如图②,则A的结构简式可能为(
)
A.CH3CH2OH
B.CH3CHO
C.HCOOH
D.CH3CH2CH2COOH
5.下列混合物能用分液法分离的是(
)
A.乙醇与乙酸
B.苯和溴苯
C.葡萄糖与果糖混合液
D.乙酸乙酯和Na2CO3溶液
6.下列物质进行核磁共振得到的核磁共振氢谱中,信号峰有4个的是(
)
A.
B.CH3CH2OCH2CH3
C.CH3CH(CH3)2
D.CH4
7.为测定某有机物的结构,用核磁共振仪处理后得到如图所示的核磁共振氢谱,则该有机物可能是(
)
A.C2H5OH
B.
C.CH3CH2CH2COOH
D.
8.某有机物完全燃烧生成CO2和H2O,将12g该有机物完全燃烧,产物通过浓硫酸,浓硫酸增重14.4g,再通过碱石灰,又增重26.4g。则该有机物的分子式为(
)
A.C4H10
B.C2H6O
C.C3H8O
D.C2H4O2
9.下列物质的核磁共振氢谱图中,吸收峰最少的是(
)
A.
B.
C.
D.
10.如图是某有机物分子的比例(填充),该有机物的分子式是(
)
A.C2H6
B.C6H6
C.C2H6O
D.C2H6O2
11.头孢克肟是第三代头孢菌素抗生素,其分子式为C16H15N5O7S2。下列有关说法不正确的是(
)
A.头孢克肟的相对分子质量是453
B.只有具备用药常识,才能避免抗生素药物的滥用
C.头孢克肟中含有的5种元素均是非金属元素
D.“OTC”药物是指处方药
12.1mol某烃在氧气中充分燃烧,需要消耗氧气179.2L(标准状况下)。它在光照的条件下与氯气反应能生成3种不同的一氯取代物。该烃的结构简式是(
)
A.
B.CH3—CH2—CH2—CH2—CH3
C.
D.
13.下列反应中,属于加成反应的是(
)
A.CH4+Cl2CH3C1+
HCI
B.2CH3CH2OH+O2
2CH3CHO+
2H2O
C.CH2=CH2+Br2
CH2Br-CH2Br
D.+HO-NO2+H2O
14.将有机物完全燃烧,生成CO2和H2O。将12g该有机物完全燃烧后的产物通过浓H2SO4,浓H2SO4增重14.4g,再通过碱石灰,碱石灰增重26.4g。该有机物分子式为(
)
A.C3H8O2
B.C2H6O
C.C3H8O
D.С3Н4O2
15.下列实验操作正确且能达到对应实验目的的是( )
A.石油的分馏
B.煤的干馏
C.除去乙烷中的乙烯
D.提纯乙酸乙酯
二、填空题
16.(1)化合物A只含C、H、N三种元素,氮的质量分数为19.7%,相对分子质量不超过100,则A的分子式为______,若A分子中含五元环结构,试用键线式表示A的结构______。
(2)无机橡胶的制取是用氯代三聚磷腈(结构类似苯)开环聚合而成,反应如下:
N(Cl2PN)3
①写出氯代三聚磷腈的结构式______
②无机橡胶中的P-Cl键对水很敏感,用有机基团取代Cl后在耐水、耐热、抗燃等性能方面会有很大改善,请写出无机橡胶与CF3-CH2-ONa反应的化学反应方程式:______。
17.某研究性学习小组为了解有机物A的性质,对A的结构进行了如下实验。
实验一:通过质谱分析仪分析得知有机物A的相对分子质量为90。
实验二:红外光谱分析:图1中不同吸收峰峰谷代表不同基团,图中有机物A中含氧官能团名称为____和____。
实验三:取0.9g有机物A完全燃烧后,测得生成物为1.32gCO2和0.54gH2O,有机物A的分子式为____。
实验四:经核磁共振检测发现图2中有机物A的谱图中H原子峰值比为____。
根据以上实验回答下列问题:
(1)有机物A的结构简式为____。
(2)有机物A在一定条件下可以发生的反应有____(填字母)。
a.消去反应
b.取代反应
c.氧化反应
d.加聚反应
(3)有机物A在浓硫酸作用下可生成多种产物。其中一种产物B的分子式为C3H4O2,B能和溴的四氯化碳溶液发生加成反应,则B的结构简式为____。
18.某研究性学习小组为确定一种从煤中提取的液态烃X的结构,对其进行探究。
步骤一:这种碳氢化合物蒸气通过热的氧化铜(催化剂),氧化成二氧化碳和水,再用装有无水氯化钙和固体氢氧化钠的吸收管完全吸收。
2.12g有机物X的蒸气氧化产生7.04g二氧化碳和1.80g水;
步骤二:通过仪器分析得知X的相对分子质量为106;
步骤三:用核磁共振仪测出X的1H核磁共振谱有2个峰,其面积之比为2∶3
(如图Ⅰ)
步骤四:利用红外光谱仪测得X分子的红外光谱如图Ⅱ,试回答:
(1)步骤二中的仪器分析方法称为
___________。
(2)X的分子式为___________;
(3)X的结构简式为___________;名称为:___________
。
19.0.2mol某烃A在氧气中充分燃烧后,生成化合物CO2、H2O各0.8mol。
(1)烃A的分子式为____________________。
(2)若取一定量的A完全燃烧后,生成CO2、H2O各2mol,则有___________g烃A参加了反应。
(3)若烃A不能使溴水褪色,则A的结构简式可能为____________________。(任写一种)
(4)若烃A能使溴水褪色,在催化剂作用下与H2加成,其加成产物分子中含有3个甲基,则A的结构简式为____________,A发生加聚反应的化学方程式为_____________。
20.为测定某有机化合物A的结构,进行如下实验:
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4
g
H2O和8.8
g
CO2,消耗氧气6.72
L(标准状况下),则该物质的实验式是________。
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为__________,该物质的分子式是________。
(3)核磁共振氢谱能对有机物分子中不同化学环境的氢原子给出不同的峰值(信号),根据峰值(信号)可以确定分子中氢原子的种类和数目。例如:甲基氯甲基醚(ClCH2OCH3)有两种氢原子如图②。经测定,有机物A的核磁共振氢谱示意图如图③,则A的结构简式为__________。
三、综合题
21.苯甲酸广泛存在于自然界,常用于合成杀菌剂和香料等。KMnO4具有强氧化性,其氧化甲苯可生成苯甲酸钾和MnO2。已知:甲苯不溶于水;苯甲酸是一元弱酸,微溶于冷水,易溶于热水,100
℃升华。实验室制备苯甲酸的步骤如下:
步骤a:向图中所示装置中加入KMnO4、H2O和甲苯,搅拌,加热至反应完全。
步骤b:冷却片刻后,加适量饱和NaHSO3溶液,充分反应。
步骤c:趁热过滤,将滤液在冰水浴中冷却。
步骤d:加浓盐酸至苯甲酸晶体完全析出。
步骤e:过滤,洗涤,干燥。
(1)水从图中仪器A的____(填“M”或“N”)端通入,仪器A的作用是____。
(2)步骤a中反应完全的现象是____。
(3)为提高苯甲酸的产率,可以洗涤步骤c中过滤所得滤渣,并将洗涤所得液体与滤液合并。
①滤渣的主要成分是____。
②洗涤滤渣适宜选用____(填字母)。
a.冷水
b.热水
c.NaOH溶液
d.盐酸
(4)步骤d中浓盐酸的作用是____(用离子方程式表示)。
(5)步骤e中,干燥时温度过高,苯甲酸的产率会降低,其主要原因是____。
22.常温下,青蒿素是一种无色针状晶体,易溶于有机溶剂,难溶于水,熔点约为156.5℃,易受湿、热的影响而分解。某实验小组对青蒿素的提取和组成进行了探究。
Ⅰ.提取流程:
(1)“破碎”的目的是________________。
(2)
操作a和操作b的名称分别是____________、____________。
Ⅱ.燃烧法测定最简式:
实验室用如图所示装置测定青蒿素(烃的含氧衍生物)中氧元素的质量分数。
(3)
A装置是提供实验所需的O2,B装置中浓硫酸的作用是_______________;C中CuO的作用是______________________。
(4)
燃烧m
g青蒿素,图中D(装无水CaCl2)、E的质量分别增重a
g、b
g,则青蒿素中氧元素的质量分数可表示为_________(只写计算式,用含有m、a、b的符号来表示,可不化简)。
(5)该装置也可以用来测其他有机物的最简式。
准确称取9.0
g某烃的含氧衍生物X的样品,经充分燃烧后,D管质量增加9.0g,E管质量增加17.6
g,则该有机物的实验式是_______,能不能确定分子式
___________(能确定写出分子式,不能确定填“否”)
23.某仅由碳、氢、氧三种元素组成的有机化合物,经测定其相对分子质量为90,有C-O键、C=O键、C-H键、O-H键,核磁共振氢谱图有四种类型的氢原子,峰面积之比为3:1:1:1。取有机物样品1.8g,在纯氧中完全燃烧,将产物先后通过浓硫酸和碱石灰,两者分别增重1.08g和2.64g。试求:
(1)该有机物的分子式____
(2)该有机物的结构简式_____
24.某同学为测定维生素C中碳、氢的质量分数,取维生素C样品研碎,称取该试样0.352g,置于铂舟并放入燃烧管中,不断通入氧气流.用酒精喷灯持续加热样品,将生成物先后通过浓硫酸和碱石灰,两者分别增重0.144g和0.528g,生成物完全被吸收.试回答以下问题:
(1)维生素C中碳的质量分数是______,氢的质量分数______
(2)维生素中是否含有氧元素?为什么?(试通过计算说明)______________
参考答案
1.C2.A3.C4.A5.D6.A7.A8.C9.A10.B11.D12.B13.C14.C15.C
16.C4H9N
+6nCF3CH2ONa+6
nNaCl
17.羟基
羧基
C3H6O3
3:1:1:1
abc
CH2=CHCOOH
18.质谱法
X的分子式为C8H10
对二甲苯(或者
1,4-二甲苯)
19.C4H8
28
n→
20.C2H6O
46
C2H6O
CH3CH2OH
21.M
冷凝回流,防止甲苯的挥发而降低产品产率
回流液无油珠
MnO2
b
C6H5COO-+H+→C6H5COOH
苯甲酸升华而损失
22.增大青蒿与乙醚的接触面积,提高青蒿素的浸取率
过滤
蒸馏
吸收水蒸气,干燥氧气
使有机物完全氧化或使有机物完全燃烧生成CO2
×100%
C2H5O
C4H10O2
23.C3H6O3
CH2(OH)CH2COOH
24.40.9%
4.5%
含有维生素中一定含有氧元素,因为C、H元素的质量之和小于维生素的质量
