课件精讲03 回归课本核心实验-2021高考化学考前30天之回归课本 (52张ppt)
文档属性
| 名称 | 课件精讲03 回归课本核心实验-2021高考化学考前30天之回归课本 (52张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 4.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-11 00:00:00 | ||
图片预览









文档简介
(共52张PPT)
03-回归课本核心实验
2021高考三轮复习之回归课本
类型1 化学实验基础
1.
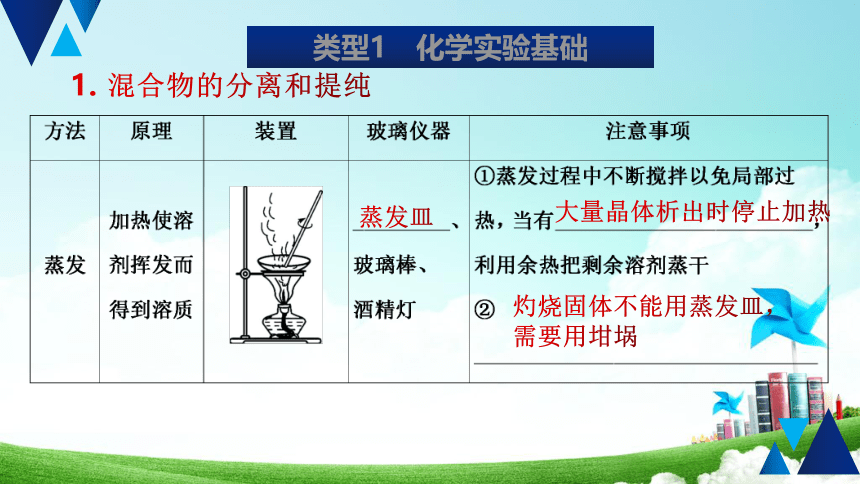
混合物的分离和提纯
蒸发皿
大量晶体析出时停止加热
灼烧固体不能用蒸发皿,
需要用坩埚
类型1 化学实验基础
1.
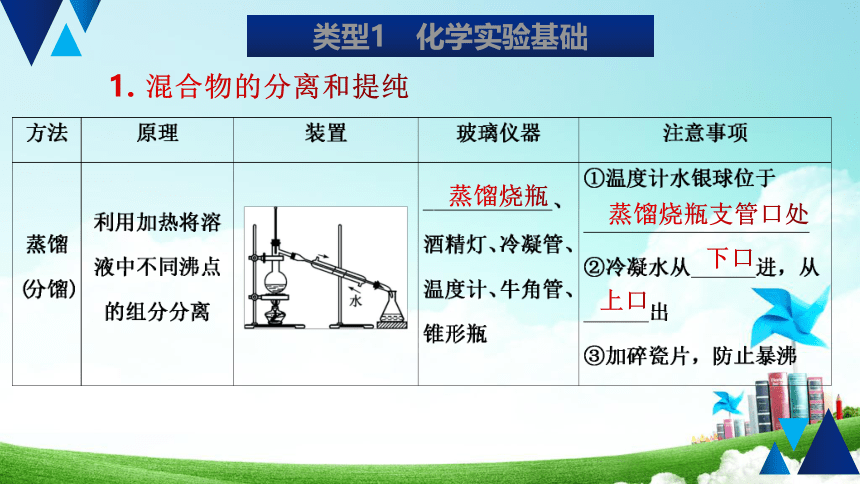
混合物的分离和提纯
蒸馏烧瓶
蒸馏烧瓶支管口处
下口
上口
类型1 化学实验基础
1.
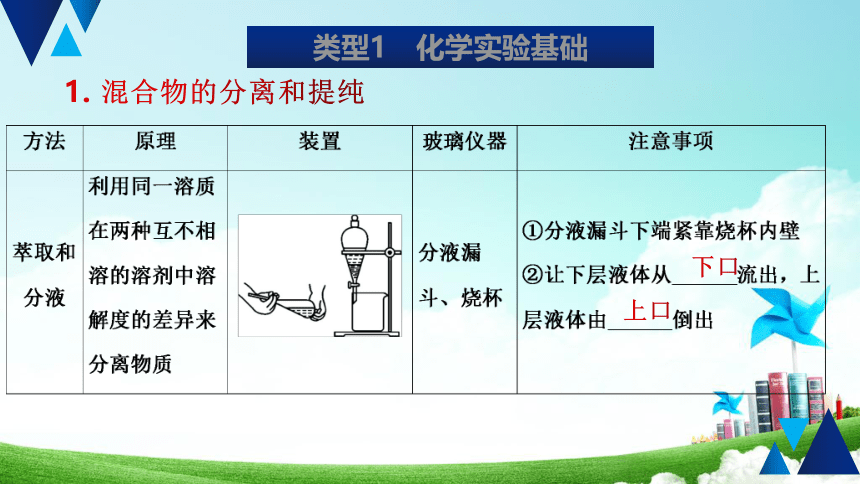
混合物的分离和提纯
下口
上口
类型1 化学实验基础
1.
混合物的分离和提纯
湿润
红色
蓝色
血红色
溶液
沉淀
2.
几种离子的检验
类型1 化学实验基础
不变红
变红
蓝色
黄色
2.
几种离子的检验
类型1 化学实验基础
白色沉淀
白色沉淀
2.
几种离子的检验
类型1 化学实验基础
玻璃棒
容量瓶
胶头滴管(定容)
不能直接在容量瓶中配制溶液,不能在容量瓶中溶解或稀释
玻璃棒引流
液面接近刻度线以下1~2
cm处,改用胶头滴管加水定容
类型1 化学实验基础
3.
配制一定物质的量浓度的溶液
熔化成小球
黄色火焰
淡黄色
类型2 金属及其化合物
类型2 金属及其化合物
过量
类型2 金属及其化合物
类型2 金属及其化合物
类型2 金属及其化合物
类型3 非金属及其化合物
饱和食盐水
氯化氢
浓硫酸
水蒸气
向上排空气法
NaOH溶液
类型3 非金属及其化合物
不稳定的无色物质
还原性
类型3 非金属及其化合物
炭化
类型3 非金属及其化合物
类型3 非金属及其化合物
类型3 非金属及其化合物
类型3 非金属及其化合物
类型4 有机化学课本实验回归
类型4 有机化学课本实验回归
类型4 有机化学课本实验回归
注意事项:加AgNO3溶液之前一定要先加稀硝酸酸化,因为水解后的溶液显碱性,此时直接加AgNO3溶液,会先生成AgOH沉淀,随即转化为棕黑色Ag2O沉淀,对实验造成干扰。
类型4 有机化学课本实验回归
注意事项:挥发出来的乙醇也能使酸性KMnO4溶液褪色,先用水除去乙醇,再检验是否生成乙烯。
类型4 有机化学课本实验回归
沉淀恰好溶解为止
注意事项:
注意滴加顺序:向1
mL
2%
AgNO3溶液中滴加2%的稀氨水。
类型4 有机化学课本实验回归
注意事项:
本实验中成功的关键是新制的Cu(OH)2中含有过量的NaOH,保证显碱性。
类型4 有机化学课本实验回归
防止倒吸
类型4 有机化学课本实验回归
类型4 有机化学课本实验回归
类型4 有机化学课本实验回归
类型4 有机化学课本实验回归
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
负极
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
一般情况下,溶解度大的沉淀转化为溶解更小的沉淀容易实现
类型5 化学反应原理课本实验回归
滴加NaCl需过量。
等浓度
类型5 化学反应原理课本实验回归
加NaOH溶液少量,
类型5 化学反应原理课本实验回归
两者Ksp相近,溶解度小的物质也可以向溶解度大的物质转化。
类型5 化学反应原理课本实验回归
(1)将MgCl2溶液加热蒸干可制备无水MgCl2。
( )
(2)用热碱水清除炊具上残留的油污发生了化学反应。( )
(3)用图1除去CO气体中的CO2气体。
( )
图1 图2
(4)用图2进行NaHCO3受热分解。
( )
(5)烧瓶、烧杯、锥形瓶、试管、量筒加热时均需垫石棉网。( )
正误判断
√
×
×
×
×
×
(6)稀盐酸和稀HNO3可分别除去烧瓶内残留的MnO2和试管内壁的银镜。
( )
(7)用玻璃棒蘸取CH3COOH溶液点在用水湿润的pH试纸上,测定该溶液的pH。
( )
(8)用图3装置可防止倒吸。
( )
(9)用H2还原CuO的实验结束时先停止通H2再停止加热。
( )
(10)用图4可量取O2的体积。
( )
×
×
×
√
√
图3
图4
正误判断
(11)除去Cu粉中混有的CuO的操作是加入稀HNO3溶解、过滤、洗涤、干燥。
( )
(12)提取海水中的Mg2+,工业生产中常选用NaOH作为沉淀剂。
( )
(13)用如图除去粗盐溶液中的不溶物。( )
(14)分离溶于水的碘可用乙醇萃取,其原理为碘在乙醇中的溶解度较大。
( )
(15)某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+。
( )
×
×
×
×
×
正误判断
(16)能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2。
( )
(17)蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热。
( )
(18)蒸馏操作时,应使温度计的水银球插入蒸馏烧瓶溶液中。
( )
(19)分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出。
( )
(20)只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液。
( )
×
×
√
×
×
正误判断
(21)能使品红褪色的气体一定是SO2。( )(22)使湿润的淀粉?KI试纸变蓝的气体一定是Cl2。( )(23)某溶液做焰色反应时呈黄色,该溶液中一定只含Na+,不含K+。( )(24)SO2中混有少量NH3,可以将混合气体通过浓硫酸除去。( )(25)除去SO2中的少量HCl,可将混合气体通过饱和Na2SO3溶液。( )
√
×
×
×
×
正误判断
(26)FeCl2溶液中混有FeCl3可加入铜粉除去。( )(27)某溶液中加入HNO3酸化的BaCl2溶液产生白色沉淀,则溶液中一定含SO42-。( )(28)加入浓NaOH溶液加热产生能使湿润的红色石蕊试纸变蓝的气体,说明该溶液中一定含有NH4+。( )(29)用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3。( )(30)提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法。( )
√
×
×
×
×
正误判断
(31)用大理石与稀硫酸反应可快速制取CO2。( )(32)将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置,下层溶液显紫红色,证明氧化性:Fe3+>I2。( )(33)分别加热Na2CO3和NaHCO3固体,试管内壁都有水珠,说明两种物质均受热分解。( )(34)可以用加热分解NH4Cl、NH4HCO3等铵盐快速制NH3。( )(35)启普发生器可用于制备H2、CO2、O2、C2H4等气体。( )
×
×
×
×
√
正误判断
(36)气体由A通入时,可用于收集NO、NO2气体,气体由B通入时,可用于收集H2、NH3、CH4等气体。( )(37)加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结,则NH4Cl固体可以升华。( )(38)容量瓶、分液漏斗、酸(碱)式滴定管使用前都要先检漏、洗涤,酸(碱)式滴定管还需用待盛液体润洗。( )(39)使食盐水中NaCl晶体析出时,常用到的仪器有坩埚、酒精灯、玻璃棒、泥三角。( )(40)用分液漏斗分离苯与四氯化碳的混合物,可将四氯化碳从下口放出,苯从上口倒出( )
×
×
×
×
√
正误判断
03-回归课本核心实验
2021高考三轮复习之回归课本
类型1 化学实验基础
1.
混合物的分离和提纯
蒸发皿
大量晶体析出时停止加热
灼烧固体不能用蒸发皿,
需要用坩埚
类型1 化学实验基础
1.
混合物的分离和提纯
蒸馏烧瓶
蒸馏烧瓶支管口处
下口
上口
类型1 化学实验基础
1.
混合物的分离和提纯
下口
上口
类型1 化学实验基础
1.
混合物的分离和提纯
湿润
红色
蓝色
血红色
溶液
沉淀
2.
几种离子的检验
类型1 化学实验基础
不变红
变红
蓝色
黄色
2.
几种离子的检验
类型1 化学实验基础
白色沉淀
白色沉淀
2.
几种离子的检验
类型1 化学实验基础
玻璃棒
容量瓶
胶头滴管(定容)
不能直接在容量瓶中配制溶液,不能在容量瓶中溶解或稀释
玻璃棒引流
液面接近刻度线以下1~2
cm处,改用胶头滴管加水定容
类型1 化学实验基础
3.
配制一定物质的量浓度的溶液
熔化成小球
黄色火焰
淡黄色
类型2 金属及其化合物
类型2 金属及其化合物
过量
类型2 金属及其化合物
类型2 金属及其化合物
类型2 金属及其化合物
类型3 非金属及其化合物
饱和食盐水
氯化氢
浓硫酸
水蒸气
向上排空气法
NaOH溶液
类型3 非金属及其化合物
不稳定的无色物质
还原性
类型3 非金属及其化合物
炭化
类型3 非金属及其化合物
类型3 非金属及其化合物
类型3 非金属及其化合物
类型3 非金属及其化合物
类型4 有机化学课本实验回归
类型4 有机化学课本实验回归
类型4 有机化学课本实验回归
注意事项:加AgNO3溶液之前一定要先加稀硝酸酸化,因为水解后的溶液显碱性,此时直接加AgNO3溶液,会先生成AgOH沉淀,随即转化为棕黑色Ag2O沉淀,对实验造成干扰。
类型4 有机化学课本实验回归
注意事项:挥发出来的乙醇也能使酸性KMnO4溶液褪色,先用水除去乙醇,再检验是否生成乙烯。
类型4 有机化学课本实验回归
沉淀恰好溶解为止
注意事项:
注意滴加顺序:向1
mL
2%
AgNO3溶液中滴加2%的稀氨水。
类型4 有机化学课本实验回归
注意事项:
本实验中成功的关键是新制的Cu(OH)2中含有过量的NaOH,保证显碱性。
类型4 有机化学课本实验回归
防止倒吸
类型4 有机化学课本实验回归
类型4 有机化学课本实验回归
类型4 有机化学课本实验回归
类型4 有机化学课本实验回归
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
负极
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
类型5 化学反应原理课本实验回归
一般情况下,溶解度大的沉淀转化为溶解更小的沉淀容易实现
类型5 化学反应原理课本实验回归
滴加NaCl需过量。
等浓度
类型5 化学反应原理课本实验回归
加NaOH溶液少量,
类型5 化学反应原理课本实验回归
两者Ksp相近,溶解度小的物质也可以向溶解度大的物质转化。
类型5 化学反应原理课本实验回归
(1)将MgCl2溶液加热蒸干可制备无水MgCl2。
( )
(2)用热碱水清除炊具上残留的油污发生了化学反应。( )
(3)用图1除去CO气体中的CO2气体。
( )
图1 图2
(4)用图2进行NaHCO3受热分解。
( )
(5)烧瓶、烧杯、锥形瓶、试管、量筒加热时均需垫石棉网。( )
正误判断
√
×
×
×
×
×
(6)稀盐酸和稀HNO3可分别除去烧瓶内残留的MnO2和试管内壁的银镜。
( )
(7)用玻璃棒蘸取CH3COOH溶液点在用水湿润的pH试纸上,测定该溶液的pH。
( )
(8)用图3装置可防止倒吸。
( )
(9)用H2还原CuO的实验结束时先停止通H2再停止加热。
( )
(10)用图4可量取O2的体积。
( )
×
×
×
√
√
图3
图4
正误判断
(11)除去Cu粉中混有的CuO的操作是加入稀HNO3溶解、过滤、洗涤、干燥。
( )
(12)提取海水中的Mg2+,工业生产中常选用NaOH作为沉淀剂。
( )
(13)用如图除去粗盐溶液中的不溶物。( )
(14)分离溶于水的碘可用乙醇萃取,其原理为碘在乙醇中的溶解度较大。
( )
(15)某溶液加入BaCl2溶液,产生不溶于稀硝酸的白色沉淀,该溶液一定含有Ag+。
( )
×
×
×
×
×
正误判断
(16)能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2。
( )
(17)蒸发操作时,应使混合物中的水分完全蒸干后,才能停止加热。
( )
(18)蒸馏操作时,应使温度计的水银球插入蒸馏烧瓶溶液中。
( )
(19)分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出。
( )
(20)只滴加氨水鉴别NaCl、AlCl3、MgCl2、Na2SO4四种溶液。
( )
×
×
√
×
×
正误判断
(21)能使品红褪色的气体一定是SO2。( )(22)使湿润的淀粉?KI试纸变蓝的气体一定是Cl2。( )(23)某溶液做焰色反应时呈黄色,该溶液中一定只含Na+,不含K+。( )(24)SO2中混有少量NH3,可以将混合气体通过浓硫酸除去。( )(25)除去SO2中的少量HCl,可将混合气体通过饱和Na2SO3溶液。( )
√
×
×
×
×
正误判断
(26)FeCl2溶液中混有FeCl3可加入铜粉除去。( )(27)某溶液中加入HNO3酸化的BaCl2溶液产生白色沉淀,则溶液中一定含SO42-。( )(28)加入浓NaOH溶液加热产生能使湿润的红色石蕊试纸变蓝的气体,说明该溶液中一定含有NH4+。( )(29)用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3。( )(30)提纯混有少量硝酸钾的氯化钠,应采用在较高温度下制得浓溶液再冷却结晶、过滤、干燥的方法。( )
√
×
×
×
×
正误判断
(31)用大理石与稀硫酸反应可快速制取CO2。( )(32)将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置,下层溶液显紫红色,证明氧化性:Fe3+>I2。( )(33)分别加热Na2CO3和NaHCO3固体,试管内壁都有水珠,说明两种物质均受热分解。( )(34)可以用加热分解NH4Cl、NH4HCO3等铵盐快速制NH3。( )(35)启普发生器可用于制备H2、CO2、O2、C2H4等气体。( )
×
×
×
×
√
正误判断
(36)气体由A通入时,可用于收集NO、NO2气体,气体由B通入时,可用于收集H2、NH3、CH4等气体。( )(37)加热盛有NH4Cl固体的试管,试管底部固体消失,试管口有晶体凝结,则NH4Cl固体可以升华。( )(38)容量瓶、分液漏斗、酸(碱)式滴定管使用前都要先检漏、洗涤,酸(碱)式滴定管还需用待盛液体润洗。( )(39)使食盐水中NaCl晶体析出时,常用到的仪器有坩埚、酒精灯、玻璃棒、泥三角。( )(40)用分液漏斗分离苯与四氯化碳的混合物,可将四氯化碳从下口放出,苯从上口倒出( )
×
×
×
×
√
正误判断
同课章节目录
