2021年北京市中考化学二轮复习:生活现象解释题突破(含答案)
文档属性
| 名称 | 2021年北京市中考化学二轮复习:生活现象解释题突破(含答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 316.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-11 00:00:00 | ||
图片预览




文档简介
2021北京中考化学二轮复习:生活现象解释题突破
一、生活现象解释题考情分析
年份 2018 2019 2020
生活现象解释题考点一 物质分类 垃圾分类 垃圾分类
生活现象解释题考点二 干热岩发电 消毒剂 消毒剂
生活现象解释题考点三 过氧化氢 水分解 海水稻种植
二、生活现象解释题重点考点梳理
1.电解水实验
1.实验用品有:水槽、试管、直流电、石墨电极(正极不能用铜等金属或与氧气反应的电极)、12V的直流电源.
2.实验过程及现象:按照上面的实物图所示,连接好装置.为增强水的导电性,可在水中加入少量稀硫酸或氢氧化钠溶液(一般不加氢氧化钠溶液,容易起泡沫).闭合电路后,会看到试管内的电极上出现气泡,过一段时间,与电源正(氧气),负极(氢气)相连的试管产生的气体体积比约为1:2.(氧气的密度为1.429g/mL,氢气的为0.089g/mL;通过计算可得氧气与氢气的质量比为8:1,氢,氧两种分子和原子个数比都是2:1).可简单概括为:“正氧负氢1:2,质量比为8:1”.
3.该实验结论或推论有:(1)水由氢、氧两种元素组成.(2)水(分子)中,氢、氧两种元素的原子个数比为2:1,两气体的分子个数比为2:1、体积比为2:1.(3)水通电生成氢气、氧气,正极产生的是氧气,负极产生的是氢气..(4)化学反应前后,原子种类、个数不变,元素种类不变.(5)在化学变化中,分子可分,而原子不可分.(6)化学反应的实质是在化学变化中分子分解成原子,原子重新组合成新的分子(或聚集后直接构成物质)(7)分子是保持物质化学性质的最小粒子.(8)原子是化学变化中的最小粒子.(9)氧气是由氧元素组成;氢气是由氢元素组成.⑽水是由水分子构成的;一个水分子是由二个氢原子和一个氧原子构成;一个氢气分子是由二个氢原子构成;一个氧气分子是由二个氧原子构成.⑾水是纯净物中的化合物中的氧化物,氧气和氢气是纯净物中的单质.⑿该实验中发生的化学反应属于分解反应.
2.溶液的酸碱性与pH的关系
其具体内容是酸性溶液的pH值<7;中性溶液的pH值=7;碱性溶液的pH值>7.可简记:“小酸大碱中7”;其含义是:“pH值<7为酸性,pH值>7为碱性,pH值=7为中性。”并且其中的“小酸大碱”还可暗示:“pH值越小,溶液的酸性越强;pH值越大,溶液的碱性越强。”
3.物质的简单分类
由于物质的分类原理是根据物质的组成物质或元素来进行分类的,所以物质的分类与其组成的关系是密不可分的,具体的详情如下:
1.从物质的分类(即混合物和纯净物)来看,物质的组成关系包含两层.第一层是混合物由纯净物组成(例如:空气是由氮气、氧气、稀有气体、二氧化碳、其他气体和杂质组成的,纯净的食盐水是由食盐和水组成的,黄铜(一种合金)是由铜和锌组成的,等等);第二层是纯净物由元素组成(例如:镁是由镁元素组成的,冰水混合物是由氢、氧两种元素组成的,氯酸钾是由钾、氯、氧三种元素组成的,等等).
2.至于纯净物的分类,是根据其组成元素的种类不同,将其分为单质和化合物.其中,单质是由同种元素组成的(例如:铁是由铁元素组成的,氢气是由氢元素组成的,氦气是由氦元素组成的,等等);化合物是由不同种元素组成的(例如:过氧化氢是由氢、氧两种元素组成的,高锰酸钾是由钾、锰、氧三种元素组成的,碳酸氢钠是由钠、氢、碳、氧四种元素组成的,等等).
3.单质的分类,是按照元素的分类来进行的.它可以分为金属单质(即由金属元素组成的单质,如铝、铜和锌等)、非金属单质(即由非金属元素组成的单质,如氧气、氮气和碳等)和稀有气体单质(即由稀有气体元素组成的单质,如氦气、氖气和氩气等).
4.化合物的分类,由于分类标准的不同,分成的类别也有所不同.一般情况下,是按照化合物的组成(或构成)不同,将其分为氧化物(即由两种元素组成的,并且其中一种是氧元素的化合物,如二氧化硫、五氧化二磷和氧化铜等)、酸(即由氢离子和酸根离子构成的化合物,如盐酸、硫酸和硝酸等)、碱(即由金属离子和氢氧根离子构成的化合物,如氢氧化钠、氢氧化钙和氢氧化钾等)、盐(即由金属离子和酸根离子构成的化合物,如氯化钠、碳酸钠和碳酸钙等).当然,有时也按化合物中是否含有碳元素分为:有机化合物(即含碳元素的化合物,如甲烷、乙醇和葡萄糖等;但有少数含碳元素的化合物,如一氧化碳、二氧化碳、碳酸和碳酸盐等具有无机化合物的特点,因此将其看做无机化合物)和无机化合物(即不含碳元素的化合物,如氯化钾、硫酸和氢氧化钠等).甚至,有时还按化合物的形成方式分为:离子化合物(即由阳离子和阴离子构成的化合物.一般是指组成中含有金属元素的化合物,如氯化钠、碳酸钠和硫酸铜等)和共价化合物(即以共用电子对形成分子的化合物.一般是指组成中不含金属元素的化合物,如氯化氢、水和二氧化碳等).
三、针对性模拟练习
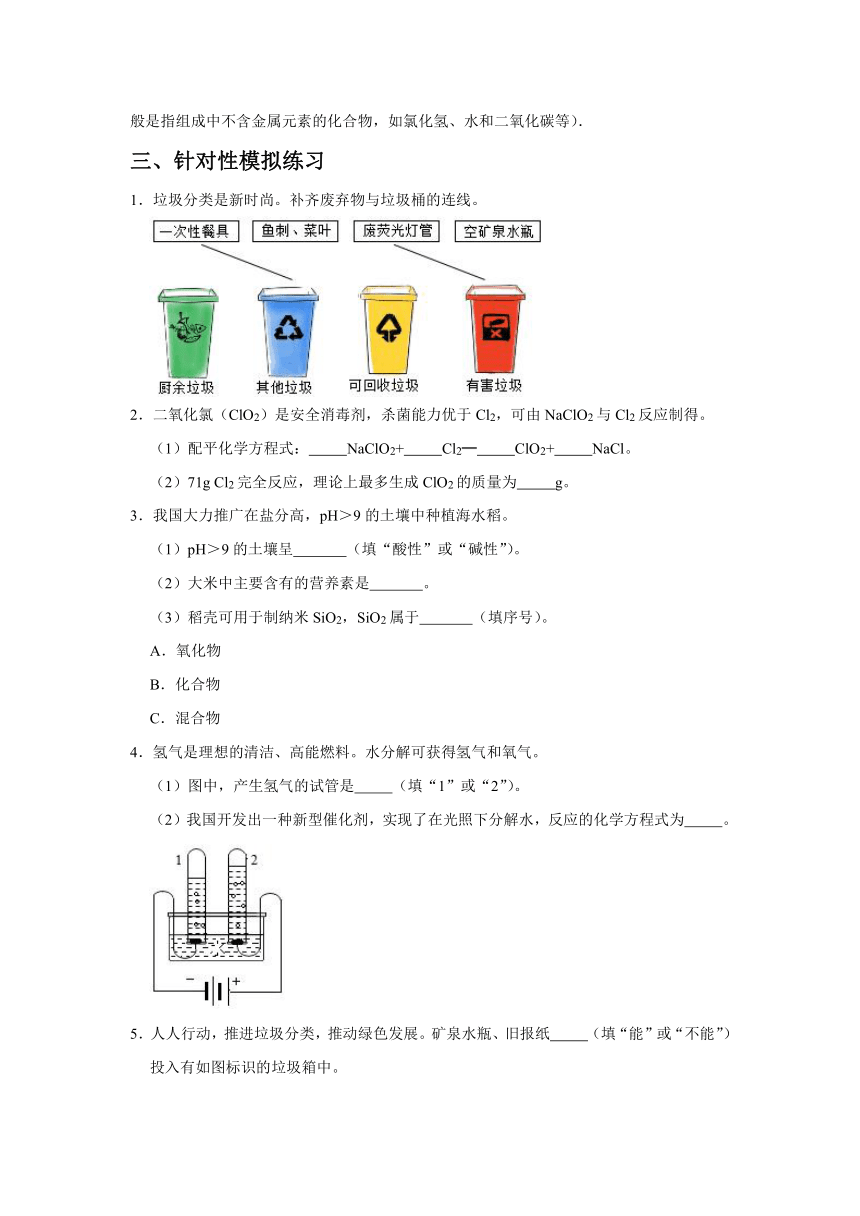
1.垃圾分类是新时尚。补齐废弃物与垃圾桶的连线。
2.二氧化氯(ClO2)是安全消毒剂,杀菌能力优于Cl2,可由NaClO2与Cl2反应制得。
(1)配平化学方程式: NaClO2+ Cl2═ ClO2+ NaCl。
(2)71g Cl2完全反应,理论上最多生成ClO2的质量为 g。
3.我国大力推广在盐分高,pH>9的土壤中种植海水稻。
(1)pH>9的土壤呈 (填“酸性”或“碱性”)。
(2)大米中主要含有的营养素是 。
(3)稻壳可用于制纳米SiO2,SiO2属于 (填序号)。
A.氧化物
B.化合物
C.混合物
4.氢气是理想的清洁、高能燃料。水分解可获得氢气和氧气。
(1)图中,产生氢气的试管是 (填“1”或“2”)。
(2)我国开发出一种新型催化剂,实现了在光照下分解水,反应的化学方程式为 。
5.人人行动,推进垃圾分类,推动绿色发展。矿泉水瓶、旧报纸 (填“能”或“不能”)投入有如图标识的垃圾箱中。
6.H2O2可作增氧剂。常温下,用4% H2O2溶液进行实验,研究pH对H2O2分解所得溶液中溶氧量的影响,测定结果如图。
(1)H2O2分解的化学方程式为 。
(2)分析如图得到的结论是 。
7.干热岩是地层深处的热岩体。如图为利用其发电的示意图。
(1)将干热岩的热量传递到热交换器的物质是 。
(2)从微粒的角度分析,水变为水蒸气时,变化的是 。
8.补齐连线。从A或B中任选一个作答,若均作答,按A计分。
A 物质﹣用途 B 物质﹣﹣主要成分
9.我国大力推广在盐分高、pH>9的土壤中种植海水稻。
(1)pH>9的土壤呈 (填“酸性”或“碱性”)。
(2)大米中主要含有的营养素是 。
(3)稻壳可用于制纳米SiO2,其中Si的化合价为 ,SiO2属于 (填序号)。
A.氧化物
B.化合物
C.混合物
10.工业酒精中所含甲醇是一种有毒,有酒味的可燃性液体.甲醇在氧气中不完全燃烧可发生下列反应:8CH3OH+11O2XCO2+2CO+16H2O试计算:
(1)X值是 ;
(2)若反应消耗4、4g氧气,则生成水的质量是多少?
11.XX冶炼厂的是我市一家以生产硫酸和金属锌为主的大型化工企业,冶炼厂进行生产的第一步是对锌精矿(主要成分是硫化锌)进行煅烧,化学反应方程式如下
2ZnS+□O2=2ZnO+□SO2
(1)在□填入合适系数,对方程式配平
(2)如需要8100吨氧化锌,进行下一步生产.则需要煅烧多少吨含硫化锌为80%的锌精矿?
12.垃圾分类就是新时尚。在去博物馆的路上,小明将空饮料瓶投入到下列 (填序号)垃圾桶中。
13.随着人类对能源的需求量益增长,可燃冰的开采、氢气的开发和利用都越来越受到人们的关注,我国在可燃冰的试开采方面已取得重大突破,形成了国际领先的新型试采工艺。
(1)可燃冰主要甲烷水合物。请写出甲烷(CH4)完全燃烧的化学方程式: 。
(2)电解水可产生氧气,如图中产生氢气的试管是 (填“1”或“2”)。
14.我们需要洁净的水源,自来水生产加入液氯的作用是 。用如图实验验证水的组成,反应的化学方程式是 。证明a管中气体的方法是 ,a和b管中气体的质量比是 。该实验证明了水是由 组成。0.5mol水中约含 个氢原子。
15.84消毒液[有效成分为次氯酸钠(NaClO)]和二氧化氯(ClO2)是常用消毒剂。
(1)NaClO中氯元素的化合价为 。
(2)ClO2属于 (填序号)。
A.混合物 B.化合物 C.氧化物
2021北京中考化学二轮复习:生活现象解释题突破
参考答案
1.垃圾分类是新时尚。补齐废弃物与垃圾桶的连线。
【解答】解:鱼刺、菜叶属于厨余垃圾;空矿泉水瓶属于可回收垃圾。
故答案为:
。
2.二氧化氯(ClO2)是安全消毒剂,杀菌能力优于Cl2,可由NaClO2与Cl2反应制得。
(1)配平化学方程式: 2 NaClO2+ 1 Cl2═ 2 ClO2+ 2 NaCl。
(2)71g Cl2完全反应,理论上最多生成ClO2的质量为 135 g。
【解答】解:(1)依据定一法,亚氯酸钠的系数定为1,所以二氧化氯、氯化钠的系数就是1,1,通过观察可知,氯气的系数为,将系数化为整数,所以化学方程式为:2NaClO2+Cl2═2ClO2+2NaCl;
(2)设理论上最多生成ClO2的质量为x
2NaClO2+Cl2═2ClO2+2NaCl
71 135
71g x
=
x=135g。
故答案为:(1)2;1;2;2;
(2)135。
3.我国大力推广在盐分高,pH>9的土壤中种植海水稻。
(1)pH>9的土壤呈 碱性 (填“酸性”或“碱性”)。
(2)大米中主要含有的营养素是 糖类 。
(3)稻壳可用于制纳米SiO2,SiO2属于 AB (填序号)。
A.氧化物
B.化合物
C.混合物
【解答】解:(1)当溶液的pH大于7时,呈碱性,pH>9的土壤呈碱性。
(2)大米中富含淀粉,淀粉属于糖类。
(3)SiO2中只含有二氧化硅一种物质,属于纯净物;是由不同种元素组成的纯净物,属于化合物;是由两种元素组成且有一种是氧元素,属于氧化物。
故答案为:
(1)碱性;
(2)糖类;
(3)AB。
4.氢气是理想的清洁、高能燃料。水分解可获得氢气和氧气。
(1)图中,产生氢气的试管是 1 (填“1”或“2”)。
(2)我国开发出一种新型催化剂,实现了在光照下分解水,反应的化学方程式为 2H2O2H2↑+O2↑ 。
【解答】解:(1)电解水时“正氧负氢,氢二氧一”,所以产生氢气的是试管1;
(2)由题意可知,我国开发出一种新型催化剂,实现了在光照下分解水,反应的化学方程式为:2H2O2H2↑+O2↑。
故答为:(1)1;(2)2H2O2H2↑+O2↑。
5.人人行动,推进垃圾分类,推动绿色发展。矿泉水瓶、旧报纸 能 (填“能”或“不能”)投入有如图标识的垃圾箱中。
【解答】解:图中标志是可回收物标志,矿泉水瓶、旧报纸属于可回收物,能投入有如图标识的垃圾箱中。
故答案为:
能。
6.H2O2可作增氧剂。常温下,用4% H2O2溶液进行实验,研究pH对H2O2分解所得溶液中溶氧量的影响,测定结果如图。
(1)H2O2分解的化学方程式为 2H2O2═2H2O+O2↑ 。
(2)分析如图得到的结论是 在常温下,当pH在8﹣12之间时,随着pH的增大,溶氧量先增大后减小,且在pH为10﹣11中间时,溶氧量达到最大值 。
【解答】解:(1)过氧化氢在常温下分解生成水和氧气,反应的化学方程式为:2H2O2═2H2O+O2↑。
(2)由pH对H2O2分解所得溶液中氧量的影响测定结果图,在常温下,当pH在8﹣12之间时,随着pH的增大,溶氧量先增大后减小,且在pH为10﹣11中间时,溶氧量达到最大值。
故答案为:
(1)2H2O2═2H2O+O2↑;
(2)在常温下,当pH在8﹣12之间时,随着pH的增大,溶氧量先增大后减小,且在pH为10﹣11中间时,溶氧量达到最大值。
7.干热岩是地层深处的热岩体。如图为利用其发电的示意图。
(1)将干热岩的热量传递到热交换器的物质是 水或水蒸气 。
(2)从微粒的角度分析,水变为水蒸气时,变化的是 分子之间的间隔 。
【解答】解:
(1)由图示可知:将干热岩的热量传递到热交换器的物质是水或水蒸气;
(2)微观角度讲,水变为水蒸气是水分子之间的间隔变大造成的,而水分子的体积不变;
答案:
(1)水或水蒸气;
(2)分子之间的间隔。
8.补齐连线。从A或B中任选一个作答,若均作答,按A计分。
A 物质﹣用途 B 物质﹣﹣主要成分
【解答】解:A干冰升华吸热,可冷藏食品;碳酸钙中含有钙元素,用于补钙剂;熟石灰呈碱性。可用于改良酸性土壤;
B天然气的主要成分是甲烷;氯化钠俗称食盐;氧化钙俗称生石灰。
答案:
9.我国大力推广在盐分高、pH>9的土壤中种植海水稻。
(1)pH>9的土壤呈 碱性 (填“酸性”或“碱性”)。
(2)大米中主要含有的营养素是 糖类 。
(3)稻壳可用于制纳米SiO2,其中Si的化合价为 +4 ,SiO2属于 AB (填序号)。
A.氧化物
B.化合物
C.混合物
【解答】解:(1)当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性,则pH>9的土壤显碱性。
(2)大米中富含淀粉,淀粉属于糖类。
(3)氧元素显﹣2价,设硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(﹣2)×2=0,则x=+4价。
SiO2是由二氧化硅一种物质组成的,属于纯净物;是由不同种元素组成的纯净物,属于化合物;是由两种元素组成的且有一种是氧元素的化合物,属于氧化物。
故答案为:
(1)碱性;
(2)糖类;
(3)+4;AB。
10.工业酒精中所含甲醇是一种有毒,有酒味的可燃性液体.甲醇在氧气中不完全燃烧可发生下列反应:8CH3OH+11O2XCO2+2CO+16H2O试计算:
(1)X值是 6 ;
(2)若反应消耗4、4g氧气,则生成水的质量是多少?
【解答】解:(1)根据化学方程式的配平的原则,C的个数在生成物中应为8,在生成物中只有2CO中有2个,故x=8﹣2=6.故答案为:6.
(2)设生成水的质量是x,
8CH3OH+11O26CO2+2CO+16H2O
352 288
4.4g x
∴
解之得:x=3.6g,
答:生成水的质量是3.6g.
11.XX冶炼厂的是我市一家以生产硫酸和金属锌为主的大型化工企业,冶炼厂进行生产的第一步是对锌精矿(主要成分是硫化锌)进行煅烧,化学反应方程式如下
2ZnS+□O2=2ZnO+□SO2
(1)在□填入合适系数,对方程式配平
(2)如需要8100吨氧化锌,进行下一步生产.则需要煅烧多少吨含硫化锌为80%的锌精矿?
【解答】解:(1)化学反应前后原子个数不变,所以化学方程式为:2ZnS+3O2=2ZnO+2SO2;
(2)设需要煅烧含硫化锌为80%的锌精矿质量为x
2ZnS+3O2=2ZnO+2SO2
194 162
x×80% 8100t
=
x=12125t
故答案为:(1)2ZnS+3O2=2ZnO+2SO2;
(2)12125t.
12.垃圾分类就是新时尚。在去博物馆的路上,小明将空饮料瓶投入到下列 A (填序号)垃圾桶中。
【解答】解:空饮料瓶可以回收,回收再利用,可以节约资源防止环境污染。
故选A。
13.随着人类对能源的需求量益增长,可燃冰的开采、氢气的开发和利用都越来越受到人们的关注,我国在可燃冰的试开采方面已取得重大突破,形成了国际领先的新型试采工艺。
(1)可燃冰主要甲烷水合物。请写出甲烷(CH4)完全燃烧的化学方程式: CH4+2O2CO2+2H2O 。
(2)电解水可产生氧气,如图中产生氢气的试管是 1 (填“1”或“2”)。
【解答】解:(1)在点燃的条件下,甲烷与氧气反应生成二氧化碳和水,化学方程式为:CH4+2O2CO2+2H2O;故填:CH4+2O2CO2+2H2O;
(2)由“正氧负氢、氢二氧一”可知,如图中产生氢气的试管是1;故填:1。
14.我们需要洁净的水源,自来水生产加入液氯的作用是 杀菌消毒 。用如图实验验证水的组成,反应的化学方程式是 2H2O2H2↑+O2↑ 。证明a管中气体的方法是 用带火星木条检验,能使带火星的木条复燃 ,a和b管中气体的质量比是 8:1 。该实验证明了水是由 氢元素和氧元素 组成。0.5mol水中约含 6.02×1023 个氢原子。
【解答】解:自来水生产通入氯气的作用是杀菌消毒;水通电分解生成氢气和氧气,反应的化学方程式为:2H2O2H2↑+O2↑.a管气体少,所收集的气体是氧气,b管气体多,所收集的气体是氢气,因为氧气具有助燃性,可用带火星检验,能使带火星的木条复燃。仪器内水通直流电生成氢气和氧气,生成氢气和氧气的体积比是2:1,质量比为:8:1,该实验证明了水是由氢元素和氧元素组成的,0.5mol水中约含1mol氢原子,即6.02×1023个氢原子;
答案:杀菌消毒;2H2O2H2↑+O2↑.用带火星木条检验,能使带火星的木条复燃;8:1;氢元素和氧元素;6.02×1023
15.84消毒液[有效成分为次氯酸钠(NaClO)]和二氧化氯(ClO2)是常用消毒剂。
(1)NaClO中氯元素的化合价为 +1 。
(2)ClO2属于 BC (填序号)。
A.混合物 B.化合物 C.氧化物
【解答】解:(1)根据在化合物中正负化合价代数和为零,设氯元素的化合价为x,钠元素的化合价为+1,氧元素的化合价为﹣2,可得NaClO中氯元素的化合价为:(+1)+x+(﹣2)=0,解答x=+1;故填:+1;
(2)二氧化氯中含有两种元素,所以为化合物;并且其中一种元素为氧元素,所以为氧化物。故填:BC。
一、生活现象解释题考情分析
年份 2018 2019 2020
生活现象解释题考点一 物质分类 垃圾分类 垃圾分类
生活现象解释题考点二 干热岩发电 消毒剂 消毒剂
生活现象解释题考点三 过氧化氢 水分解 海水稻种植
二、生活现象解释题重点考点梳理
1.电解水实验
1.实验用品有:水槽、试管、直流电、石墨电极(正极不能用铜等金属或与氧气反应的电极)、12V的直流电源.
2.实验过程及现象:按照上面的实物图所示,连接好装置.为增强水的导电性,可在水中加入少量稀硫酸或氢氧化钠溶液(一般不加氢氧化钠溶液,容易起泡沫).闭合电路后,会看到试管内的电极上出现气泡,过一段时间,与电源正(氧气),负极(氢气)相连的试管产生的气体体积比约为1:2.(氧气的密度为1.429g/mL,氢气的为0.089g/mL;通过计算可得氧气与氢气的质量比为8:1,氢,氧两种分子和原子个数比都是2:1).可简单概括为:“正氧负氢1:2,质量比为8:1”.
3.该实验结论或推论有:(1)水由氢、氧两种元素组成.(2)水(分子)中,氢、氧两种元素的原子个数比为2:1,两气体的分子个数比为2:1、体积比为2:1.(3)水通电生成氢气、氧气,正极产生的是氧气,负极产生的是氢气..(4)化学反应前后,原子种类、个数不变,元素种类不变.(5)在化学变化中,分子可分,而原子不可分.(6)化学反应的实质是在化学变化中分子分解成原子,原子重新组合成新的分子(或聚集后直接构成物质)(7)分子是保持物质化学性质的最小粒子.(8)原子是化学变化中的最小粒子.(9)氧气是由氧元素组成;氢气是由氢元素组成.⑽水是由水分子构成的;一个水分子是由二个氢原子和一个氧原子构成;一个氢气分子是由二个氢原子构成;一个氧气分子是由二个氧原子构成.⑾水是纯净物中的化合物中的氧化物,氧气和氢气是纯净物中的单质.⑿该实验中发生的化学反应属于分解反应.
2.溶液的酸碱性与pH的关系
其具体内容是酸性溶液的pH值<7;中性溶液的pH值=7;碱性溶液的pH值>7.可简记:“小酸大碱中7”;其含义是:“pH值<7为酸性,pH值>7为碱性,pH值=7为中性。”并且其中的“小酸大碱”还可暗示:“pH值越小,溶液的酸性越强;pH值越大,溶液的碱性越强。”
3.物质的简单分类
由于物质的分类原理是根据物质的组成物质或元素来进行分类的,所以物质的分类与其组成的关系是密不可分的,具体的详情如下:
1.从物质的分类(即混合物和纯净物)来看,物质的组成关系包含两层.第一层是混合物由纯净物组成(例如:空气是由氮气、氧气、稀有气体、二氧化碳、其他气体和杂质组成的,纯净的食盐水是由食盐和水组成的,黄铜(一种合金)是由铜和锌组成的,等等);第二层是纯净物由元素组成(例如:镁是由镁元素组成的,冰水混合物是由氢、氧两种元素组成的,氯酸钾是由钾、氯、氧三种元素组成的,等等).
2.至于纯净物的分类,是根据其组成元素的种类不同,将其分为单质和化合物.其中,单质是由同种元素组成的(例如:铁是由铁元素组成的,氢气是由氢元素组成的,氦气是由氦元素组成的,等等);化合物是由不同种元素组成的(例如:过氧化氢是由氢、氧两种元素组成的,高锰酸钾是由钾、锰、氧三种元素组成的,碳酸氢钠是由钠、氢、碳、氧四种元素组成的,等等).
3.单质的分类,是按照元素的分类来进行的.它可以分为金属单质(即由金属元素组成的单质,如铝、铜和锌等)、非金属单质(即由非金属元素组成的单质,如氧气、氮气和碳等)和稀有气体单质(即由稀有气体元素组成的单质,如氦气、氖气和氩气等).
4.化合物的分类,由于分类标准的不同,分成的类别也有所不同.一般情况下,是按照化合物的组成(或构成)不同,将其分为氧化物(即由两种元素组成的,并且其中一种是氧元素的化合物,如二氧化硫、五氧化二磷和氧化铜等)、酸(即由氢离子和酸根离子构成的化合物,如盐酸、硫酸和硝酸等)、碱(即由金属离子和氢氧根离子构成的化合物,如氢氧化钠、氢氧化钙和氢氧化钾等)、盐(即由金属离子和酸根离子构成的化合物,如氯化钠、碳酸钠和碳酸钙等).当然,有时也按化合物中是否含有碳元素分为:有机化合物(即含碳元素的化合物,如甲烷、乙醇和葡萄糖等;但有少数含碳元素的化合物,如一氧化碳、二氧化碳、碳酸和碳酸盐等具有无机化合物的特点,因此将其看做无机化合物)和无机化合物(即不含碳元素的化合物,如氯化钾、硫酸和氢氧化钠等).甚至,有时还按化合物的形成方式分为:离子化合物(即由阳离子和阴离子构成的化合物.一般是指组成中含有金属元素的化合物,如氯化钠、碳酸钠和硫酸铜等)和共价化合物(即以共用电子对形成分子的化合物.一般是指组成中不含金属元素的化合物,如氯化氢、水和二氧化碳等).
三、针对性模拟练习
1.垃圾分类是新时尚。补齐废弃物与垃圾桶的连线。
2.二氧化氯(ClO2)是安全消毒剂,杀菌能力优于Cl2,可由NaClO2与Cl2反应制得。
(1)配平化学方程式: NaClO2+ Cl2═ ClO2+ NaCl。
(2)71g Cl2完全反应,理论上最多生成ClO2的质量为 g。
3.我国大力推广在盐分高,pH>9的土壤中种植海水稻。
(1)pH>9的土壤呈 (填“酸性”或“碱性”)。
(2)大米中主要含有的营养素是 。
(3)稻壳可用于制纳米SiO2,SiO2属于 (填序号)。
A.氧化物
B.化合物
C.混合物
4.氢气是理想的清洁、高能燃料。水分解可获得氢气和氧气。
(1)图中,产生氢气的试管是 (填“1”或“2”)。
(2)我国开发出一种新型催化剂,实现了在光照下分解水,反应的化学方程式为 。
5.人人行动,推进垃圾分类,推动绿色发展。矿泉水瓶、旧报纸 (填“能”或“不能”)投入有如图标识的垃圾箱中。
6.H2O2可作增氧剂。常温下,用4% H2O2溶液进行实验,研究pH对H2O2分解所得溶液中溶氧量的影响,测定结果如图。
(1)H2O2分解的化学方程式为 。
(2)分析如图得到的结论是 。
7.干热岩是地层深处的热岩体。如图为利用其发电的示意图。
(1)将干热岩的热量传递到热交换器的物质是 。
(2)从微粒的角度分析,水变为水蒸气时,变化的是 。
8.补齐连线。从A或B中任选一个作答,若均作答,按A计分。
A 物质﹣用途 B 物质﹣﹣主要成分
9.我国大力推广在盐分高、pH>9的土壤中种植海水稻。
(1)pH>9的土壤呈 (填“酸性”或“碱性”)。
(2)大米中主要含有的营养素是 。
(3)稻壳可用于制纳米SiO2,其中Si的化合价为 ,SiO2属于 (填序号)。
A.氧化物
B.化合物
C.混合物
10.工业酒精中所含甲醇是一种有毒,有酒味的可燃性液体.甲醇在氧气中不完全燃烧可发生下列反应:8CH3OH+11O2XCO2+2CO+16H2O试计算:
(1)X值是 ;
(2)若反应消耗4、4g氧气,则生成水的质量是多少?
11.XX冶炼厂的是我市一家以生产硫酸和金属锌为主的大型化工企业,冶炼厂进行生产的第一步是对锌精矿(主要成分是硫化锌)进行煅烧,化学反应方程式如下
2ZnS+□O2=2ZnO+□SO2
(1)在□填入合适系数,对方程式配平
(2)如需要8100吨氧化锌,进行下一步生产.则需要煅烧多少吨含硫化锌为80%的锌精矿?
12.垃圾分类就是新时尚。在去博物馆的路上,小明将空饮料瓶投入到下列 (填序号)垃圾桶中。
13.随着人类对能源的需求量益增长,可燃冰的开采、氢气的开发和利用都越来越受到人们的关注,我国在可燃冰的试开采方面已取得重大突破,形成了国际领先的新型试采工艺。
(1)可燃冰主要甲烷水合物。请写出甲烷(CH4)完全燃烧的化学方程式: 。
(2)电解水可产生氧气,如图中产生氢气的试管是 (填“1”或“2”)。
14.我们需要洁净的水源,自来水生产加入液氯的作用是 。用如图实验验证水的组成,反应的化学方程式是 。证明a管中气体的方法是 ,a和b管中气体的质量比是 。该实验证明了水是由 组成。0.5mol水中约含 个氢原子。
15.84消毒液[有效成分为次氯酸钠(NaClO)]和二氧化氯(ClO2)是常用消毒剂。
(1)NaClO中氯元素的化合价为 。
(2)ClO2属于 (填序号)。
A.混合物 B.化合物 C.氧化物
2021北京中考化学二轮复习:生活现象解释题突破
参考答案
1.垃圾分类是新时尚。补齐废弃物与垃圾桶的连线。
【解答】解:鱼刺、菜叶属于厨余垃圾;空矿泉水瓶属于可回收垃圾。
故答案为:
。
2.二氧化氯(ClO2)是安全消毒剂,杀菌能力优于Cl2,可由NaClO2与Cl2反应制得。
(1)配平化学方程式: 2 NaClO2+ 1 Cl2═ 2 ClO2+ 2 NaCl。
(2)71g Cl2完全反应,理论上最多生成ClO2的质量为 135 g。
【解答】解:(1)依据定一法,亚氯酸钠的系数定为1,所以二氧化氯、氯化钠的系数就是1,1,通过观察可知,氯气的系数为,将系数化为整数,所以化学方程式为:2NaClO2+Cl2═2ClO2+2NaCl;
(2)设理论上最多生成ClO2的质量为x
2NaClO2+Cl2═2ClO2+2NaCl
71 135
71g x
=
x=135g。
故答案为:(1)2;1;2;2;
(2)135。
3.我国大力推广在盐分高,pH>9的土壤中种植海水稻。
(1)pH>9的土壤呈 碱性 (填“酸性”或“碱性”)。
(2)大米中主要含有的营养素是 糖类 。
(3)稻壳可用于制纳米SiO2,SiO2属于 AB (填序号)。
A.氧化物
B.化合物
C.混合物
【解答】解:(1)当溶液的pH大于7时,呈碱性,pH>9的土壤呈碱性。
(2)大米中富含淀粉,淀粉属于糖类。
(3)SiO2中只含有二氧化硅一种物质,属于纯净物;是由不同种元素组成的纯净物,属于化合物;是由两种元素组成且有一种是氧元素,属于氧化物。
故答案为:
(1)碱性;
(2)糖类;
(3)AB。
4.氢气是理想的清洁、高能燃料。水分解可获得氢气和氧气。
(1)图中,产生氢气的试管是 1 (填“1”或“2”)。
(2)我国开发出一种新型催化剂,实现了在光照下分解水,反应的化学方程式为 2H2O2H2↑+O2↑ 。
【解答】解:(1)电解水时“正氧负氢,氢二氧一”,所以产生氢气的是试管1;
(2)由题意可知,我国开发出一种新型催化剂,实现了在光照下分解水,反应的化学方程式为:2H2O2H2↑+O2↑。
故答为:(1)1;(2)2H2O2H2↑+O2↑。
5.人人行动,推进垃圾分类,推动绿色发展。矿泉水瓶、旧报纸 能 (填“能”或“不能”)投入有如图标识的垃圾箱中。
【解答】解:图中标志是可回收物标志,矿泉水瓶、旧报纸属于可回收物,能投入有如图标识的垃圾箱中。
故答案为:
能。
6.H2O2可作增氧剂。常温下,用4% H2O2溶液进行实验,研究pH对H2O2分解所得溶液中溶氧量的影响,测定结果如图。
(1)H2O2分解的化学方程式为 2H2O2═2H2O+O2↑ 。
(2)分析如图得到的结论是 在常温下,当pH在8﹣12之间时,随着pH的增大,溶氧量先增大后减小,且在pH为10﹣11中间时,溶氧量达到最大值 。
【解答】解:(1)过氧化氢在常温下分解生成水和氧气,反应的化学方程式为:2H2O2═2H2O+O2↑。
(2)由pH对H2O2分解所得溶液中氧量的影响测定结果图,在常温下,当pH在8﹣12之间时,随着pH的增大,溶氧量先增大后减小,且在pH为10﹣11中间时,溶氧量达到最大值。
故答案为:
(1)2H2O2═2H2O+O2↑;
(2)在常温下,当pH在8﹣12之间时,随着pH的增大,溶氧量先增大后减小,且在pH为10﹣11中间时,溶氧量达到最大值。
7.干热岩是地层深处的热岩体。如图为利用其发电的示意图。
(1)将干热岩的热量传递到热交换器的物质是 水或水蒸气 。
(2)从微粒的角度分析,水变为水蒸气时,变化的是 分子之间的间隔 。
【解答】解:
(1)由图示可知:将干热岩的热量传递到热交换器的物质是水或水蒸气;
(2)微观角度讲,水变为水蒸气是水分子之间的间隔变大造成的,而水分子的体积不变;
答案:
(1)水或水蒸气;
(2)分子之间的间隔。
8.补齐连线。从A或B中任选一个作答,若均作答,按A计分。
A 物质﹣用途 B 物质﹣﹣主要成分
【解答】解:A干冰升华吸热,可冷藏食品;碳酸钙中含有钙元素,用于补钙剂;熟石灰呈碱性。可用于改良酸性土壤;
B天然气的主要成分是甲烷;氯化钠俗称食盐;氧化钙俗称生石灰。
答案:
9.我国大力推广在盐分高、pH>9的土壤中种植海水稻。
(1)pH>9的土壤呈 碱性 (填“酸性”或“碱性”)。
(2)大米中主要含有的营养素是 糖类 。
(3)稻壳可用于制纳米SiO2,其中Si的化合价为 +4 ,SiO2属于 AB (填序号)。
A.氧化物
B.化合物
C.混合物
【解答】解:(1)当溶液的pH等于7时,呈中性;当溶液的pH小于7时,呈酸性;当溶液的pH大于7时,呈碱性,则pH>9的土壤显碱性。
(2)大米中富含淀粉,淀粉属于糖类。
(3)氧元素显﹣2价,设硅元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(﹣2)×2=0,则x=+4价。
SiO2是由二氧化硅一种物质组成的,属于纯净物;是由不同种元素组成的纯净物,属于化合物;是由两种元素组成的且有一种是氧元素的化合物,属于氧化物。
故答案为:
(1)碱性;
(2)糖类;
(3)+4;AB。
10.工业酒精中所含甲醇是一种有毒,有酒味的可燃性液体.甲醇在氧气中不完全燃烧可发生下列反应:8CH3OH+11O2XCO2+2CO+16H2O试计算:
(1)X值是 6 ;
(2)若反应消耗4、4g氧气,则生成水的质量是多少?
【解答】解:(1)根据化学方程式的配平的原则,C的个数在生成物中应为8,在生成物中只有2CO中有2个,故x=8﹣2=6.故答案为:6.
(2)设生成水的质量是x,
8CH3OH+11O26CO2+2CO+16H2O
352 288
4.4g x
∴
解之得:x=3.6g,
答:生成水的质量是3.6g.
11.XX冶炼厂的是我市一家以生产硫酸和金属锌为主的大型化工企业,冶炼厂进行生产的第一步是对锌精矿(主要成分是硫化锌)进行煅烧,化学反应方程式如下
2ZnS+□O2=2ZnO+□SO2
(1)在□填入合适系数,对方程式配平
(2)如需要8100吨氧化锌,进行下一步生产.则需要煅烧多少吨含硫化锌为80%的锌精矿?
【解答】解:(1)化学反应前后原子个数不变,所以化学方程式为:2ZnS+3O2=2ZnO+2SO2;
(2)设需要煅烧含硫化锌为80%的锌精矿质量为x
2ZnS+3O2=2ZnO+2SO2
194 162
x×80% 8100t
=
x=12125t
故答案为:(1)2ZnS+3O2=2ZnO+2SO2;
(2)12125t.
12.垃圾分类就是新时尚。在去博物馆的路上,小明将空饮料瓶投入到下列 A (填序号)垃圾桶中。
【解答】解:空饮料瓶可以回收,回收再利用,可以节约资源防止环境污染。
故选A。
13.随着人类对能源的需求量益增长,可燃冰的开采、氢气的开发和利用都越来越受到人们的关注,我国在可燃冰的试开采方面已取得重大突破,形成了国际领先的新型试采工艺。
(1)可燃冰主要甲烷水合物。请写出甲烷(CH4)完全燃烧的化学方程式: CH4+2O2CO2+2H2O 。
(2)电解水可产生氧气,如图中产生氢气的试管是 1 (填“1”或“2”)。
【解答】解:(1)在点燃的条件下,甲烷与氧气反应生成二氧化碳和水,化学方程式为:CH4+2O2CO2+2H2O;故填:CH4+2O2CO2+2H2O;
(2)由“正氧负氢、氢二氧一”可知,如图中产生氢气的试管是1;故填:1。
14.我们需要洁净的水源,自来水生产加入液氯的作用是 杀菌消毒 。用如图实验验证水的组成,反应的化学方程式是 2H2O2H2↑+O2↑ 。证明a管中气体的方法是 用带火星木条检验,能使带火星的木条复燃 ,a和b管中气体的质量比是 8:1 。该实验证明了水是由 氢元素和氧元素 组成。0.5mol水中约含 6.02×1023 个氢原子。
【解答】解:自来水生产通入氯气的作用是杀菌消毒;水通电分解生成氢气和氧气,反应的化学方程式为:2H2O2H2↑+O2↑.a管气体少,所收集的气体是氧气,b管气体多,所收集的气体是氢气,因为氧气具有助燃性,可用带火星检验,能使带火星的木条复燃。仪器内水通直流电生成氢气和氧气,生成氢气和氧气的体积比是2:1,质量比为:8:1,该实验证明了水是由氢元素和氧元素组成的,0.5mol水中约含1mol氢原子,即6.02×1023个氢原子;
答案:杀菌消毒;2H2O2H2↑+O2↑.用带火星木条检验,能使带火星的木条复燃;8:1;氢元素和氧元素;6.02×1023
15.84消毒液[有效成分为次氯酸钠(NaClO)]和二氧化氯(ClO2)是常用消毒剂。
(1)NaClO中氯元素的化合价为 +1 。
(2)ClO2属于 BC (填序号)。
A.混合物 B.化合物 C.氧化物
【解答】解:(1)根据在化合物中正负化合价代数和为零,设氯元素的化合价为x,钠元素的化合价为+1,氧元素的化合价为﹣2,可得NaClO中氯元素的化合价为:(+1)+x+(﹣2)=0,解答x=+1;故填:+1;
(2)二氧化氯中含有两种元素,所以为化合物;并且其中一种元素为氧元素,所以为氧化物。故填:BC。
同课章节目录
