第1节 性质活泼的氧气 课件(35张PPT)
文档属性
| 名称 | 第1节 性质活泼的氧气 课件(35张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-11 00:00:00 | ||
图片预览











文档简介
(共35张PPT)
身边的化学物质2-1
性质活泼的氧气
一、氧
气
的
性
质
1.氧气的物理性质
通常状况下,氧气是一种无色无味的气体
氧气密度稍大于空气
氧气不易溶于水
在外界条件改变时,氧气可变为淡蓝色的
液体和固体
2.
氧
气
的
化
学
性
质
⑴.蜡烛在氧气中燃烧
现
象
①发出白光
②放出热量
③产生使澄清石灰水变浑浊的气体
④集气瓶内壁有小液滴产生
石蜡
+氧气
二氧化碳
+水
点燃
蜡烛在氧气中燃烧比空气中更剧烈
燃烧物自上而下缓慢伸入集气瓶的原因
充分利用集气瓶内的氧气
⑵木炭在氧气中燃烧
现象
①发出白光
②放出热量
③产生使澄清石灰水变浑浊的气体
碳
+
氧气
二氧化碳
点燃
在空气中保持红热,在氧气中剧烈燃烧
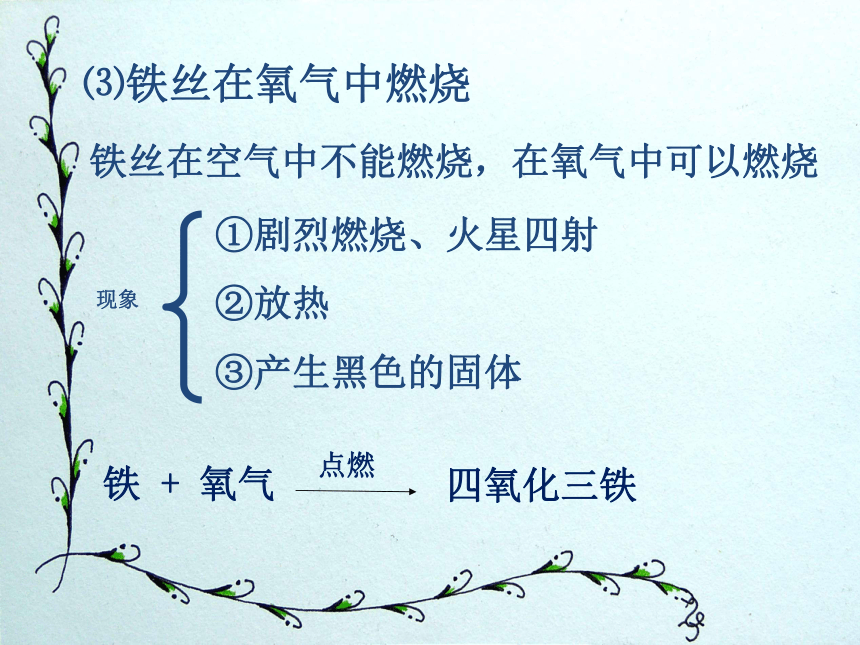
⑶铁丝在氧气中燃烧
现象
①剧烈燃烧、火星四射
②放热
③产生黑色的固体
铁
+
氧气
四氧化三铁
点燃
铁丝在空气中不能燃烧,在氧气中可以燃烧
预先在集气瓶底加少量水(或铺少量沙子)的原因:
防止反应生成的固体物质溅落瓶底,致使集气瓶炸裂
铁丝绕成螺旋状的原因:
便于传热,有利于点燃
等火柴快要燃尽时再将铁丝放入集气瓶中的原因
防止火柴消耗瓶内的氧气
⑷硫在氧气中燃烧
现象
①剧烈燃烧、明亮的蓝紫色火焰
②放出热量
③生成一种有刺激性气味的无色气体
硫在空气中燃烧发出微弱的淡蓝色火焰
硫
+
氧气
二氧化硫
点燃
集气瓶底部放少量水的原因:
吸收生成的有害气体
小结
氧气具有助燃性
氧气是一种化学性质比较活泼的气体
氧化反应
剧烈氧化
缓慢氧化
镁
+
氧气
氧化镁
点燃
二氧化碳
+
水
碳酸
硅
+
氧气
二氧化硅
高温
甲烷+氧气
二氧化碳+水
点燃
判断下列反应是否为氧化反应
碳酸钙
二氧化碳
+
氧化钙
高温
汞
+
氧气
氧化汞
加热
二、氧气的用途
供给呼吸
支持燃烧
三、氧气在自然界的存在
1.空气中各组分气体的体积分数
氮气
78
%
氧气
21%
稀有气体
0.94%
二氧化碳
0.03%
其它气体和杂质
0.03%
2.氧气在自然界中的循环
产生途径:植物的光合作用
消耗途径:呼吸作用、可燃物的燃烧等
四、氧气的制法
1、自然界中氧气的来源
光合作用:
光照
叶绿素
氧气+葡萄糖
水+二氧化碳
能量转化:太阳能
化学能
生物质能
2.氧气的工业制法
方法:分离液态空气法
原理:利用液态氮气与液态氧气的沸点不同,采取低温蒸发让氮气首先从液态空气中蒸发出来,剩下的主要就是液态氧。
过程:
3.
氧
气
的
实
验
室
制
法
方法一:加热高锰酸钾法
药品:高锰酸钾
KMnO4
仪器:
实验发生装置:
装置要点:
A.试管口要略向下倾斜
B.先预热试管,然后集中在试管底部加热
C.铁夹夹在离试管口的1/3处
表达式
KMnO4
加热
K2MnO4
+
MnO2
+
O2
高锰酸钾
锰酸钾
+二氧化锰
+氧气
加热
氧气的收集装置
氧气的物理性质
密度大于空气
不易溶于水
收集方法
排水集气法
向上排空气法
加热高锰酸钾制取氧气的操作过程及要点
查
检查装置气密性
装
填装药品(KMnO4)
定
固定装置
点
点燃酒精灯
收
收集氧气(导管口有
连续均匀气泡冒出再收集)
离
将导管移出水槽
熄
熄灭酒精灯
等导管口有大量气泡冒出再收集的原因
先取出水槽中的导管,再熄灭酒精灯的原因
刚开始排出的气泡是使试管中的空气
防止水倒吸炸裂试管。
试管口要堵一小团棉花的原因
防止粉末状药品随气流进入导管或水槽.
检验氧气集满
氧气的物理性质
密度大于空气
不易溶于水
收集方法
验满方法
向上排空气法
排水集气法
将带火星的木条放在瓶口,木条复燃,说明已集满
有大气泡从瓶口逸出
方法二:加热氯酸钾和二氧化锰的混合物
药品:氯酸钾、二氧化锰
仪器:
制备装置:
KClO3
KCl
+
O2
MnO2
加热
氯酸钾
氯化钾
氧气
方法三:双氧水(过氧化氢H2O2)分解法
药品:双氧水(过氧化氢H2O2溶液)、
二氧化锰
MnO2(黑色粉末状固体)
实验发生装置:
H2O2
MnO2
H2O
+
O2
过氧化氢
水
氧气
二氧化锰的作用:
催化剂——在化学反应中能增大化学反应速率,但本身的质量和化学性质在反应前后都没有发生变化的物质。
即“催化作用”
“加快过氧化氢反应生成氧气的速度”
Life
is
the
art
of
drawing
without
an
eraser
身边的化学物质2-1
性质活泼的氧气
一、氧
气
的
性
质
1.氧气的物理性质
通常状况下,氧气是一种无色无味的气体
氧气密度稍大于空气
氧气不易溶于水
在外界条件改变时,氧气可变为淡蓝色的
液体和固体
2.
氧
气
的
化
学
性
质
⑴.蜡烛在氧气中燃烧
现
象
①发出白光
②放出热量
③产生使澄清石灰水变浑浊的气体
④集气瓶内壁有小液滴产生
石蜡
+氧气
二氧化碳
+水
点燃
蜡烛在氧气中燃烧比空气中更剧烈
燃烧物自上而下缓慢伸入集气瓶的原因
充分利用集气瓶内的氧气
⑵木炭在氧气中燃烧
现象
①发出白光
②放出热量
③产生使澄清石灰水变浑浊的气体
碳
+
氧气
二氧化碳
点燃
在空气中保持红热,在氧气中剧烈燃烧
⑶铁丝在氧气中燃烧
现象
①剧烈燃烧、火星四射
②放热
③产生黑色的固体
铁
+
氧气
四氧化三铁
点燃
铁丝在空气中不能燃烧,在氧气中可以燃烧
预先在集气瓶底加少量水(或铺少量沙子)的原因:
防止反应生成的固体物质溅落瓶底,致使集气瓶炸裂
铁丝绕成螺旋状的原因:
便于传热,有利于点燃
等火柴快要燃尽时再将铁丝放入集气瓶中的原因
防止火柴消耗瓶内的氧气
⑷硫在氧气中燃烧
现象
①剧烈燃烧、明亮的蓝紫色火焰
②放出热量
③生成一种有刺激性气味的无色气体
硫在空气中燃烧发出微弱的淡蓝色火焰
硫
+
氧气
二氧化硫
点燃
集气瓶底部放少量水的原因:
吸收生成的有害气体
小结
氧气具有助燃性
氧气是一种化学性质比较活泼的气体
氧化反应
剧烈氧化
缓慢氧化
镁
+
氧气
氧化镁
点燃
二氧化碳
+
水
碳酸
硅
+
氧气
二氧化硅
高温
甲烷+氧气
二氧化碳+水
点燃
判断下列反应是否为氧化反应
碳酸钙
二氧化碳
+
氧化钙
高温
汞
+
氧气
氧化汞
加热
二、氧气的用途
供给呼吸
支持燃烧
三、氧气在自然界的存在
1.空气中各组分气体的体积分数
氮气
78
%
氧气
21%
稀有气体
0.94%
二氧化碳
0.03%
其它气体和杂质
0.03%
2.氧气在自然界中的循环
产生途径:植物的光合作用
消耗途径:呼吸作用、可燃物的燃烧等
四、氧气的制法
1、自然界中氧气的来源
光合作用:
光照
叶绿素
氧气+葡萄糖
水+二氧化碳
能量转化:太阳能
化学能
生物质能
2.氧气的工业制法
方法:分离液态空气法
原理:利用液态氮气与液态氧气的沸点不同,采取低温蒸发让氮气首先从液态空气中蒸发出来,剩下的主要就是液态氧。
过程:
3.
氧
气
的
实
验
室
制
法
方法一:加热高锰酸钾法
药品:高锰酸钾
KMnO4
仪器:
实验发生装置:
装置要点:
A.试管口要略向下倾斜
B.先预热试管,然后集中在试管底部加热
C.铁夹夹在离试管口的1/3处
表达式
KMnO4
加热
K2MnO4
+
MnO2
+
O2
高锰酸钾
锰酸钾
+二氧化锰
+氧气
加热
氧气的收集装置
氧气的物理性质
密度大于空气
不易溶于水
收集方法
排水集气法
向上排空气法
加热高锰酸钾制取氧气的操作过程及要点
查
检查装置气密性
装
填装药品(KMnO4)
定
固定装置
点
点燃酒精灯
收
收集氧气(导管口有
连续均匀气泡冒出再收集)
离
将导管移出水槽
熄
熄灭酒精灯
等导管口有大量气泡冒出再收集的原因
先取出水槽中的导管,再熄灭酒精灯的原因
刚开始排出的气泡是使试管中的空气
防止水倒吸炸裂试管。
试管口要堵一小团棉花的原因
防止粉末状药品随气流进入导管或水槽.
检验氧气集满
氧气的物理性质
密度大于空气
不易溶于水
收集方法
验满方法
向上排空气法
排水集气法
将带火星的木条放在瓶口,木条复燃,说明已集满
有大气泡从瓶口逸出
方法二:加热氯酸钾和二氧化锰的混合物
药品:氯酸钾、二氧化锰
仪器:
制备装置:
KClO3
KCl
+
O2
MnO2
加热
氯酸钾
氯化钾
氧气
方法三:双氧水(过氧化氢H2O2)分解法
药品:双氧水(过氧化氢H2O2溶液)、
二氧化锰
MnO2(黑色粉末状固体)
实验发生装置:
H2O2
MnO2
H2O
+
O2
过氧化氢
水
氧气
二氧化锰的作用:
催化剂——在化学反应中能增大化学反应速率,但本身的质量和化学性质在反应前后都没有发生变化的物质。
即“催化作用”
“加快过氧化氢反应生成氧气的速度”
Life
is
the
art
of
drawing
without
an
eraser
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
