高中化学人教版(2019) 必修 第一册 第一章 物质及其变化 第一节 物质的分类及转化 课件(25张ppt)
文档属性
| 名称 | 高中化学人教版(2019) 必修 第一册 第一章 物质及其变化 第一节 物质的分类及转化 课件(25张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-14 00:00:00 | ||
图片预览






文档简介
(共25张PPT)
第一节
物质的分类及转化
第1课时
物质的分类
一、物质的分类
人们常根据物质的组成,结构,性质
或者用途等进行分类
1、根据物质的组成和性质分类
由同一种元素形成几种性质不同的单质称为同素异形体
思考:O2和O3有什么相同点和不同点
化学物质
单质
化合物
酸
碱
盐
氧化物
纯净物
混合物
混合物
混合物
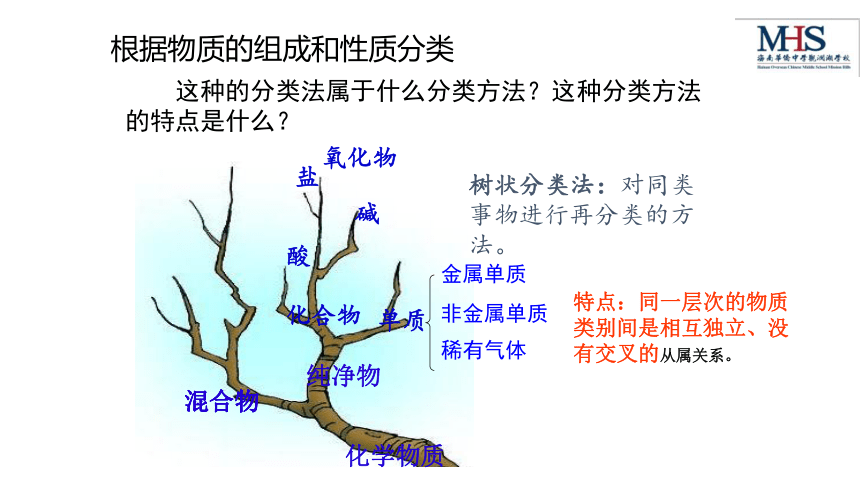
树状分类法:对同类事物进行再分类的方法。
这种的分类法属于什么分类方法?这种分类方法的特点是什么?
特点:同一层次的物质类别间是相互独立、没有交叉的从属关系。
金属单质
非金属单质
稀有气体
根据物质的组成和性质分类
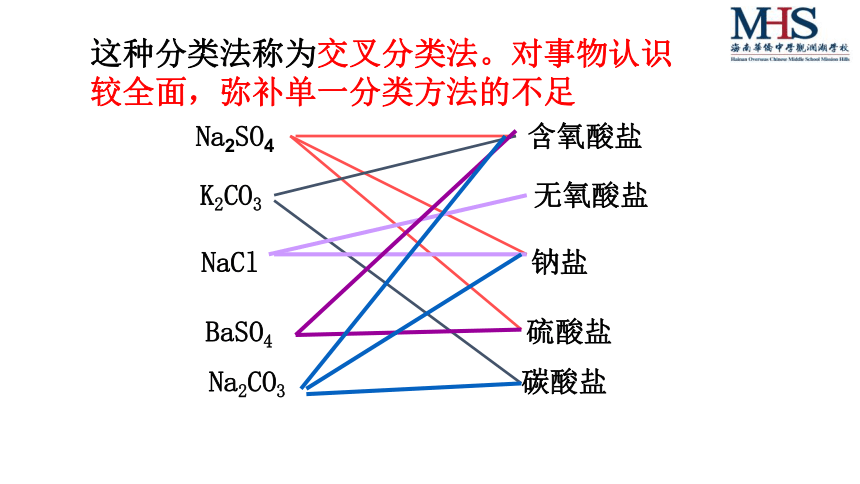
这种分类法称为交叉分类法。对事物认识较全面,弥补单一分类方法的不足
Na2SO4
含氧酸盐
K2CO3
无氧酸盐
Na2CO3
碳酸盐
NaCl
钠盐
BaSO4
硫酸盐
氧化物的分类
按组成元素分类
金属氧化物(CuO)
非金属氧化物(CO2)
按化学性质分类
酸性氧化物(CO2,SO2)
碱性氧化物(CuO,Fe2O3)
两性氧化物(Al2O3)
不成盐氧化物(CO,NO)
课堂训练
1.按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便。下列各组物质中,按“氧化物—酸—碱—盐”顺序排列的是(
)
A.CO HNO3 NaOH KNO3
B.CO2 H2CO3 Na2CO3 Ca(HCO3)2
C.H2SO4 HCl Mg(OH)2 MgCl2
D.SO3 NaHCO3 NaOH Na2SO4
2.化学概念在逻辑上存在如下关系:
对下列概念的说法正确的是(
)
A.化合物与纯净物属于重叠关系
B.化合物与碱性氧化物属于交叉关系
C.分解反应与复分解反应属于并列关系
D.钠盐与碳酸盐属于并列关系
A
C
2、分散系和胶体
一、分散系:
分散质:
分散剂:
把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。
被分散的物质。
起容纳分散质作用的物质。
分散质
分散剂
气
液
液
固
气
固
思考:你能用交叉分类法说出它们能组成哪些种分散系吗
9种分散系
(2)分散剂是液体时,按照分散质粒子的大小来分:
分散系
胶体
溶液
浊液
悬浊液
(固+水)
乳浊液
(油+水)
本质区别
[思考]有些液溶胶是透明的,用肉眼很难区别与溶液和胶体。那么,用什么方法能够将它们区别开呢?
[实验1-1]
Fe(OH)3胶体的制备
(1)实验操作
(2)实验现象:烧杯中溶液呈
色
红褐
丁达尔效应:鉴别胶体与溶液的一种常用物理方法。
应用:区别胶体与溶液
[生活中的应用]
思考:生活中还有哪些现象属于胶体的应用
溶
液
胶
体
浊
液
微粒直径d
外
观
能否通过
滤纸
丁达尔效应
能否通过半透膜
实例
<1n
m
1~100n
m
>100n
m
均一、稳定
不均一、不稳定
均一、介稳定
能
能
不能
有
能
不能
不能
食盐水
蛋白溶液、
淀粉溶液
石灰乳、
油水混合物
无
无
溶液、胶体、浊液的区别
本质特征
物理鉴别
渗析法
课堂训练
1.
下列事实与胶体性质无关的是(
)
A.
在豆浆里加入盐卤做豆腐
B.
在河流入海口处易形成沙洲
C.
一束平行光线照射蛋白质溶液时,从侧面可以看到一条光亮的通路
D.
三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀
2.
氯化铁溶液与氢氧化铁胶体具有的共同性质是(
)
A.
分散质颗粒直径都在1~100
nm之间
B.
能透过半透膜
C.
能透过滤纸
D.
呈红褐色
D
C
第2课时
物质的转化
[思考与讨论]
(1)
酸的主要化学性质归纳如下,完成下表
酸的主要化学性质
反应实例(写出化学反应方程式)
与活泼金属反应
与碱性氧化物反应
与碱反应
与某些盐反应
酸
H2SO4、HNO3、H3PO4、H2CO3
HCl、H2S
H2SO4、HNO3、HCl
H2CO3
是否含氧元素
酸性强弱
电离产生的H+数目
无氧酸
含氧酸
弱酸
强酸
一元酸
二元酸
三元酸
HNO3、HCl
H2SO4、H2CO3
H3PO4
从性质分
易挥发性酸
难挥发性酸
HCl、HNO3
H2SO4、
H3PO4
(1)酸的分类
二、物质的转化
(2)请分别归纳碱和盐这两类物质的主要化学性质
碱的化学通性:
①
酸碱指示剂:
②
+酸性氧化物→
③
+酸→
④+盐→
盐的化学通性:
①+酸→
②+碱→
③+盐2→
使紫色石蕊试液变蓝色;无色酚酞试液变红色
盐+水
盐+水
新盐+新碱
新盐+新酸
新盐+新碱
新盐3+新盐4
碱
溶解性
性质强弱
可溶性碱
强碱
弱碱
Fe(OH)3、Al(OH)3
Mg(OH)2、Cu(OH)2
NaOH、Ba(OH)2
电离出OH-的个数
难溶性碱
一元碱
二元碱
多元碱
NaOH、KOH
Mg(OH)2、
Ba(OH)2
NaOH、Ba(OH)2、KOH
NH3·H2O、Mg(OH)2
二、物质的转化
[思考与讨论]
(1)写出下列物质之间转化的化学方程式,体会金属单质到盐,非金属单质到盐的转化关系。
Ca
CaO
Ca(OH)2
CaSO4
C
CO2
H2
CO3
CaCO3
(2)对于上述转化关系,从物质分类的角度看,你有什么规律,总结并交流。
课本12页习题6,7
课堂练习
1.请按下列线索提示画出Fe、Cu、S、H2、HCl、NaOH、H2SO4、Ba(OH)2、NaHCO3、K2O、CuO、NaCl的树状分类图:
答案:Fe、Cu
S、H2 HCl、H2SO4 NaOH、Ba(OH)2
NaCl、NaHCO3 K2O、CuO
2.下列说法中正确的是( )
A.酸只有一类分类方法,可分为含氧酸和无氧酸
B.碱只有两类分类方法,可分为强碱和弱碱、一元碱和二元碱
C.氧化物不可进一步分类
D.树状分类法和交叉分类法都是常用分类方法
D
第一节
物质的分类及转化
第1课时
物质的分类
一、物质的分类
人们常根据物质的组成,结构,性质
或者用途等进行分类
1、根据物质的组成和性质分类
由同一种元素形成几种性质不同的单质称为同素异形体
思考:O2和O3有什么相同点和不同点
化学物质
单质
化合物
酸
碱
盐
氧化物
纯净物
混合物
混合物
混合物
树状分类法:对同类事物进行再分类的方法。
这种的分类法属于什么分类方法?这种分类方法的特点是什么?
特点:同一层次的物质类别间是相互独立、没有交叉的从属关系。
金属单质
非金属单质
稀有气体
根据物质的组成和性质分类
这种分类法称为交叉分类法。对事物认识较全面,弥补单一分类方法的不足
Na2SO4
含氧酸盐
K2CO3
无氧酸盐
Na2CO3
碳酸盐
NaCl
钠盐
BaSO4
硫酸盐
氧化物的分类
按组成元素分类
金属氧化物(CuO)
非金属氧化物(CO2)
按化学性质分类
酸性氧化物(CO2,SO2)
碱性氧化物(CuO,Fe2O3)
两性氧化物(Al2O3)
不成盐氧化物(CO,NO)
课堂训练
1.按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便。下列各组物质中,按“氧化物—酸—碱—盐”顺序排列的是(
)
A.CO HNO3 NaOH KNO3
B.CO2 H2CO3 Na2CO3 Ca(HCO3)2
C.H2SO4 HCl Mg(OH)2 MgCl2
D.SO3 NaHCO3 NaOH Na2SO4
2.化学概念在逻辑上存在如下关系:
对下列概念的说法正确的是(
)
A.化合物与纯净物属于重叠关系
B.化合物与碱性氧化物属于交叉关系
C.分解反应与复分解反应属于并列关系
D.钠盐与碳酸盐属于并列关系
A
C
2、分散系和胶体
一、分散系:
分散质:
分散剂:
把一种(或多种)物质分散在另一种(或多种)物质中所得到的体系。
被分散的物质。
起容纳分散质作用的物质。
分散质
分散剂
气
液
液
固
气
固
思考:你能用交叉分类法说出它们能组成哪些种分散系吗
9种分散系
(2)分散剂是液体时,按照分散质粒子的大小来分:
分散系
胶体
溶液
浊液
悬浊液
(固+水)
乳浊液
(油+水)
本质区别
[思考]有些液溶胶是透明的,用肉眼很难区别与溶液和胶体。那么,用什么方法能够将它们区别开呢?
[实验1-1]
Fe(OH)3胶体的制备
(1)实验操作
(2)实验现象:烧杯中溶液呈
色
红褐
丁达尔效应:鉴别胶体与溶液的一种常用物理方法。
应用:区别胶体与溶液
[生活中的应用]
思考:生活中还有哪些现象属于胶体的应用
溶
液
胶
体
浊
液
微粒直径d
外
观
能否通过
滤纸
丁达尔效应
能否通过半透膜
实例
<1n
m
1~100n
m
>100n
m
均一、稳定
不均一、不稳定
均一、介稳定
能
能
不能
有
能
不能
不能
食盐水
蛋白溶液、
淀粉溶液
石灰乳、
油水混合物
无
无
溶液、胶体、浊液的区别
本质特征
物理鉴别
渗析法
课堂训练
1.
下列事实与胶体性质无关的是(
)
A.
在豆浆里加入盐卤做豆腐
B.
在河流入海口处易形成沙洲
C.
一束平行光线照射蛋白质溶液时,从侧面可以看到一条光亮的通路
D.
三氯化铁溶液中滴入氢氧化钠溶液出现红褐色沉淀
2.
氯化铁溶液与氢氧化铁胶体具有的共同性质是(
)
A.
分散质颗粒直径都在1~100
nm之间
B.
能透过半透膜
C.
能透过滤纸
D.
呈红褐色
D
C
第2课时
物质的转化
[思考与讨论]
(1)
酸的主要化学性质归纳如下,完成下表
酸的主要化学性质
反应实例(写出化学反应方程式)
与活泼金属反应
与碱性氧化物反应
与碱反应
与某些盐反应
酸
H2SO4、HNO3、H3PO4、H2CO3
HCl、H2S
H2SO4、HNO3、HCl
H2CO3
是否含氧元素
酸性强弱
电离产生的H+数目
无氧酸
含氧酸
弱酸
强酸
一元酸
二元酸
三元酸
HNO3、HCl
H2SO4、H2CO3
H3PO4
从性质分
易挥发性酸
难挥发性酸
HCl、HNO3
H2SO4、
H3PO4
(1)酸的分类
二、物质的转化
(2)请分别归纳碱和盐这两类物质的主要化学性质
碱的化学通性:
①
酸碱指示剂:
②
+酸性氧化物→
③
+酸→
④+盐→
盐的化学通性:
①+酸→
②+碱→
③+盐2→
使紫色石蕊试液变蓝色;无色酚酞试液变红色
盐+水
盐+水
新盐+新碱
新盐+新酸
新盐+新碱
新盐3+新盐4
碱
溶解性
性质强弱
可溶性碱
强碱
弱碱
Fe(OH)3、Al(OH)3
Mg(OH)2、Cu(OH)2
NaOH、Ba(OH)2
电离出OH-的个数
难溶性碱
一元碱
二元碱
多元碱
NaOH、KOH
Mg(OH)2、
Ba(OH)2
NaOH、Ba(OH)2、KOH
NH3·H2O、Mg(OH)2
二、物质的转化
[思考与讨论]
(1)写出下列物质之间转化的化学方程式,体会金属单质到盐,非金属单质到盐的转化关系。
Ca
CaO
Ca(OH)2
CaSO4
C
CO2
H2
CO3
CaCO3
(2)对于上述转化关系,从物质分类的角度看,你有什么规律,总结并交流。
课本12页习题6,7
课堂练习
1.请按下列线索提示画出Fe、Cu、S、H2、HCl、NaOH、H2SO4、Ba(OH)2、NaHCO3、K2O、CuO、NaCl的树状分类图:
答案:Fe、Cu
S、H2 HCl、H2SO4 NaOH、Ba(OH)2
NaCl、NaHCO3 K2O、CuO
2.下列说法中正确的是( )
A.酸只有一类分类方法,可分为含氧酸和无氧酸
B.碱只有两类分类方法,可分为强碱和弱碱、一元碱和二元碱
C.氧化物不可进一步分类
D.树状分类法和交叉分类法都是常用分类方法
D
