水与常见的溶液
图片预览








文档简介
(共32张PPT)
水与常见的溶液
水与常见的溶液
海洋是巨大的资源宝库
O、H
H2O
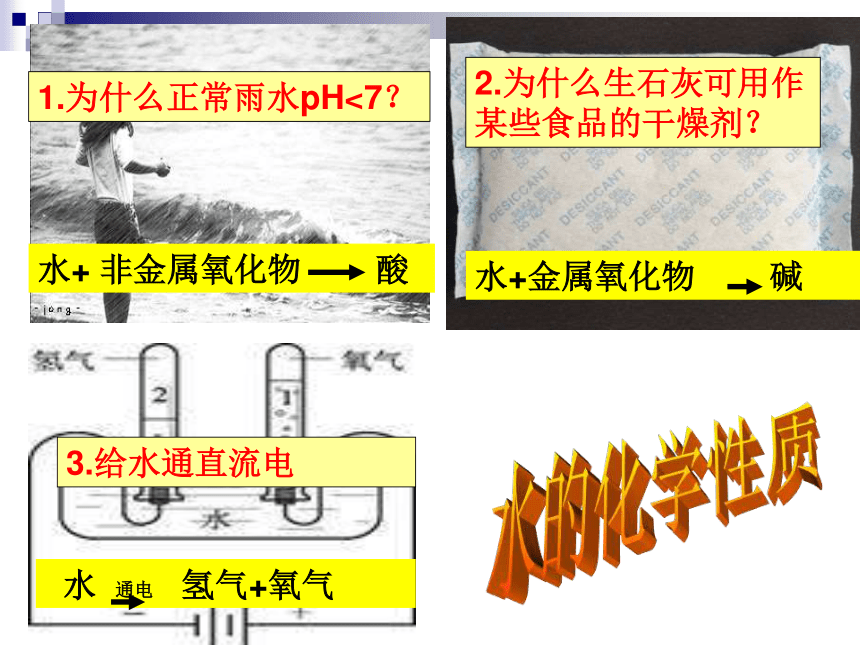
1.为什么正常雨水pH<7?
2.为什么生石灰可用作某些食品的干燥剂?
水+ 非金属氧化物 酸
水+金属氧化物 碱
3.给水通直流电
通电
水 通电 氢气+氧气
1、下列物质溶于水所得溶液的pH>7的( )
A、CaO
B、SO2
C、NaCl
D Na2CO3
AD
2、2008年5月12日14时28分,在四川汶川县发生了 8.0级地震。震后水源受到污染,人民日常用水要经过一系列的净化才能使用。请你解决如下问题:
(1)为了除去水中的不溶性杂质,可采取的操作是____,为了除去水中的异味,可以加入_____,起_____作用
(2)为降低水的硬度,在家里可以通过___________的方法实现。为了检验所得的水是软水,可以向水中加入_______。
(3)有人说:“饮用天然矿泉水对人体健康有利,矿泉水中微量元素的含量越多越好。”你认为这种说法是否正确,为什么?_____________________________________
活性炭
肥皂水
不正确,因为人体内的元素应达到平衡
加热煮沸
过滤
吸附
1、水 + 某些金属氧化物 碱
2、水 + 某些非金属氧化物 酸
3、水 氢气 + 氧气
通电
水的化学性质
盐碱湖
1、水 + 某些金属氧化物 碱
2、水 + 某些非金属氧化物 酸
3、水 氢气 + 氧气
通电
水的化学性质
夏天晒盐
冬天捞碱
1、溶液的定义、组成、基本特征是什么?
2、溶液中只能有一种溶质吗?溶质一定是固体吗?
溶剂只能是水吗?
3、物质溶于水形成溶液时有无能量的变化?举例说明。
4、溶液配制的一般步骤?每步各需用到哪些仪器?
5、什么是饱和溶液、不饱和溶液?二者如何转化?
如何让硝酸钾的饱和溶液变为不饱和溶液?
如何让氢氧化钙的不饱和溶液变为饱和溶液?
6、什么是溶解度?溶解度四要素有哪些?溶解度规律?溶解度曲线上任一点及交点的意义?
7、物质的溶解性与溶解度的关系?如何根据溶解度来确定溶解性?
8、结晶的两种方法?各适用于什么范围?
9、气体溶解度的影响因素有?它们是如何影响的?
夏天晒盐
冬天捞碱
问题组2:
结合食盐和纯碱的溶解度曲线
a、你能说出夏天晒盐冬天捞碱的道理吗?
b、如何选择物质的结晶方法?
C、食盐中混有少量纯碱如何提纯?反之?
溶解度/g
0
温度/ ℃
食盐
纯碱
问题组1:在“夏天晒盐、冬天捞碱”的过程中
a、溶液的状态发生什么变化?
b、这种变化是怎么实现的?
C、还有哪些方法可以改变溶液的状态?
1、下列关于溶液的说法中,正确的是( )
A.物质的溶解通常都伴随着能量的变化
B.溶质可以是固体,也可以不是
C.均一、稳定的液体一定是溶液
D.泥水中,泥是溶质,水是溶剂
2、下列物质不属于溶液的是( )
A. 碘酒 B.食盐水 C.盐酸 D.乙醇
AB
D
3、有一瓶饱和溶液,在温度不改变的条件下,当溶液部分蒸发而有溶质析出时,则溶液( ) A.变成不饱和溶液 B.仍是饱和溶液
C.溶质的溶解度变小D.溶质的溶解度增大
4、60℃硝酸钾溶解度为110g,该温下硝酸钾饱和溶液中有关质量关系错误的是( )
A、溶剂质量:溶液质量=10:21
B、溶剂质量:溶质质量=11:10
C、溶质质量:溶液质量=11:21
D、溶剂质量:溶质质量=10:11
B
B
5、甲、乙两种物质的溶解度曲线如右图所示。
(1)20℃时,甲物质的溶解度为_______此温度下甲物质饱和溶液中的溶质质量分数是__________
(2)根据溶解度曲线,乙物质的溶解性为____溶(易/可/微/难),欲将乙物质的饱和溶液变为不饱和溶液,可采用的方法是____________
(3)40℃时,将甲、乙两物质的饱和溶液各100g,分别降温到20℃,所得甲物质溶液的质量_________(选填“>”“=”或“<”)乙物质溶液的质量。
溶解度/g
0
温度/ ℃
乙
甲
40
20
40
40g
28.6%
<
加水,降温
易
6.下图是A、B、C三种物质的溶解度曲线,
根据图来回答:
(1)t1℃时A、B、C三种物质的溶解度
由大到小的顺序是________________
(2)t1℃时30g A物质加入到50g水中
不断搅拌,形成的溶液的质量是 _____________
(3)将t1℃时A、B、C三种物质
饱和溶液的温度升高到t2℃时,
三种溶液的溶质质量分数
由大到小的顺序是_____________
B>C>A
65g
B>C>A
- - - - - - - - -
我会总结:
能力要培养!
基础要夯实!
方法要形成!
O、H、Cl、Na、Mg ······
NaCl
混合物
H2O
分离
方法
过滤
蒸馏
结晶
蒸发结晶
降温结晶
溶液
组成
特征
配制
溶液的计算
分类
①
②
稀溶液
浓溶液
不饱和溶液
饱和溶液
溶解度
定义
四要素
表示方法
溶解度曲线
O、H、Cl、Na、Mg ······
NaCl
混合物
H2O
分离
方法
过滤
蒸馏
结晶
蒸发结晶
降温结晶
溶液
组成
特征
配制
溶液的计算
分类
①
②
稀溶液
浓溶液
不饱和溶液
饱和溶液
溶解度
定义
四要素
表示方法
溶解度曲线
元素观
微粒观
分类观
能量观
变化观
1、下列说法中正确的是( )
A.用洗洁精洗去餐具上的油污,洗洁精起到溶解作用
B.温度一定时,析出硝酸钾晶体的溶液未必是硝酸钾的饱和溶液
C.水浑浊时可加入明矾,使杂质沉降除去
D.75%的医用酒精消毒液,溶剂是酒精
C
2、下列说法正确的是( )
A、溶液的组成中一定含水
B、浓溶液不一定是饱和溶液
C、温度升高时物质的溶解度增大 。
D、20℃时36g氯化钠溶于100g水中,恰好达到饱和,则溶液中溶质的质量分数为36%
B
①卤水中含有MgCl2、KCl和MgSO4等物质,右图是它们的溶解度曲线。t1℃时,三种物质的饱和溶液中,溶质质量分数最大的是______。将t1℃的三种物质的饱和溶液加热到t2℃以上时,_______会析出晶体。
MgSO4
溶解度/g
温度/ ℃
0
t1
t2
MgCl2
KCl
MgSO4
MgCl2
3、海洋是地球上最大的储水库,浩瀚的海洋蕴含着丰富
的化学资源。我市具有较长的海岸线,海洋资源开发前景
广阔。海水晒盐能够得到粗盐和卤水。
②将粗盐提纯可以得到纯净的NaCl。欲用纯净的NaCl配制100g 0.9%的生理盐水,需要NaCl的质量为_____。配制该溶液时需要用到的玻璃仪器有________________。
如果配制的溶液的溶质质量分数低于0.9%,可能的原因是_______________(任写一个)
③在粗盐提纯的过程中,用到的分离混合物的方法有哪些?
0.9g
烧杯、玻璃棒、量筒、胶头滴管
量水时仰视读数
过滤、蒸发
4、
C
节约 用水
爱护 水资源
你懂得!
1、完成复习指导:
P26--29
2、海洋是人类千万年
来取之不尽、用之不竭
的巨大资源宝库。我们
还可以从海洋中获得哪
些物质?具体的方法是?
请你进行整理。利用学
案后面的补充习题进行
自我检测。
祝 同 学 们:在知识的海洋里自由翱翔!
O、H、Cl、Na、Mg ······
NaCl
混合物
H2O
分离
方法
过滤
蒸馏
结晶
蒸发结晶
降温结晶
溶液
组成
特征
配制
溶液的计算
分类
①
②
稀溶液
浓溶液
不饱和溶液
饱和溶液
溶解度
定义
四要素
表示方法
溶解度曲线
O、H
H2O
、Cl、Na、Mg······
NaCl
水与常见的溶液
水与常见的溶液
海洋是巨大的资源宝库
O、H
H2O
1.为什么正常雨水pH<7?
2.为什么生石灰可用作某些食品的干燥剂?
水+ 非金属氧化物 酸
水+金属氧化物 碱
3.给水通直流电
通电
水 通电 氢气+氧气
1、下列物质溶于水所得溶液的pH>7的( )
A、CaO
B、SO2
C、NaCl
D Na2CO3
AD
2、2008年5月12日14时28分,在四川汶川县发生了 8.0级地震。震后水源受到污染,人民日常用水要经过一系列的净化才能使用。请你解决如下问题:
(1)为了除去水中的不溶性杂质,可采取的操作是____,为了除去水中的异味,可以加入_____,起_____作用
(2)为降低水的硬度,在家里可以通过___________的方法实现。为了检验所得的水是软水,可以向水中加入_______。
(3)有人说:“饮用天然矿泉水对人体健康有利,矿泉水中微量元素的含量越多越好。”你认为这种说法是否正确,为什么?_____________________________________
活性炭
肥皂水
不正确,因为人体内的元素应达到平衡
加热煮沸
过滤
吸附
1、水 + 某些金属氧化物 碱
2、水 + 某些非金属氧化物 酸
3、水 氢气 + 氧气
通电
水的化学性质
盐碱湖
1、水 + 某些金属氧化物 碱
2、水 + 某些非金属氧化物 酸
3、水 氢气 + 氧气
通电
水的化学性质
夏天晒盐
冬天捞碱
1、溶液的定义、组成、基本特征是什么?
2、溶液中只能有一种溶质吗?溶质一定是固体吗?
溶剂只能是水吗?
3、物质溶于水形成溶液时有无能量的变化?举例说明。
4、溶液配制的一般步骤?每步各需用到哪些仪器?
5、什么是饱和溶液、不饱和溶液?二者如何转化?
如何让硝酸钾的饱和溶液变为不饱和溶液?
如何让氢氧化钙的不饱和溶液变为饱和溶液?
6、什么是溶解度?溶解度四要素有哪些?溶解度规律?溶解度曲线上任一点及交点的意义?
7、物质的溶解性与溶解度的关系?如何根据溶解度来确定溶解性?
8、结晶的两种方法?各适用于什么范围?
9、气体溶解度的影响因素有?它们是如何影响的?
夏天晒盐
冬天捞碱
问题组2:
结合食盐和纯碱的溶解度曲线
a、你能说出夏天晒盐冬天捞碱的道理吗?
b、如何选择物质的结晶方法?
C、食盐中混有少量纯碱如何提纯?反之?
溶解度/g
0
温度/ ℃
食盐
纯碱
问题组1:在“夏天晒盐、冬天捞碱”的过程中
a、溶液的状态发生什么变化?
b、这种变化是怎么实现的?
C、还有哪些方法可以改变溶液的状态?
1、下列关于溶液的说法中,正确的是( )
A.物质的溶解通常都伴随着能量的变化
B.溶质可以是固体,也可以不是
C.均一、稳定的液体一定是溶液
D.泥水中,泥是溶质,水是溶剂
2、下列物质不属于溶液的是( )
A. 碘酒 B.食盐水 C.盐酸 D.乙醇
AB
D
3、有一瓶饱和溶液,在温度不改变的条件下,当溶液部分蒸发而有溶质析出时,则溶液( ) A.变成不饱和溶液 B.仍是饱和溶液
C.溶质的溶解度变小D.溶质的溶解度增大
4、60℃硝酸钾溶解度为110g,该温下硝酸钾饱和溶液中有关质量关系错误的是( )
A、溶剂质量:溶液质量=10:21
B、溶剂质量:溶质质量=11:10
C、溶质质量:溶液质量=11:21
D、溶剂质量:溶质质量=10:11
B
B
5、甲、乙两种物质的溶解度曲线如右图所示。
(1)20℃时,甲物质的溶解度为_______此温度下甲物质饱和溶液中的溶质质量分数是__________
(2)根据溶解度曲线,乙物质的溶解性为____溶(易/可/微/难),欲将乙物质的饱和溶液变为不饱和溶液,可采用的方法是____________
(3)40℃时,将甲、乙两物质的饱和溶液各100g,分别降温到20℃,所得甲物质溶液的质量_________(选填“>”“=”或“<”)乙物质溶液的质量。
溶解度/g
0
温度/ ℃
乙
甲
40
20
40
40g
28.6%
<
加水,降温
易
6.下图是A、B、C三种物质的溶解度曲线,
根据图来回答:
(1)t1℃时A、B、C三种物质的溶解度
由大到小的顺序是________________
(2)t1℃时30g A物质加入到50g水中
不断搅拌,形成的溶液的质量是 _____________
(3)将t1℃时A、B、C三种物质
饱和溶液的温度升高到t2℃时,
三种溶液的溶质质量分数
由大到小的顺序是_____________
B>C>A
65g
B>C>A
- - - - - - - - -
我会总结:
能力要培养!
基础要夯实!
方法要形成!
O、H、Cl、Na、Mg ······
NaCl
混合物
H2O
分离
方法
过滤
蒸馏
结晶
蒸发结晶
降温结晶
溶液
组成
特征
配制
溶液的计算
分类
①
②
稀溶液
浓溶液
不饱和溶液
饱和溶液
溶解度
定义
四要素
表示方法
溶解度曲线
O、H、Cl、Na、Mg ······
NaCl
混合物
H2O
分离
方法
过滤
蒸馏
结晶
蒸发结晶
降温结晶
溶液
组成
特征
配制
溶液的计算
分类
①
②
稀溶液
浓溶液
不饱和溶液
饱和溶液
溶解度
定义
四要素
表示方法
溶解度曲线
元素观
微粒观
分类观
能量观
变化观
1、下列说法中正确的是( )
A.用洗洁精洗去餐具上的油污,洗洁精起到溶解作用
B.温度一定时,析出硝酸钾晶体的溶液未必是硝酸钾的饱和溶液
C.水浑浊时可加入明矾,使杂质沉降除去
D.75%的医用酒精消毒液,溶剂是酒精
C
2、下列说法正确的是( )
A、溶液的组成中一定含水
B、浓溶液不一定是饱和溶液
C、温度升高时物质的溶解度增大 。
D、20℃时36g氯化钠溶于100g水中,恰好达到饱和,则溶液中溶质的质量分数为36%
B
①卤水中含有MgCl2、KCl和MgSO4等物质,右图是它们的溶解度曲线。t1℃时,三种物质的饱和溶液中,溶质质量分数最大的是______。将t1℃的三种物质的饱和溶液加热到t2℃以上时,_______会析出晶体。
MgSO4
溶解度/g
温度/ ℃
0
t1
t2
MgCl2
KCl
MgSO4
MgCl2
3、海洋是地球上最大的储水库,浩瀚的海洋蕴含着丰富
的化学资源。我市具有较长的海岸线,海洋资源开发前景
广阔。海水晒盐能够得到粗盐和卤水。
②将粗盐提纯可以得到纯净的NaCl。欲用纯净的NaCl配制100g 0.9%的生理盐水,需要NaCl的质量为_____。配制该溶液时需要用到的玻璃仪器有________________。
如果配制的溶液的溶质质量分数低于0.9%,可能的原因是_______________(任写一个)
③在粗盐提纯的过程中,用到的分离混合物的方法有哪些?
0.9g
烧杯、玻璃棒、量筒、胶头滴管
量水时仰视读数
过滤、蒸发
4、
C
节约 用水
爱护 水资源
你懂得!
1、完成复习指导:
P26--29
2、海洋是人类千万年
来取之不尽、用之不竭
的巨大资源宝库。我们
还可以从海洋中获得哪
些物质?具体的方法是?
请你进行整理。利用学
案后面的补充习题进行
自我检测。
祝 同 学 们:在知识的海洋里自由翱翔!
O、H、Cl、Na、Mg ······
NaCl
混合物
H2O
分离
方法
过滤
蒸馏
结晶
蒸发结晶
降温结晶
溶液
组成
特征
配制
溶液的计算
分类
①
②
稀溶液
浓溶液
不饱和溶液
饱和溶液
溶解度
定义
四要素
表示方法
溶解度曲线
O、H
H2O
、Cl、Na、Mg······
NaCl
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
