2020-2021学年人教版初中化学九年级下册第八单元课题3 金属资源的利用和保护 课 件(共29张PPT)
文档属性
| 名称 | 2020-2021学年人教版初中化学九年级下册第八单元课题3 金属资源的利用和保护 课 件(共29张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-14 00:00:00 | ||
图片预览







文档简介
(共29张PPT)
1.金属活动性顺序表:
K
Ca
Na
Mg
Al
Zn
Fe
Sn
Pb
(H)
Cu
Hg
Ag
Pt
Au
金属活动性由强逐渐减弱
前提测评
(1)铝与稀硫酸
(2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液
(4)镁与硝酸银溶液
(5)银与稀盐酸
(6)铜与氯化银固体
2.、下列物质能否发生反应?写出能发生反应的化学方程式。
人类生活离不开金属
金属有广泛的用途,对于人类社会起着不可替代的作用!
军事与科技也需要大量的金属
学习目标
知道一些常见金属如铁、铝、铜等矿石。
了解从铁矿石中将铁还原出来的原理,方法及操作。
会根据化学方程式对某些含有杂质的反应物或生成物进行有关计算。
预习检测
1、地球上的金属资源除少数很不活泼的金属如
等有单质形式存在,其余都以化合物存在。
2.
写出以下矿石的主要成分。赤铁
矿
磁铁矿
3.CO还原氧化铁:(1)实验现象
(2)化学方程式为
_。
4.某钢铁厂高炉炼铁的主要原料是焦炭,磁铁矿石,空气等,主要反应过程如下
焦炭
------------------→
(
)----------------
→
②
(
)——————→
③铁
1.在上面方框中填写化学式。
2.写出2,3两步的化学方程式。
②
C
+
CO2
═
2CO
③
Fe3O4
+
4CO═
3Fe
+
4CO2
______________________________________________
Fe3O4+
4CO
═
3
Fe
+4CO2
__________________________________________________
过量空气,高温
焦炭,高温
磁铁矿,高温
金,银
Fe2O3
Fe3O4
红色粉末逐渐变为黑色,
澄清的石灰水变浑浊
CO2
高温
CO
高温
Fe2O3
+
3CO
═
2Fe
+
3CO2
高温
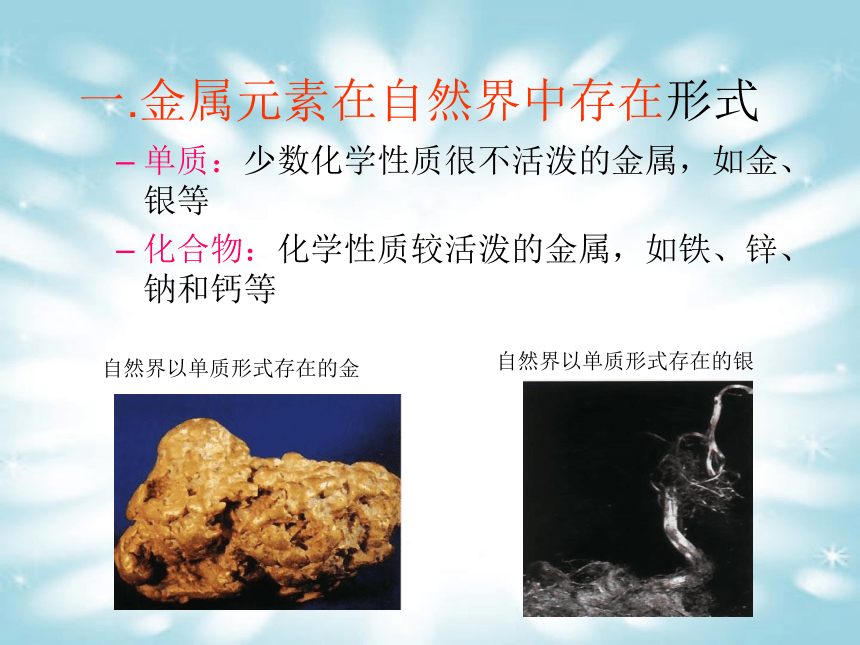
一.金属元素在自然界中存在形式
单质:少数化学性质很不活泼的金属,如金、银等
化合物:化学性质较活泼的金属,如铁、锌、钠和钙等
孔雀石(Cu2(OH)2CO3
)
自然界以单质形式存在的金
自然界以单质形式存在的银
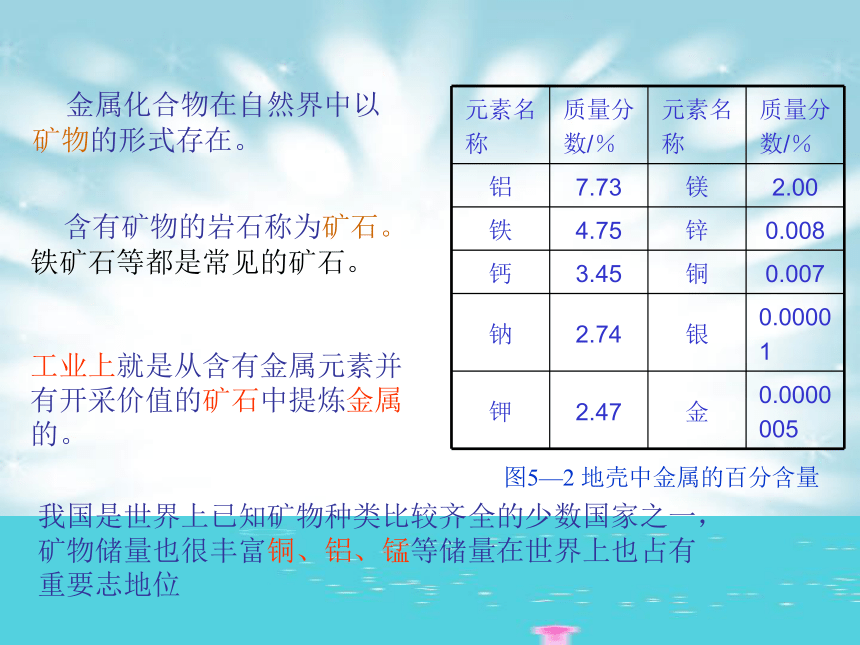
图5—2
地壳中金属的百分含量
含有矿物的岩石称为矿石。铁矿石等都是常见的矿石。
工业上就是从含有金属元素并有开采价值的矿石中提炼金属的。
金属化合物在自然界中以矿物的形式存在。
元素名称
质量分数/%
元素名称
质量分数/%
铝
7.73
镁
2.00
铁
4.75
锌
0.008
钙
3.45
铜
0.007
钠
2.74
银
0.00001
钾
2.47
金
0.0000005
我国是世界上已知矿物种类比较齐全的少数国家之一,矿物储量也很丰富铜、铝、锰等储量在世界上也占有重要志地位
赤铁矿
黄铁矿FeS2
菱铁矿FeCO3
铝士矿Al2O3
孔雀石
Fe2O3
常见几种金属矿物的成分
孔雀石(Cu2(OH)2CO3
)
磁铁矿(主要成分Fe3O4)
讨论
你认为哪一种铁矿石最不适宜于炼铁?
你认为最适宜炼铁的矿石是什么?
2、铁矿和赤铁矿最适宜炼铁。因为这两种矿石含铁量高,便于冶炼污染小。
1、黄铁矿不适宜炼铁。因为黄铁矿含铁量少,而且含硫元素,在冶炼过程中会产生SO2的有害气体。工业上主要用黄铁矿来制造硫酸。
为纪念1996年中国钢产产量突破1亿吨而发行的邮票
上海宝山钢铁公司炼铁高炉
目前人类从自然界提取量最大的金属是铁
二.
铁的冶炼
早在春秋战国时期,我国就开始生产和使用铁器,
从公元1世纪起,铁便成了一种最主要的金属材料。
炼铁的设备是高炉。
炼铁的主要原料是铁矿石、焦炭、石灰石和空气。
炼铁的原理:在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
工业炼铁
讨论
1.高炉炼铁时焦炭的作用是什么?
2.石灰石的作用是什么?
3.为什么生铁出口低于炉渣出口?
1.焦炭的作用是提供热量,产生CO。
2.石灰石的作用是将矿石中的二氧化硅转化为炉渣。
3
.因为生铁的密度大于炉渣。
实验室模拟冶炼铁的实验装置图
实验步骤:
1、检查装置气密性
2、将适量的氧化铁装入试管并固定装置
3、点燃右边酒精灯
4、通入一氧化碳气体
5、点燃酒精喷灯给氧化铁加热
6、待硬质玻璃管内红色物质完全变为黑色时停止加热
7、待玻璃管内固体冷却后停止通入一氧化碳,然后熄灭右边酒精灯
讨论与交流
1.实验前为什么先通入CO再用酒精喷灯加热?
2
.实验结束时,为什么熄灯后还要继续通入CO直至装置冷却?
3.实验尾气为什么要用酒精灯烧掉?还有什么方法处理?
4.实验过程中会看到什么现象?
5.写出相关的化学方程式方程式。
1.先通后点的原因是为了防止加热一氧化碳和空气的混合气而发生爆炸。
2.实验结束时,先熄灯后继续通气,直至装置冷却的原因是为了防止氧化铁被还原成铁后,在较高温度下又被氧化。
3.
尾气中的CO有毒,会产生大气污染。其他处理方法:a.在装置末端连接一根尖嘴导管导出尾气,深入酒精喷灯的火焰中供热.
b.在装置尾部用气球收集产生的尾气,再处理。c.用排水法收集尾气,留做CO性质时使用,即回收利用。
结论
现象:红色粉末变成黑色,澄清的石灰水变浑浊。
点燃尾气有蓝色火焰
结论:
实验室
相关的化学方程式:
Fe2O3
+
3CO
2Fe
+
3CO2
CO2
+
Ca(OH)2
CaCO3
↓+
H2O
2CO
+
O2
2CO2
点燃
高温
例题:用1000
t含氧化铁80%的赤铁矿石,理论上可以
炼出含铁96%的生铁多少
t
?
解:设理论上可以炼出含铁96%的生铁的质量为x
Fe2O3
+
3CO
═
2
Fe
+3CO2
160
2×56
1000t×80%
x·96%
∵
160
2×56
1000t×80%
x·96%
∴
x=
2×56×
1000t×80%
160×96%
=
583
.3t
答:略。
方法一
高温
分析:赤铁矿石—氧化铁—铁—生铁
方法二
分析:利用化学反应前后元素守恒。氧化铁中铁元素质量等于生成物铁的质量。
解:生铁质量为
1000t×80%
×70%÷96%=583.3t
当堂检测
1、某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,该厂理论上可以日产Fe98%的生铁多少t?
2、冶炼2000t含杂质3%的生铁,需要含Fe3O4
90%的赤铁矿石多少t?
习题1、某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,
该厂理论上可以日产Fe98%的生铁多少t?
:
解:设理论上可以炼出含铁76%的生铁的质量为x
Fe2O3
+
3CO
═
2
Fe
+3CO2
160
2×56
5000t×76%
x·98%
∵
160
2×56
5000t×76%
x·98%
∴
x=
2×56×
5000t×76%
160×98%
≈
2714t
答:略。
方法一
高温
习题2、冶炼2000t含杂质3%的生铁,需要含Fe3O4
90%
的赤铁矿
石多少t?
解:设理论上需要含Fe3O4
90%
的磁铁矿质量为x
Fe3O4+
4CO
═
3
Fe
+4CO2
232
3×56
90%x
2000t×97%
∵
232
3×56
90%
x
2000t×97%
∴
x=
232×
2000t×97%
3×56×90%
≈
2977t
答:略。
方法一
高温
巩固提升:
为了检测钢铁厂生铁样品的质量,在实验室中称去生铁屑样品10.0克放入烧杯中,加入足量的稀硫酸。加热,使之充分反应(杂质不参加反应),然后冷却称量。反应后烧杯中的质量比反应前减少了0.34克。
(1)求生铁样品中杂质的含量。
(2)生产100t这种生铁,至少需要多少吨含氧化铁80%的赤铁矿?
小结
一般含杂质计算题的思路:
1.把含杂质物质质量换算成纯物质质量。
2.利用化学方程式求出所需物质中纯物质质量。
3.再把纯物质质量换算成所需不纯物质质量。
金属冶炼的方法
金属活动性介于Zn∽Cu之间的金属,可用还原剂还原金属氧化物的方法来冶炼。
谢
谢!
1.金属活动性顺序表:
K
Ca
Na
Mg
Al
Zn
Fe
Sn
Pb
(H)
Cu
Hg
Ag
Pt
Au
金属活动性由强逐渐减弱
前提测评
(1)铝与稀硫酸
(2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液
(4)镁与硝酸银溶液
(5)银与稀盐酸
(6)铜与氯化银固体
2.、下列物质能否发生反应?写出能发生反应的化学方程式。
人类生活离不开金属
金属有广泛的用途,对于人类社会起着不可替代的作用!
军事与科技也需要大量的金属
学习目标
知道一些常见金属如铁、铝、铜等矿石。
了解从铁矿石中将铁还原出来的原理,方法及操作。
会根据化学方程式对某些含有杂质的反应物或生成物进行有关计算。
预习检测
1、地球上的金属资源除少数很不活泼的金属如
等有单质形式存在,其余都以化合物存在。
2.
写出以下矿石的主要成分。赤铁
矿
磁铁矿
3.CO还原氧化铁:(1)实验现象
(2)化学方程式为
_。
4.某钢铁厂高炉炼铁的主要原料是焦炭,磁铁矿石,空气等,主要反应过程如下
焦炭
------------------→
(
)----------------
→
②
(
)——————→
③铁
1.在上面方框中填写化学式。
2.写出2,3两步的化学方程式。
②
C
+
CO2
═
2CO
③
Fe3O4
+
4CO═
3Fe
+
4CO2
______________________________________________
Fe3O4+
4CO
═
3
Fe
+4CO2
__________________________________________________
过量空气,高温
焦炭,高温
磁铁矿,高温
金,银
Fe2O3
Fe3O4
红色粉末逐渐变为黑色,
澄清的石灰水变浑浊
CO2
高温
CO
高温
Fe2O3
+
3CO
═
2Fe
+
3CO2
高温
一.金属元素在自然界中存在形式
单质:少数化学性质很不活泼的金属,如金、银等
化合物:化学性质较活泼的金属,如铁、锌、钠和钙等
孔雀石(Cu2(OH)2CO3
)
自然界以单质形式存在的金
自然界以单质形式存在的银
图5—2
地壳中金属的百分含量
含有矿物的岩石称为矿石。铁矿石等都是常见的矿石。
工业上就是从含有金属元素并有开采价值的矿石中提炼金属的。
金属化合物在自然界中以矿物的形式存在。
元素名称
质量分数/%
元素名称
质量分数/%
铝
7.73
镁
2.00
铁
4.75
锌
0.008
钙
3.45
铜
0.007
钠
2.74
银
0.00001
钾
2.47
金
0.0000005
我国是世界上已知矿物种类比较齐全的少数国家之一,矿物储量也很丰富铜、铝、锰等储量在世界上也占有重要志地位
赤铁矿
黄铁矿FeS2
菱铁矿FeCO3
铝士矿Al2O3
孔雀石
Fe2O3
常见几种金属矿物的成分
孔雀石(Cu2(OH)2CO3
)
磁铁矿(主要成分Fe3O4)
讨论
你认为哪一种铁矿石最不适宜于炼铁?
你认为最适宜炼铁的矿石是什么?
2、铁矿和赤铁矿最适宜炼铁。因为这两种矿石含铁量高,便于冶炼污染小。
1、黄铁矿不适宜炼铁。因为黄铁矿含铁量少,而且含硫元素,在冶炼过程中会产生SO2的有害气体。工业上主要用黄铁矿来制造硫酸。
为纪念1996年中国钢产产量突破1亿吨而发行的邮票
上海宝山钢铁公司炼铁高炉
目前人类从自然界提取量最大的金属是铁
二.
铁的冶炼
早在春秋战国时期,我国就开始生产和使用铁器,
从公元1世纪起,铁便成了一种最主要的金属材料。
炼铁的设备是高炉。
炼铁的主要原料是铁矿石、焦炭、石灰石和空气。
炼铁的原理:在高温下,利用焦炭与氧气反应生成的一氧化碳把铁从铁矿石里还原出来。
工业炼铁
讨论
1.高炉炼铁时焦炭的作用是什么?
2.石灰石的作用是什么?
3.为什么生铁出口低于炉渣出口?
1.焦炭的作用是提供热量,产生CO。
2.石灰石的作用是将矿石中的二氧化硅转化为炉渣。
3
.因为生铁的密度大于炉渣。
实验室模拟冶炼铁的实验装置图
实验步骤:
1、检查装置气密性
2、将适量的氧化铁装入试管并固定装置
3、点燃右边酒精灯
4、通入一氧化碳气体
5、点燃酒精喷灯给氧化铁加热
6、待硬质玻璃管内红色物质完全变为黑色时停止加热
7、待玻璃管内固体冷却后停止通入一氧化碳,然后熄灭右边酒精灯
讨论与交流
1.实验前为什么先通入CO再用酒精喷灯加热?
2
.实验结束时,为什么熄灯后还要继续通入CO直至装置冷却?
3.实验尾气为什么要用酒精灯烧掉?还有什么方法处理?
4.实验过程中会看到什么现象?
5.写出相关的化学方程式方程式。
1.先通后点的原因是为了防止加热一氧化碳和空气的混合气而发生爆炸。
2.实验结束时,先熄灯后继续通气,直至装置冷却的原因是为了防止氧化铁被还原成铁后,在较高温度下又被氧化。
3.
尾气中的CO有毒,会产生大气污染。其他处理方法:a.在装置末端连接一根尖嘴导管导出尾气,深入酒精喷灯的火焰中供热.
b.在装置尾部用气球收集产生的尾气,再处理。c.用排水法收集尾气,留做CO性质时使用,即回收利用。
结论
现象:红色粉末变成黑色,澄清的石灰水变浑浊。
点燃尾气有蓝色火焰
结论:
实验室
相关的化学方程式:
Fe2O3
+
3CO
2Fe
+
3CO2
CO2
+
Ca(OH)2
CaCO3
↓+
H2O
2CO
+
O2
2CO2
点燃
高温
例题:用1000
t含氧化铁80%的赤铁矿石,理论上可以
炼出含铁96%的生铁多少
t
?
解:设理论上可以炼出含铁96%的生铁的质量为x
Fe2O3
+
3CO
═
2
Fe
+3CO2
160
2×56
1000t×80%
x·96%
∵
160
2×56
1000t×80%
x·96%
∴
x=
2×56×
1000t×80%
160×96%
=
583
.3t
答:略。
方法一
高温
分析:赤铁矿石—氧化铁—铁—生铁
方法二
分析:利用化学反应前后元素守恒。氧化铁中铁元素质量等于生成物铁的质量。
解:生铁质量为
1000t×80%
×70%÷96%=583.3t
当堂检测
1、某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,该厂理论上可以日产Fe98%的生铁多少t?
2、冶炼2000t含杂质3%的生铁,需要含Fe3O4
90%的赤铁矿石多少t?
习题1、某钢铁厂每天需消耗5000t含氧化铁76%的赤铁矿石,
该厂理论上可以日产Fe98%的生铁多少t?
:
解:设理论上可以炼出含铁76%的生铁的质量为x
Fe2O3
+
3CO
═
2
Fe
+3CO2
160
2×56
5000t×76%
x·98%
∵
160
2×56
5000t×76%
x·98%
∴
x=
2×56×
5000t×76%
160×98%
≈
2714t
答:略。
方法一
高温
习题2、冶炼2000t含杂质3%的生铁,需要含Fe3O4
90%
的赤铁矿
石多少t?
解:设理论上需要含Fe3O4
90%
的磁铁矿质量为x
Fe3O4+
4CO
═
3
Fe
+4CO2
232
3×56
90%x
2000t×97%
∵
232
3×56
90%
x
2000t×97%
∴
x=
232×
2000t×97%
3×56×90%
≈
2977t
答:略。
方法一
高温
巩固提升:
为了检测钢铁厂生铁样品的质量,在实验室中称去生铁屑样品10.0克放入烧杯中,加入足量的稀硫酸。加热,使之充分反应(杂质不参加反应),然后冷却称量。反应后烧杯中的质量比反应前减少了0.34克。
(1)求生铁样品中杂质的含量。
(2)生产100t这种生铁,至少需要多少吨含氧化铁80%的赤铁矿?
小结
一般含杂质计算题的思路:
1.把含杂质物质质量换算成纯物质质量。
2.利用化学方程式求出所需物质中纯物质质量。
3.再把纯物质质量换算成所需不纯物质质量。
金属冶炼的方法
金属活动性介于Zn∽Cu之间的金属,可用还原剂还原金属氧化物的方法来冶炼。
谢
谢!
同课章节目录
