2020—2021学年高二化学人教版选修3---2.2分子的立体构型 课件(18张ppt)
文档属性
| 名称 | 2020—2021学年高二化学人教版选修3---2.2分子的立体构型 课件(18张ppt) |
|
|
| 格式 | ppt | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-16 00:00:00 | ||
图片预览




文档简介
(共18张PPT)
第二节、分子的立体构型
(第1课时)
一、形形色色的分子
1、典型分子的空间构型
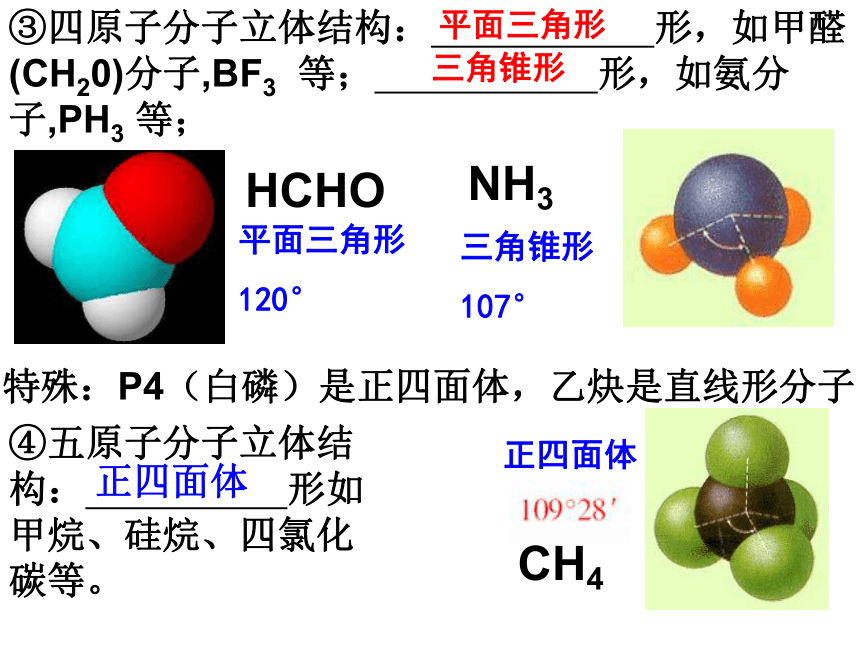
①二原子分子立体结构:一定是
形,如:HCl
CO
N2
直线
O2
HCl
②三原子分子立体结构:
形,如C02
、CS2等;
形,如H2O、S02等
直线
“V”
直线形
180°
V形
105°
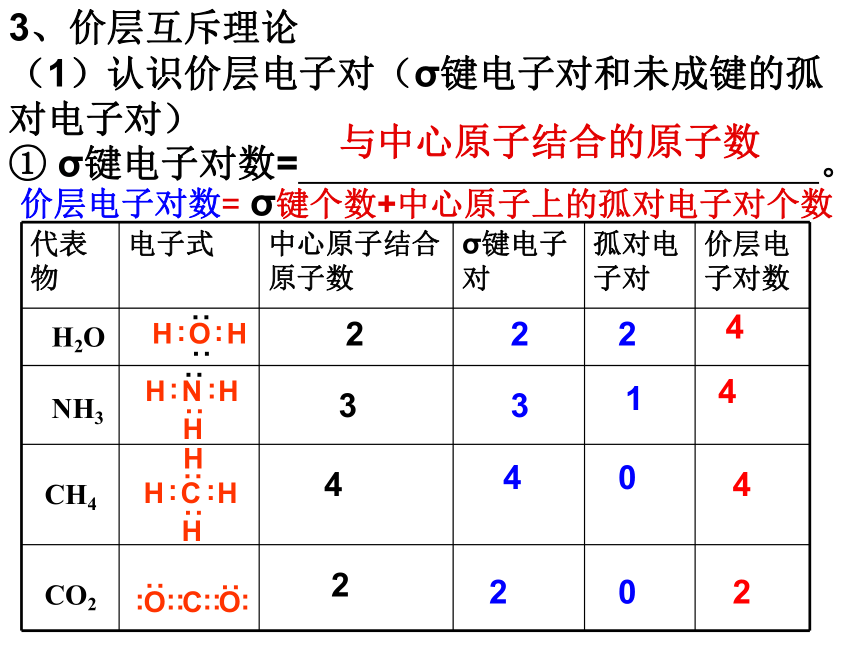
③四原子分子立体结构:
形,如甲醛(CH20)分子,BF3
等;
形,如氨分子,PH3
等;
平面三角形
三角锥形
HCHO
NH3
平面三角形
120°
三角锥形
107°
特殊:P4(白磷)是正四面体,乙炔是直线形分子。
④五原子分子立体结构:
形如甲烷、硅烷、四氯化碳等。
正四面体
CH4
正四面体
六原子分子乙烯,12原子分子苯是平面形分子。
2、测分子体结构:红外光谱仪→吸收峰→分析。
二、问题思考:同为三原子分子,CO2
和
H2O
分子的空间结构却不同,同为四原子分子,CH2O与
NH3
分子的的空间结构也不同,什么原因?
1、价层电子对互斥理论:
对ABn型的分子或离子,中心原子A价层电子对(包括用于形成共价键的共用电子对(σ键电子对)和没有成键的孤对电子)之间存在排斥力,将使分子中的原子处于尽可能远的相对位置上,以使彼此之间斥力最小,分子体系能量最低。
2、价层电子对互斥模型:
(1)中心原子上的价电子都用于形成共价键:分子中的价电子对相互排斥的结果
(2)中心原子上有孤对电子:孤对电子也要占据中心原子周围的空间,并参与互相排斥,使分子的空间结构发生变化。
(3)价电子对之间的斥力①电子对(包括共用电子对和孤对电子)之间的夹角越小,排斥力越大。
②由于成键电子对受两个原子核的吸引,所以电子云比较紧缩,而孤对电子只受到中心原子的吸引,电子云比较“肥大”,对邻近电子对的斥力较大,所以电子对之间的斥力大小顺序如下:孤电子对—孤电子对>孤电子对—成键电子>成键电子—成键电子。
价层电子对包括σ键电子对和没有成键的孤对电子
3、价层互斥理论
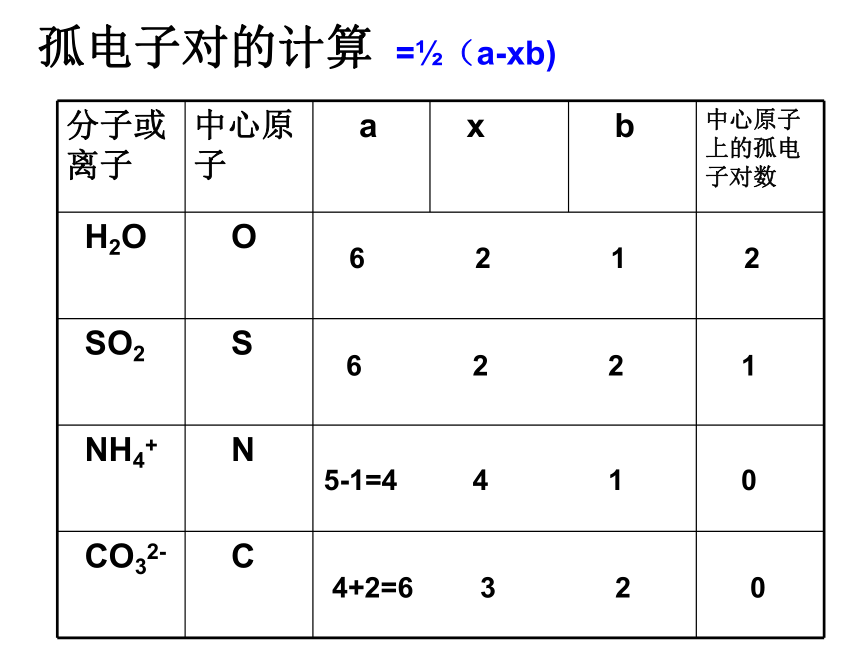
(1)认识价层电子对(σ键电子对和未成键的孤对电子对)
①
σ键电子对数=
。
与中心原子结合的原子数
=
σ键个数+中心原子上的孤对电子对个数
价层电子对数
代表物
电子式
中心原子结合原子数
σ键电子对
孤对电子对
价层电子对数
:
:
:
H
O
H
:
:
:
:
H
N
H
:
H
:
:
:
H
C
H
:
H
H
O
C
O
::
::
:
:
:
:
H2O
NH3
CO2
CH4
2
3
4
2
2
2
4
3
1
4
4
0
4
2
0
2
③中心原子上的孤电子对数=
?(a-xb)
a:
对于原子:为中心原子的
电子数。(对于阳离子:a为中心原子的
最外层电子数减去离子的
数;对于阴离子:
a为中心原子
的最外层电子数加上离子的
数)
x
为与中心原子结合的
数
b
为与中心原子结合的原子最多能接受的电子数(H为1,其他原子为“8-该原子的
电子数)
为中心原子的最外层电子数
电荷
电荷
原子
最外层
:
:
:
H
O
H
:
H2O
孤对电子对
。
O
C
O
::
::
:
:
:
:
CO2
孤对电子对
。
2
0
分子或离子
中心原子
a
x
b
中心原子上的孤电子对数
H2O
O
SO2
S
NH4+
N
CO32-
C
6
1
5-1=4
0
4+2=6
0
2
2
4
1
3
2
孤电子对的计算
6
2
2
1
=?(a-xb)
3、价层电子对互斥理论应用
①理论:对ABn型的分子或离子,中心原子A价层电子对之间存在排斥力,将使分子中的原子处于尽可能远的相对位置上,以使彼此之间斥力最小,分子体系能量最低。
②中心原子的孤对电子也要占据中心原子的空间,并与成键电子对互相排斥。价层电子对相对位置(价电子对的空间构型即VSEPR模型):
价层电子对为2
3
4
3.价电子对的空间构型即VSEPR模型
电子对数目:2
3
4
VSEPR模型:
二、价层互斥理论
直线
平面三角形
正四面体
③价电子对的空间构型即VSEPR模型应用
CH4价层电子对:
σ键电子对
。孤对电子
甲烷的VSEPR模型
空间
形。
4
0
正四面体
正四面体
NH3价层电子对:
σ键电子对
。
孤对电子
氨气的VSEPR模型
。
空间
形,氨气分子立体构型(从VSEPR模型中去掉孤对电子剩余部分)
为
及名称
。
3
1
四面体
三角锥
4
4
H2O价层电子对:
σ键电子对
。
孤对电子
。
水的VSEPR模型
。
空间
形,水分子立体构型(从VSEPR模型中去掉孤对电子剩余部分为
及名称
。
2
2
四面体
“V”形结构
4
分子或离子
σ键电子对数
孤电子对数
VSEPR模型及名称
分子的立体构型及名称
CO2
CO32-
SO2
2
3
2
0
0
1
C
O
O
C
O
O
O
S
O
O
直线形
直线形
平面三角形
平面三角形
V形
平面三角形
课堂练习:
化学式
中心原子
孤对电子数
σ键电子对数
VSEPR模型
H2S
BF3
NH2-
2
0
2
3
空间构型
V形
平面三角形
V
形
2
2
平面三角形
四面体
四面体
4、总结
(1)、ABn
型分子中心原子上的价电子都用于形成共价键,VSEPR模型和分子立体构型相同
ABn
立体结构
范例
n=2
直线型
C02、BeCl2
n=3
平面三角形
CH20、BF3
n=4
正四面体型
CH4、CCl4
n=5
三角双锥形
PCl5
n=6
正八面体形
SF6
ABn
型分子的VSEPR模型和立体结构
VSEPR
模型
成键电子对数
孤对电子对数
分子类型
电子对的排布模型
立体结构
实
例
2
3
平面
三角
形
2
0
AB2
直线形
CO2
3
0
AB3
2
1
AB2
价
层
电
子
对
数
平面三角形
BF3
V形
SO2
直线形
价层电子对数
VSEPR
模型
成键电子对数
孤对电子对数
分子类型
电子对的排布
分子构型
实
例
模型
4
正四面
体
4
0
AB4
3
1
AB3
2
2
AB2
正四面体
CH4
三角锥形
NH3
V形
H2O
第二节、分子的立体构型
(第1课时)
一、形形色色的分子
1、典型分子的空间构型
①二原子分子立体结构:一定是
形,如:HCl
CO
N2
直线
O2
HCl
②三原子分子立体结构:
形,如C02
、CS2等;
形,如H2O、S02等
直线
“V”
直线形
180°
V形
105°
③四原子分子立体结构:
形,如甲醛(CH20)分子,BF3
等;
形,如氨分子,PH3
等;
平面三角形
三角锥形
HCHO
NH3
平面三角形
120°
三角锥形
107°
特殊:P4(白磷)是正四面体,乙炔是直线形分子。
④五原子分子立体结构:
形如甲烷、硅烷、四氯化碳等。
正四面体
CH4
正四面体
六原子分子乙烯,12原子分子苯是平面形分子。
2、测分子体结构:红外光谱仪→吸收峰→分析。
二、问题思考:同为三原子分子,CO2
和
H2O
分子的空间结构却不同,同为四原子分子,CH2O与
NH3
分子的的空间结构也不同,什么原因?
1、价层电子对互斥理论:
对ABn型的分子或离子,中心原子A价层电子对(包括用于形成共价键的共用电子对(σ键电子对)和没有成键的孤对电子)之间存在排斥力,将使分子中的原子处于尽可能远的相对位置上,以使彼此之间斥力最小,分子体系能量最低。
2、价层电子对互斥模型:
(1)中心原子上的价电子都用于形成共价键:分子中的价电子对相互排斥的结果
(2)中心原子上有孤对电子:孤对电子也要占据中心原子周围的空间,并参与互相排斥,使分子的空间结构发生变化。
(3)价电子对之间的斥力①电子对(包括共用电子对和孤对电子)之间的夹角越小,排斥力越大。
②由于成键电子对受两个原子核的吸引,所以电子云比较紧缩,而孤对电子只受到中心原子的吸引,电子云比较“肥大”,对邻近电子对的斥力较大,所以电子对之间的斥力大小顺序如下:孤电子对—孤电子对>孤电子对—成键电子>成键电子—成键电子。
价层电子对包括σ键电子对和没有成键的孤对电子
3、价层互斥理论
(1)认识价层电子对(σ键电子对和未成键的孤对电子对)
①
σ键电子对数=
。
与中心原子结合的原子数
=
σ键个数+中心原子上的孤对电子对个数
价层电子对数
代表物
电子式
中心原子结合原子数
σ键电子对
孤对电子对
价层电子对数
:
:
:
H
O
H
:
:
:
:
H
N
H
:
H
:
:
:
H
C
H
:
H
H
O
C
O
::
::
:
:
:
:
H2O
NH3
CO2
CH4
2
3
4
2
2
2
4
3
1
4
4
0
4
2
0
2
③中心原子上的孤电子对数=
?(a-xb)
a:
对于原子:为中心原子的
电子数。(对于阳离子:a为中心原子的
最外层电子数减去离子的
数;对于阴离子:
a为中心原子
的最外层电子数加上离子的
数)
x
为与中心原子结合的
数
b
为与中心原子结合的原子最多能接受的电子数(H为1,其他原子为“8-该原子的
电子数)
为中心原子的最外层电子数
电荷
电荷
原子
最外层
:
:
:
H
O
H
:
H2O
孤对电子对
。
O
C
O
::
::
:
:
:
:
CO2
孤对电子对
。
2
0
分子或离子
中心原子
a
x
b
中心原子上的孤电子对数
H2O
O
SO2
S
NH4+
N
CO32-
C
6
1
5-1=4
0
4+2=6
0
2
2
4
1
3
2
孤电子对的计算
6
2
2
1
=?(a-xb)
3、价层电子对互斥理论应用
①理论:对ABn型的分子或离子,中心原子A价层电子对之间存在排斥力,将使分子中的原子处于尽可能远的相对位置上,以使彼此之间斥力最小,分子体系能量最低。
②中心原子的孤对电子也要占据中心原子的空间,并与成键电子对互相排斥。价层电子对相对位置(价电子对的空间构型即VSEPR模型):
价层电子对为2
3
4
3.价电子对的空间构型即VSEPR模型
电子对数目:2
3
4
VSEPR模型:
二、价层互斥理论
直线
平面三角形
正四面体
③价电子对的空间构型即VSEPR模型应用
CH4价层电子对:
σ键电子对
。孤对电子
甲烷的VSEPR模型
空间
形。
4
0
正四面体
正四面体
NH3价层电子对:
σ键电子对
。
孤对电子
氨气的VSEPR模型
。
空间
形,氨气分子立体构型(从VSEPR模型中去掉孤对电子剩余部分)
为
及名称
。
3
1
四面体
三角锥
4
4
H2O价层电子对:
σ键电子对
。
孤对电子
。
水的VSEPR模型
。
空间
形,水分子立体构型(从VSEPR模型中去掉孤对电子剩余部分为
及名称
。
2
2
四面体
“V”形结构
4
分子或离子
σ键电子对数
孤电子对数
VSEPR模型及名称
分子的立体构型及名称
CO2
CO32-
SO2
2
3
2
0
0
1
C
O
O
C
O
O
O
S
O
O
直线形
直线形
平面三角形
平面三角形
V形
平面三角形
课堂练习:
化学式
中心原子
孤对电子数
σ键电子对数
VSEPR模型
H2S
BF3
NH2-
2
0
2
3
空间构型
V形
平面三角形
V
形
2
2
平面三角形
四面体
四面体
4、总结
(1)、ABn
型分子中心原子上的价电子都用于形成共价键,VSEPR模型和分子立体构型相同
ABn
立体结构
范例
n=2
直线型
C02、BeCl2
n=3
平面三角形
CH20、BF3
n=4
正四面体型
CH4、CCl4
n=5
三角双锥形
PCl5
n=6
正八面体形
SF6
ABn
型分子的VSEPR模型和立体结构
VSEPR
模型
成键电子对数
孤对电子对数
分子类型
电子对的排布模型
立体结构
实
例
2
3
平面
三角
形
2
0
AB2
直线形
CO2
3
0
AB3
2
1
AB2
价
层
电
子
对
数
平面三角形
BF3
V形
SO2
直线形
价层电子对数
VSEPR
模型
成键电子对数
孤对电子对数
分子类型
电子对的排布
分子构型
实
例
模型
4
正四面
体
4
0
AB4
3
1
AB3
2
2
AB2
正四面体
CH4
三角锥形
NH3
V形
H2O
