2020-2021学年人教版高二化学选修5有机化学基础4-2糖类(1)课件 (34张ppt)
文档属性
| 名称 | 2020-2021学年人教版高二化学选修5有机化学基础4-2糖类(1)课件 (34张ppt) |

|
|
| 格式 | pptx | ||
| 文件大小 | 55.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-16 00:00:00 | ||
图片预览









文档简介
第四章
生命中的基础有机化学物质
2021.05: W
学习
目标
第二节
糖类
1.了解糖类的定义和简单分类,了解葡萄糖和果糖的结构特点,掌握葡萄糖的化学性质。
2. 了解蔗糖、麦芽糖结构和组成的关系,能区分二者的化学性质。
3.了解淀粉、纤维素的组成和性质,了解淀粉的水解反应实验。
4.掌握糖类重要的代表物葡萄糖、蔗糖、淀粉、纤维素的组成和重要性质
你吃过这些吗?
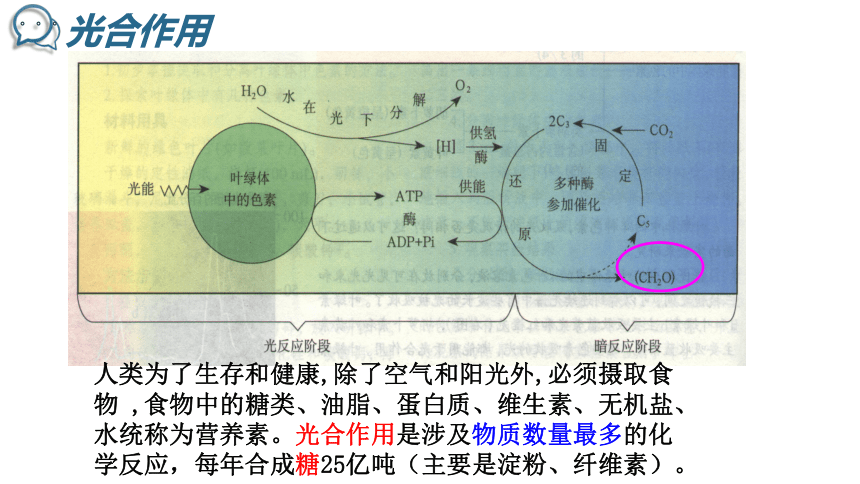
光合作用
人类为了生存和健康,除了空气和阳光外,必须摄取食物 ,食物中的糖类、油脂、蛋白质、维生素、无机盐、水统称为营养素。光合作用是涉及物质数量最多的化学反应,每年合成糖25亿吨(主要是淀粉、纤维素)。
1.阅读教材79页第1、2段和资料卡片,回答下列问题:
(1)什么是糖,由哪几种元素组成?
(2)糖是怎样分类的?
(3)糖类就是碳水化合物吗?
(4)糖都是甜的吗?
阅读思考
一.糖类
1、定义
从分子结构上看,糖类可定义为:多羟基醛、多羟基酮和它们的脱水缩合物。组成:C、H、O
2、分类
糖类
(1)单糖(不能水解成更简单的糖)葡萄糖、果糖、半乳糖、山梨糖) ,它们的分子式都为C6H12O6
(2)低聚糖( 1mol 水解产生 2 mol 单糖) (低聚糖)中最重要的是二糖:蔗糖、麦芽糖、纤维二糖和乳糖,它们的分子式都是C12H22O11
(3)多糖( 1 mol 水解产生许多摩单糖)淀粉、纤维素
1.阅读教材79页第1、2段和资料卡片,回答下列问题:
(1)什么是糖,由哪几种元素组成?
(2)糖是怎样分类的?
(3)糖类就是碳水化合物吗?
(4)糖都是甜的吗?
阅读思考
符合Cm(H2O)n通式的不一定是糖。例如:乙酸C2H4O2、乳酸C3H6O3。
有的糖不一定符合Cm(H2O)n通式。例如:脱氧核糖C5H10O4、鼠李糖
C6H12O5
有甜味的不一定是糖。如:某些食品添加剂、甘油。
糖不一定都有甜味。淀粉、纤维素就没有甜味。
糖类
碳水化合物
甜味物质
糖类
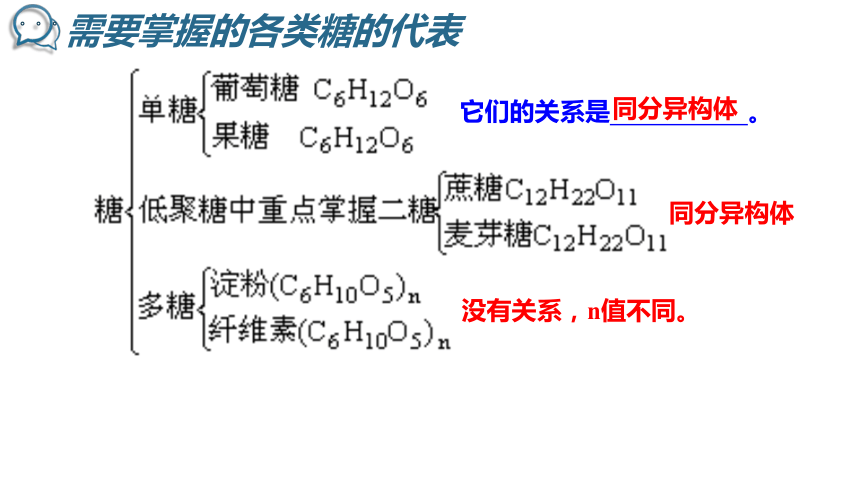
需要掌握的各类糖的代表
它们的关系是 。
同分异构体
同分异构体
没有关系,n值不同。
二.葡萄糖和果糖
1、葡萄糖
(1)物理性质
阅读教材79页第三段,了解葡萄糖的存在和物理性质。
白色晶体,熔点146℃,有甜味,但甜度不如蔗糖,易溶于水,稍溶于乙醇,不溶于乙醚。
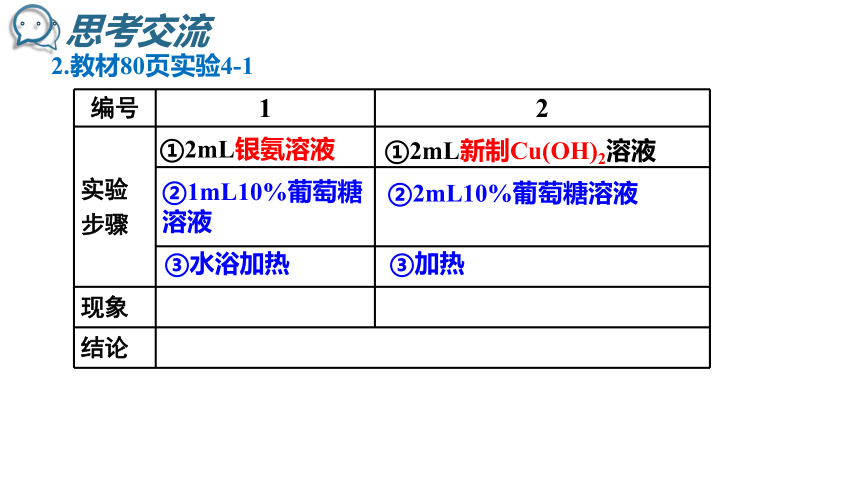
2.教材80页实验4-1
思考交流
编号
1
2
实验
步骤
现象
结论
①2mL银氨溶液
②1mL10%葡萄糖溶液
③水浴加热
①2mL新制Cu(OH)2溶液
③加热
②2mL10%葡萄糖溶液
观察学习
观察学习
2.教材80页实验4-1
思考交流
编号
1
2
实验
步骤
现象
结论
①2mL银氨溶液
②1mL10%葡萄糖溶液
③水浴加热
①2mL新制Cu(OH)2溶液
③加热
②2mL10%葡萄糖溶液
有银镜生成
有红色沉淀生成
葡萄糖分子中有醛基
1、葡萄糖
(2)葡萄糖的组成和结构
①分子式:C6H12O6
②结构式:
多羟基醛
③结构简式:
CH2OH —(CHOH )4—CHO
④官能团:(1)醛基;(2)醇羟基
3.根据葡萄糖的结构,推测应该有什么化学性质?
CH2OH —(CHOH )4—CHO
思考交流
醇的性质:置换、消去、取代、氧化
醛的性质:氧化、还原
1、葡萄糖
(3)化学性质
①加成反应(还原反应)
-CHO的性质:
CH2OH(CHOH)4CHO + H2
Ni
△
CH2OH(CHOH)4CH2OH
正己六醇
②氧化反应
使酸性KMnO4和溴水褪色、催化氧化,银镜反应及与新制Cu(OH)2反应
CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH → H2O + 2Ag↓+
CH2OH(CHOH)4COONH4+3NH3
CH2OH(CHOH)4CHO+2Cu(OH)2 +NaOH → Cu2O↓+
CH2OH(CHOH)4COONa+3H2O
1、葡萄糖
(3)化学性质
-OH的性质:
①与Na反应放出氢气;
1mol葡萄糖能与足量钠生成 mol氢气。
②Cu/Ag催化下与O2催化氧化成醛/酮
③与羧酸发生酯化反应。
1mol葡萄糖最多能与 mol乙酸反应。
④与浓HX,△,生成卤代烃和水
⑤浓H2SO4,△,生成烯烃和水。
2.5
5
1、葡萄糖
(3)化学性质
完全氧化:
C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l)
△H= – 2804 kJ/mol
发酵生成酒精:
C6H12O6 2C2H5OH +2CO2
酒化酶
1、葡萄糖
(4)用途
①生活上-----糖类;
②工业上-----制镜;
③医药上-----迅速补充营养、制葡萄糖酸钙等。
营养物质
镀银工业
制药工业
制酒工业
出现红色沉淀:有大量Cu2O生成,尿液中葡萄糖含量较高,病情较重,用“++++”表示;
出现土黄色:含糖量为中等,用“+++”表示;
出现黄绿色:含糖量为少量,用“++”表示;
出现绿色:含糖量为微量,用“+”表示;
如仍保持原来的蓝色:证明尿液中不含葡萄糖,用“—”表示。
小常识:尿糖的检验
二.葡萄糖和果糖
2、果糖
(1)分子式:
阅读教材80页果糖,了解果糖的结构、存在和物理性质。
C6H12O6
(2)结构式:
(3)结构简式:
CH2OH-CHOH-CHOH-CHOH-CO-CH2OH
或CH2OH-(CHOH)3-CO-CH2OH
(4)官能团:
羟基:-OH
羰基:
-C-
O
(5)存在:
蜂蜜、水果中
(6)物理性质:
教材80页,无色晶体,熔点103~105℃,最甜的糖,不易结晶,通常为液体,易溶于水、乙醇和乙醚。
(7)化学性质:
羟基的性质,羰基的加成。
4.教材80页【科学探究】:葡萄糖是醛糖,有还原性,葡萄糖是酮糖,是否也具有还原性?请设计实验证明果糖是否具有还原性。
思考交流
醇的性质:置换、消去、取代、氧化
醛的性质:氧化、还原
观察学习
酮糖具有酮羰基,但在碱性条件下易转化为烯二醇中间体,它可异构化为醛式,所以酮糖也易被吐伦试剂、菲林试剂氧化。(碱性条件)
拓展提升
例如:乳酸分子
CH3 C COOH
H
OH
的中间碳原子就是手性碳原子。
*
它在空间的构型有两种:(呈镜像对称,但不能完全重叠。)
象人的两只手,由于五指的构型不同,左手和右手互为实物和镜像关系,但不能完全重叠,称为手性。
分子的手性
分子的手性
HO— C —H
CHO
CH2—OH
H— C —OH
CHO
CH2—OH
D-甘油醛
L-甘油醛
分子的手性
组成:
定义:
分类
C、H、O
多羟基醛,多羟基酮和它们的脱水缩合物
单糖:葡萄糖、果糖、核糖
多糖:淀粉、纤维素
糖类
低聚糖:麦芽糖、蔗糖、乳糖
课堂小结
分子式:
结构简式:
官能团:
C6H12O6
CH2OH(CHOH )4CHO
醛基、醇羟基
醛基的性质
醇羟基的性质
葡萄糖
化学性质
用途
果糖:CH2OH(CHOH )3COCH2OH
同分异构体
课堂小结
1、葡萄糖是单糖的主要原因是( )
A、在糖类物质中含碳原子最少
B、不能水解成更简单的糖
C、分子中只有一个醛基
D、结构最简单
B
课堂练习
A. CH2OH–CHOH- CHOH-CHOH-CH2OH
B. CH2OH–CHOH- CHO
C. CH3–CHOH- COOH
木糖醇
甘油醛
乳酸
CO
SO2
N
Na
D.
糖精
B
2.下列物质属于糖类( )
3.在一定的条件下,既可以发生氧化反应又可以发生还原反应,还可以和酸发生酯化反应的是( )
A. 乙醇 B. 乙醛
C. 乙酸 D. 葡萄糖
D
课堂练习
4、下列物质具有相同的最简式的组是( )
A、乙醛 葡萄糖
B、乙酸 乙醛
C、甲醛 葡萄糖
D、乙醇 葡萄糖
C
课堂练习
7、下列反应中,葡萄糖被还原的是( )
A、葡萄糖在人体中变为CO2和H2O
B、葡萄糖发生银镜反应
C、葡萄糖加氢变为己六醇
D、葡萄糖变为乙酸葡萄糖酯
C
谢谢欣赏
生命中的基础有机化学物质
2021.05: W
学习
目标
第二节
糖类
1.了解糖类的定义和简单分类,了解葡萄糖和果糖的结构特点,掌握葡萄糖的化学性质。
2. 了解蔗糖、麦芽糖结构和组成的关系,能区分二者的化学性质。
3.了解淀粉、纤维素的组成和性质,了解淀粉的水解反应实验。
4.掌握糖类重要的代表物葡萄糖、蔗糖、淀粉、纤维素的组成和重要性质
你吃过这些吗?
光合作用
人类为了生存和健康,除了空气和阳光外,必须摄取食物 ,食物中的糖类、油脂、蛋白质、维生素、无机盐、水统称为营养素。光合作用是涉及物质数量最多的化学反应,每年合成糖25亿吨(主要是淀粉、纤维素)。
1.阅读教材79页第1、2段和资料卡片,回答下列问题:
(1)什么是糖,由哪几种元素组成?
(2)糖是怎样分类的?
(3)糖类就是碳水化合物吗?
(4)糖都是甜的吗?
阅读思考
一.糖类
1、定义
从分子结构上看,糖类可定义为:多羟基醛、多羟基酮和它们的脱水缩合物。组成:C、H、O
2、分类
糖类
(1)单糖(不能水解成更简单的糖)葡萄糖、果糖、半乳糖、山梨糖) ,它们的分子式都为C6H12O6
(2)低聚糖( 1mol 水解产生 2 mol 单糖) (低聚糖)中最重要的是二糖:蔗糖、麦芽糖、纤维二糖和乳糖,它们的分子式都是C12H22O11
(3)多糖( 1 mol 水解产生许多摩单糖)淀粉、纤维素
1.阅读教材79页第1、2段和资料卡片,回答下列问题:
(1)什么是糖,由哪几种元素组成?
(2)糖是怎样分类的?
(3)糖类就是碳水化合物吗?
(4)糖都是甜的吗?
阅读思考
符合Cm(H2O)n通式的不一定是糖。例如:乙酸C2H4O2、乳酸C3H6O3。
有的糖不一定符合Cm(H2O)n通式。例如:脱氧核糖C5H10O4、鼠李糖
C6H12O5
有甜味的不一定是糖。如:某些食品添加剂、甘油。
糖不一定都有甜味。淀粉、纤维素就没有甜味。
糖类
碳水化合物
甜味物质
糖类
需要掌握的各类糖的代表
它们的关系是 。
同分异构体
同分异构体
没有关系,n值不同。
二.葡萄糖和果糖
1、葡萄糖
(1)物理性质
阅读教材79页第三段,了解葡萄糖的存在和物理性质。
白色晶体,熔点146℃,有甜味,但甜度不如蔗糖,易溶于水,稍溶于乙醇,不溶于乙醚。
2.教材80页实验4-1
思考交流
编号
1
2
实验
步骤
现象
结论
①2mL银氨溶液
②1mL10%葡萄糖溶液
③水浴加热
①2mL新制Cu(OH)2溶液
③加热
②2mL10%葡萄糖溶液
观察学习
观察学习
2.教材80页实验4-1
思考交流
编号
1
2
实验
步骤
现象
结论
①2mL银氨溶液
②1mL10%葡萄糖溶液
③水浴加热
①2mL新制Cu(OH)2溶液
③加热
②2mL10%葡萄糖溶液
有银镜生成
有红色沉淀生成
葡萄糖分子中有醛基
1、葡萄糖
(2)葡萄糖的组成和结构
①分子式:C6H12O6
②结构式:
多羟基醛
③结构简式:
CH2OH —(CHOH )4—CHO
④官能团:(1)醛基;(2)醇羟基
3.根据葡萄糖的结构,推测应该有什么化学性质?
CH2OH —(CHOH )4—CHO
思考交流
醇的性质:置换、消去、取代、氧化
醛的性质:氧化、还原
1、葡萄糖
(3)化学性质
①加成反应(还原反应)
-CHO的性质:
CH2OH(CHOH)4CHO + H2
Ni
△
CH2OH(CHOH)4CH2OH
正己六醇
②氧化反应
使酸性KMnO4和溴水褪色、催化氧化,银镜反应及与新制Cu(OH)2反应
CH2OH(CHOH)4CHO+2[Ag(NH3)2]OH → H2O + 2Ag↓+
CH2OH(CHOH)4COONH4+3NH3
CH2OH(CHOH)4CHO+2Cu(OH)2 +NaOH → Cu2O↓+
CH2OH(CHOH)4COONa+3H2O
1、葡萄糖
(3)化学性质
-OH的性质:
①与Na反应放出氢气;
1mol葡萄糖能与足量钠生成 mol氢气。
②Cu/Ag催化下与O2催化氧化成醛/酮
③与羧酸发生酯化反应。
1mol葡萄糖最多能与 mol乙酸反应。
④与浓HX,△,生成卤代烃和水
⑤浓H2SO4,△,生成烯烃和水。
2.5
5
1、葡萄糖
(3)化学性质
完全氧化:
C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l)
△H= – 2804 kJ/mol
发酵生成酒精:
C6H12O6 2C2H5OH +2CO2
酒化酶
1、葡萄糖
(4)用途
①生活上-----糖类;
②工业上-----制镜;
③医药上-----迅速补充营养、制葡萄糖酸钙等。
营养物质
镀银工业
制药工业
制酒工业
出现红色沉淀:有大量Cu2O生成,尿液中葡萄糖含量较高,病情较重,用“++++”表示;
出现土黄色:含糖量为中等,用“+++”表示;
出现黄绿色:含糖量为少量,用“++”表示;
出现绿色:含糖量为微量,用“+”表示;
如仍保持原来的蓝色:证明尿液中不含葡萄糖,用“—”表示。
小常识:尿糖的检验
二.葡萄糖和果糖
2、果糖
(1)分子式:
阅读教材80页果糖,了解果糖的结构、存在和物理性质。
C6H12O6
(2)结构式:
(3)结构简式:
CH2OH-CHOH-CHOH-CHOH-CO-CH2OH
或CH2OH-(CHOH)3-CO-CH2OH
(4)官能团:
羟基:-OH
羰基:
-C-
O
(5)存在:
蜂蜜、水果中
(6)物理性质:
教材80页,无色晶体,熔点103~105℃,最甜的糖,不易结晶,通常为液体,易溶于水、乙醇和乙醚。
(7)化学性质:
羟基的性质,羰基的加成。
4.教材80页【科学探究】:葡萄糖是醛糖,有还原性,葡萄糖是酮糖,是否也具有还原性?请设计实验证明果糖是否具有还原性。
思考交流
醇的性质:置换、消去、取代、氧化
醛的性质:氧化、还原
观察学习
酮糖具有酮羰基,但在碱性条件下易转化为烯二醇中间体,它可异构化为醛式,所以酮糖也易被吐伦试剂、菲林试剂氧化。(碱性条件)
拓展提升
例如:乳酸分子
CH3 C COOH
H
OH
的中间碳原子就是手性碳原子。
*
它在空间的构型有两种:(呈镜像对称,但不能完全重叠。)
象人的两只手,由于五指的构型不同,左手和右手互为实物和镜像关系,但不能完全重叠,称为手性。
分子的手性
分子的手性
HO— C —H
CHO
CH2—OH
H— C —OH
CHO
CH2—OH
D-甘油醛
L-甘油醛
分子的手性
组成:
定义:
分类
C、H、O
多羟基醛,多羟基酮和它们的脱水缩合物
单糖:葡萄糖、果糖、核糖
多糖:淀粉、纤维素
糖类
低聚糖:麦芽糖、蔗糖、乳糖
课堂小结
分子式:
结构简式:
官能团:
C6H12O6
CH2OH(CHOH )4CHO
醛基、醇羟基
醛基的性质
醇羟基的性质
葡萄糖
化学性质
用途
果糖:CH2OH(CHOH )3COCH2OH
同分异构体
课堂小结
1、葡萄糖是单糖的主要原因是( )
A、在糖类物质中含碳原子最少
B、不能水解成更简单的糖
C、分子中只有一个醛基
D、结构最简单
B
课堂练习
A. CH2OH–CHOH- CHOH-CHOH-CH2OH
B. CH2OH–CHOH- CHO
C. CH3–CHOH- COOH
木糖醇
甘油醛
乳酸
CO
SO2
N
Na
D.
糖精
B
2.下列物质属于糖类( )
3.在一定的条件下,既可以发生氧化反应又可以发生还原反应,还可以和酸发生酯化反应的是( )
A. 乙醇 B. 乙醛
C. 乙酸 D. 葡萄糖
D
课堂练习
4、下列物质具有相同的最简式的组是( )
A、乙醛 葡萄糖
B、乙酸 乙醛
C、甲醛 葡萄糖
D、乙醇 葡萄糖
C
课堂练习
7、下列反应中,葡萄糖被还原的是( )
A、葡萄糖在人体中变为CO2和H2O
B、葡萄糖发生银镜反应
C、葡萄糖加氢变为己六醇
D、葡萄糖变为乙酸葡萄糖酯
C
谢谢欣赏
