实验活动6酸、碱的化学性质 课件(21张ppt)
文档属性
| 名称 | 实验活动6酸、碱的化学性质 课件(21张ppt) |

|
|
| 格式 | ppt | ||
| 文件大小 | 697.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-21 00:00:00 | ||
图片预览







文档简介
实验活动6 酸、碱的化学性质
课前学案
1.常见的酸有 等,在它们的水溶
液里由于存在相同的 (填符号),因此,
它们有很多相似的化学性质如:(写两条即可)
___________________________________________;
___________________________________________。
能使酸碱指示剂变色
盐酸、硫酸
H+
能与氢前金属反应
课前学案
2.常用的碱有 等,在它们的水
溶液里由于存在相同的 (填符号),因此,
它们有很多相似的化学性质如:(写两条即可)
___________________________________________;
___________________________________________。
能使酸碱指示剂变色
氢氧化钠、氢氧化钙
OH-
能与某些非金属氧化物反应
课堂导案
物
质
盐酸
硫酸
通性
现象或化学
方程式
现象或化学
方程式
现象或化学
方程式
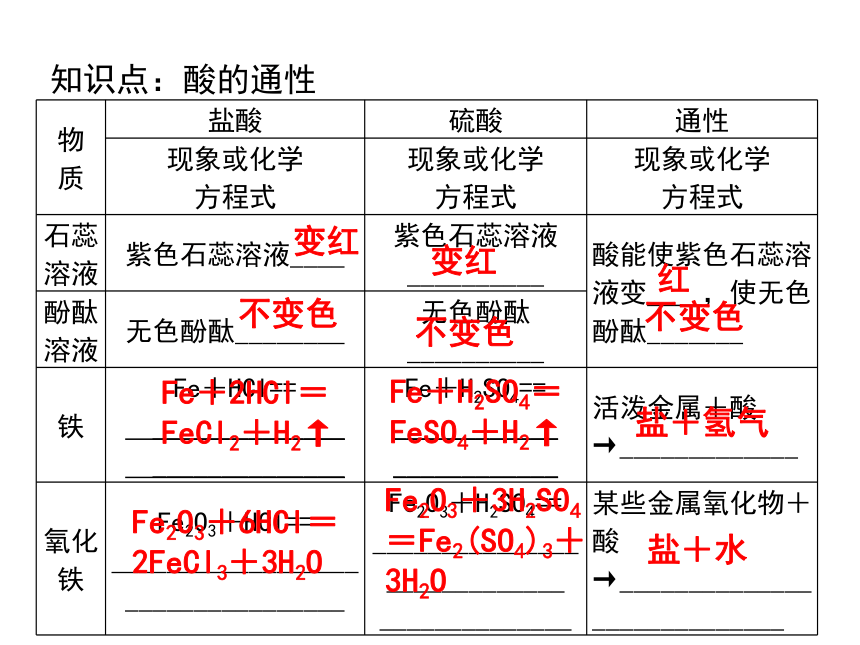
石蕊
溶液
紫色石蕊溶液____
紫色石蕊溶液__________
酸能使紫色石蕊溶液变 ,使无色酚酞_______
酚酞
溶液
无色酚酞________
无色酚酞__________
铁
Fe+HCl==
______________
______________
Fe+H2SO4==
____________
____________
活泼金属+酸
→_____________
氧化
铁
Fe2O3+HCl==
__________________________________
Fe2O3+H2SO4==
____________________________
______________
某些金属氧化物+酸→____________________________
变红
变红
不变色
不变色
红
知识点:酸的通性
不变色
Fe+2HCl=
FeCl2+H2↑
Fe+H2SO4=FeSO4+H2↑
盐+氢气
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2SO4
=Fe2(SO4)3+3H2O
盐+水
课堂导案
氢氧
化铜
2HCl+HCl===
____________________________________
Cu(OH)2+H2SO4===
__________________________________
碱+酸→
___________
碳酸
钠
Na2CO3+HCl===
___________________________________________________
Na2CO3+H2SO4===
___________________________________________________
某些盐+酸→
____________
2HCl+Cu(OH)2=CuCl2+2H2O
H2SO4+Cu(OH)2=CuSO4+2H2O
盐+水
Na2CO3+2HCl=2NaCl+H2O+CO2↑
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
新盐+新酸
课堂导案
物
质
氢氧化钠
氢氧化钙
通性
现象或化
学方程式
现象或化学
方程式
现象或化学方程式
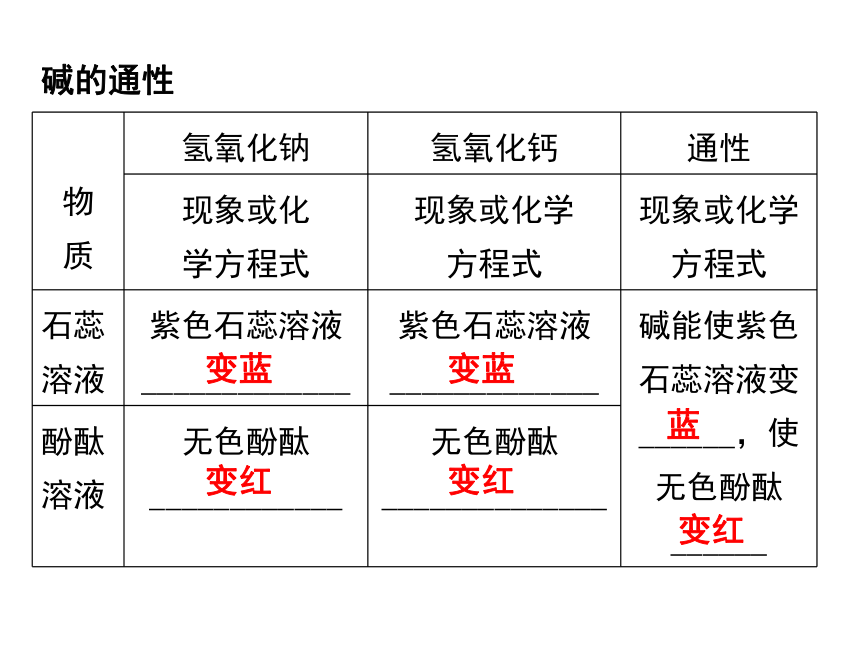
石蕊
溶液
紫色石蕊溶液_____________
紫色石蕊溶液_____________
碱能使紫色石蕊溶液变______,使无色酚酞______
酚酞
溶液
无色酚酞
____________
无色酚酞
______________
变蓝
变蓝
变红
变红
蓝
变红
碱的通性
课堂导案
二氧
化碳
CO2+NaOH═________________________________
CO2+Ca(OH)2═_____________________________
某些非金属氧化物+碱→________
硫酸
H2SO4+NaOH═______________________________
H2SO4+Ca(OH)2═__________________________
______________
酸+碱→________
硫酸
铜
CuSO4+NaOH═______________________________
_____________
CuSO4+Ca(OH)2═__________________________
______________
某些盐+碱→____________________
2NaOH+CO2=Na2CO3+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
盐+水
H2SO4+2NaOH=Na2SO4+2H2O
H2SO4+Ca(OH)2=CaSO4+2H2O
盐+水
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
CuSO4+Ca(OH)2=Cu(OH)2↓+
CaSO4
新盐+新碱
课堂导案
随堂检测
知识点1:酸、碱的通性
1.下列关于H2SO4性质描述中,不属于酸的通性的
是( )
A.使紫色石蕊溶液变红
B.与NaOH发生中和反应
C.浓硫酸滴到白纸上使纸变黑
D.与Mg反应放出氢气
C
随堂检测
A
2.有关NaOH和Ca(OH)2的说法中,正确的是
( )
A.它们的溶液都能使无色酚酞溶液变红
B.都常用于改良酸性土壤
C.它们的溶液可用稀盐酸区分
D.物理性质完全相同
课后练案
B
3.盐酸先生闯迷宫(见下图),请你帮他选择
行进路线(不发生化学反应)( )
B
4.物质X可发生以下两个反应,则X可能是( )
(1)X+碱=盐+水
(2)X+金属氧化物=盐+水
A.CaO B.H2SO4
C.NaOH D.CO
课后练案
5.碱溶液中都含有OH-,因此不同碱变现出一些
共同的性质,下列关于Ba(OH)2性质的描述
中不属于碱的共同性质的是( )
A.能与盐酸反应生成水
B.能使紫色石蕊溶液变蓝色
C.能与Na2SO4溶液反应生成BaSO4沉淀
D.能与CO2反应生成水
C
课后练案
6.要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
①固体硝酸铵和水
②镁和稀硫酸
③固体氢氧化钠和水
④氯化钠和水
⑤石灰石和稀盐酸
A.①②③④⑤ B.②③④⑤
C.①②④ D.②③⑤
课后练案
D
课后练案
偏大
7.如图是小柯同学在复习化学
时,构建酸通性的“手掌图”,
其中五个手指表示能与酸发生
化学反应的五类物质。
(1)如用湿润的pH试纸测定盐酸的pH,则结果
会 (选填“偏大”“偏小”或
“无影响”)。
(2)紫色石蕊溶液遇盐酸的现象是
____________________________________
石蕊试液变红
(3)酸能与金属氧化物反应,请你写出一点该性
质的用途:_____________。
(4)无名指上漏填的一类物质是____________。
课后练案
除铁锈
碱
H2SO4+CuO=CuSO4+H2O
课后练案
8.归纳总结是学习化学的一种方法.请结合小明同
学对碱的四点化学性质的归纳图完成下列问题。
(箭头上方的物质是指与碱反应的物质)
(1)碱溶液能使无色酚酞溶液变 。
(2)氢氧化钠暴露在空气中变质的化学方程式为
_______________________________________,
所以氢氧化钠必须 保存。
2NaOH+CO2=Na2CO3+H2O
红色
密封
课后练案
(3)请帮小明补充完整性质3箭头上方的反 应
物质是 (选填“酸”或“碱”
或“盐”)。
(4)碱溶液有相似的化学性质,是因为碱溶液
中都含有 (填化学符号)。
酸
OH-
拓展提升
9.现有以下曲线,与之对应的叙述不相符的是( )
A
拓展提升
10. 酸是一类非常重要的化合物,请回答下列问题:
(1)向氧化铁粉末中加入足量的稀盐酸,反应
的现象是 ,其
中反应的方程式为
_______________________________________。
Fe2O3+6HCl===2FeCl3+3H2O
氧化铁粉末溶解,生成黄色溶液
拓展提升
(2)白醋、柠檬酸溶液也能与氧化铁粉末发生类
似的反应,说明白醋、柠檬酸溶液、盐酸中都含
有的离子是 。(填离子符号)
(3)甲酸可解离出H+和HCOO-,甲酸与氢氧化钠
反应的方程式为HCOOH+NaOH===HCOONa+H2O,请
写出镁和甲酸反应的化学方程式
_________________________________________。
Mg+2HCOOH===(HCOO)2Mg+H2↑
H+
课前学案
1.常见的酸有 等,在它们的水溶
液里由于存在相同的 (填符号),因此,
它们有很多相似的化学性质如:(写两条即可)
___________________________________________;
___________________________________________。
能使酸碱指示剂变色
盐酸、硫酸
H+
能与氢前金属反应
课前学案
2.常用的碱有 等,在它们的水
溶液里由于存在相同的 (填符号),因此,
它们有很多相似的化学性质如:(写两条即可)
___________________________________________;
___________________________________________。
能使酸碱指示剂变色
氢氧化钠、氢氧化钙
OH-
能与某些非金属氧化物反应
课堂导案
物
质
盐酸
硫酸
通性
现象或化学
方程式
现象或化学
方程式
现象或化学
方程式
石蕊
溶液
紫色石蕊溶液____
紫色石蕊溶液__________
酸能使紫色石蕊溶液变 ,使无色酚酞_______
酚酞
溶液
无色酚酞________
无色酚酞__________
铁
Fe+HCl==
______________
______________
Fe+H2SO4==
____________
____________
活泼金属+酸
→_____________
氧化
铁
Fe2O3+HCl==
__________________________________
Fe2O3+H2SO4==
____________________________
______________
某些金属氧化物+酸→____________________________
变红
变红
不变色
不变色
红
知识点:酸的通性
不变色
Fe+2HCl=
FeCl2+H2↑
Fe+H2SO4=FeSO4+H2↑
盐+氢气
Fe2O3+6HCl=2FeCl3+3H2O
Fe2O3+3H2SO4
=Fe2(SO4)3+3H2O
盐+水
课堂导案
氢氧
化铜
2HCl+HCl===
____________________________________
Cu(OH)2+H2SO4===
__________________________________
碱+酸→
___________
碳酸
钠
Na2CO3+HCl===
___________________________________________________
Na2CO3+H2SO4===
___________________________________________________
某些盐+酸→
____________
2HCl+Cu(OH)2=CuCl2+2H2O
H2SO4+Cu(OH)2=CuSO4+2H2O
盐+水
Na2CO3+2HCl=2NaCl+H2O+CO2↑
Na2CO3+H2SO4=Na2SO4+H2O+CO2↑
新盐+新酸
课堂导案
物
质
氢氧化钠
氢氧化钙
通性
现象或化
学方程式
现象或化学
方程式
现象或化学方程式
石蕊
溶液
紫色石蕊溶液_____________
紫色石蕊溶液_____________
碱能使紫色石蕊溶液变______,使无色酚酞______
酚酞
溶液
无色酚酞
____________
无色酚酞
______________
变蓝
变蓝
变红
变红
蓝
变红
碱的通性
课堂导案
二氧
化碳
CO2+NaOH═________________________________
CO2+Ca(OH)2═_____________________________
某些非金属氧化物+碱→________
硫酸
H2SO4+NaOH═______________________________
H2SO4+Ca(OH)2═__________________________
______________
酸+碱→________
硫酸
铜
CuSO4+NaOH═______________________________
_____________
CuSO4+Ca(OH)2═__________________________
______________
某些盐+碱→____________________
2NaOH+CO2=Na2CO3+H2O
CO2+Ca(OH)2=CaCO3↓+H2O
盐+水
H2SO4+2NaOH=Na2SO4+2H2O
H2SO4+Ca(OH)2=CaSO4+2H2O
盐+水
CuSO4+2NaOH=Cu(OH)2↓+Na2SO4
CuSO4+Ca(OH)2=Cu(OH)2↓+
CaSO4
新盐+新碱
课堂导案
随堂检测
知识点1:酸、碱的通性
1.下列关于H2SO4性质描述中,不属于酸的通性的
是( )
A.使紫色石蕊溶液变红
B.与NaOH发生中和反应
C.浓硫酸滴到白纸上使纸变黑
D.与Mg反应放出氢气
C
随堂检测
A
2.有关NaOH和Ca(OH)2的说法中,正确的是
( )
A.它们的溶液都能使无色酚酞溶液变红
B.都常用于改良酸性土壤
C.它们的溶液可用稀盐酸区分
D.物理性质完全相同
课后练案
B
3.盐酸先生闯迷宫(见下图),请你帮他选择
行进路线(不发生化学反应)( )
B
4.物质X可发生以下两个反应,则X可能是( )
(1)X+碱=盐+水
(2)X+金属氧化物=盐+水
A.CaO B.H2SO4
C.NaOH D.CO
课后练案
5.碱溶液中都含有OH-,因此不同碱变现出一些
共同的性质,下列关于Ba(OH)2性质的描述
中不属于碱的共同性质的是( )
A.能与盐酸反应生成水
B.能使紫色石蕊溶液变蓝色
C.能与Na2SO4溶液反应生成BaSO4沉淀
D.能与CO2反应生成水
C
课后练案
6.要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
①固体硝酸铵和水
②镁和稀硫酸
③固体氢氧化钠和水
④氯化钠和水
⑤石灰石和稀盐酸
A.①②③④⑤ B.②③④⑤
C.①②④ D.②③⑤
课后练案
D
课后练案
偏大
7.如图是小柯同学在复习化学
时,构建酸通性的“手掌图”,
其中五个手指表示能与酸发生
化学反应的五类物质。
(1)如用湿润的pH试纸测定盐酸的pH,则结果
会 (选填“偏大”“偏小”或
“无影响”)。
(2)紫色石蕊溶液遇盐酸的现象是
____________________________________
石蕊试液变红
(3)酸能与金属氧化物反应,请你写出一点该性
质的用途:_____________。
(4)无名指上漏填的一类物质是____________。
课后练案
除铁锈
碱
H2SO4+CuO=CuSO4+H2O
课后练案
8.归纳总结是学习化学的一种方法.请结合小明同
学对碱的四点化学性质的归纳图完成下列问题。
(箭头上方的物质是指与碱反应的物质)
(1)碱溶液能使无色酚酞溶液变 。
(2)氢氧化钠暴露在空气中变质的化学方程式为
_______________________________________,
所以氢氧化钠必须 保存。
2NaOH+CO2=Na2CO3+H2O
红色
密封
课后练案
(3)请帮小明补充完整性质3箭头上方的反 应
物质是 (选填“酸”或“碱”
或“盐”)。
(4)碱溶液有相似的化学性质,是因为碱溶液
中都含有 (填化学符号)。
酸
OH-
拓展提升
9.现有以下曲线,与之对应的叙述不相符的是( )
A
拓展提升
10. 酸是一类非常重要的化合物,请回答下列问题:
(1)向氧化铁粉末中加入足量的稀盐酸,反应
的现象是 ,其
中反应的方程式为
_______________________________________。
Fe2O3+6HCl===2FeCl3+3H2O
氧化铁粉末溶解,生成黄色溶液
拓展提升
(2)白醋、柠檬酸溶液也能与氧化铁粉末发生类
似的反应,说明白醋、柠檬酸溶液、盐酸中都含
有的离子是 。(填离子符号)
(3)甲酸可解离出H+和HCOO-,甲酸与氢氧化钠
反应的方程式为HCOOH+NaOH===HCOONa+H2O,请
写出镁和甲酸反应的化学方程式
_________________________________________。
Mg+2HCOOH===(HCOO)2Mg+H2↑
H+
同课章节目录
