福建省南安市侨光一高2020-2021学年高一下学期期中阶段考试化学试题 Word版含答案
文档属性
| 名称 | 福建省南安市侨光一高2020-2021学年高一下学期期中阶段考试化学试题 Word版含答案 |  | |
| 格式 | docx | ||
| 文件大小 | 160.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-25 08:12:10 | ||
图片预览



文档简介
侨光一高2020-2021学年高一下学期期中阶段考试
化学试卷
考试时间:90分钟 满分:100
可能用到的相对原子质量:H 1 C 12 O 16
第Ⅰ卷
一、单选题(1-10每小题2分,11-18每小题3分,共44分)
1.被称为人体冷冻学之父的罗伯特·埃廷格在1962年写出《不朽的前景》一书。他在书中列举了大量事实,证明了冷冻复活的可能。比如,许多昆虫和低等生物冬天都冻僵起来,春天又自动复活。下列结论中与上述信息相关的是
A.化学反应前后质量守恒 B.低温下分子无法运动
C.温度降低,化学反应停止 D.温度越低,化学反应越慢
2.球形尖晶石(LiMn2O4)属于等轴晶系,可作耐火材料,常用低温电解法制备,制备过程中的能量转化形式是
A.电能转化为化学能 B.化学能转化为电能
C.机械能转化为化学能 D.化学能转化为机械能
3. 纪录片《舌尖上的中国》展示了中华饮食文化的博大精深。下列烹饪用品的调味成分属于酯类的是
A.食盐 B.大豆油 C.陈醋 D.蔗糖
4.下列化合物中,不能由单质直接化合而得到的是
A. Fe3O4 B. Na2O2 C. FeCl2 D. CuCl2
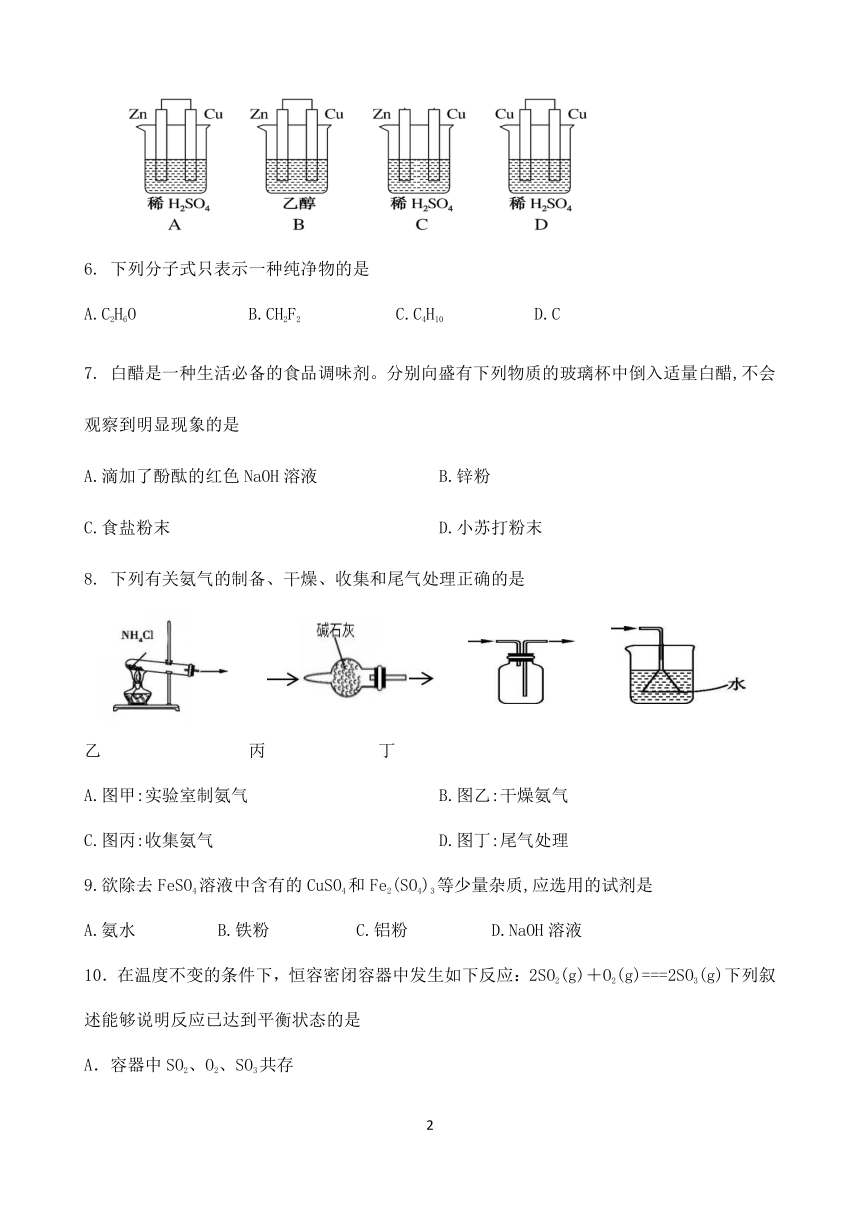
5.下列装置属于原电池装置的是
下列分子式只表示一种纯净物的是
A.C2H6O B.CH2F2 C.C4H10 D.C
7. 白醋是一种生活必备的食品调味剂。分别向盛有下列物质的玻璃杯中倒入适量白醋,不会观察到明显现象的是
A.滴加了酚酞的红色NaOH溶液 B.锌粉
C.食盐粉末 D.小苏打粉末
8. 下列有关氨气的制备、干燥、收集和尾气处理正确的是
1336675889001238252286040576501733552959100268605
甲 乙 丙 丁
A.图甲:实验室制氨气 B.图乙:干燥氨气
C.图丙:收集氨气 D.图丁:尾气处理
9.欲除去FeSO4溶液中含有的CuSO4和Fe2(SO4)3等少量杂质,应选用的试剂是
A.氨水 B.铁粉 C.铝粉 D.NaOH溶液
10.在温度不变的条件下,恒容密闭容器中发生如下反应:2SO2(g)+O2(g)===2SO3(g)下列叙述能够说明反应已达到平衡状态的是
A.容器中SO2、O2、SO3共存
B.单位时间内生成2 mol SO2的同时消耗2 mol SO3
C.容器中SO2、O2、SO3的物质的量之比为2︰1︰2
D.反应容器中压强不随时间变化
447675085979011.最近美国宇航局马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”——全氟丙烷(C3F8),并提出用其“温室化火星”使火星成为第二个地球的计划。下列有关全氟丙烷的说法正确的是
A.分子中三个碳原子可能处于同一直线上 B.全氟丙烷的电子式为
C.C3F8与C3H8互为同分异构体 D.C3F8与C4H2F8互为同系物
12.由乙烯推测丙烯(CH2CH—CH3)的结构或性质正确的是
A.不能使酸性高锰酸钾溶液褪色 B.不能在空气中燃烧
C.能使溴水褪色 D.与HCl在一定条件下加成只得到一种产物
331787537909513.图为某同学用镁带、铜丝和苹果设计的水果电池的装置图,下列有关该装置的说法正确的是
A.镁带为正极
B.铜丝发生氧化反应
C.电子由镁带经导线流向铜丝
D.该装置可将电能转化为化学能
14. 室温下,某兴趣小组在通风橱中进行如下实验:
实验
现象
试管Ⅰ中开始无明显现象,逐渐有微小气泡生成,反应越来越剧
烈,液面上方出现浅红棕色气体,溶液呈蓝色
试管Ⅱ中剧烈反应,迅速生成大量红棕色气体,溶液呈绿色;之后
向绿色溶液中持续通入N2,溶液变为蓝色
下列说法正确的是
A.试管Ⅰ中浅红棕色气体为 NO2,是硝酸被还原生成的
B.等质量的Cu完全溶解时,试管Ⅰ中消耗的HNO3更多
C.换成Fe之后重复实验,依然是试管Ⅱ中反应更剧烈
D.试管Ⅱ中反应后溶液颜色与试管Ⅰ中的不同, 是由于其溶有NO2
384492543815015. 如图所示的实验,发现烧杯中酸性KMnO4溶液褪色。若将烧杯中的溶液换成含有少量KSCN的FeSO4溶液,溶液呈血红色。判断下列说法中不正确的是
A.该条件下H2燃烧生成的物质既具有氧化性又有还原性
B.该条件下H2燃烧的产物中可能含有一定量的H2O2
C.将烧杯中溶液换成KI淀粉溶液也能验证生成物具有还原性
D.酸性FeSO4溶液中加入双氧水的离子反应为2Fe2++H2O2+2H+2Fe3++2H2O
16.下列叙述错误的是
A.1 mol CH2=CH2先与HCl发生加成反应,再与Cl2发生取代反应,最多消耗Cl2 2.5 mol
4201160100330B.实验室中可用如图所示方法除去CH3CH3气体中的CH2=CH2气体
C.实验室中可用酸性KMnO4溶液鉴别CH3CH3气体和CH2=CH2气体
D.工业上可利用CH2=CH2与HCl的加成反应制得较纯净的CH3CH2Cl
17.C2H6O分子可能存在CH3CH2OH和CH3OCH3两种结构。能够证明乙醇的结构是CH3CH2OH的最充分的理由是
A.乙醇可以发生氧化反应
B.1 mol乙醇充分燃烧生成2 mol CO2和3 mol H2O,消耗3 mol O2
C.乙醇的沸点高于乙烷
D.23 g乙醇与足量的金属钠反应,可以放出0.25 mol氢气
18.巴豆酸的结构简式为CH3—CHCH—COOH。现有①氯气、②溴水、③纯碱溶液、④酸化的KMnO4溶液、⑤乙醇。在一定条件下,上述物质能与巴豆酸反应的组合是( )。
A.②③④⑤ B.①②③④⑤ C.①②③ D.①③④
第Ⅱ卷
二、非选择题(共6小题56分)
19.(12分)某化学兴趣小组开展模拟工业合成氨的制备实验,在2 L密闭容器内,T ℃时发生反应:N2(g)+3H2(g)===2NH3(g),在体系中,n(N2)随时间的变化如下表:
时间(min)
0
1
2
3
4
5
N2的物质的量(mol)
0.20
0.10
0.08
0.06
0.06
0.06
(1)上述反应在第5 min时,N2的转化率(已反应的浓度与起始浓度的比例,用百分数表示)为 %;
(2)用H2表示从0~2 min内该反应的平均速率v(H2)=___________________________;
(3)T ℃时,在4个均为2 L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为________________(用字母填空,下同);
a.v(NH3)=0.05 mol ·L-1·min-1 b.v(H2)=0.005 mol·L-1·s-1
c.v(N2)=0.02 mol·L-1·min-1 d.v(H2)=0.01 mol·L-1·min-1
(4)下列表述能作为上述实验中可逆反应达到化学平衡状态的标志是_________________;
a.反应速率v(N2)︰v(H2)︰v(NH3)=1︰3︰2 b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变 d.混合气体的密度不变
e.单位时间内生成n mol N2的同时,生成3n mol H2 f.v(N2)消耗=2 v(NH3)消耗
g.单位时间内3 mol H—H键断裂的同时2 mol N—H键也断裂
(5)下列措施不能使上述化学反应速率加快的是________________。
a.及时分离出NH3气体 b.适当升高温度
c.增大N2的浓度 d.选择高效催化剂
(6)写出实验室用固固加热法制备氨气的化学方程式:
355917546736020.(4分)运动会中的火炬一般采用丙烷(C3H8)为燃料。丙烷热值较高,污染较小,是一种优良的燃料。试回答下列问题:
(1)如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“-”。
(2)写出表示丙烷标准燃烧热的热化学方程式:
_______________________________________________。
21.(10分)实验室制取的乙烯中常混有少量的SO2,有人设计如图所示实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
13049252540
(1)图中a、b、c、d装置盛放的试剂依次是 (填字母,可重复使用)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明SO2存在的实验现象是 。?
(3)使用装置b的目的是? 。?
(4)使用装置c的目的是 。?
(5)能证明混合气体中含有乙烯的现象是? 。?
22.(10分)已知下列转化关系:
(1)写出A的结构简式: 。?
(2)含A的体积分数为75%的水溶液可以用作 。?
(3)写出①②③反应的化学方程式:
① 。?
② 。?
③ 。?
(4)反应③说明A具有 性。?
23.(8分)苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等功效。苹果酸是这种饮品的主要酸性物质。苹果酸是一种常见的有机酸,其结构简式为。
(1)苹果酸中含有的官能团的名称是 、 。?
(2)苹果酸的分子式为 。?
(3)1 mol苹果酸与足量金属钠反应,能生成标准状况下的氢气 L。?
(4)苹果酸可能发生的反应是 。?
A.与酚酞溶液作用显红色 B.与NaOH溶液反应
C.与乙酸在一定条件下酯化 D.与H2在一定条件下加成
24.(12分)(1)A是一种酯,分子式为C2H4O2,A可以由醇B与酸C发生酯化反应得到,B氧化可得C。则:
(1)①写出下列化合物的结构简式:
B________________,C________________。
②写出A在碱性条件下水解的化学方程式:____________________。
③A中混有少量的B和C,除去C选用的试剂是________,分离方法是________。
④B和C的酯化反应和A的水解反应中都用到硫酸,其作用分别是________(填字母)。
a.催化剂、脱水剂;催化剂 b.催化剂、吸水剂;催化剂
c.都作催化剂 d.吸水剂;催化剂
(2)在酸性条件下,CH3CO18OC2H5的水解产物是______ __。
(3)劣质植物油中的亚油酸[CH3(CH2)4—CH===CH—CH2—CH===CH—(CH2)7COOH]含量很低。下列关于亚油酸的说法不正确的是________(填字母)。
a.一定条件下能与甘油发生酯化反应
b.能与NaOH溶液反应
c.能使酸性KMnO4溶液褪色
d.1 mol亚油酸最多能与4 mol Br2发生加成反应
2020-2021学年高一下学期期中阶段考试
参考答案
单选题
1-5DABCA 6-10BCCBD 11-15DCCDC 16-18ADB
非选择题
(12分)
(1)70 (2)0.09molL-1min-1 (3)b>a>c>d
(4)bc (5)a (6)略
(4分)
(1)- (2)略
(10分)
(1)ABAD (2)a中品红溶液褪色 (3)除去SO2
(4)检验SO2是否除尽 (5)c中品红溶液不褪色,d中高锰酸钾溶液褪色
22.(10分)
(1)略 (2)消毒剂 (3)略 (4)还原性
23.(8分)
(1)羟基 羧基 (2)C4H6O5 (3)33.6 (4)BC
24.(12分)
(1)①略②略③饱和碳酸钠溶液 分液④b
(2)CH3COOH、C2H518OH
(3)d
化学试卷
考试时间:90分钟 满分:100
可能用到的相对原子质量:H 1 C 12 O 16
第Ⅰ卷
一、单选题(1-10每小题2分,11-18每小题3分,共44分)
1.被称为人体冷冻学之父的罗伯特·埃廷格在1962年写出《不朽的前景》一书。他在书中列举了大量事实,证明了冷冻复活的可能。比如,许多昆虫和低等生物冬天都冻僵起来,春天又自动复活。下列结论中与上述信息相关的是
A.化学反应前后质量守恒 B.低温下分子无法运动
C.温度降低,化学反应停止 D.温度越低,化学反应越慢
2.球形尖晶石(LiMn2O4)属于等轴晶系,可作耐火材料,常用低温电解法制备,制备过程中的能量转化形式是
A.电能转化为化学能 B.化学能转化为电能
C.机械能转化为化学能 D.化学能转化为机械能
3. 纪录片《舌尖上的中国》展示了中华饮食文化的博大精深。下列烹饪用品的调味成分属于酯类的是
A.食盐 B.大豆油 C.陈醋 D.蔗糖
4.下列化合物中,不能由单质直接化合而得到的是
A. Fe3O4 B. Na2O2 C. FeCl2 D. CuCl2
5.下列装置属于原电池装置的是
下列分子式只表示一种纯净物的是
A.C2H6O B.CH2F2 C.C4H10 D.C
7. 白醋是一种生活必备的食品调味剂。分别向盛有下列物质的玻璃杯中倒入适量白醋,不会观察到明显现象的是
A.滴加了酚酞的红色NaOH溶液 B.锌粉
C.食盐粉末 D.小苏打粉末
8. 下列有关氨气的制备、干燥、收集和尾气处理正确的是
1336675889001238252286040576501733552959100268605
甲 乙 丙 丁
A.图甲:实验室制氨气 B.图乙:干燥氨气
C.图丙:收集氨气 D.图丁:尾气处理
9.欲除去FeSO4溶液中含有的CuSO4和Fe2(SO4)3等少量杂质,应选用的试剂是
A.氨水 B.铁粉 C.铝粉 D.NaOH溶液
10.在温度不变的条件下,恒容密闭容器中发生如下反应:2SO2(g)+O2(g)===2SO3(g)下列叙述能够说明反应已达到平衡状态的是
A.容器中SO2、O2、SO3共存
B.单位时间内生成2 mol SO2的同时消耗2 mol SO3
C.容器中SO2、O2、SO3的物质的量之比为2︰1︰2
D.反应容器中压强不随时间变化
447675085979011.最近美国宇航局马里诺娃博士找到了一种比二氧化碳有效104倍的“超级温室气体”——全氟丙烷(C3F8),并提出用其“温室化火星”使火星成为第二个地球的计划。下列有关全氟丙烷的说法正确的是
A.分子中三个碳原子可能处于同一直线上 B.全氟丙烷的电子式为
C.C3F8与C3H8互为同分异构体 D.C3F8与C4H2F8互为同系物
12.由乙烯推测丙烯(CH2CH—CH3)的结构或性质正确的是
A.不能使酸性高锰酸钾溶液褪色 B.不能在空气中燃烧
C.能使溴水褪色 D.与HCl在一定条件下加成只得到一种产物
331787537909513.图为某同学用镁带、铜丝和苹果设计的水果电池的装置图,下列有关该装置的说法正确的是
A.镁带为正极
B.铜丝发生氧化反应
C.电子由镁带经导线流向铜丝
D.该装置可将电能转化为化学能
14. 室温下,某兴趣小组在通风橱中进行如下实验:
实验
现象
试管Ⅰ中开始无明显现象,逐渐有微小气泡生成,反应越来越剧
烈,液面上方出现浅红棕色气体,溶液呈蓝色
试管Ⅱ中剧烈反应,迅速生成大量红棕色气体,溶液呈绿色;之后
向绿色溶液中持续通入N2,溶液变为蓝色
下列说法正确的是
A.试管Ⅰ中浅红棕色气体为 NO2,是硝酸被还原生成的
B.等质量的Cu完全溶解时,试管Ⅰ中消耗的HNO3更多
C.换成Fe之后重复实验,依然是试管Ⅱ中反应更剧烈
D.试管Ⅱ中反应后溶液颜色与试管Ⅰ中的不同, 是由于其溶有NO2
384492543815015. 如图所示的实验,发现烧杯中酸性KMnO4溶液褪色。若将烧杯中的溶液换成含有少量KSCN的FeSO4溶液,溶液呈血红色。判断下列说法中不正确的是
A.该条件下H2燃烧生成的物质既具有氧化性又有还原性
B.该条件下H2燃烧的产物中可能含有一定量的H2O2
C.将烧杯中溶液换成KI淀粉溶液也能验证生成物具有还原性
D.酸性FeSO4溶液中加入双氧水的离子反应为2Fe2++H2O2+2H+2Fe3++2H2O
16.下列叙述错误的是
A.1 mol CH2=CH2先与HCl发生加成反应,再与Cl2发生取代反应,最多消耗Cl2 2.5 mol
4201160100330B.实验室中可用如图所示方法除去CH3CH3气体中的CH2=CH2气体
C.实验室中可用酸性KMnO4溶液鉴别CH3CH3气体和CH2=CH2气体
D.工业上可利用CH2=CH2与HCl的加成反应制得较纯净的CH3CH2Cl
17.C2H6O分子可能存在CH3CH2OH和CH3OCH3两种结构。能够证明乙醇的结构是CH3CH2OH的最充分的理由是
A.乙醇可以发生氧化反应
B.1 mol乙醇充分燃烧生成2 mol CO2和3 mol H2O,消耗3 mol O2
C.乙醇的沸点高于乙烷
D.23 g乙醇与足量的金属钠反应,可以放出0.25 mol氢气
18.巴豆酸的结构简式为CH3—CHCH—COOH。现有①氯气、②溴水、③纯碱溶液、④酸化的KMnO4溶液、⑤乙醇。在一定条件下,上述物质能与巴豆酸反应的组合是( )。
A.②③④⑤ B.①②③④⑤ C.①②③ D.①③④
第Ⅱ卷
二、非选择题(共6小题56分)
19.(12分)某化学兴趣小组开展模拟工业合成氨的制备实验,在2 L密闭容器内,T ℃时发生反应:N2(g)+3H2(g)===2NH3(g),在体系中,n(N2)随时间的变化如下表:
时间(min)
0
1
2
3
4
5
N2的物质的量(mol)
0.20
0.10
0.08
0.06
0.06
0.06
(1)上述反应在第5 min时,N2的转化率(已反应的浓度与起始浓度的比例,用百分数表示)为 %;
(2)用H2表示从0~2 min内该反应的平均速率v(H2)=___________________________;
(3)T ℃时,在4个均为2 L密闭容器中不同投料下进行合成氨反应。根据在相同时间内测定的结果,判断该反应进行快慢的顺序为________________(用字母填空,下同);
a.v(NH3)=0.05 mol ·L-1·min-1 b.v(H2)=0.005 mol·L-1·s-1
c.v(N2)=0.02 mol·L-1·min-1 d.v(H2)=0.01 mol·L-1·min-1
(4)下列表述能作为上述实验中可逆反应达到化学平衡状态的标志是_________________;
a.反应速率v(N2)︰v(H2)︰v(NH3)=1︰3︰2 b.各组分的物质的量浓度不再改变
c.混合气体的平均相对分子质量不再改变 d.混合气体的密度不变
e.单位时间内生成n mol N2的同时,生成3n mol H2 f.v(N2)消耗=2 v(NH3)消耗
g.单位时间内3 mol H—H键断裂的同时2 mol N—H键也断裂
(5)下列措施不能使上述化学反应速率加快的是________________。
a.及时分离出NH3气体 b.适当升高温度
c.增大N2的浓度 d.选择高效催化剂
(6)写出实验室用固固加热法制备氨气的化学方程式:
355917546736020.(4分)运动会中的火炬一般采用丙烷(C3H8)为燃料。丙烷热值较高,污染较小,是一种优良的燃料。试回答下列问题:
(1)如图是一定量丙烷完全燃烧生成CO2和1 mol H2O(l)过程中的能量变化图,请在图中的括号内填入“+”或“-”。
(2)写出表示丙烷标准燃烧热的热化学方程式:
_______________________________________________。
21.(10分)实验室制取的乙烯中常混有少量的SO2,有人设计如图所示实验装置以证明上述混合气体中含有乙烯和二氧化硫。试回答下列问题:
13049252540
(1)图中a、b、c、d装置盛放的试剂依次是 (填字母,可重复使用)。
A.品红溶液 B.NaOH溶液 C.浓硫酸 D.酸性高锰酸钾溶液
(2)能说明SO2存在的实验现象是 。?
(3)使用装置b的目的是? 。?
(4)使用装置c的目的是 。?
(5)能证明混合气体中含有乙烯的现象是? 。?
22.(10分)已知下列转化关系:
(1)写出A的结构简式: 。?
(2)含A的体积分数为75%的水溶液可以用作 。?
(3)写出①②③反应的化学方程式:
① 。?
② 。?
③ 。?
(4)反应③说明A具有 性。?
23.(8分)苹果醋(ACV)是一种由苹果发酵而成的酸性饮品,具有解毒、降脂等功效。苹果酸是这种饮品的主要酸性物质。苹果酸是一种常见的有机酸,其结构简式为。
(1)苹果酸中含有的官能团的名称是 、 。?
(2)苹果酸的分子式为 。?
(3)1 mol苹果酸与足量金属钠反应,能生成标准状况下的氢气 L。?
(4)苹果酸可能发生的反应是 。?
A.与酚酞溶液作用显红色 B.与NaOH溶液反应
C.与乙酸在一定条件下酯化 D.与H2在一定条件下加成
24.(12分)(1)A是一种酯,分子式为C2H4O2,A可以由醇B与酸C发生酯化反应得到,B氧化可得C。则:
(1)①写出下列化合物的结构简式:
B________________,C________________。
②写出A在碱性条件下水解的化学方程式:____________________。
③A中混有少量的B和C,除去C选用的试剂是________,分离方法是________。
④B和C的酯化反应和A的水解反应中都用到硫酸,其作用分别是________(填字母)。
a.催化剂、脱水剂;催化剂 b.催化剂、吸水剂;催化剂
c.都作催化剂 d.吸水剂;催化剂
(2)在酸性条件下,CH3CO18OC2H5的水解产物是______ __。
(3)劣质植物油中的亚油酸[CH3(CH2)4—CH===CH—CH2—CH===CH—(CH2)7COOH]含量很低。下列关于亚油酸的说法不正确的是________(填字母)。
a.一定条件下能与甘油发生酯化反应
b.能与NaOH溶液反应
c.能使酸性KMnO4溶液褪色
d.1 mol亚油酸最多能与4 mol Br2发生加成反应
2020-2021学年高一下学期期中阶段考试
参考答案
单选题
1-5DABCA 6-10BCCBD 11-15DCCDC 16-18ADB
非选择题
(12分)
(1)70 (2)0.09molL-1min-1 (3)b>a>c>d
(4)bc (5)a (6)略
(4分)
(1)- (2)略
(10分)
(1)ABAD (2)a中品红溶液褪色 (3)除去SO2
(4)检验SO2是否除尽 (5)c中品红溶液不褪色,d中高锰酸钾溶液褪色
22.(10分)
(1)略 (2)消毒剂 (3)略 (4)还原性
23.(8分)
(1)羟基 羧基 (2)C4H6O5 (3)33.6 (4)BC
24.(12分)
(1)①略②略③饱和碳酸钠溶液 分液④b
(2)CH3COOH、C2H518OH
(3)d
同课章节目录
