吉林省长春市第20高中2020-2021学年高一下学期5月第二次质量测试化学试卷 Word版含答案
文档属性
| 名称 | 吉林省长春市第20高中2020-2021学年高一下学期5月第二次质量测试化学试卷 Word版含答案 |  | |
| 格式 | doc | ||
| 文件大小 | 621.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-05-25 20:14:37 | ||
图片预览



文档简介
长春市第20高中2020-2021学年高一下学期5月第二次质量测
化学试题
一、选择题(每题2分共60分)
1.下列物质能在空气中燃烧的是( )
A.N2 B.CH4 C.H2O D.CO2
2.下列官能团名称与对应的结构简式书写错误的是( )
A.羟基: B.羧基: C.醛基: D.碳碳三键:
3.可以用来衡量一个国家石油化工水平的标志是( )
A.乙烯的产量 B.石油的产量
C.乙醇的消费量 D.苯的使用量
4.下列物质对应名称不正确的是( )
A.NaOH:烧碱 B.CuSO4:胆矾 C.:纯碱 D.:乙烷
5.下列化合物中,在常温常压下为液态的是( )
A.甲烷 B.丙烯 C.丁烷 D.CCl4
6.浓硫酸与下列物质作用时,表现脱水性的是( )
A.红热的木炭 B.胆矾晶体 C.氧化亚铁 D.使蔗糖变黑
7.下列说法不正确的是( )
A.1H2和2H2互为同位素 B.白磷和红磷互为同素异形体
C.CH4和C3H8互为同系物 D.CH3CH2CH2CH3和CH3CH(CH3)CH3互为同分异构体
8.下列关于甲烷的说法正确的是( )
A.甲烷分子中,四个氢原子的空间位置等效
B.甲烷分子的二氯代物有两种
C.甲烷与氯气在光照条件下发生取代反应后,产物最多的是CCl4
D.甲烷分子中,氢元素的质量分数在所有烷烃中最低
9.下列有关化学用语表示正确的是( )
A.NH3 的电子式: B.F-的结构示意图:
C.甲烷的比例模型为: D.次氯酸的结构式:H-Cl-O
10.可以用来鉴别甲烷和乙烯的试剂是( )
A.水 B.溴水 C.紫色石蕊溶液 D.NaOH溶液
11.下列气体呈红棕色的是 ( )
A.Н2 B.C12 C.NO D.NO2
12.下列关于乙烯和乙烷的说法不正确的是( )
A.乙烯是不饱和烃,乙烷是饱和烃
B.乙烯比乙烷化学性质更稳定
C.乙烯能使酸性KMnO4溶液和Br2的CCl4溶液褪色,乙烷则不能
D.乙烯分子为平面结构,乙烷分子为立体结构
13.从2008年6月1日起,我国禁止生产、销售、使用超薄塑料购物袋.下列对聚乙烯塑料叙述不正确的是( )
A.它属于有机高分子,无固定熔沸点 B.它能产生“白色污染”
C.它能使溴水褪色 D.形成它的单体是乙烯
14.下列反应属于取代反应的是( )
A.C2H4+3O22CO2+2H2O B.Zn+CuSO4=ZnSO4+Cu
C.CH2Cl2+Cl2CHCl3+HCl D.CH2=CH2+Br2→
15.下列关于乙烯的描述错误的是( )
A.所有原子都在同一直线上 B.乙烯能使溴水褪色
C.乙烯可作为制备乙醇的原料 D.乙烯属于不饱和烃
16.目前,新型冠状病毒仍在世界各地蔓延,科学防护对预防新型冠状病毒感染非常重要。下列说法错误的是( )
A.含有病毒的飞沫扩散到空气中形成气溶胶,气溶胶分散质粒子直径在1nm~100nm之间
B.医用外科口罩核心功能层熔喷布的主要成分聚丙烯属于有机高分子材料
C.核酸检测是确认病毒类型的有效手段,核酸是一类含磷的生物高分子化合物
D.使用75%的酒精、0.1%的次氯酸钠溶液和0.9%的食盐水均可以快速、高效杀死新型冠状病毒
17.下列有机反应类型正确的是( )
A.加成反应 CH2=CH2+Br2→CH2BrCH2Br
B.取代反应 nCH2=CH2
C.酯化反应CH4+Cl2CH3Cl+HCl
D.氧化反应 CH2=CH2 + H2O CH3CH2OH
18.图为实验室制取少量乙酸乙酯的装置图.下列关于该实验的叙述不正确的是( )
A.加热和浓硫酸均能加快反应速率
B.试管b中盛放的是氢氧化钠溶液,用于除去乙酸乙酯中的杂质
C.试管b中导管下端不能浸入液面以下是为了防止实验过程中发生倒吸
D.制得的乙酸乙酯是一种无色透明、有香味的油状液体,密度比水小
19.手机芯片是一种在半导体材料上集合多种电子元器件的电路模块。下列可用作半导体材料的是( )
A.硅 B.铝 C.铁 D.玻璃
20.下列物质的电子式书写正确的是( )
A. B. C. D.
21.下列有机物和乙醇具有相同官能团的是( )
A.苯乙烯() B.丙三醇()
C.丙酮() D.乙醚(CH3CH2—O—CH2CH3)
22.乙醇分子中不同的化学键如图所示,则乙醇在发生酯化反应时,化学键断裂的位置是( )
A.① B.② C.③ D.④
23.下列物质中能使湿润的红色石蕊试纸变蓝的是( )
A.NH3 B.SO3 C.HCl D.NO2
24.反应为吸热反应,反应速率为v1,反应N2+3H22NH3为放热反应,反应速率为v2.对于上述反应,当温度升高时,v1和v2的变化情况为( )
A.均增大 B.均减小 C.v1增大,v2减小 D.v1减小,v2增大
25.反应3X(g)+Y(g) 2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的速率v为( )
A.v (X)=0.05mol·L-1·min-1 B.v (Z)= 0.10mol·L-1·min-1
C.v (Y)=0.10mol·L-1·min-1 D.v (W)=0.05mol·L-1·min-1
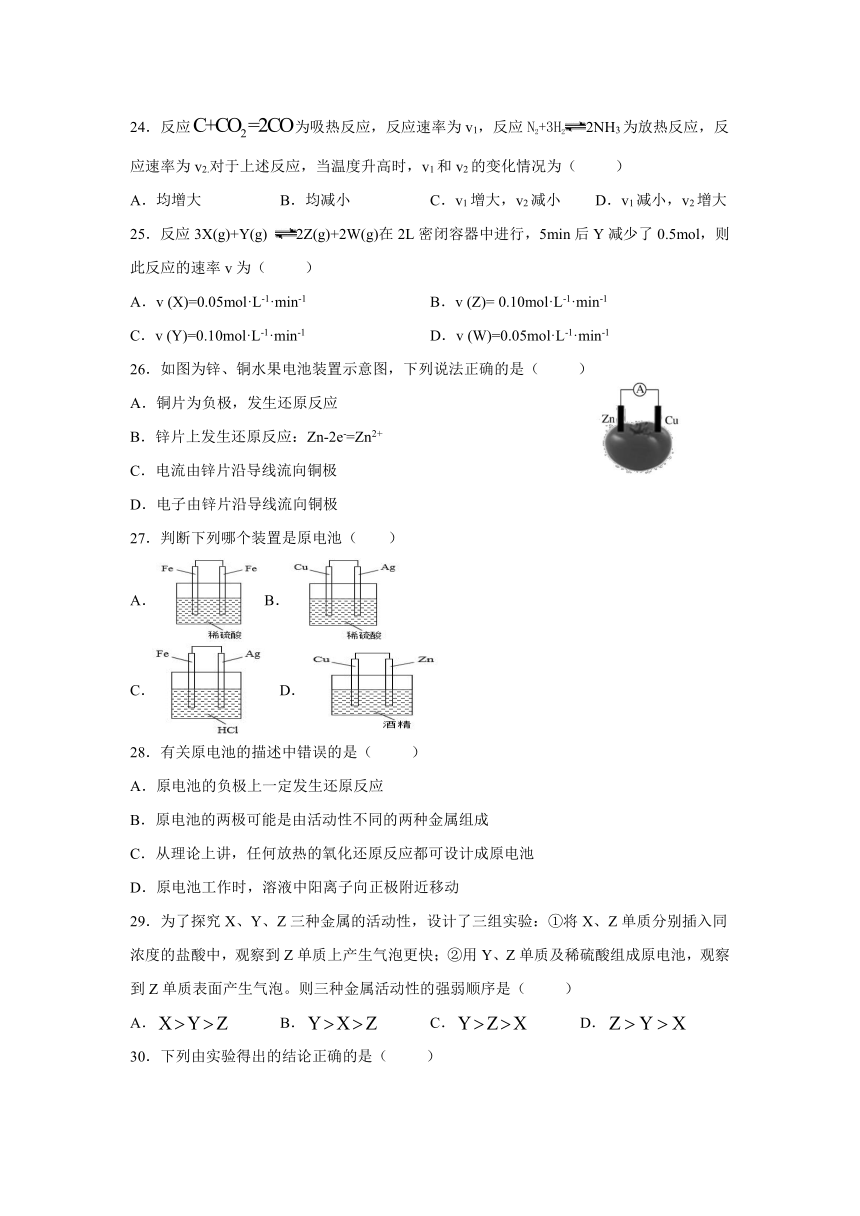
26.如图为锌、铜水果电池装置示意图,下列说法正确的是( )
A.铜片为负极,发生还原反应
B.锌片上发生还原反应:Zn-2e-=Zn2+
C.电流由锌片沿导线流向铜极
D.电子由锌片沿导线流向铜极
27.判断下列哪个装置是原电池( )
A. B.
C. D.
28.有关原电池的描述中错误的是( )
A.原电池的负极上一定发生还原反应
B.原电池的两极可能是由活动性不同的两种金属组成
C.从理论上讲,任何放热的氧化还原反应都可设计成原电池
D.原电池工作时,溶液中阳离子向正极附近移动
29.为了探究X、Y、Z三种金属的活动性,设计了三组实验:①将X、Z单质分别插入同浓度的盐酸中,观察到Z单质上产生气泡更快;②用Y、Z单质及稀硫酸组成原电池,观察到Z单质表面产生气泡。则三种金属活动性的强弱顺序是( )
A. B. C. D.
30.下列由实验得出的结论正确的是( )
实验 结论
A 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色 生成的1,2-二溴乙烷无色
B 乙醇和水都可与金属钠反应产生可燃性气体 乙醇分子中的氢与水分子中的氢具有相同的活泼性
C 乙烯和乙炔都能使溴水褪色 乙烯和乙炔都有碳碳双键
D 甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红 生成的一氯甲烷具有酸性
A.A B.B C.C D.D
二、填空题(每空2分,共30分)
31.原电池是一种将________能转化为_______能的装置。如图所示的原电池装置中,锌片发生_________(填“氧化”或“还原”)反应。铜片上能够观察到
的现象是_______________,该电极反应式是__________________。
32.依据A~E几种烃分子的示意图填空。
B的名称是____________。 (2)D的分子式是________________。
(3)最简单的饱和烃是______(填序号)。 (4)属于同一物质的是_______(填序号)。
(5)上述分子中属于C的同系物的是_____________(填序号)。
33.按要求填空
(1)浓硫酸具有如下的性质:A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑___________ ②碳投入热的浓硫酸中溶解___________
③浓硫酸与氧化铜反应___________ ④浓硫酸干燥氢气___________
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存___________ ②稀硝酸使紫色石蕊溶液变红___________
(3)二氧化硫气体在下列反应中表现的性质填写在横线上。
A.氧化性 B.漂白性 C.还原性 D.酸性氧化物的性质
①使品红溶液褪色___________ ②SO2+2H2S=3S↓+2H2O___________
③SO2+Ca(OH)2=CaSO3↓+H2O___________ ④SO2+Cl2+2H2O=2HCl+H2SO4___________
三、简答题(每题5分,共10分)
34.碳酸钠俗名纯碱或苏打,在外观上与食盐相似,可用于洗涤厨房用具的油污等,请你至少用三种方法区分厨房中的食盐和纯碱。
35.新制氯水滴加到紫色石蕊溶液中,为什么溶液颜色先变红后褪色?请用必要的文字叙述和化学方程式加以说明。
化学试题
一、选择题(每题2分共60分)
1.下列物质能在空气中燃烧的是( )
A.N2 B.CH4 C.H2O D.CO2
2.下列官能团名称与对应的结构简式书写错误的是( )
A.羟基: B.羧基: C.醛基: D.碳碳三键:
3.可以用来衡量一个国家石油化工水平的标志是( )
A.乙烯的产量 B.石油的产量
C.乙醇的消费量 D.苯的使用量
4.下列物质对应名称不正确的是( )
A.NaOH:烧碱 B.CuSO4:胆矾 C.:纯碱 D.:乙烷
5.下列化合物中,在常温常压下为液态的是( )
A.甲烷 B.丙烯 C.丁烷 D.CCl4
6.浓硫酸与下列物质作用时,表现脱水性的是( )
A.红热的木炭 B.胆矾晶体 C.氧化亚铁 D.使蔗糖变黑
7.下列说法不正确的是( )
A.1H2和2H2互为同位素 B.白磷和红磷互为同素异形体
C.CH4和C3H8互为同系物 D.CH3CH2CH2CH3和CH3CH(CH3)CH3互为同分异构体
8.下列关于甲烷的说法正确的是( )
A.甲烷分子中,四个氢原子的空间位置等效
B.甲烷分子的二氯代物有两种
C.甲烷与氯气在光照条件下发生取代反应后,产物最多的是CCl4
D.甲烷分子中,氢元素的质量分数在所有烷烃中最低
9.下列有关化学用语表示正确的是( )
A.NH3 的电子式: B.F-的结构示意图:
C.甲烷的比例模型为: D.次氯酸的结构式:H-Cl-O
10.可以用来鉴别甲烷和乙烯的试剂是( )
A.水 B.溴水 C.紫色石蕊溶液 D.NaOH溶液
11.下列气体呈红棕色的是 ( )
A.Н2 B.C12 C.NO D.NO2
12.下列关于乙烯和乙烷的说法不正确的是( )
A.乙烯是不饱和烃,乙烷是饱和烃
B.乙烯比乙烷化学性质更稳定
C.乙烯能使酸性KMnO4溶液和Br2的CCl4溶液褪色,乙烷则不能
D.乙烯分子为平面结构,乙烷分子为立体结构
13.从2008年6月1日起,我国禁止生产、销售、使用超薄塑料购物袋.下列对聚乙烯塑料叙述不正确的是( )
A.它属于有机高分子,无固定熔沸点 B.它能产生“白色污染”
C.它能使溴水褪色 D.形成它的单体是乙烯
14.下列反应属于取代反应的是( )
A.C2H4+3O22CO2+2H2O B.Zn+CuSO4=ZnSO4+Cu
C.CH2Cl2+Cl2CHCl3+HCl D.CH2=CH2+Br2→
15.下列关于乙烯的描述错误的是( )
A.所有原子都在同一直线上 B.乙烯能使溴水褪色
C.乙烯可作为制备乙醇的原料 D.乙烯属于不饱和烃
16.目前,新型冠状病毒仍在世界各地蔓延,科学防护对预防新型冠状病毒感染非常重要。下列说法错误的是( )
A.含有病毒的飞沫扩散到空气中形成气溶胶,气溶胶分散质粒子直径在1nm~100nm之间
B.医用外科口罩核心功能层熔喷布的主要成分聚丙烯属于有机高分子材料
C.核酸检测是确认病毒类型的有效手段,核酸是一类含磷的生物高分子化合物
D.使用75%的酒精、0.1%的次氯酸钠溶液和0.9%的食盐水均可以快速、高效杀死新型冠状病毒
17.下列有机反应类型正确的是( )
A.加成反应 CH2=CH2+Br2→CH2BrCH2Br
B.取代反应 nCH2=CH2
C.酯化反应CH4+Cl2CH3Cl+HCl
D.氧化反应 CH2=CH2 + H2O CH3CH2OH
18.图为实验室制取少量乙酸乙酯的装置图.下列关于该实验的叙述不正确的是( )
A.加热和浓硫酸均能加快反应速率
B.试管b中盛放的是氢氧化钠溶液,用于除去乙酸乙酯中的杂质
C.试管b中导管下端不能浸入液面以下是为了防止实验过程中发生倒吸
D.制得的乙酸乙酯是一种无色透明、有香味的油状液体,密度比水小
19.手机芯片是一种在半导体材料上集合多种电子元器件的电路模块。下列可用作半导体材料的是( )
A.硅 B.铝 C.铁 D.玻璃
20.下列物质的电子式书写正确的是( )
A. B. C. D.
21.下列有机物和乙醇具有相同官能团的是( )
A.苯乙烯() B.丙三醇()
C.丙酮() D.乙醚(CH3CH2—O—CH2CH3)
22.乙醇分子中不同的化学键如图所示,则乙醇在发生酯化反应时,化学键断裂的位置是( )
A.① B.② C.③ D.④
23.下列物质中能使湿润的红色石蕊试纸变蓝的是( )
A.NH3 B.SO3 C.HCl D.NO2
24.反应为吸热反应,反应速率为v1,反应N2+3H22NH3为放热反应,反应速率为v2.对于上述反应,当温度升高时,v1和v2的变化情况为( )
A.均增大 B.均减小 C.v1增大,v2减小 D.v1减小,v2增大
25.反应3X(g)+Y(g) 2Z(g)+2W(g)在2L密闭容器中进行,5min后Y减少了0.5mol,则此反应的速率v为( )
A.v (X)=0.05mol·L-1·min-1 B.v (Z)= 0.10mol·L-1·min-1
C.v (Y)=0.10mol·L-1·min-1 D.v (W)=0.05mol·L-1·min-1
26.如图为锌、铜水果电池装置示意图,下列说法正确的是( )
A.铜片为负极,发生还原反应
B.锌片上发生还原反应:Zn-2e-=Zn2+
C.电流由锌片沿导线流向铜极
D.电子由锌片沿导线流向铜极
27.判断下列哪个装置是原电池( )
A. B.
C. D.
28.有关原电池的描述中错误的是( )
A.原电池的负极上一定发生还原反应
B.原电池的两极可能是由活动性不同的两种金属组成
C.从理论上讲,任何放热的氧化还原反应都可设计成原电池
D.原电池工作时,溶液中阳离子向正极附近移动
29.为了探究X、Y、Z三种金属的活动性,设计了三组实验:①将X、Z单质分别插入同浓度的盐酸中,观察到Z单质上产生气泡更快;②用Y、Z单质及稀硫酸组成原电池,观察到Z单质表面产生气泡。则三种金属活动性的强弱顺序是( )
A. B. C. D.
30.下列由实验得出的结论正确的是( )
实验 结论
A 将乙烯通入溴的四氯化碳溶液,溶液最终变为无色 生成的1,2-二溴乙烷无色
B 乙醇和水都可与金属钠反应产生可燃性气体 乙醇分子中的氢与水分子中的氢具有相同的活泼性
C 乙烯和乙炔都能使溴水褪色 乙烯和乙炔都有碳碳双键
D 甲烷与氯气在光照下反应后的混合气体能使湿润的石蕊试纸变红 生成的一氯甲烷具有酸性
A.A B.B C.C D.D
二、填空题(每空2分,共30分)
31.原电池是一种将________能转化为_______能的装置。如图所示的原电池装置中,锌片发生_________(填“氧化”或“还原”)反应。铜片上能够观察到
的现象是_______________,该电极反应式是__________________。
32.依据A~E几种烃分子的示意图填空。
B的名称是____________。 (2)D的分子式是________________。
(3)最简单的饱和烃是______(填序号)。 (4)属于同一物质的是_______(填序号)。
(5)上述分子中属于C的同系物的是_____________(填序号)。
33.按要求填空
(1)浓硫酸具有如下的性质:A.酸性B.强氧化性C.吸水性D.脱水性,E难挥发性。下列事实主要表现浓硫酸的什么性质(填字母序号)。
①浓硫酸使蔗糖变黑___________ ②碳投入热的浓硫酸中溶解___________
③浓硫酸与氧化铜反应___________ ④浓硫酸干燥氢气___________
(2)浓硝酸具有如下的性质:A.酸性B.强氧化性C.不稳定性,下列事实主要表现浓硝酸的什么性质(填字母序号)。
①浓硝酸需避光保存___________ ②稀硝酸使紫色石蕊溶液变红___________
(3)二氧化硫气体在下列反应中表现的性质填写在横线上。
A.氧化性 B.漂白性 C.还原性 D.酸性氧化物的性质
①使品红溶液褪色___________ ②SO2+2H2S=3S↓+2H2O___________
③SO2+Ca(OH)2=CaSO3↓+H2O___________ ④SO2+Cl2+2H2O=2HCl+H2SO4___________
三、简答题(每题5分,共10分)
34.碳酸钠俗名纯碱或苏打,在外观上与食盐相似,可用于洗涤厨房用具的油污等,请你至少用三种方法区分厨房中的食盐和纯碱。
35.新制氯水滴加到紫色石蕊溶液中,为什么溶液颜色先变红后褪色?请用必要的文字叙述和化学方程式加以说明。
同课章节目录
