初三化学专题复习:物质的除杂
图片预览


文档简介
(共10张PPT)
《物质的除杂》
初三化学专题复习
我们的生活中无处不存在着物质的净化、分离、提纯等事实,如生活用水的净化、废水的处理、硬水的软化、色素的吸附、房间的除臭等等。
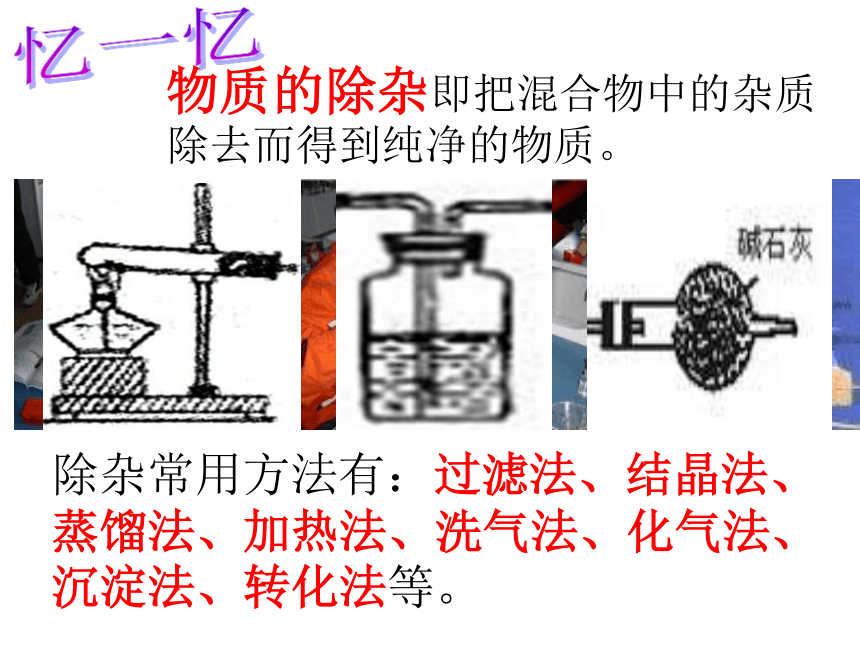
物质的除杂即把混合物中的杂质除去而得到纯净的物质。
除杂常用方法有:过滤法、结晶法、蒸馏法、加热法、洗气法、化气法、沉淀法、转化法等。
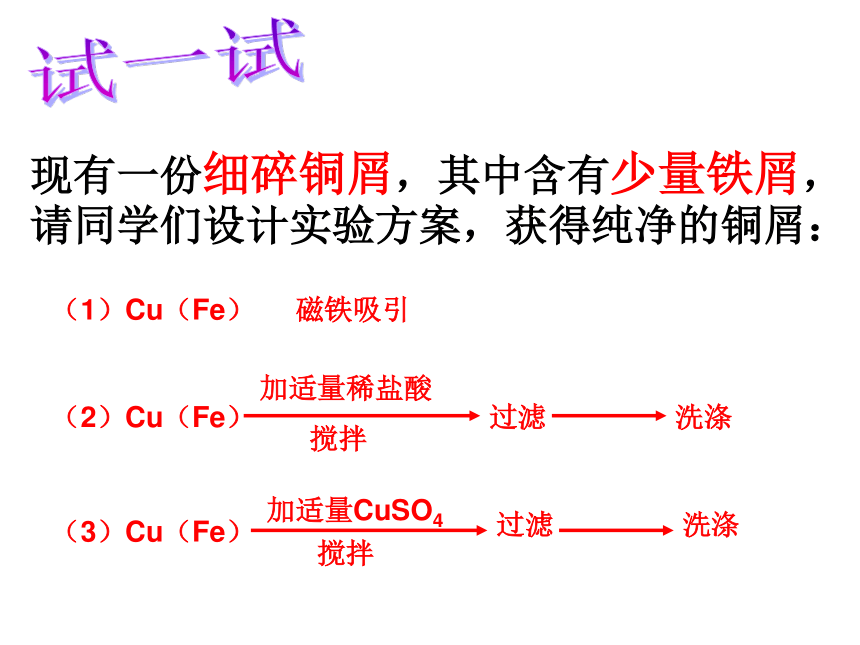
现有一份细碎铜屑,其中含有少量铁屑,请同学们设计实验方案,获得纯净的铜屑:
(2)Cu(Fe)
加适量稀盐酸
搅拌
过滤
洗涤
(3)Cu(Fe)
加适量CuSO4
搅拌
过滤
洗涤
(1)Cu(Fe)
磁铁吸引
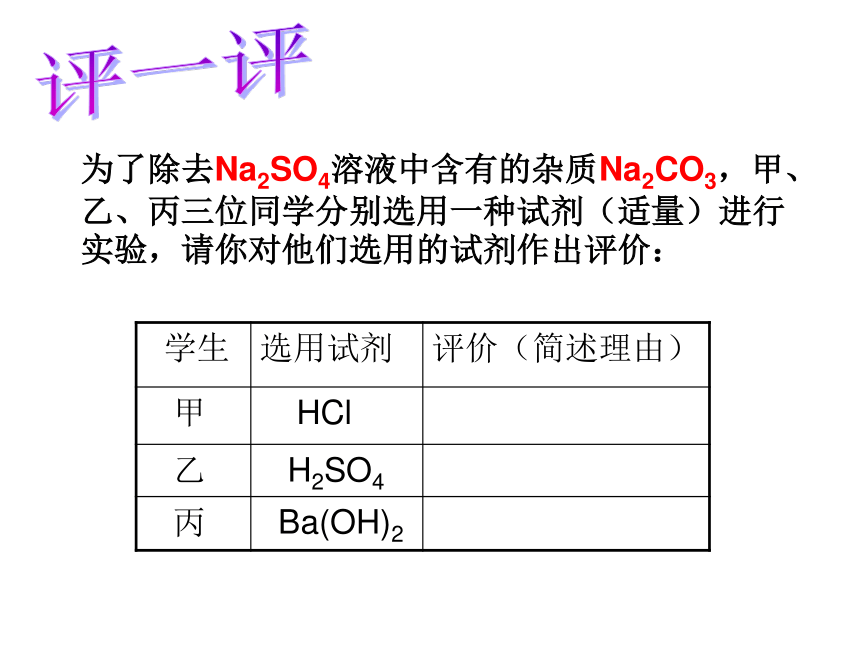
为了除去Na2SO4溶液中含有的杂质Na2CO3,甲、乙、丙三位同学分别选用一种试剂(适量)进行实验,请你对他们选用的试剂作出评价:
学生 选用试剂 评价(简述理由)
甲 HCl
乙 H2SO4
丙 Ba(OH)2
以无招胜有招
以无剑胜有剑
以无形胜有形
乃武学的最高境界
学习的最高境界呢?
物质的除杂 “心法口诀”:
不增(不引入新杂质)
不减(不与原物质反应)
易分(生成不同状态的物质,如沉淀、气体、水)
揪其根本(可从离子、原子角度去判断杂质)
沾亲带故(试剂中部分离子与原物质相同)
NH3(H2O)
NaCl(CaCl2)
HCl(H2SO4)
KCl(K2CO3)
NaCl(NH4Cl)
NaOH(Na2CO3)
Cu(CuO)
KCl(CuCl2)
CuO(C)
H2(CO2)
CO2(CO)
KNO3(CuSO4)
1分题
2分题
3分题
4分题
选择合适的试剂除去括号中的杂质
在物质除杂的过程中,若有多种杂质时,需注意除杂的先后顺序。
混合气体
灼热的氧化铜
N2
CO2
H2O
NaOH溶液
N2
H2O
浓硫酸
N2
例2:如何除去N2中混有少量H2、CO、CO2、H2O
例1:如何除去N2中混有少量CO2、H2O
经海水蒸发结晶而来的粗盐主要成分为NaCl,常含有泥沙、MgCl2、CaCl2等杂质,如何提纯粗盐?
请设计除杂的流程并书写相关的化学方程式
→
?
我们的收获
我学到了……
《物质的除杂》
初三化学专题复习
我们的生活中无处不存在着物质的净化、分离、提纯等事实,如生活用水的净化、废水的处理、硬水的软化、色素的吸附、房间的除臭等等。
物质的除杂即把混合物中的杂质除去而得到纯净的物质。
除杂常用方法有:过滤法、结晶法、蒸馏法、加热法、洗气法、化气法、沉淀法、转化法等。
现有一份细碎铜屑,其中含有少量铁屑,请同学们设计实验方案,获得纯净的铜屑:
(2)Cu(Fe)
加适量稀盐酸
搅拌
过滤
洗涤
(3)Cu(Fe)
加适量CuSO4
搅拌
过滤
洗涤
(1)Cu(Fe)
磁铁吸引
为了除去Na2SO4溶液中含有的杂质Na2CO3,甲、乙、丙三位同学分别选用一种试剂(适量)进行实验,请你对他们选用的试剂作出评价:
学生 选用试剂 评价(简述理由)
甲 HCl
乙 H2SO4
丙 Ba(OH)2
以无招胜有招
以无剑胜有剑
以无形胜有形
乃武学的最高境界
学习的最高境界呢?
物质的除杂 “心法口诀”:
不增(不引入新杂质)
不减(不与原物质反应)
易分(生成不同状态的物质,如沉淀、气体、水)
揪其根本(可从离子、原子角度去判断杂质)
沾亲带故(试剂中部分离子与原物质相同)
NH3(H2O)
NaCl(CaCl2)
HCl(H2SO4)
KCl(K2CO3)
NaCl(NH4Cl)
NaOH(Na2CO3)
Cu(CuO)
KCl(CuCl2)
CuO(C)
H2(CO2)
CO2(CO)
KNO3(CuSO4)
1分题
2分题
3分题
4分题
选择合适的试剂除去括号中的杂质
在物质除杂的过程中,若有多种杂质时,需注意除杂的先后顺序。
混合气体
灼热的氧化铜
N2
CO2
H2O
NaOH溶液
N2
H2O
浓硫酸
N2
例2:如何除去N2中混有少量H2、CO、CO2、H2O
例1:如何除去N2中混有少量CO2、H2O
经海水蒸发结晶而来的粗盐主要成分为NaCl,常含有泥沙、MgCl2、CaCl2等杂质,如何提纯粗盐?
请设计除杂的流程并书写相关的化学方程式
→
?
我们的收获
我学到了……
