卤代烃
图片预览






文档简介
(共24张PPT)
卤代烃
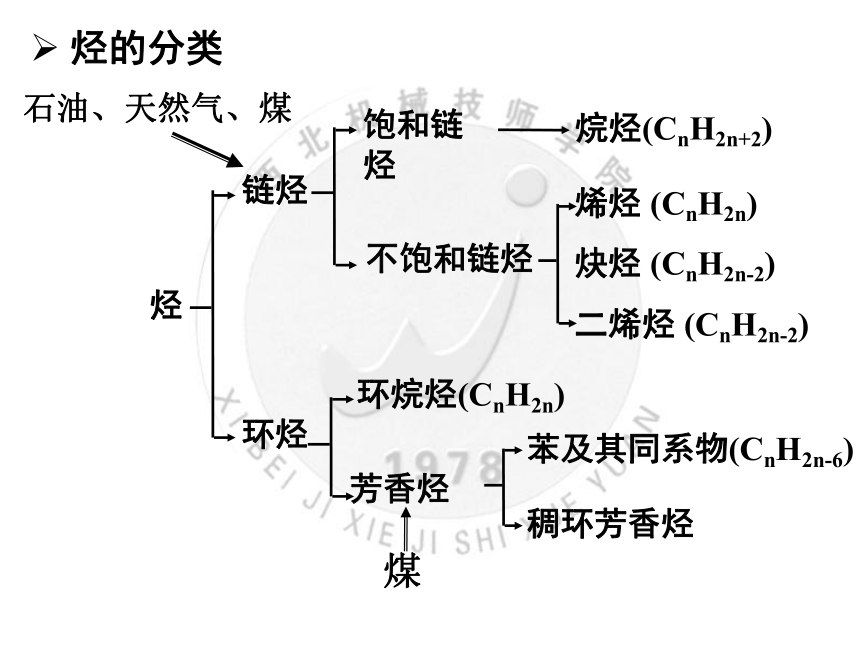
烃的分类
烃
链烃
环烃
石油、天然气、煤
饱和链烃
不饱和链烃
烷烃(CnH2n+2)
烯烃 (CnH2n)
炔烃 (CnH2n-2)
二烯烃 (CnH2n-2)
环烷烃(CnH2n)
芳香烃
苯及其同系物(CnH2n-6)
稠环芳香烃
煤
烃的衍生物
烃分子里的氢原子被其他原子或原子团取代所生成的一系列新的有机化合物
除烃基外
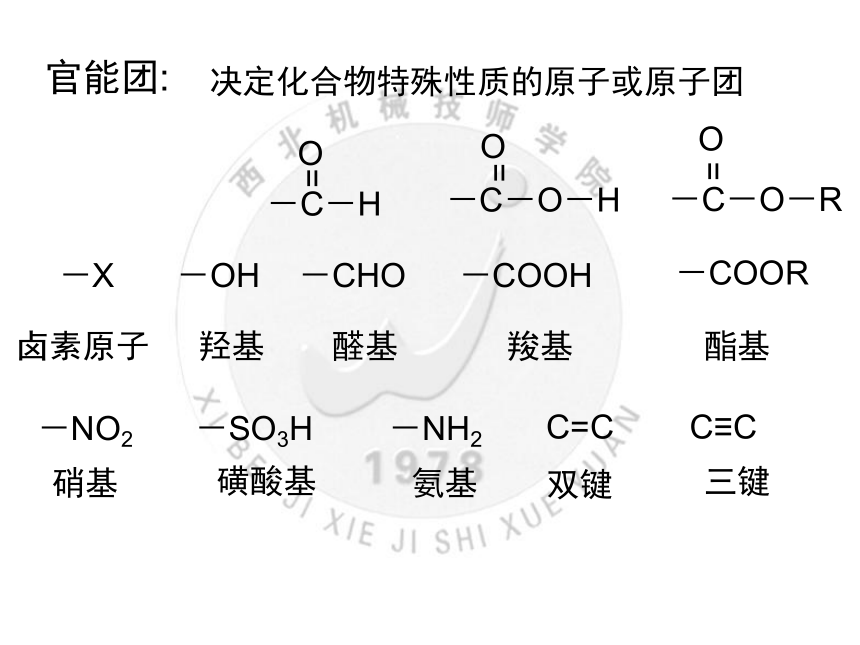
官能团:
-X
-OH
-CHO
-COOH
-COOR
卤素原子
羟基
醛基
羧基
-C-H
=
O
-C-O-H
=
O
-C-O-R
=
O
酯基
-NO2
-SO3H
-NH2
硝基
磺酸基
氨基
C=C
C≡C
决定化合物特殊性质的原子或原子团
双键
三键
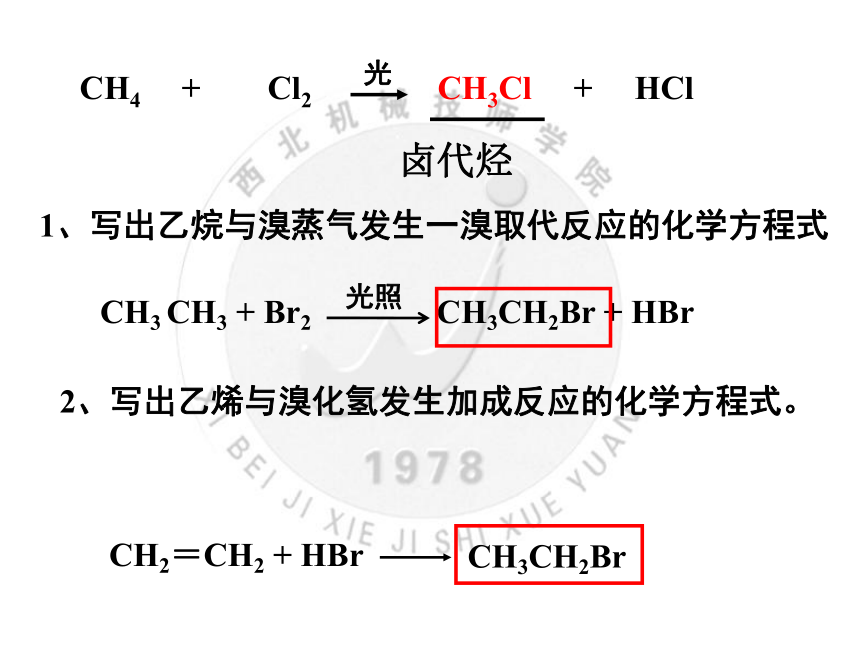
CH4 + Cl2 CH3Cl + HCl
光
CH3 CH3 + Br2 CH3CH2Br + HBr
光照
CH2=CH2 + HBr
CH3CH2Br
1、写出乙烷与溴蒸气发生一溴取代反应的化学方程式
2、写出乙烯与溴化氢发生加成反应的化学方程式。
卤代烃
第五章、卤代烃
一、慨念:
烃分子中的氢原子被卤素原子取代后
生成的化合物。
二、通式:
R—X(R为烃基,X为卤素原子)
饱和一卤代烷的通式:CnH2n+1X
三. 分类:
含X原子数目:一卤代烃、二卤代烃、多卤代烃
CHF2Cl CH3Br CHI3 CCl4 CH2ClCH2Cl
( X=F、Cl、Br、I)
2. 烃基种类
(1)卤代烷 R-X R:1°、2°、3°
CH3CH2CH2CH2I (CH3)3C-Cl
(2) 卤代烯(炔)烃
CH2=CHCl CH2=CHCH2Cl CH3C≡CCl
CH2BrCH=CHCH2Br F2C=CF2
(3) 卤代芳烃
3. 按所含卤原子种类分:氟代烃、氯代烃、溴代烃.
四. 物理通性:
1).常温下,卤代烃中除一氯甲烷、氯乙烷、氯乙烯 等少数为气体外,其余为液体或固体.
(2).卤代烃,如一氯代烷的物理性质变化规律是:随着碳原子数(式量)增加,其熔、沸点和密度也增大.(且沸点和熔点大于相应的烃)
(3).难溶于水,易溶于有机溶剂.除脂肪烃的一氟代物、一氯代物等部分卤代烃外,液态卤代烃的密度一般比水大.密度一般随烃基中碳原子数增加而减小.
CH3CH2Br
分子式
C2H5Br
或 C2H5Br
C C
H
H
Br
H
H
H
H H
H︰C︰C︰Br︰
H H
‥
‥
‥
‥
‥
‥
结构简式
五、溴乙烷
结构式
电子式
1)、物理性质:
无色液体,沸点38.4℃,难溶于水,密度比水大。
2)、化学性质:
C2H5-Br+NaOH C2H5-OH+NaBr
水
△
A、溴乙烷水解反应
——取代反应
反应条件:
水溶液、加热
实验步骤:取一支试管,滴入10滴~15滴溴乙烷,再加入1mL5%的NaOH溶液,充分振荡、
静置,待液体分层后,用滴管小心吸入10滴上层水溶液,移入另一盛有10mL稀硝酸溶液的试管中,然后加入2滴~3滴2%的AgNO3溶液,观察反应现象。
现象:看到反应中有浅黄色沉淀生成
B、溴乙烷与NaOH的醇溶液反应
反应条件:
醇溶液、加热
定义:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HBr等),而形成含不饱和键化合物的反应,叫做消去反应。
消去反应:
——消去反应
2、溴乙烷的消去反应
实验步骤:在试管里加入2mL溴乙烷和5 mL10%NaOH的乙醇溶液。在另一支试管中加入少量酸性高锰酸钾溶液。用水浴加热试管里的混合物(注意不要使水沸腾),持续加热一段时间后,把生成的气体通入酸性高锰酸钾溶液中,观察有什么现象发生。 。
现象:酸性高锰酸钾溶液褪色
+NaOH
—C—C—
H
X
△
醇
C=C
+NaX+H2O
发生消去反应的条件:
1、烃中碳原子数≥2
2、接卤素原子的碳邻近的碳原子上有氢原子
3、反应条件:强碱和醇溶液中加热。
下列卤代烃是否能发生消去反应、若能,请写出有机产物的结构简式:
A、CH3Cl
D 、
知识点训练
E、CH3-CH2-CH-CH3
Br
C、CH3-C-CH2-Cl
CH3
CH3
B、CH3-CH-CH3
Br
CH3
思考与交流:比较溴乙烷的取代反应和消去反应,并完成下表,体会反应条件对化学反应的影响。
取代反应 消去反应
反应物
反应条件
生成物
结论
溴乙烷和NaOH
溴乙烷和NaOH
水 加热
乙醇 加热
乙醇、NaBr
乙烯、 NaBr 、水
溴乙烷和NaOH在不同溶剂中发生不同类型
的反应,生成不同的产物
卤代烃的用途
聚氯乙烯
聚四氟乙烯
氟利昂是freon的音译名,是多种含氟含氯的烷烃生物的总称,简写为CFC。常见的有氟利昂—11(CCl3F,沸点297K),氟利昂—12(CCl2F2,沸点243.2K)等。它们是无色、无臭、无毒、易挥发,化学性质极稳定,被大量用于冷冻剂和烟雾分散剂的许多方面。由于其性质稳定,在被多年使用后,其蒸汽聚积滞留在大气中,估计每年逸散到大气中的CFC达70万,使它在大气中的含量每年递增5%。其主要降解途径是随气流上升,在平流层中受紫外光的作用分解。由CFC生成的氯原子能引起耗臭氧的循环反应,其后果是破坏了平流层中的臭氧层。有关反应是:
O3 O2+O Cl+O3→ClO+O2 ClO+O→Cl+O2
总反应:2O3→3O2
因此CFC才被定为大气污染物。这类污染物的严重性在于它不易被消除,即使立即禁用,已积累在大气中的CFC还要危害多年(甚至上百年),因而这是一很难解决的问题。
光
Cl
思考题:
1,2—二溴乙烷在氢氧化钠溶液中水解后的产物是什么?在氢氧化钠的醇溶液中发生消去反应后的产物是什么?
卤代烃
烃的分类
烃
链烃
环烃
石油、天然气、煤
饱和链烃
不饱和链烃
烷烃(CnH2n+2)
烯烃 (CnH2n)
炔烃 (CnH2n-2)
二烯烃 (CnH2n-2)
环烷烃(CnH2n)
芳香烃
苯及其同系物(CnH2n-6)
稠环芳香烃
煤
烃的衍生物
烃分子里的氢原子被其他原子或原子团取代所生成的一系列新的有机化合物
除烃基外
官能团:
-X
-OH
-CHO
-COOH
-COOR
卤素原子
羟基
醛基
羧基
-C-H
=
O
-C-O-H
=
O
-C-O-R
=
O
酯基
-NO2
-SO3H
-NH2
硝基
磺酸基
氨基
C=C
C≡C
决定化合物特殊性质的原子或原子团
双键
三键
CH4 + Cl2 CH3Cl + HCl
光
CH3 CH3 + Br2 CH3CH2Br + HBr
光照
CH2=CH2 + HBr
CH3CH2Br
1、写出乙烷与溴蒸气发生一溴取代反应的化学方程式
2、写出乙烯与溴化氢发生加成反应的化学方程式。
卤代烃
第五章、卤代烃
一、慨念:
烃分子中的氢原子被卤素原子取代后
生成的化合物。
二、通式:
R—X(R为烃基,X为卤素原子)
饱和一卤代烷的通式:CnH2n+1X
三. 分类:
含X原子数目:一卤代烃、二卤代烃、多卤代烃
CHF2Cl CH3Br CHI3 CCl4 CH2ClCH2Cl
( X=F、Cl、Br、I)
2. 烃基种类
(1)卤代烷 R-X R:1°、2°、3°
CH3CH2CH2CH2I (CH3)3C-Cl
(2) 卤代烯(炔)烃
CH2=CHCl CH2=CHCH2Cl CH3C≡CCl
CH2BrCH=CHCH2Br F2C=CF2
(3) 卤代芳烃
3. 按所含卤原子种类分:氟代烃、氯代烃、溴代烃.
四. 物理通性:
1).常温下,卤代烃中除一氯甲烷、氯乙烷、氯乙烯 等少数为气体外,其余为液体或固体.
(2).卤代烃,如一氯代烷的物理性质变化规律是:随着碳原子数(式量)增加,其熔、沸点和密度也增大.(且沸点和熔点大于相应的烃)
(3).难溶于水,易溶于有机溶剂.除脂肪烃的一氟代物、一氯代物等部分卤代烃外,液态卤代烃的密度一般比水大.密度一般随烃基中碳原子数增加而减小.
CH3CH2Br
分子式
C2H5Br
或 C2H5Br
C C
H
H
Br
H
H
H
H H
H︰C︰C︰Br︰
H H
‥
‥
‥
‥
‥
‥
结构简式
五、溴乙烷
结构式
电子式
1)、物理性质:
无色液体,沸点38.4℃,难溶于水,密度比水大。
2)、化学性质:
C2H5-Br+NaOH C2H5-OH+NaBr
水
△
A、溴乙烷水解反应
——取代反应
反应条件:
水溶液、加热
实验步骤:取一支试管,滴入10滴~15滴溴乙烷,再加入1mL5%的NaOH溶液,充分振荡、
静置,待液体分层后,用滴管小心吸入10滴上层水溶液,移入另一盛有10mL稀硝酸溶液的试管中,然后加入2滴~3滴2%的AgNO3溶液,观察反应现象。
现象:看到反应中有浅黄色沉淀生成
B、溴乙烷与NaOH的醇溶液反应
反应条件:
醇溶液、加热
定义:有机化合物在一定条件下,从一个分子中脱去一个或几个小分子(如H2O、HBr等),而形成含不饱和键化合物的反应,叫做消去反应。
消去反应:
——消去反应
2、溴乙烷的消去反应
实验步骤:在试管里加入2mL溴乙烷和5 mL10%NaOH的乙醇溶液。在另一支试管中加入少量酸性高锰酸钾溶液。用水浴加热试管里的混合物(注意不要使水沸腾),持续加热一段时间后,把生成的气体通入酸性高锰酸钾溶液中,观察有什么现象发生。 。
现象:酸性高锰酸钾溶液褪色
+NaOH
—C—C—
H
X
△
醇
C=C
+NaX+H2O
发生消去反应的条件:
1、烃中碳原子数≥2
2、接卤素原子的碳邻近的碳原子上有氢原子
3、反应条件:强碱和醇溶液中加热。
下列卤代烃是否能发生消去反应、若能,请写出有机产物的结构简式:
A、CH3Cl
D 、
知识点训练
E、CH3-CH2-CH-CH3
Br
C、CH3-C-CH2-Cl
CH3
CH3
B、CH3-CH-CH3
Br
CH3
思考与交流:比较溴乙烷的取代反应和消去反应,并完成下表,体会反应条件对化学反应的影响。
取代反应 消去反应
反应物
反应条件
生成物
结论
溴乙烷和NaOH
溴乙烷和NaOH
水 加热
乙醇 加热
乙醇、NaBr
乙烯、 NaBr 、水
溴乙烷和NaOH在不同溶剂中发生不同类型
的反应,生成不同的产物
卤代烃的用途
聚氯乙烯
聚四氟乙烯
氟利昂是freon的音译名,是多种含氟含氯的烷烃生物的总称,简写为CFC。常见的有氟利昂—11(CCl3F,沸点297K),氟利昂—12(CCl2F2,沸点243.2K)等。它们是无色、无臭、无毒、易挥发,化学性质极稳定,被大量用于冷冻剂和烟雾分散剂的许多方面。由于其性质稳定,在被多年使用后,其蒸汽聚积滞留在大气中,估计每年逸散到大气中的CFC达70万,使它在大气中的含量每年递增5%。其主要降解途径是随气流上升,在平流层中受紫外光的作用分解。由CFC生成的氯原子能引起耗臭氧的循环反应,其后果是破坏了平流层中的臭氧层。有关反应是:
O3 O2+O Cl+O3→ClO+O2 ClO+O→Cl+O2
总反应:2O3→3O2
因此CFC才被定为大气污染物。这类污染物的严重性在于它不易被消除,即使立即禁用,已积累在大气中的CFC还要危害多年(甚至上百年),因而这是一很难解决的问题。
光
Cl
思考题:
1,2—二溴乙烷在氢氧化钠溶液中水解后的产物是什么?在氢氧化钠的醇溶液中发生消去反应后的产物是什么?
