2021年浙江省中考科学复习课件第38讲 金属(课件 36张PPT)
文档属性
| 名称 | 2021年浙江省中考科学复习课件第38讲 金属(课件 36张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 757.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-06-01 00:00:00 | ||
图片预览


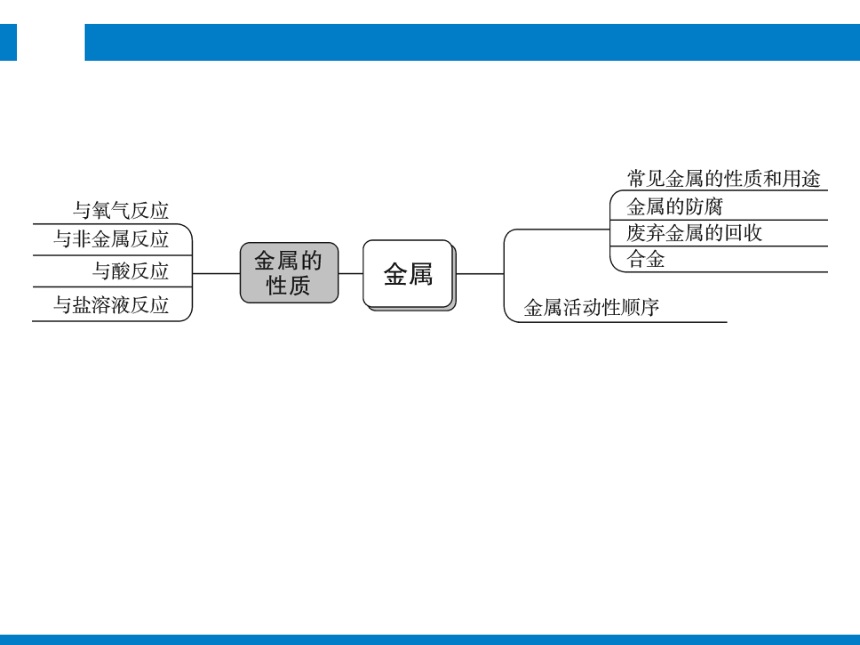









文档简介
第38讲 金属
思维导图
考点扫描
1.金属的普遍特性:固态(除汞外),有 ,是良好的 ,有 性,密度和熔点高。
2.非金属的性质:固、液、气态,有多种颜色,不具备金属特性,性质不一,应用不一。
考点一 金属与非金属(九上教材P36)
金属光泽
导电、导热体
延展
3.常见金属的主要性质和用途
?
主要性质
用途
铁
银白色金属光泽,质软
制各种铁合金,用于机械、建筑、医疗等行业
铜
紫红色金属光泽,纯铜质软、韧性好
制造电线、电缆及导热器具,用于制各种铜合金
铝
银白色金属光泽,密度小,抗腐蚀性强
制造电线、电缆、铝箔包装,用于建筑装饰材料及汽车等的材料
1.(2020,益阳)国产飞机C919机壳采用了先进的铝锂合金材料。下列有关说法错误的是( )
A.铝锂合金密度小
B.铝锂合金的硬度比纯铝大
C.铝锂合金抗腐蚀性强
D.铝锂合金是合成材料
D
1.金属活动性顺序
2.金属活动性的应用
(1)金属的位置越靠前,在水溶液里就越容易 电子,活动性就 。
考点二 金属活动性顺序(九上教材P43)
失去
越强
(2)金属与酸反应时,排在____前面的金属能置换出酸里的____。
(3)金属与盐发生反应时,只有活动性____的金属才能把活动性弱的金属从它的盐溶液中置换出来。K、Ca、Na会与盐溶液中的水反应,生成碱和氢气。
氢
氢
强
2.下列四种金属中,有一种金属的盐溶液与其他三种金属都能发生置换反应,这种金属是( )
A.Ag B.Cu C.Fe D.Mg
A
1.金属腐蚀的条件:(1)外因:水分、氧气等物质的作用;(2)内因:金属的内部结构。
2.防止金属腐蚀的常用方法
(1)改变金属的 ,如在普通钢中加入铬、镍等金属元素制成不锈钢;
(2)表面覆盖 ,如刷漆、涂机油、涂搪瓷、电镀、烤蓝等。
考点三 金属的防腐(九上教材P46)
内部结构
保护膜
3.(2020,雅安)下列措施中,不能防止金属制品锈蚀的是( )
A.在表面刷漆
B.改用不锈钢
C.在表面镀铬
D.用湿布擦拭
D
由于垃圾填埋处理后,金属不会自行分解,并且铅、镉等金属被腐蚀后,会形成溶于水的有毒的金属离子,污染土壤和地下水源。因此废弃金属将对环境造成严重的污染,大部分金属应通过回收使其循环再利用。
考点四 废弃金属对环境的影响(八下教材P189)
1.合金:一种金属跟其他一种或几种金属(或非金属)一起熔合而成的具有金属特征的物质。
2.改善金属材料性能的主要方法是改变金属的内部结构和外部条件。
考点五 金属材料的发展(九上教材P38)
精讲释疑
金属的用途是重要考点,用途是由其性质决定的,因此考查用途时应紧密联系金属的性质。如物理性质:导电性、延展性、导热性等;化学性质:与氧反应、活动性强弱等。
题型一 金属的性质和用途
【例1】 (2019,衡阳)下列有关金属材料的说法中正确的是( )
A.地壳中含量最高的金属元素是铁
B.钢的性能优良,所以钢是纯净的铁
C.多数合金的抗腐蚀性能比组成它们的纯金属更好
D.银的导电性最好,大多数电线都是用银作材料
C
1.(2020,长沙)北斗系统的全面建成彰显了中国航天的力量,在航天科技中会用到大量金属材料。下列有关金属材料的说法正确的是( )
A.合金中一定只含金属元素
B.纯铜比黄铜的硬度更大
C.生锈的钢铁制品没有回收价值
D.钛和钛合金被广泛用于火箭、导弹等
D
熟悉金属活动性顺序,应用金属活动性顺序时需要注意:金属与酸反应时,浓硫酸和硝酸与金属不发生置换反应。特别活泼的金属如钾、钙、钠等与盐溶液反应时,是先和水反应,故不能置换出盐溶液中的金属元素。
题型二 金属活动性顺序
【例2】 某废液中只含有Fe(NO3)2、Cu(NO3)2、Ba(NO3)2三种溶质,为了回收金属、保护环境,小科设计了如图方案(所加试剂均过量),下列判断正确的是( )
A.固体a是铜
B.X一定是Na2SO4
C.溶液B中含有的盐有Ba(NO3)2、NaNO3
D.若回收到6.4 g固体a,则加入的铁屑质量为5.6 g
C
2.(2020,锦州)将一定量的锌粉加入到硝酸镁和硝酸铜的混合液中,充分反应后过滤,得到滤渣和滤液。下列判断正确的是( )
A.若滤液为蓝色,则滤渣中一定有锌、镁、铜
B.若向滤渣中加入稀盐酸有气泡产生,则滤液中一定有硝酸镁、硝酸锌、硝酸铜
D
C.若向滤液中加入氢氧化钠溶液,则一定有氢氧化铜生成
D.滤渣中一定含有铜,滤液中一定含有硝酸镁和硝酸锌
金属锈蚀是与水和空气中的氧气等反应,分析金属生锈的原因要从内因和外因两个方面考虑。针对产生的原因寻找相应的防锈措施。关于金属锈蚀的实验探究设计要注意控制变量。
题型三 金属腐蚀条件的研究
【例3】 某同学根据铜绿的成分Cu2(OH)2CO3作出猜想:金属铜锈蚀的条件除有氧气和水外,还必须有二氧化碳。为证明“必须有二氧化碳”,需要进行如图所示实验中的( )
A.甲和乙
B.甲和丁
C.乙和丁
D.丙和丁
B
3.(2020,日照)如图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法不正确的是( )
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
A
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
诊断自测
1.(2020,湘潭)我国第一艘国产航母“山东舰”在制造的过程中使用了大量的金属材料,下列有关金属材料的说法错误的是( )
A.合金的硬度一般比组成它们的纯金属更高
B.钢铁是使用最多的金属材料
C.金属在常温下都是固体
D.大多数金属为电和热的优良导体
C
2.如图是包含物质a、b、c、d和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生化学反应。单质a不可能是( )
A.Mg B.Fe
C.Ag D.Zn
C
3.(2020,滨州)现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是( )
A.完全反应所需时间:丙>甲>乙
B.生成氢气的质量:甲>乙>丙
C.相对原子质量:乙>丙>甲
D.消耗硫酸的质量:甲>乙>丙
C
4.(2020,咸宁)将一定质量的锌粉加入到Cu(NO3)2、AgNO3两种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是( )
A.若滤液为蓝色,则滤渣中一定有银和铜
B.若滤液为无色,则滤渣中一定有银和锌,可能含有铜
D
C.若向滤液中加入稀盐酸有白色沉淀生成,则原滤液中溶质只有AgNO3和Zn(NO3)2
D.若向滤渣中加入稀盐酸有气泡产生,则滤液中溶质只有Zn(NO3)2
5.(2020,抚顺)金属材料对于促进生产发展、改善人类生活发挥了重大作用。
(1)铝具有很好的抗腐蚀性能,原因是
。
(2)一氧化碳的还原性可用于冶金工业,写出一氧化碳和氧化铜反应的化学方程式 。
常温下铝与空气中的氧气反应,表面生成一层致密的
氧化铝薄膜,阻止铝进一步氧化
(3)向含有硫酸铜和硫酸锌的混合溶液中,加入过量的铁粉,充分反应后过滤,得到滤液和滤渣,滤渣中含有的物质是 。
铁、铜
(4)下列保护金属资源的做法不正确的是 (填字母序号)。
A.任意开采矿物
B.回收利用废旧金属
C.铁制品存放在潮湿的环境中
D.用塑料代替金属材料制造管道
AC
思维导图
考点扫描
1.金属的普遍特性:固态(除汞外),有 ,是良好的 ,有 性,密度和熔点高。
2.非金属的性质:固、液、气态,有多种颜色,不具备金属特性,性质不一,应用不一。
考点一 金属与非金属(九上教材P36)
金属光泽
导电、导热体
延展
3.常见金属的主要性质和用途
?
主要性质
用途
铁
银白色金属光泽,质软
制各种铁合金,用于机械、建筑、医疗等行业
铜
紫红色金属光泽,纯铜质软、韧性好
制造电线、电缆及导热器具,用于制各种铜合金
铝
银白色金属光泽,密度小,抗腐蚀性强
制造电线、电缆、铝箔包装,用于建筑装饰材料及汽车等的材料
1.(2020,益阳)国产飞机C919机壳采用了先进的铝锂合金材料。下列有关说法错误的是( )
A.铝锂合金密度小
B.铝锂合金的硬度比纯铝大
C.铝锂合金抗腐蚀性强
D.铝锂合金是合成材料
D
1.金属活动性顺序
2.金属活动性的应用
(1)金属的位置越靠前,在水溶液里就越容易 电子,活动性就 。
考点二 金属活动性顺序(九上教材P43)
失去
越强
(2)金属与酸反应时,排在____前面的金属能置换出酸里的____。
(3)金属与盐发生反应时,只有活动性____的金属才能把活动性弱的金属从它的盐溶液中置换出来。K、Ca、Na会与盐溶液中的水反应,生成碱和氢气。
氢
氢
强
2.下列四种金属中,有一种金属的盐溶液与其他三种金属都能发生置换反应,这种金属是( )
A.Ag B.Cu C.Fe D.Mg
A
1.金属腐蚀的条件:(1)外因:水分、氧气等物质的作用;(2)内因:金属的内部结构。
2.防止金属腐蚀的常用方法
(1)改变金属的 ,如在普通钢中加入铬、镍等金属元素制成不锈钢;
(2)表面覆盖 ,如刷漆、涂机油、涂搪瓷、电镀、烤蓝等。
考点三 金属的防腐(九上教材P46)
内部结构
保护膜
3.(2020,雅安)下列措施中,不能防止金属制品锈蚀的是( )
A.在表面刷漆
B.改用不锈钢
C.在表面镀铬
D.用湿布擦拭
D
由于垃圾填埋处理后,金属不会自行分解,并且铅、镉等金属被腐蚀后,会形成溶于水的有毒的金属离子,污染土壤和地下水源。因此废弃金属将对环境造成严重的污染,大部分金属应通过回收使其循环再利用。
考点四 废弃金属对环境的影响(八下教材P189)
1.合金:一种金属跟其他一种或几种金属(或非金属)一起熔合而成的具有金属特征的物质。
2.改善金属材料性能的主要方法是改变金属的内部结构和外部条件。
考点五 金属材料的发展(九上教材P38)
精讲释疑
金属的用途是重要考点,用途是由其性质决定的,因此考查用途时应紧密联系金属的性质。如物理性质:导电性、延展性、导热性等;化学性质:与氧反应、活动性强弱等。
题型一 金属的性质和用途
【例1】 (2019,衡阳)下列有关金属材料的说法中正确的是( )
A.地壳中含量最高的金属元素是铁
B.钢的性能优良,所以钢是纯净的铁
C.多数合金的抗腐蚀性能比组成它们的纯金属更好
D.银的导电性最好,大多数电线都是用银作材料
C
1.(2020,长沙)北斗系统的全面建成彰显了中国航天的力量,在航天科技中会用到大量金属材料。下列有关金属材料的说法正确的是( )
A.合金中一定只含金属元素
B.纯铜比黄铜的硬度更大
C.生锈的钢铁制品没有回收价值
D.钛和钛合金被广泛用于火箭、导弹等
D
熟悉金属活动性顺序,应用金属活动性顺序时需要注意:金属与酸反应时,浓硫酸和硝酸与金属不发生置换反应。特别活泼的金属如钾、钙、钠等与盐溶液反应时,是先和水反应,故不能置换出盐溶液中的金属元素。
题型二 金属活动性顺序
【例2】 某废液中只含有Fe(NO3)2、Cu(NO3)2、Ba(NO3)2三种溶质,为了回收金属、保护环境,小科设计了如图方案(所加试剂均过量),下列判断正确的是( )
A.固体a是铜
B.X一定是Na2SO4
C.溶液B中含有的盐有Ba(NO3)2、NaNO3
D.若回收到6.4 g固体a,则加入的铁屑质量为5.6 g
C
2.(2020,锦州)将一定量的锌粉加入到硝酸镁和硝酸铜的混合液中,充分反应后过滤,得到滤渣和滤液。下列判断正确的是( )
A.若滤液为蓝色,则滤渣中一定有锌、镁、铜
B.若向滤渣中加入稀盐酸有气泡产生,则滤液中一定有硝酸镁、硝酸锌、硝酸铜
D
C.若向滤液中加入氢氧化钠溶液,则一定有氢氧化铜生成
D.滤渣中一定含有铜,滤液中一定含有硝酸镁和硝酸锌
金属锈蚀是与水和空气中的氧气等反应,分析金属生锈的原因要从内因和外因两个方面考虑。针对产生的原因寻找相应的防锈措施。关于金属锈蚀的实验探究设计要注意控制变量。
题型三 金属腐蚀条件的研究
【例3】 某同学根据铜绿的成分Cu2(OH)2CO3作出猜想:金属铜锈蚀的条件除有氧气和水外,还必须有二氧化碳。为证明“必须有二氧化碳”,需要进行如图所示实验中的( )
A.甲和乙
B.甲和丁
C.乙和丁
D.丙和丁
B
3.(2020,日照)如图是探究铁钉锈蚀条件的4个实验,一段时间后观察现象。下列说法不正确的是( )
A.①中甲、乙、丙三处比较,生锈最明显的地方是甲
A
B.①②对比说明铁生锈需要空气,①③对比说明铁生锈需要水
C.③中附着在棉花上的氯化钙的作用是作干燥剂
D.四个实验中,生锈最快的是④中的铁钉
诊断自测
1.(2020,湘潭)我国第一艘国产航母“山东舰”在制造的过程中使用了大量的金属材料,下列有关金属材料的说法错误的是( )
A.合金的硬度一般比组成它们的纯金属更高
B.钢铁是使用最多的金属材料
C.金属在常温下都是固体
D.大多数金属为电和热的优良导体
C
2.如图是包含物质a、b、c、d和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生化学反应。单质a不可能是( )
A.Mg B.Fe
C.Ag D.Zn
C
3.(2020,滨州)现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是( )
A.完全反应所需时间:丙>甲>乙
B.生成氢气的质量:甲>乙>丙
C.相对原子质量:乙>丙>甲
D.消耗硫酸的质量:甲>乙>丙
C
4.(2020,咸宁)将一定质量的锌粉加入到Cu(NO3)2、AgNO3两种物质的混合溶液中,充分反应后过滤,得到滤液和滤渣。下列有关说法正确的是( )
A.若滤液为蓝色,则滤渣中一定有银和铜
B.若滤液为无色,则滤渣中一定有银和锌,可能含有铜
D
C.若向滤液中加入稀盐酸有白色沉淀生成,则原滤液中溶质只有AgNO3和Zn(NO3)2
D.若向滤渣中加入稀盐酸有气泡产生,则滤液中溶质只有Zn(NO3)2
5.(2020,抚顺)金属材料对于促进生产发展、改善人类生活发挥了重大作用。
(1)铝具有很好的抗腐蚀性能,原因是
。
(2)一氧化碳的还原性可用于冶金工业,写出一氧化碳和氧化铜反应的化学方程式 。
常温下铝与空气中的氧气反应,表面生成一层致密的
氧化铝薄膜,阻止铝进一步氧化
(3)向含有硫酸铜和硫酸锌的混合溶液中,加入过量的铁粉,充分反应后过滤,得到滤液和滤渣,滤渣中含有的物质是 。
铁、铜
(4)下列保护金属资源的做法不正确的是 (填字母序号)。
A.任意开采矿物
B.回收利用废旧金属
C.铁制品存放在潮湿的环境中
D.用塑料代替金属材料制造管道
AC
同课章节目录
