2020-2021学年高一下学期苏教版化学必修二专题3第一单元煤、苯 课件(29张ppt)
文档属性
| 名称 | 2020-2021学年高一下学期苏教版化学必修二专题3第一单元煤、苯 课件(29张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-01 00:00:00 | ||
图片预览





文档简介
(共29张PPT)
2、有机化合物分子可以看成是由原子或原子
团相互结合形成的。
如:一氯甲烷(CH3Cl)分子是由甲基(—CH3)
原子团和氯原子结合而成的;
硝基苯分子是由苯基(—C6H5)和硝基
(—NO2)原子团结合而成的。
1、有机化合物分子中的基团很多。
如:甲基(—CH3)、乙基(—C2H5)、苯基(—C6H5)
羟基(—OH)、醛基(—CHO)、羧基(—COOH)
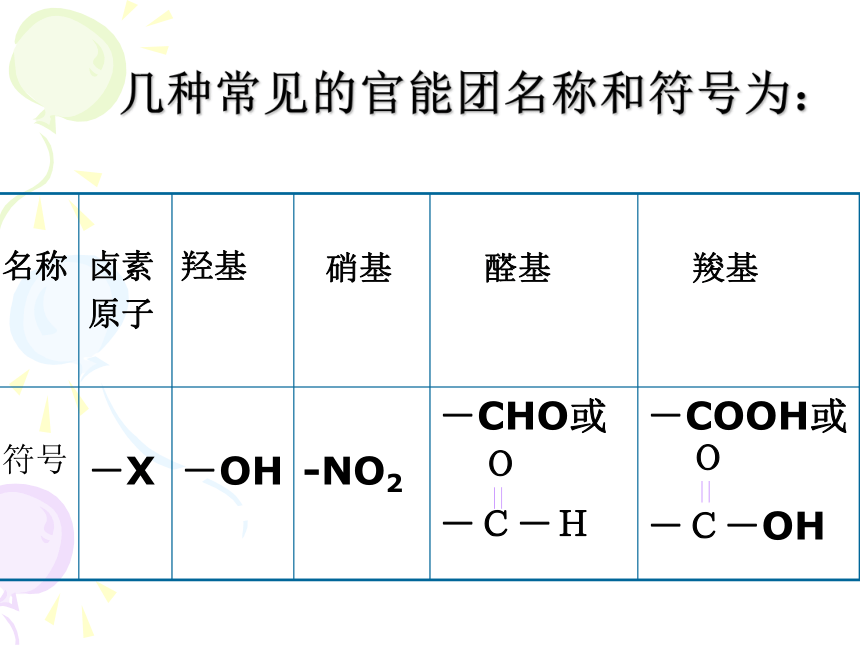
几种常见的官能团名称和符号为:
名称
卤素
原子
羟基
硝基
醛基
羧基
符号
-X
-OH
-NO2
-CHO或
-C-H
-COOH或
-C-OH
O
O
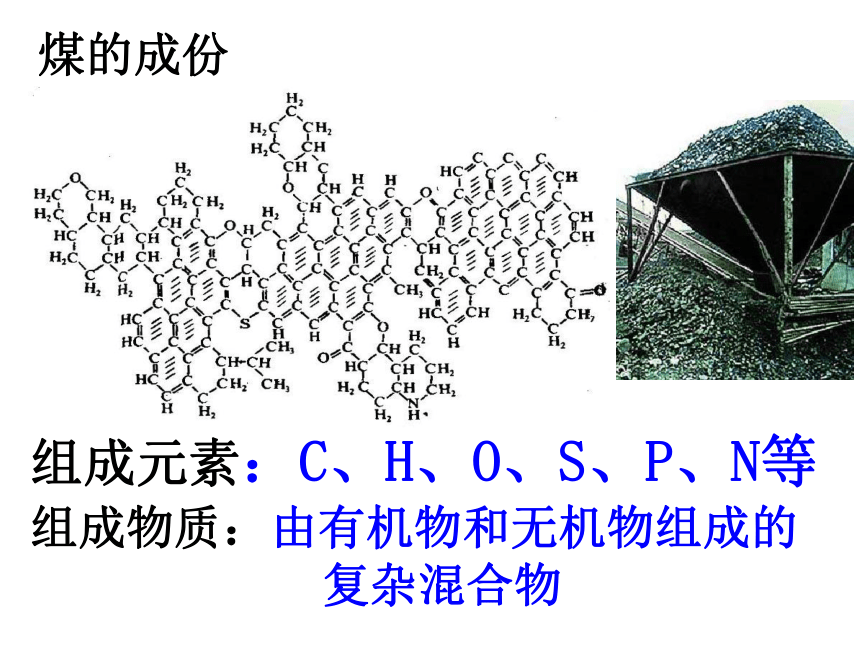
煤的成份
组成元素:C、H、O、S、P、N等
组成物质:由有机物和无机物组成的
复杂混合物
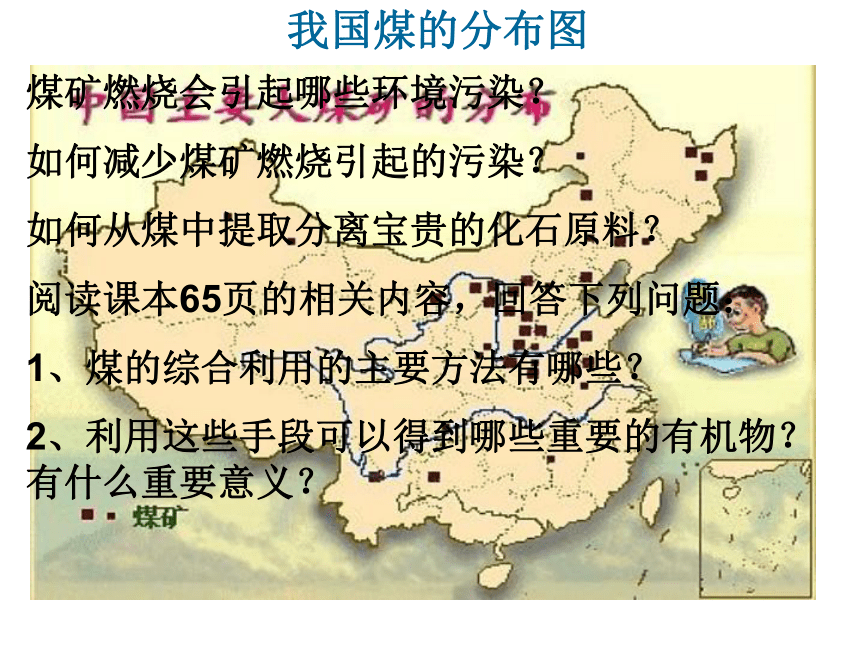
我国煤的分布图
煤矿燃烧会引起哪些环境污染?
如何减少煤矿燃烧引起的污染?
如何从煤中提取分离宝贵的化石原料?
阅读课本65页的相关内容,回答下列问题:
1、煤的综合利用的主要方法有哪些?
2、利用这些手段可以得到哪些重要的有机物?有什么重要意义?
煤的干馏
煤的液化
煤的气化
焦炭、煤焦油、焦炉气、粗苯、粗氨水
氢气、一氧化碳
C+H2O=CO+H2
液态烃和有机化合物
C+H2
汽油(C5-C12)
CO+2H2
CH3OH
复杂的物理、化学变化
19世纪,欧洲许多国家都使用煤气照明。煤气通常是压缩在桶里贮运的,人们发现这种桶里总有一种油状液体,但长时间无人问津。英国科学家法拉第对这种液体产生浓厚的兴趣,他花了整整五年时间提取这种液体,从中得到了苯:一种无色油状液体。
苯的发现史
·
动
探
读
一
读
1.苯的物理性质
(色、态、味、密度、熔点、沸点、溶解性、特性)
无色、有特殊气味的有毒液体
苯的密度比水小,且难溶于水
熔沸点低,常温下易挥发
可作为提取溴、碘的良好萃取剂!!!
算
一
算
法拉第发现苯后,对苯的组成进行测定:
他发现苯仅由碳、氢两种元素组成,其中碳的质量分数为92.3%,苯蒸气密度为同温同压下乙炔气体密度的3倍,请确定苯的分子式。
苯的分子式为:
C6H6
当时的科学家测定出苯的分子式后,但苯分子结构是十九世纪化学的一大谜。根据当时的理论,却怎么也写不出符合苯的实际化学性质的链状结构式。1865年的一个冬夜里,凯库勒一直在想着怎样在教材中写苯的结构这一难题,然而百思不得其解,只好停笔,偎炉休息。他面对炉中飘忽不定的火苗陷入了沉思,不知不觉进入了梦乡。朦胧之中,凯库勒仿佛觉得有一些碳原子在自己的面前跳起舞来,它们排成蛇的形状,一会儿在火焰中翻滚,一会儿卷曲起来,突然,原子“蛇”的头咬住了自己的尾巴,形成一个环状,不停地旋转起来。凯库勒猛然惊醒,根据梦中受到的启示,他迅速画起苯的封闭式结构式来。经过若干次的修正,最后他决定用六角环状结构来描述苯的分子结构。
凯库勒发现苯环结构
凯库勒提出两个假说:
1.苯的6个碳原子形成环状闭链,即平面六边形环。
2.各碳原子之间存在单双键交替形式。
苯的发现
凯库勒(Friedrich?August?Kekulé,1829-1896),德国化学家.
凯库勒式
2、从键长、键角的角度分析
碳碳单键键长:1.54×10-10m
碳碳双键键长:1.34×10-10m
苯分子中C-C键长都相等,为1.40×10-10m
苯不能像烯烃、炔烃那样使酸性KMnO4溶液褪色,不能通过化学反应使溴水褪色。
1、用实验事实说明
往苯中加入酸性KMnO4溶液:
往苯中加入溴水:
上层无色,下层紫红色
上层橙红色,下层无色
苯分子结构的探究
问题解决
下列两个结构简式所表示的有机化合物是同一种物质还是同分异构体?请说明你判断的理由。
3、用取代产物验证
苯的邻位二取代物只有一种
苯中不存在单双键交替结构,而是所有碳碳键完全相同的判断依据有:
1、苯不能使酸性高锰酸钾溶液褪色
2、苯不能使溴水褪色
3、苯中所有的键长都相同,为同一种键
4、苯的邻位取代产物只有一种
科学研究表明:苯分子里6个C原子之间的键完全相同,是一种介于单键和双键之间的特殊(独特)的键。
鲍林式
(3)特点
苯分子具有平面正六边形结构。分子中的六个碳原子和六个氢原子均在同一平面,苯分子里六个碳原子之间的键完全相同,是一种介于碳碳单键和碳碳双键之间的特殊的键。
(1)
分子式
最简式
(2)
结构式
结构简式
或
2、苯分子结构特点
C6H6
C
H
(1).氧化反应
a.不能被高锰酸钾氧化(溶液不褪色)
。
b.可燃性。实验现象:火焰明亮且伴有浓烟(与乙炔燃烧现象相同)
3.苯的化学性质
用玻璃棒蘸一些苯,在酒精灯上点燃,观察燃烧现象。
点燃
2
+15O2
12CO2+6H2O
(2).苯的取代反应
①跟卤素的取代反应:(苯与溴单质的反应)
+Br2
Br
+
HBr
FeBr3
溴苯(无色油状液体,P>P水)
FeBr3
+Br2
Br
+
HBr
FeBr3
苯的溴代反应实验注意问题
(1)反应用的是液溴,而不是溴水(发生萃取,分层)。
(2)制溴苯反应中,实际起催化作用的是FeBr3 2Fe+3Br2=2FeBr3
(3)导管口附近出现的白雾是HBr遇水蒸气所形成的。
(4)黄色沉淀是因为发生:AgNO3
+
HBr
=
AgBr↓
+
HNO3
溴苯(无色油状液体,P>P水)
四氯化碳的作用是吸收挥发的溴蒸汽
(无色油状液体,密度比水大)
硝基苯
水浴加热
②.苯的硝化反应:
催化剂、吸水剂
实验现象:在混合物中有淡黄色的油状液体生成,密度比水大,不溶于水。(常因混有NO2而呈淡黄色)
玻璃管
③苯的磺化反应:
+
HO-SO3H
70℃~80℃
-SO3H
+
H2O
苯磺酸
(3).苯的加成反应:苯不能与溴水发生加成反应(但能萃取溴而使水层褪色),说明它比烯烃、炔烃难进行加成反应。特殊条件下可与H2发生反应
环己烷
+
H2
Ni
△
工业制取环己烷的主要方法
总结:
苯的特殊结构
苯的特殊性质
饱和烃
不饱和烃
取代反应
加成反应
2.易取代,难加成。
苯的化学性质(较稳定):
1、难氧化(只可燃);
1、
1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列事实
A.苯不能使溴水褪色
B苯能与H2发生加成反应
C.溴苯没有同分异构体
D.邻二溴苯只有一种
AD
2、下列物质不能使酸性高锰酸钾溶液褪色的是(
)。
A.二氧化硫
B.苯
C.丙烷
D.乙烯
BC
3、只用一种试剂就能将苯、己烯、四氯化碳、碘化钾溶液区分开来,这种试剂是
A、溴水
B、溴化钾溶液
C、硝酸银溶液
D、酸性高锰酸钾溶液
4、相同体积的下列气体,在同一条件下燃烧,所需氧气的体积最多的是
A、甲烷
B、乙烷
C、乙烯
D、氢气
A
B
对比与归纳
烷烃
烯烃、炔烃
苯
与Br2作用
试剂Br2
反应条件
反应类型
与KMnO4作用
点燃
现象
结论
纯溴
溴水
纯溴
溴水
光照
取代
加成
Fe粉
取代
萃取
无反应
现象
结论
不褪色
褪色
不褪色
不被KMnO4氧化
易被KMnO4氧化
苯环难被KMnO4氧化
焰色浅,无烟
烯焰色亮有烟
炔焰色明亮,浓烟
焰色亮,浓烟
C%低
C%烯较高炔高
C%高
液苯泄露一片火海
邯郸消防激战4小时
新闻链接
2、有机化合物分子可以看成是由原子或原子
团相互结合形成的。
如:一氯甲烷(CH3Cl)分子是由甲基(—CH3)
原子团和氯原子结合而成的;
硝基苯分子是由苯基(—C6H5)和硝基
(—NO2)原子团结合而成的。
1、有机化合物分子中的基团很多。
如:甲基(—CH3)、乙基(—C2H5)、苯基(—C6H5)
羟基(—OH)、醛基(—CHO)、羧基(—COOH)
几种常见的官能团名称和符号为:
名称
卤素
原子
羟基
硝基
醛基
羧基
符号
-X
-OH
-NO2
-CHO或
-C-H
-COOH或
-C-OH
O
O
煤的成份
组成元素:C、H、O、S、P、N等
组成物质:由有机物和无机物组成的
复杂混合物
我国煤的分布图
煤矿燃烧会引起哪些环境污染?
如何减少煤矿燃烧引起的污染?
如何从煤中提取分离宝贵的化石原料?
阅读课本65页的相关内容,回答下列问题:
1、煤的综合利用的主要方法有哪些?
2、利用这些手段可以得到哪些重要的有机物?有什么重要意义?
煤的干馏
煤的液化
煤的气化
焦炭、煤焦油、焦炉气、粗苯、粗氨水
氢气、一氧化碳
C+H2O=CO+H2
液态烃和有机化合物
C+H2
汽油(C5-C12)
CO+2H2
CH3OH
复杂的物理、化学变化
19世纪,欧洲许多国家都使用煤气照明。煤气通常是压缩在桶里贮运的,人们发现这种桶里总有一种油状液体,但长时间无人问津。英国科学家法拉第对这种液体产生浓厚的兴趣,他花了整整五年时间提取这种液体,从中得到了苯:一种无色油状液体。
苯的发现史
·
动
探
读
一
读
1.苯的物理性质
(色、态、味、密度、熔点、沸点、溶解性、特性)
无色、有特殊气味的有毒液体
苯的密度比水小,且难溶于水
熔沸点低,常温下易挥发
可作为提取溴、碘的良好萃取剂!!!
算
一
算
法拉第发现苯后,对苯的组成进行测定:
他发现苯仅由碳、氢两种元素组成,其中碳的质量分数为92.3%,苯蒸气密度为同温同压下乙炔气体密度的3倍,请确定苯的分子式。
苯的分子式为:
C6H6
当时的科学家测定出苯的分子式后,但苯分子结构是十九世纪化学的一大谜。根据当时的理论,却怎么也写不出符合苯的实际化学性质的链状结构式。1865年的一个冬夜里,凯库勒一直在想着怎样在教材中写苯的结构这一难题,然而百思不得其解,只好停笔,偎炉休息。他面对炉中飘忽不定的火苗陷入了沉思,不知不觉进入了梦乡。朦胧之中,凯库勒仿佛觉得有一些碳原子在自己的面前跳起舞来,它们排成蛇的形状,一会儿在火焰中翻滚,一会儿卷曲起来,突然,原子“蛇”的头咬住了自己的尾巴,形成一个环状,不停地旋转起来。凯库勒猛然惊醒,根据梦中受到的启示,他迅速画起苯的封闭式结构式来。经过若干次的修正,最后他决定用六角环状结构来描述苯的分子结构。
凯库勒发现苯环结构
凯库勒提出两个假说:
1.苯的6个碳原子形成环状闭链,即平面六边形环。
2.各碳原子之间存在单双键交替形式。
苯的发现
凯库勒(Friedrich?August?Kekulé,1829-1896),德国化学家.
凯库勒式
2、从键长、键角的角度分析
碳碳单键键长:1.54×10-10m
碳碳双键键长:1.34×10-10m
苯分子中C-C键长都相等,为1.40×10-10m
苯不能像烯烃、炔烃那样使酸性KMnO4溶液褪色,不能通过化学反应使溴水褪色。
1、用实验事实说明
往苯中加入酸性KMnO4溶液:
往苯中加入溴水:
上层无色,下层紫红色
上层橙红色,下层无色
苯分子结构的探究
问题解决
下列两个结构简式所表示的有机化合物是同一种物质还是同分异构体?请说明你判断的理由。
3、用取代产物验证
苯的邻位二取代物只有一种
苯中不存在单双键交替结构,而是所有碳碳键完全相同的判断依据有:
1、苯不能使酸性高锰酸钾溶液褪色
2、苯不能使溴水褪色
3、苯中所有的键长都相同,为同一种键
4、苯的邻位取代产物只有一种
科学研究表明:苯分子里6个C原子之间的键完全相同,是一种介于单键和双键之间的特殊(独特)的键。
鲍林式
(3)特点
苯分子具有平面正六边形结构。分子中的六个碳原子和六个氢原子均在同一平面,苯分子里六个碳原子之间的键完全相同,是一种介于碳碳单键和碳碳双键之间的特殊的键。
(1)
分子式
最简式
(2)
结构式
结构简式
或
2、苯分子结构特点
C6H6
C
H
(1).氧化反应
a.不能被高锰酸钾氧化(溶液不褪色)
。
b.可燃性。实验现象:火焰明亮且伴有浓烟(与乙炔燃烧现象相同)
3.苯的化学性质
用玻璃棒蘸一些苯,在酒精灯上点燃,观察燃烧现象。
点燃
2
+15O2
12CO2+6H2O
(2).苯的取代反应
①跟卤素的取代反应:(苯与溴单质的反应)
+Br2
Br
+
HBr
FeBr3
溴苯(无色油状液体,P>P水)
FeBr3
+Br2
Br
+
HBr
FeBr3
苯的溴代反应实验注意问题
(1)反应用的是液溴,而不是溴水(发生萃取,分层)。
(2)制溴苯反应中,实际起催化作用的是FeBr3 2Fe+3Br2=2FeBr3
(3)导管口附近出现的白雾是HBr遇水蒸气所形成的。
(4)黄色沉淀是因为发生:AgNO3
+
HBr
=
AgBr↓
+
HNO3
溴苯(无色油状液体,P>P水)
四氯化碳的作用是吸收挥发的溴蒸汽
(无色油状液体,密度比水大)
硝基苯
水浴加热
②.苯的硝化反应:
催化剂、吸水剂
实验现象:在混合物中有淡黄色的油状液体生成,密度比水大,不溶于水。(常因混有NO2而呈淡黄色)
玻璃管
③苯的磺化反应:
+
HO-SO3H
70℃~80℃
-SO3H
+
H2O
苯磺酸
(3).苯的加成反应:苯不能与溴水发生加成反应(但能萃取溴而使水层褪色),说明它比烯烃、炔烃难进行加成反应。特殊条件下可与H2发生反应
环己烷
+
H2
Ni
△
工业制取环己烷的主要方法
总结:
苯的特殊结构
苯的特殊性质
饱和烃
不饱和烃
取代反应
加成反应
2.易取代,难加成。
苯的化学性质(较稳定):
1、难氧化(只可燃);
1、
1866年凯库勒提出了苯的单、双键交替的正六边形平面结构,解释了苯的部分性质,但还有一些问题尚未解决,它不能解释下列事实
A.苯不能使溴水褪色
B苯能与H2发生加成反应
C.溴苯没有同分异构体
D.邻二溴苯只有一种
AD
2、下列物质不能使酸性高锰酸钾溶液褪色的是(
)。
A.二氧化硫
B.苯
C.丙烷
D.乙烯
BC
3、只用一种试剂就能将苯、己烯、四氯化碳、碘化钾溶液区分开来,这种试剂是
A、溴水
B、溴化钾溶液
C、硝酸银溶液
D、酸性高锰酸钾溶液
4、相同体积的下列气体,在同一条件下燃烧,所需氧气的体积最多的是
A、甲烷
B、乙烷
C、乙烯
D、氢气
A
B
对比与归纳
烷烃
烯烃、炔烃
苯
与Br2作用
试剂Br2
反应条件
反应类型
与KMnO4作用
点燃
现象
结论
纯溴
溴水
纯溴
溴水
光照
取代
加成
Fe粉
取代
萃取
无反应
现象
结论
不褪色
褪色
不褪色
不被KMnO4氧化
易被KMnO4氧化
苯环难被KMnO4氧化
焰色浅,无烟
烯焰色亮有烟
炔焰色明亮,浓烟
焰色亮,浓烟
C%低
C%烯较高炔高
C%高
液苯泄露一片火海
邯郸消防激战4小时
新闻链接
