必修2第二章化学反应速率和限度化学平衡常数(浓度平衡常数)及转化率的应用
文档属性
| 名称 | 必修2第二章化学反应速率和限度化学平衡常数(浓度平衡常数)及转化率的应用 |

|
|
| 格式 | zip | ||
| 文件大小 | 169.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-04-03 00:00:00 | ||
图片预览


文档简介
一、化学平衡常数(浓度平衡常数)及转化率的应用
1、化学平衡常数
(1)化学平衡常数的数学表达式
(2)化学平衡常数表示的意义
平衡常数数值的大小可以反映可逆反应进行的程度大小,K值越大,反应进行越完全,反应物转化率越高,反之则越低。
2、有关化学平衡的基本计算
(1)物质浓度的变化关系
反应物:平衡浓度=起始浓度-转化浓度 生成物:平衡浓度=起始浓度+转化浓度
其中,各物质的转化浓度之比等于它们在化学方程式中物质的计量数之比。
(2)反应的转化率(α):α=×100%
(3)在密闭容器中有气体参加的可逆反应,在计算时经常用到阿伏加德罗定律的两个推论:
恒温、恒容时: ;恒温、恒压时:n1/n2=V1/V2
(4)计算模式
浓度(或物质的量) aA(g)+bB(g) cC(g)+dD(g)
起始 m n O O
转化 ax bx cx dx
平衡 m-ax n-bx cx dx
α(A)=(ax/m)×100%
ω(C)=×100%
(3)化学平衡计算的关键是准确掌握相关的基本概念及它们相互之间的关系。化学平衡的计算步骤,通常是先写出有关的化学方程式,列出反应起始时或平衡时有关物质的浓度或物质的量,然后再通过相关的转换,分别求出其他物质的浓度或物质的量和转化率。概括为:建立解题模式、确立平衡状态方程。说明:
①反应起始时,反应物和生成物可能同时存在;
②由于起始浓度是人为控制的,故不同的物质起始浓度不一定是化学计量数比,若反应物起始浓度呈现计量数比,则隐含反应物转化率相等,且平衡时反应物的浓度成计量数比的条件。
③起始浓度,平衡浓度不一定呈现计量数比,但物质之间是按计量数反应和生成的,故各物质的浓度变化一定成计量数比,这是计算的关键。
例1、对达到平衡状态的可逆反应X+YZ+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图1所示,则图象中关于X、Y、Z、W四种物质的聚集状态为( )
A.Z、W均为气体,X、Y中有一种是气体
B.Z、W中有一种是气体,X、Y皆非气体
C.X、Y、Z、W皆非气体D.X、Y均为气体,Z、W中有一种为气体
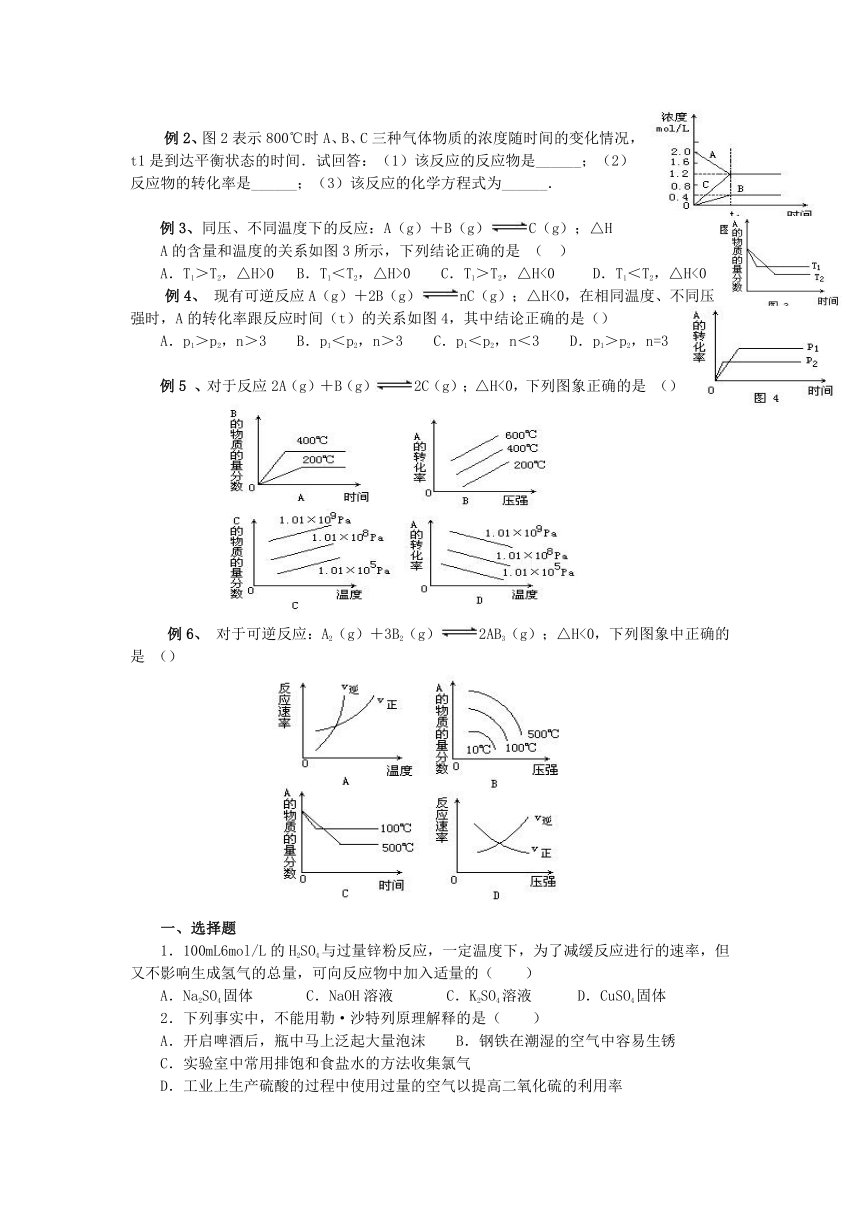
例2、图2表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间.试回答:(1)该反应的反应物是______;(2)反应物的转化率是______;(3)该反应的化学方程式为______.
例3、同压、不同温度下的反应:A(g)+B(g)C(g);△H
A的含量和温度的关系如图3所示,下列结论正确的是 ( )
A.T1>T2,△H>0 B.T1<T2,△H>0 C.T1>T2,△H<0 D.T1<T2,△H<0
例4、 现有可逆反应A(g)+2B(g)nC(g);△H<0,在相同温度、不同压强时,A的转化率跟反应时间(t)的关系如图4,其中结论正确的是()
A.p1>p2,n>3 B.p1<p2,n>3 C.p1<p2,n<3 D.p1>p2,n=3
例5 、对于反应2A(g)+B(g)2C(g);△H<0,下列图象正确的是 ()
例6、 对于可逆反应:A2(g)+3B2(g)2AB3(g);△H<0,下列图象中正确的是 ()
一、选择题
1.100mL6mol/L的H2SO4与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
A.Na2SO4固体 C.NaOH溶液 C.K2SO4溶液 D.CuSO4固体
2.下列事实中,不能用勒·沙特列原理解释的是( )
A.开启啤酒后,瓶中马上泛起大量泡沫 B.钢铁在潮湿的空气中容易生锈
C.实验室中常用排饱和食盐水的方法收集氯气
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
3.NO2溶于水生成硝酸的反应为:3NO2(g)+H2O(1) 2HNO3(1)+NO(g);△H<0。为了提高硝酸的产率,工业生产中常采取的措施是( )
A.升温 B.加水 C.通往过量的氧气 D.减压
4.将a g块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如图的实线所示,在相同的条件下,将b g(a>b)粉末状碳酸钙与同浓度盐酸反应,则相应的曲线(图中虚线所示)正确的是( )
5.在容积固定的密闭容器中存在如下反应:A(g)+3B(g) 2C(g);△H<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
下列判断一定错误的是( )
A.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
6、同温同压下,当反应物分解了8%时,总体积也增加8%的是
A.2NH3(g) N2(g)+3H2(g) B.2NO(g) N2(g)+O2(g)
C.2NO3(g) 4NO2(g)+O2(g) D.2NO2(g) 2NO(g)+O2(g)
7、对于反应2SO2+O2 2SO3,下列判断正确的是
A.2体积2SO2和足量O2反应,必定生成2体积SO3 B.其他条件不变,增大压强,平衡必定向右移动
C.平衡时,SO2消耗速度必定等于O2生成速度的两倍 D.平衡时,SO2浓度必定等于O2浓度的两倍
8、反应:L(固)+aG(气)bR(气)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2, x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断
A.上述反应是放热反应 B.上述反应是吸热反应 C.a>b D.a<b
9、压强变化不会使下列化学反应的平衡发生移动的是
A.H2(g)+ I2(g) 2 HI(g) B.3H2(g)+N2(g) 2NH3(g)
C.2SO2(g)+O2(g) 2SO3(g) D.C(s)+ CO2(g) 2CO(g)
10、放热反应CO(g)+H2O(g) CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0 mol/L,其平衡常数为K1。升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则
A.K2 和K1的单位均为mol/L B.K2c2(CO)
11、在一定温度下,向a L密闭容器中加入1mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)2Z(g) 此反应达到平衡的标志是
A.容器内压强不随时间变化 B.容器内各物质的浓度不随时间变化
C.容器内X、Y、Z的浓度之比为1︰2︰2 D.单位时间消耗0.1mol X同时生成0.2mol Z
12、1mol X气体跟a rnol Y气体在体积可变的密闭容器中发生如下反应:X(g)+a Y(g) b Z(g)反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
A.a=1,b=1 B.a=2,b=1 C.a=2,b=2 D.a=3,b=2
13、在0.lmol/L的CH3COOH溶液中存在如下电离平衡:CH3COOHCH3COO-+H+对于该平衡,下列叙述正确的是
A.加入少量NaOH固体,平衡向正反应方向移动B.加水,反应速率增大,平衡向逆反应力向移动
C.滴加少量0.lmol/L HCl溶液,溶液中c(H+)减少D.加入少量CH3COONa固体,平衡向正反应方向移动
14、恒温恒压下,在容积可变的器血中,反应2NO2(气) N2O4(气)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
A.不变 B.增大 C.减小 D.无法判断
15.哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充人1mol N2和3mol H2,在一定条件下使该反应发生。下列有关说法正确的是
A 达到化学平衡时,N2将完全转化为NH3B 达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
C 达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D 达到化学平衡时,正反应和逆反应的速率都为零
16.在一定温度不同压强(P1<P2)下,可逆反应2X(g) 2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是 ( )
17、在密闭容器中,在一定条件下,进行下列反应:NO(g) + CO(g) 1/2N2(g) + CO2(g);△H = -373.2 KJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
A.加催化剂同时升高温度 B.加催化剂同时增大压强
C.升高温度同时充入N2 D.降低温度同时增大压强
二、填空题
18、在密闭容器中,由一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内的分压与反应温度的关系如右图所示(己知气体的分压之比等于物质的量之比)。
(1)420K时,发生反应的化学方程式为:____________________________;若反应中消耗l mol Xe,则转移电子______________mol。
(2)600~800K时,会发生反应:XeF6(g)?XeF4(g)+ F2(g),其反应热△H _______0(填“>”“=”或“<”)。理由是____________________________________。
(3)900K时,容器中存在的组分有________________________________
19、将2mol H2O和2mol CO置于1L容器中,在一定条件下,加热至高温,发生如下可逆反应:2H2O(g)2H2+O2 2CO+O22CO2
(1)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是 和 ,或 和 。(填它们的分子式)
(2)若平衡时O2和CO2的物质的量分别为 n(O2)平=a mol, n(CO2)平=b mol。试求n(H2O)平= 。(用含a、b的代数式表示)。
20、在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ 700 800 830 1000 1200
K 0.6 0.9 1.0 1.7 2.6
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
(a)容器中压强不变 (b)混合气体中 c(CO)不变 (c)v正(H2)=v逆(H2O) (d)c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式: c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
21.氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图所示,已知这个反应速率随着溶液中c(H+)增大而加快。
(1)反应的离子方程式为________________。
(2)t1~t2时刻内反应速率增大的原因为_______________________________。
(3)t2~t3时刻内反应速率又减小的主要原因为__________________________。
22、(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示_________________,K值大小与温度的关系是:温度升高,K值______________(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)十H2O(g) CO2(g)十H2 (g) ;△H<0,
CO和H2O浓度变化如下图,则 0—4min的平均反应速率v(CO)=______ mol/(L·min)
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min—4min之间反应处于_________状态; C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4min—5min问,平衡向逆方向移动,可能的原因是________(单选),表中5min—6min之间数值发生变化,可能的原因是__________(单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
23、在20L恒容的密闭容器中,加入3molSO3(g)和1mol氧气,在某温度下使其反应,反应至4min时,氧气的浓度为0.06mol/L,当反应到8min时,反应到达平衡。
(1)0min—4min内生成O2的平均速率
v(O2)=________________
(2)整个过程中,各物质的浓度与时间关系如图所示,则该温度下的平衡常数
K=_____________________
(3)若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于0.05mol/L的是__________,此时的平衡常数与(2)小题比较_____________(填“大于”、“小于”或“等于”)
A B C D
SO3 1mol 3mol 3mol 0mol
SO2 2mol 1.5mol 0mol 6mol
O 2 2mol 1mol 0mol 5mol
(4)物质的浓度不再改变标志该反应已达平衡,下列还可以说明该反应已达平衡的是_____(填序号)
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均分子量不再改变
④
⑤
24、2L容积不变的密闭容器中,加入1.0molA和2.2molB,进行如下反应:A(g)+2B(g)C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图
试回答下列问题:
(1)800℃时。0—5min内,以B表示的平均反应速率为 。
(2)能判断该反应达到化学平衡状态的标志是 。
A.容器压强不变 B.混合气体中c(A)不变 C.2v正(B)=v逆(D) D.c(A)=c(C) E. 混合气体密度不变
(3)利用图中数据计算800℃时的平衡常数K= ,B的平衡转化率为: 。该反应为 反应(填吸热或放热)。
(4)700℃时,另一2L容积不变的密闭容器中,测得某时刻各物质的量如下:n(A)=2.2mol,n(B)=5.2mol,n(C)=1.8mol,n(D)=1.8mol,则此时该反应 进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
参考答案:
1、C 2 、B3 、C4、C5、AB6、A7、BC8、D9、A10、BC11、AB12、AD13、A14、A15、C16、 B 17、B
18.(1) Xe + 3 F2 === Xe F6 6 (2) >随着温度的升高,Xe F6(g)? Xe F4 (g) + F2 (g)平衡向右移动,根据温度升高平衡向吸热反应方向移动的原理,则该反应的ΔH>0。
(3) Xe F6 、Xe F4 、Xe F2 、Xe 、F2
19、(1)H2O H2, CO CO2 (2)(2-2a-b) mol
20、(1) (2)吸热 (3)b、c (4)830
21、 (1)ClO3-+3HSO3-=Cl-+3SO42-+3H+ (2)开始时,c(H+)增大,反应速率加快。(3)随着反应的进行,反应的物浓度减小,反应速率减慢。
22.(1) 可逆反应的进行程度越大 可能增大也可能减小(2) 0.03 (3) ①平衡> ②d a
23(1) (2) (3)BD, 等于 (4)①③④
24、(1)0.12mol·L—1·min—1 (2)AB(2分,漏一个扣1分,错选不得分)
(3)1.8(mol·L—1)—1(单位可不写)54.5% 吸热 (4)向正反应方向
1、化学平衡常数
(1)化学平衡常数的数学表达式
(2)化学平衡常数表示的意义
平衡常数数值的大小可以反映可逆反应进行的程度大小,K值越大,反应进行越完全,反应物转化率越高,反之则越低。
2、有关化学平衡的基本计算
(1)物质浓度的变化关系
反应物:平衡浓度=起始浓度-转化浓度 生成物:平衡浓度=起始浓度+转化浓度
其中,各物质的转化浓度之比等于它们在化学方程式中物质的计量数之比。
(2)反应的转化率(α):α=×100%
(3)在密闭容器中有气体参加的可逆反应,在计算时经常用到阿伏加德罗定律的两个推论:
恒温、恒容时: ;恒温、恒压时:n1/n2=V1/V2
(4)计算模式
浓度(或物质的量) aA(g)+bB(g) cC(g)+dD(g)
起始 m n O O
转化 ax bx cx dx
平衡 m-ax n-bx cx dx
α(A)=(ax/m)×100%
ω(C)=×100%
(3)化学平衡计算的关键是准确掌握相关的基本概念及它们相互之间的关系。化学平衡的计算步骤,通常是先写出有关的化学方程式,列出反应起始时或平衡时有关物质的浓度或物质的量,然后再通过相关的转换,分别求出其他物质的浓度或物质的量和转化率。概括为:建立解题模式、确立平衡状态方程。说明:
①反应起始时,反应物和生成物可能同时存在;
②由于起始浓度是人为控制的,故不同的物质起始浓度不一定是化学计量数比,若反应物起始浓度呈现计量数比,则隐含反应物转化率相等,且平衡时反应物的浓度成计量数比的条件。
③起始浓度,平衡浓度不一定呈现计量数比,但物质之间是按计量数反应和生成的,故各物质的浓度变化一定成计量数比,这是计算的关键。
例1、对达到平衡状态的可逆反应X+YZ+W,在其他条件不变的情况下,增大压强,反应速率变化图象如图1所示,则图象中关于X、Y、Z、W四种物质的聚集状态为( )
A.Z、W均为气体,X、Y中有一种是气体
B.Z、W中有一种是气体,X、Y皆非气体
C.X、Y、Z、W皆非气体D.X、Y均为气体,Z、W中有一种为气体
例2、图2表示800℃时A、B、C三种气体物质的浓度随时间的变化情况,t1是到达平衡状态的时间.试回答:(1)该反应的反应物是______;(2)反应物的转化率是______;(3)该反应的化学方程式为______.
例3、同压、不同温度下的反应:A(g)+B(g)C(g);△H
A的含量和温度的关系如图3所示,下列结论正确的是 ( )
A.T1>T2,△H>0 B.T1<T2,△H>0 C.T1>T2,△H<0 D.T1<T2,△H<0
例4、 现有可逆反应A(g)+2B(g)nC(g);△H<0,在相同温度、不同压强时,A的转化率跟反应时间(t)的关系如图4,其中结论正确的是()
A.p1>p2,n>3 B.p1<p2,n>3 C.p1<p2,n<3 D.p1>p2,n=3
例5 、对于反应2A(g)+B(g)2C(g);△H<0,下列图象正确的是 ()
例6、 对于可逆反应:A2(g)+3B2(g)2AB3(g);△H<0,下列图象中正确的是 ()
一、选择题
1.100mL6mol/L的H2SO4与过量锌粉反应,一定温度下,为了减缓反应进行的速率,但又不影响生成氢气的总量,可向反应物中加入适量的( )
A.Na2SO4固体 C.NaOH溶液 C.K2SO4溶液 D.CuSO4固体
2.下列事实中,不能用勒·沙特列原理解释的是( )
A.开启啤酒后,瓶中马上泛起大量泡沫 B.钢铁在潮湿的空气中容易生锈
C.实验室中常用排饱和食盐水的方法收集氯气
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
3.NO2溶于水生成硝酸的反应为:3NO2(g)+H2O(1) 2HNO3(1)+NO(g);△H<0。为了提高硝酸的产率,工业生产中常采取的措施是( )
A.升温 B.加水 C.通往过量的氧气 D.减压
4.将a g块状碳酸钙跟足量盐酸反应,反应物损失的质量随时间的变化曲线如图的实线所示,在相同的条件下,将b g(a>b)粉末状碳酸钙与同浓度盐酸反应,则相应的曲线(图中虚线所示)正确的是( )
5.在容积固定的密闭容器中存在如下反应:A(g)+3B(g) 2C(g);△H<0。某研究小组研究了其他条件不变时,改变某一条件对上述反应的影响,并根据实验数据作出下列关系图:
下列判断一定错误的是( )
A.图I研究的是不同催化剂对反应的影响,且乙使用的催化剂效率较高
B.图Ⅱ研究的是压强对反应的影响,且甲的压强较高
C.图Ⅱ研究的是温度对反应的影响,且甲的温度较高
D.图Ⅲ研究的是不同催化剂对反应的影响,且甲使用的催化剂效率较高
6、同温同压下,当反应物分解了8%时,总体积也增加8%的是
A.2NH3(g) N2(g)+3H2(g) B.2NO(g) N2(g)+O2(g)
C.2NO3(g) 4NO2(g)+O2(g) D.2NO2(g) 2NO(g)+O2(g)
7、对于反应2SO2+O2 2SO3,下列判断正确的是
A.2体积2SO2和足量O2反应,必定生成2体积SO3 B.其他条件不变,增大压强,平衡必定向右移动
C.平衡时,SO2消耗速度必定等于O2生成速度的两倍 D.平衡时,SO2浓度必定等于O2浓度的两倍
8、反应:L(固)+aG(气)bR(气)达到平衡时,温度和压强对该反应的影响图所示:图中:压强p1>p2, x轴表示温度,y轴表示平衡混合气中G的体积分数。据此可判断
A.上述反应是放热反应 B.上述反应是吸热反应 C.a>b D.a<b
9、压强变化不会使下列化学反应的平衡发生移动的是
A.H2(g)+ I2(g) 2 HI(g) B.3H2(g)+N2(g) 2NH3(g)
C.2SO2(g)+O2(g) 2SO3(g) D.C(s)+ CO2(g) 2CO(g)
10、放热反应CO(g)+H2O(g) CO2(g)+H2(g)在温度t1时达到平衡,c1(CO)=c1(H2O)=1.0 mol/L,其平衡常数为K1。升高反应体系的温度至t2时,反应物的平衡浓度分别为c2(CO)和c2(H2O),平衡常数为K2,则
A.K2 和K1的单位均为mol/L B.K2
11、在一定温度下,向a L密闭容器中加入1mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)2Z(g) 此反应达到平衡的标志是
A.容器内压强不随时间变化 B.容器内各物质的浓度不随时间变化
C.容器内X、Y、Z的浓度之比为1︰2︰2 D.单位时间消耗0.1mol X同时生成0.2mol Z
12、1mol X气体跟a rnol Y气体在体积可变的密闭容器中发生如下反应:X(g)+a Y(g) b Z(g)反应达到平衡后,测得X的转化率为50%。而且,在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的3/4,则a和b的数值可能是
A.a=1,b=1 B.a=2,b=1 C.a=2,b=2 D.a=3,b=2
13、在0.lmol/L的CH3COOH溶液中存在如下电离平衡:CH3COOHCH3COO-+H+对于该平衡,下列叙述正确的是
A.加入少量NaOH固体,平衡向正反应方向移动B.加水,反应速率增大,平衡向逆反应力向移动
C.滴加少量0.lmol/L HCl溶液,溶液中c(H+)减少D.加入少量CH3COONa固体,平衡向正反应方向移动
14、恒温恒压下,在容积可变的器血中,反应2NO2(气) N2O4(气)达到平衡后,再向容器内通入一定量NO2,又达到平衡时,N2O4的体积分数
A.不变 B.增大 C.减小 D.无法判断
15.哈伯因发明了由氮气和氢气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充人1mol N2和3mol H2,在一定条件下使该反应发生。下列有关说法正确的是
A 达到化学平衡时,N2将完全转化为NH3B 达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
C 达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D 达到化学平衡时,正反应和逆反应的速率都为零
16.在一定温度不同压强(P1<P2)下,可逆反应2X(g) 2Y(g) + Z(g)中,生成物Z在反应混合物中的体积分数(ψ)与反应时间(t)的关系有以下图示,正确的是 ( )
17、在密闭容器中,在一定条件下,进行下列反应:NO(g) + CO(g) 1/2N2(g) + CO2(g);△H = -373.2 KJ/mol,达到平衡后,为提高该反应的速率和NO的转化率,采取的正确措施是
A.加催化剂同时升高温度 B.加催化剂同时增大压强
C.升高温度同时充入N2 D.降低温度同时增大压强
二、填空题
18、在密闭容器中,由一定起始浓度的氙(Xe)和F2反应,可得到3种氟化物。各种生成物在平衡体系内的分压与反应温度的关系如右图所示(己知气体的分压之比等于物质的量之比)。
(1)420K时,发生反应的化学方程式为:____________________________;若反应中消耗l mol Xe,则转移电子______________mol。
(2)600~800K时,会发生反应:XeF6(g)?XeF4(g)+ F2(g),其反应热△H _______0(填“>”“=”或“<”)。理由是____________________________________。
(3)900K时,容器中存在的组分有________________________________
19、将2mol H2O和2mol CO置于1L容器中,在一定条件下,加热至高温,发生如下可逆反应:2H2O(g)2H2+O2 2CO+O22CO2
(1)当上述系统达到平衡时,欲求其混合气体的平衡组成,则至少还需要知道两种气体的平衡浓度,但这两种气体不能同时是 和 ,或 和 。(填它们的分子式)
(2)若平衡时O2和CO2的物质的量分别为 n(O2)平=a mol, n(CO2)平=b mol。试求n(H2O)平= 。(用含a、b的代数式表示)。
20、在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ 700 800 830 1000 1200
K 0.6 0.9 1.0 1.7 2.6
回答下列问题:
(1)该反应的化学平衡常数表达式为K= 。
(2)该反应为 反应(选填吸热、放热)。
(3)能判断该反应是否达到化学平衡状态的依据是 (多选扣分)。
(a)容器中压强不变 (b)混合气体中 c(CO)不变 (c)v正(H2)=v逆(H2O) (d)c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式: c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为 ℃。
21.氯酸钾和亚硫酸氢钠发生氧化还原反应生成Cl(-1价)和S(+6价)的速率如图所示,已知这个反应速率随着溶液中c(H+)增大而加快。
(1)反应的离子方程式为________________。
(2)t1~t2时刻内反应速率增大的原因为_______________________________。
(3)t2~t3时刻内反应速率又减小的主要原因为__________________________。
22、(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示_________________,K值大小与温度的关系是:温度升高,K值______________(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)十H2O(g) CO2(g)十H2 (g) ;△H<0,
CO和H2O浓度变化如下图,则 0—4min的平均反应速率v(CO)=______ mol/(L·min)
(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min—4min之间反应处于_________状态; C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4min—5min问,平衡向逆方向移动,可能的原因是________(单选),表中5min—6min之间数值发生变化,可能的原因是__________(单选)。
a.增加水蒸气 b.降低温度 c.使用催化剂 d.增加氢气浓度
23、在20L恒容的密闭容器中,加入3molSO3(g)和1mol氧气,在某温度下使其反应,反应至4min时,氧气的浓度为0.06mol/L,当反应到8min时,反应到达平衡。
(1)0min—4min内生成O2的平均速率
v(O2)=________________
(2)整个过程中,各物质的浓度与时间关系如图所示,则该温度下的平衡常数
K=_____________________
(3)若起始时按下表数据投料,相同温度下达到平衡时,三氧化硫浓度大于0.05mol/L的是__________,此时的平衡常数与(2)小题比较_____________(填“大于”、“小于”或“等于”)
A B C D
SO3 1mol 3mol 3mol 0mol
SO2 2mol 1.5mol 0mol 6mol
O 2 2mol 1mol 0mol 5mol
(4)物质的浓度不再改变标志该反应已达平衡,下列还可以说明该反应已达平衡的是_____(填序号)
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均分子量不再改变
④
⑤
24、2L容积不变的密闭容器中,加入1.0molA和2.2molB,进行如下反应:A(g)+2B(g)C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图
试回答下列问题:
(1)800℃时。0—5min内,以B表示的平均反应速率为 。
(2)能判断该反应达到化学平衡状态的标志是 。
A.容器压强不变 B.混合气体中c(A)不变 C.2v正(B)=v逆(D) D.c(A)=c(C) E. 混合气体密度不变
(3)利用图中数据计算800℃时的平衡常数K= ,B的平衡转化率为: 。该反应为 反应(填吸热或放热)。
(4)700℃时,另一2L容积不变的密闭容器中,测得某时刻各物质的量如下:n(A)=2.2mol,n(B)=5.2mol,n(C)=1.8mol,n(D)=1.8mol,则此时该反应 进行(填“向正反应方向”“向逆反应方向”或“处于平衡状态”)。
参考答案:
1、C 2 、B3 、C4、C5、AB6、A7、BC8、D9、A10、BC11、AB12、AD13、A14、A15、C16、 B 17、B
18.(1) Xe + 3 F2 === Xe F6 6 (2) >随着温度的升高,Xe F6(g)? Xe F4 (g) + F2 (g)平衡向右移动,根据温度升高平衡向吸热反应方向移动的原理,则该反应的ΔH>0。
(3) Xe F6 、Xe F4 、Xe F2 、Xe 、F2
19、(1)H2O H2, CO CO2 (2)(2-2a-b) mol
20、(1) (2)吸热 (3)b、c (4)830
21、 (1)ClO3-+3HSO3-=Cl-+3SO42-+3H+ (2)开始时,c(H+)增大,反应速率加快。(3)随着反应的进行,反应的物浓度减小,反应速率减慢。
22.(1) 可逆反应的进行程度越大 可能增大也可能减小(2) 0.03 (3) ①平衡> ②d a
23(1) (2) (3)BD, 等于 (4)①③④
24、(1)0.12mol·L—1·min—1 (2)AB(2分,漏一个扣1分,错选不得分)
(3)1.8(mol·L—1)—1(单位可不写)54.5% 吸热 (4)向正反应方向
