2020-2021学年九年级下学期化学京改版(2013)第12章 盐检测题(有答案)
文档属性
| 名称 | 2020-2021学年九年级下学期化学京改版(2013)第12章 盐检测题(有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 104.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 北京课改版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-07 00:00:00 | ||
图片预览



文档简介
《盐》检测题
一、单选题
1.下列应用、相应的原理(用化学方程式表示)及基本反应类型均正确的是(
)
A.拉瓦锡研究空气的成分
2Hg+O2Hg2O
化合反应
B.除去银粉中的铜粉
Cu+2AgCl=2Ag
+
CuCl2
置换反应
C.实验室用氯酸钾制氧气
2KClO32KCl
+
3O2↑
分解反应
D.盐酸除水垢的反应之一
2HCl
+CaCO3=CaCl2+H2O
+CO2↑
复分解反应
2.下列化学用语书写正确的是( )
A.两个氢原子:H2
B.纯碱:NaHCO3
C.硝酸根离子NO3﹣
D.+2价的铜元素:Cu2+
3.缺磷小麦生长缓慢,为了促进其生长,应该施用的化肥是
A.CO(NH2)2
B.K2SO4
C.NH4HCO3
D.Ca(H2PO4)2
4.分类是种重要的学习方法,下列有关分类的说法正确的是( )
A.C2H5OH和NaOH都属于碱B.甲烷、冰水混合物都是化合物
C.纯碱、小苏打、石灰石都是盐D.生铁、铜、不锈钢都是合金
5.物质的化学名与俗名,对应错误的是
A.汞——水银
B.氯化钠——食盐
C.乙醇——酒精
D.甲烷——液化气
6.下列物质按照酸、碱、盐、氧化物顺序排列的是
A.K2SO4
Ba(OH)2
KCl
KClO3
B.HNO3
NaOH
HCl
CuO
C.HCl
Ca(OH)2
AgCl
NO2
D.H2SO4
KNO3
NH4C1
CH4
7.小乐将铁粉和硫粉以适当的质量比混合,堆放在石棉网上,然后用烧红的玻璃棒一端接触混合物,等部分混合物迅速变红热状态后,撤离玻璃棒,反应能继续进行,直至全部混合物都呈红热的状态,冷却后得到一种黑色固态物质,下列分析正确的是( )
A.参与反应的铁和硫都属于金属单质,生成的黑色固体物质属于盐
B.混合物有红热现象,可作为此变化是化学变化的证据
C.反应需要用红热的玻璃棒加热,说明此反应为吸热反应
D.用磁铁吸引可以证实反应中铁已从游离态变成化合态
8.8.下列物质间的转化不能通过一步反应实现的是
A.Fe→Fe3O4
B.S→SO3
C.CO2→CO
D.Na2CO3→NaCl
9.除去物质中的少量杂质,下列方法不能达到目的的是( )
选项
物质
杂质
除去杂质的方法
A
硫酸亚铁溶液
硫酸铜
加入足量的铁粉,充分反应后过滤
B
二氧化碳
氯化氢
依次通过足量的氢氧化钠溶液、浓硫酸
C
硫酸钠溶液
碳酸钠
加入适量稀硫酸至恰好不再产生气泡
D
碳酸钙
氯化钙
加足量的水溶解、过滤、洗涤、干燥
A.A
B.B
C.C
D.D
10.区分下列物质的方法中不可行的是
A.用闻气味的方法区别氧气和二氧化碳B.用水区分硝酸铵和食盐两种固体
C.用肥皂水鉴别硬水和软水D.用稀硫酸区分黄铜(Cu、Zn)和青铜(Cu、Sn)
11.实验方法能达到实验目的的是
选项
实验目的
实验方法
A
除去NaOH溶液中Na2CO3
加入适量稀盐酸至不再产生气泡
B
检验CH4中是否含有CO
将气体点燃
C
除去粗盐中的难溶性杂质
加入足量水,溶解、蒸发、结晶
D
比较Fe、Cu、Ag的金属活动性
将Fe和Ag分别放入Cu(NO3)2溶液中
A.A
B.B
C.C
D.D
12.甲、乙、丙三种物质只通过一步反应,不能实现如图所示的转化关系的是(
)
选项
甲
乙
丙
A
B
C
C
D
A.A
B.B
C.C
D.D
13.下列物质的转化(“→”表示一种物质转化为另一种物质)中,每次转化只通过一步反应,不可能全部实现的是( )
A.H2O2→O2→CO2→H2CO3
B.NaOH→NaNO3→Na2CO3→NaCl
C.CaCO3→CaO→Ca(OH)2→KOH
D.Mg→H2→HCl→AlCl3
二、填空题
14.许多化学知识可以解决生活中的实际问题,请按要求填空。
(1)由于水质原因,水壶用久后,会沉积水垢,水垢的主要成分是碳酸钙和氢氧化镁,其中碳酸钙的化学式为_____。写出用盐酸除去水垢的一个化学方程式____________。
(2)蒸馒头时,向发酵的面团内加入一定量的碳酸氢钠粉末,该物质能与面团中的___(填微粒符号)发生反应产生二氧化碳。
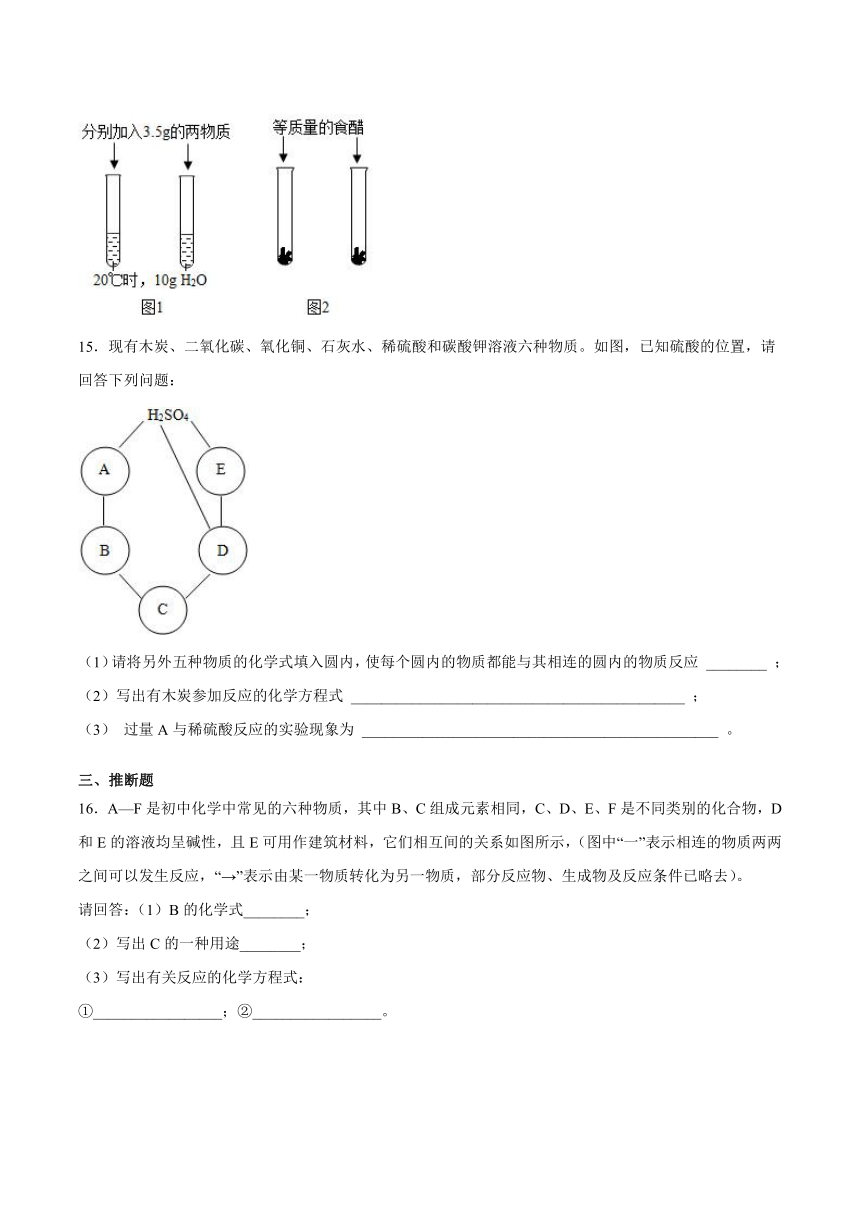
(3)要区分厨房中的食盐和纯碱,人们通常采用如下两种方法。
方法
1:如图
1所示,充分溶解后,可观察到_________,从而区分出二者。(查阅信息,20℃时,NaCl的溶解度为
36g,Na2CO3的溶解度为
21.5g)
方法
2:如图
2所示,分别向盛有两物质的试管内加入等质量的食醋,可观察到______,从而区分出二者。
15.现有木炭、二氧化碳、氧化铜、石灰水、稀硫酸和碳酸钾溶液六种物质。如图,已知硫酸的位置,请回答下列问题:
(1)请将另外五种物质的化学式填入圆内,使每个圆内的物质都能与其相连的圆内的物质反应
________
;
(2)写出有木炭参加反应的化学方程式
____________________________________________
;
(3)
过量A与稀硫酸反应的实验现象为
_______________________________________________
。
三、推断题
16.A—F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“一”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去)。
请回答:(1)B的化学式________;
(2)写出C的一种用途________;
(3)写出有关反应的化学方程式:
①_________________;②_________________。
17.实验室内有一包不纯的氯化钾粉末,含有的杂质可能是氯化铜、硝酸钾、硝酸钙、氯化钠、碳酸钠中的一种或几种,为确定其成分,进行如下实验。
(1)取少许该粉末,加入足量的蒸馏水,使其完全溶解,只得到无色澄清溶液。则杂质一定不含______。
(2)取(1)中无色溶液加入BaCl2溶液,产生白色沉淀,则杂质一定含有______。
(3)另称取14.9g该粉末于烧杯中,加入蒸馏水使其完全溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后生成28.7g白色沉淀,则杂质还一定含有______。通过以上三个实验还不能确定含有的杂质是______。
18.A~F
是初中化学常见的六种物质,可以构建如图所示的反应及转化关系。其中的一个反应关系能实现波尔多液的配制,一个相互转化关系能实现自然界中的碳、氧循环。E是地壳中含量最高的金属。(用“—”或“⌒”表示两种物质能发生反应,用“”或
“?”、“”表示两种物质能单向或双向转化。部分反应物、生成物及反应条件已略去,
图中部分反应需在溶液中进行,物质是溶液的只考虑溶质。)
(1)写出C、D
物质(或溶质)的化学式:①C:
_______;②D:
_______;
(2)通过非基本反应类型实现
BA
的化学方程式为
_______;
(3)足量(打磨过的)E
与F
反应的实验现象是
_______。
四、实验题
19.实验室常用下图所示的一些装置制取气体,请回答:
(1)写出标号①的仪器名称:
___
。
(2)用B装置制取氧气时,有关的化学方程式是
___
。
(3)实验室制得的CO2中常混有酸雾和水蒸气,可以按照“发生装置→F→F→收集装置”的顺序得到高纯度的CO2,其中第一个F装置(内盛半瓶饱和的小苏打溶液)的作用是
__
(用化学方程式说明),第二个F装置中盛放的试剂是
__
。
(4)加热氯化铵与熟石灰的固体混合物制NH3,发生装置选
___
。用F装置收集NH3(密度比空气小),进气管是
___
(填a或b)。
20.实验室某种废液中含有碳酸钠、氢氧化钠、硫酸铜、盐酸一种或种溶质。为确定其组成设计并进行如下实验。
实验:
现象:无色液体、酚酞变红、______
结论:废液中一定含有碳酸钠、氢氧化钠。
分析:废液中一定没有的硫酸铜原因是__________。用一个化学方程式说明溶液中一定没有盐酸,该化学方程式是_______。
五、计算题
21.100
g
某盐酸溶液恰好与
10.6
g
碳酸钠完全反应。请计算:
(1)生成二氧化碳气体的质量为
___g;
(2)该盐酸溶液中溶质的质量分数______。(计算结果保留到
0.1%)
22.某实验小组的同学为了测定实验室中氯酸钾样品的杂质含量,取一定质量的该样品与1g二氧化锰混合,其总质量为6g,然后依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
加热时间
t1
t2
t3
t4
剩余固体质量(g)
4.24
4.16
4.08
4.08
试计算:
(1)完全反应后产生的氧气的总质量是
(2)原样品中杂质的质量是多少?
参考答案
1.D
2.C
3.D
4.B
5.D
6.C
7.D
8.B
9.B
10.A
11.D
12.B
13.B
14.CaCO3
CaCO3+2HCl=CaCl2+H2O+CO2↑(或2HCl+Mg(OH)2=MgCl2+2H2O)
H+
一种物质全部溶解,一种物质部分溶解
一支试管有气泡产生,一支试管无明显现象
15.A为氧化铜,B为木炭,C为二氧化碳,D为石灰水,E为碳酸钾溶液
C+
2CuO
高温2Cu
+
CO2↑或
C
+
CO2高温
2CO
黑色固体逐渐减少(不消失),溶液由无色变为蓝色
16.CO
灭火(人工降雨等)
17.氯化铜
碳酸钠
氯化钠
硝酸钾
18.H2O
Ca(OH)2
CH4+2O2CO2+2H2O
银白色固体表面有紫红色物质析出,溶液由蓝色变为无色
19.水槽
2H2O2
2H2O+O2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
浓硫酸
A
b
20.有白色沉淀生成,溶液仍为红色
废液呈无色,而硫酸铜溶液是蓝色的
(或
)
21.(1)4.4g(2)7.3%
22.(1)1.92g(2)0.1
g
一、单选题
1.下列应用、相应的原理(用化学方程式表示)及基本反应类型均正确的是(
)
A.拉瓦锡研究空气的成分
2Hg+O2Hg2O
化合反应
B.除去银粉中的铜粉
Cu+2AgCl=2Ag
+
CuCl2
置换反应
C.实验室用氯酸钾制氧气
2KClO32KCl
+
3O2↑
分解反应
D.盐酸除水垢的反应之一
2HCl
+CaCO3=CaCl2+H2O
+CO2↑
复分解反应
2.下列化学用语书写正确的是( )
A.两个氢原子:H2
B.纯碱:NaHCO3
C.硝酸根离子NO3﹣
D.+2价的铜元素:Cu2+
3.缺磷小麦生长缓慢,为了促进其生长,应该施用的化肥是
A.CO(NH2)2
B.K2SO4
C.NH4HCO3
D.Ca(H2PO4)2
4.分类是种重要的学习方法,下列有关分类的说法正确的是( )
A.C2H5OH和NaOH都属于碱B.甲烷、冰水混合物都是化合物
C.纯碱、小苏打、石灰石都是盐D.生铁、铜、不锈钢都是合金
5.物质的化学名与俗名,对应错误的是
A.汞——水银
B.氯化钠——食盐
C.乙醇——酒精
D.甲烷——液化气
6.下列物质按照酸、碱、盐、氧化物顺序排列的是
A.K2SO4
Ba(OH)2
KCl
KClO3
B.HNO3
NaOH
HCl
CuO
C.HCl
Ca(OH)2
AgCl
NO2
D.H2SO4
KNO3
NH4C1
CH4
7.小乐将铁粉和硫粉以适当的质量比混合,堆放在石棉网上,然后用烧红的玻璃棒一端接触混合物,等部分混合物迅速变红热状态后,撤离玻璃棒,反应能继续进行,直至全部混合物都呈红热的状态,冷却后得到一种黑色固态物质,下列分析正确的是( )
A.参与反应的铁和硫都属于金属单质,生成的黑色固体物质属于盐
B.混合物有红热现象,可作为此变化是化学变化的证据
C.反应需要用红热的玻璃棒加热,说明此反应为吸热反应
D.用磁铁吸引可以证实反应中铁已从游离态变成化合态
8.8.下列物质间的转化不能通过一步反应实现的是
A.Fe→Fe3O4
B.S→SO3
C.CO2→CO
D.Na2CO3→NaCl
9.除去物质中的少量杂质,下列方法不能达到目的的是( )
选项
物质
杂质
除去杂质的方法
A
硫酸亚铁溶液
硫酸铜
加入足量的铁粉,充分反应后过滤
B
二氧化碳
氯化氢
依次通过足量的氢氧化钠溶液、浓硫酸
C
硫酸钠溶液
碳酸钠
加入适量稀硫酸至恰好不再产生气泡
D
碳酸钙
氯化钙
加足量的水溶解、过滤、洗涤、干燥
A.A
B.B
C.C
D.D
10.区分下列物质的方法中不可行的是
A.用闻气味的方法区别氧气和二氧化碳B.用水区分硝酸铵和食盐两种固体
C.用肥皂水鉴别硬水和软水D.用稀硫酸区分黄铜(Cu、Zn)和青铜(Cu、Sn)
11.实验方法能达到实验目的的是
选项
实验目的
实验方法
A
除去NaOH溶液中Na2CO3
加入适量稀盐酸至不再产生气泡
B
检验CH4中是否含有CO
将气体点燃
C
除去粗盐中的难溶性杂质
加入足量水,溶解、蒸发、结晶
D
比较Fe、Cu、Ag的金属活动性
将Fe和Ag分别放入Cu(NO3)2溶液中
A.A
B.B
C.C
D.D
12.甲、乙、丙三种物质只通过一步反应,不能实现如图所示的转化关系的是(
)
选项
甲
乙
丙
A
B
C
C
D
A.A
B.B
C.C
D.D
13.下列物质的转化(“→”表示一种物质转化为另一种物质)中,每次转化只通过一步反应,不可能全部实现的是( )
A.H2O2→O2→CO2→H2CO3
B.NaOH→NaNO3→Na2CO3→NaCl
C.CaCO3→CaO→Ca(OH)2→KOH
D.Mg→H2→HCl→AlCl3
二、填空题
14.许多化学知识可以解决生活中的实际问题,请按要求填空。
(1)由于水质原因,水壶用久后,会沉积水垢,水垢的主要成分是碳酸钙和氢氧化镁,其中碳酸钙的化学式为_____。写出用盐酸除去水垢的一个化学方程式____________。
(2)蒸馒头时,向发酵的面团内加入一定量的碳酸氢钠粉末,该物质能与面团中的___(填微粒符号)发生反应产生二氧化碳。
(3)要区分厨房中的食盐和纯碱,人们通常采用如下两种方法。
方法
1:如图
1所示,充分溶解后,可观察到_________,从而区分出二者。(查阅信息,20℃时,NaCl的溶解度为
36g,Na2CO3的溶解度为
21.5g)
方法
2:如图
2所示,分别向盛有两物质的试管内加入等质量的食醋,可观察到______,从而区分出二者。
15.现有木炭、二氧化碳、氧化铜、石灰水、稀硫酸和碳酸钾溶液六种物质。如图,已知硫酸的位置,请回答下列问题:
(1)请将另外五种物质的化学式填入圆内,使每个圆内的物质都能与其相连的圆内的物质反应
________
;
(2)写出有木炭参加反应的化学方程式
____________________________________________
;
(3)
过量A与稀硫酸反应的实验现象为
_______________________________________________
。
三、推断题
16.A—F是初中化学中常见的六种物质,其中B、C组成元素相同,C、D、E、F是不同类别的化合物,D和E的溶液均呈碱性,且E可用作建筑材料,它们相互间的关系如图所示,(图中“一”表示相连的物质两两之间可以发生反应,“→”表示由某一物质转化为另一物质,部分反应物、生成物及反应条件已略去)。
请回答:(1)B的化学式________;
(2)写出C的一种用途________;
(3)写出有关反应的化学方程式:
①_________________;②_________________。
17.实验室内有一包不纯的氯化钾粉末,含有的杂质可能是氯化铜、硝酸钾、硝酸钙、氯化钠、碳酸钠中的一种或几种,为确定其成分,进行如下实验。
(1)取少许该粉末,加入足量的蒸馏水,使其完全溶解,只得到无色澄清溶液。则杂质一定不含______。
(2)取(1)中无色溶液加入BaCl2溶液,产生白色沉淀,则杂质一定含有______。
(3)另称取14.9g该粉末于烧杯中,加入蒸馏水使其完全溶解,再加入足量的硝酸银溶液和稀硝酸,充分反应后生成28.7g白色沉淀,则杂质还一定含有______。通过以上三个实验还不能确定含有的杂质是______。
18.A~F
是初中化学常见的六种物质,可以构建如图所示的反应及转化关系。其中的一个反应关系能实现波尔多液的配制,一个相互转化关系能实现自然界中的碳、氧循环。E是地壳中含量最高的金属。(用“—”或“⌒”表示两种物质能发生反应,用“”或
“?”、“”表示两种物质能单向或双向转化。部分反应物、生成物及反应条件已略去,
图中部分反应需在溶液中进行,物质是溶液的只考虑溶质。)
(1)写出C、D
物质(或溶质)的化学式:①C:
_______;②D:
_______;
(2)通过非基本反应类型实现
BA
的化学方程式为
_______;
(3)足量(打磨过的)E
与F
反应的实验现象是
_______。
四、实验题
19.实验室常用下图所示的一些装置制取气体,请回答:
(1)写出标号①的仪器名称:
___
。
(2)用B装置制取氧气时,有关的化学方程式是
___
。
(3)实验室制得的CO2中常混有酸雾和水蒸气,可以按照“发生装置→F→F→收集装置”的顺序得到高纯度的CO2,其中第一个F装置(内盛半瓶饱和的小苏打溶液)的作用是
__
(用化学方程式说明),第二个F装置中盛放的试剂是
__
。
(4)加热氯化铵与熟石灰的固体混合物制NH3,发生装置选
___
。用F装置收集NH3(密度比空气小),进气管是
___
(填a或b)。
20.实验室某种废液中含有碳酸钠、氢氧化钠、硫酸铜、盐酸一种或种溶质。为确定其组成设计并进行如下实验。
实验:
现象:无色液体、酚酞变红、______
结论:废液中一定含有碳酸钠、氢氧化钠。
分析:废液中一定没有的硫酸铜原因是__________。用一个化学方程式说明溶液中一定没有盐酸,该化学方程式是_______。
五、计算题
21.100
g
某盐酸溶液恰好与
10.6
g
碳酸钠完全反应。请计算:
(1)生成二氧化碳气体的质量为
___g;
(2)该盐酸溶液中溶质的质量分数______。(计算结果保留到
0.1%)
22.某实验小组的同学为了测定实验室中氯酸钾样品的杂质含量,取一定质量的该样品与1g二氧化锰混合,其总质量为6g,然后依次加热该混合物t1、t2、t3、t4时间后,分别冷却称量剩余固体质量,记录的有关数据如下表(样品中的杂质不参与化学反应)
加热时间
t1
t2
t3
t4
剩余固体质量(g)
4.24
4.16
4.08
4.08
试计算:
(1)完全反应后产生的氧气的总质量是
(2)原样品中杂质的质量是多少?
参考答案
1.D
2.C
3.D
4.B
5.D
6.C
7.D
8.B
9.B
10.A
11.D
12.B
13.B
14.CaCO3
CaCO3+2HCl=CaCl2+H2O+CO2↑(或2HCl+Mg(OH)2=MgCl2+2H2O)
H+
一种物质全部溶解,一种物质部分溶解
一支试管有气泡产生,一支试管无明显现象
15.A为氧化铜,B为木炭,C为二氧化碳,D为石灰水,E为碳酸钾溶液
C+
2CuO
高温2Cu
+
CO2↑或
C
+
CO2高温
2CO
黑色固体逐渐减少(不消失),溶液由无色变为蓝色
16.CO
灭火(人工降雨等)
17.氯化铜
碳酸钠
氯化钠
硝酸钾
18.H2O
Ca(OH)2
CH4+2O2CO2+2H2O
银白色固体表面有紫红色物质析出,溶液由蓝色变为无色
19.水槽
2H2O2
2H2O+O2↑
NaHCO3+HCl=NaCl+H2O+CO2↑
浓硫酸
A
b
20.有白色沉淀生成,溶液仍为红色
废液呈无色,而硫酸铜溶液是蓝色的
(或
)
21.(1)4.4g(2)7.3%
22.(1)1.92g(2)0.1
g
