2021年科学 中考二轮专题复习:化学基础 (基础巩固)(含答案)
文档属性
| 名称 | 2021年科学 中考二轮专题复习:化学基础 (基础巩固)(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 264.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-06-08 15:09:47 | ||
图片预览



文档简介
中考二轮专题复习:化学基础 (基础巩固)
一、单选题(共20题;共40分)
1.“丹砂烧之成水银”中的“丹砂”指的是硫化汞,该反应的微观示意图如下。有关说法错误的是(?? )
A.?是一种氧化物???????????????????????????????????????B.?此反应遵循质量守恒定律
C.?反应前后分子的种类发生改变?????????????????????????????D.?反应前后各元素的化合价都不变
2.构成人体骨骼和牙齿的无机盐称为骨盐,其中含有氟化钙(CaF2)。氟化钙中氟(F)元素的化合价为(? )
A.??2????????????????????????????????????????B.??1????????????????????????????????????????C.?+1????????????????????????????????????????D.?+2
3.某化工厂以石灰石(CaCO3)和水为主要原料制取熟石灰[Ca(OH)2]。其制取过程中的变化关系可表示为CaCO3 →高温 CaO →+H2O Ca(OH)2。
上述两步变化过程中依次涉及到的化学反应类型是(??? )
A.?分解反应和氧化反应???????????????????????????????????????????B.?化合反应和分解反应
C.?分解反应和化合反应???????????????????????????????????????????D.?氧化反应和化合反应
4.?下列物质中所含氮元素化合价最低的是( )
A.?NO2???????????????????????????????????B.?N2???????????????????????????????????C.?NH4Cl???????????????????????????????????D.?HNO3
5.碳一12是指含6个中子的碳原子,下列对氧一16和氧一18两种氧原子的说法正确的是(?? )
A.?质子数相同??????????????????B.?质量相同??????????????????C.?电子数不相同??????????????????D.?16和18表示原子个数
6.?科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置,如图是该反应的微观示意图,下列说法错误的是( )
A.?化学反应前后原子的种类、个数、质量均保持不变?????B.?W物质中碳元素的质量分数为75%
C.?参加反应的X、Y两物质的粒子个数比为3:4??????????????D.??该反应不属于置换反应
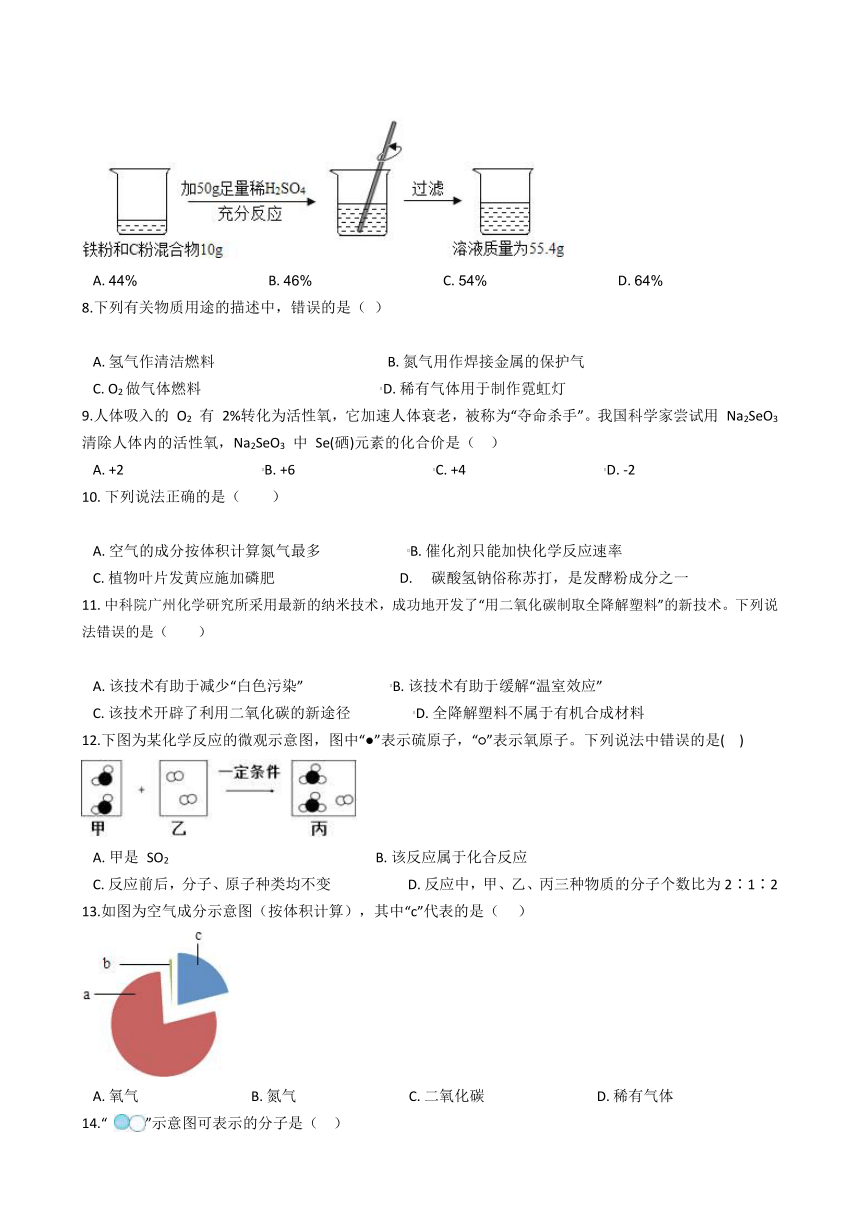
7.?根据下面的实验过程和提供的数据,可知样品中碳的质量分数为( )
A.?44% ????????????????????????????????????B.?46% ????????????????????????????????????C.?54% ????????????????????????????????????D.?64%
8.下列有关物质用途的描述中,错误的是( )
A.?氢气作清洁燃料??????????????????????????????????????????????????B.?氮气用作焊接金属的保护气
C.?O2做气体燃料????????????????????????????????????????????????????D.?稀有气体用于制作霓虹灯
9.人体吸入的 O2 有 2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用 Na2SeO3 清除人体内的活性氧,Na2SeO3 中 Se(硒)元素的化合价是(?? )
A.?+2????????????????????????????????????????B.?+6????????????????????????????????????????C.?+4????????????????????????????????????????D.?-2
10.?下列说法正确的是( )
A.?空气的成分按体积计算氮气最多?????????????????????????B.?催化剂只能加快化学反应速率
C.?植物叶片发黄应施加磷肥????????????????????????????????????D.??碳酸氢钠俗称苏打,是发酵粉成分之一
11.?中科院广州化学研究所采用最新的纳米技术,成功地开发了“用二氧化碳制取全降解塑料”的新技术。下列说法错误的是( )
A.?该技术有助于减少“白色污染”?????????????????????????B.?该技术有助于缓解“温室效应”
C.?该技术开辟了利用二氧化碳的新途径??????????????????D.?全降解塑料不属于有机合成材料
12.下图为某化学反应的微观示意图,图中“●”表示硫原子,“○”表示氧原子。下列说法中错误的是(?? )
A.?甲是 SO2????????????????????????????????????????????????????????????B.?该反应属于化合反应
C.?反应前后,分子、原子种类均不变??????????????????????D.?反应中,甲、乙、丙三种物质的分子个数比为2∶1∶2
13.如图为空气成分示意图(按体积计算),其中“c”代表的是(??? )
A.?氧气????????????????????????????????B.?氮气????????????????????????????????C.?二氧化碳????????????????????????????????D.?稀有气体
14.“ ”示意图可表示的分子是(?? )
A.?He??????????????????????????????????????B.?Cl2??????????????????????????????????????C.?CO??????????????????????????????????????D.?CH4
15.美国曾发射“嗅碳”卫星,用于探测大气中二氧化碳含量。如果每个小球表示一个原子 ,则下列可以表示一个二氧化碳分子模型的是 ( ????)
A.?????????????????????????????B.?????????????????????????????C.?????????????????????????????D.?
16.通过化学式“H2O”可以获取的信息错误的是 (?? )
A.?水这种物质?????????????????????????????????????????????????????????B.?一个水分子
C.?水分子是由氢、氧两种元素组成?????????????????????????D.?一个水分子是由两个氢原子和一个氧原子构成
17.人体主要的呼吸肌是(? )
A.?胸大肌和膈肌??????????????????B.?肋间肌和膈肌??????????????????C.?背阔肌和膈肌??????????????????D.?腹直肌和膈肌
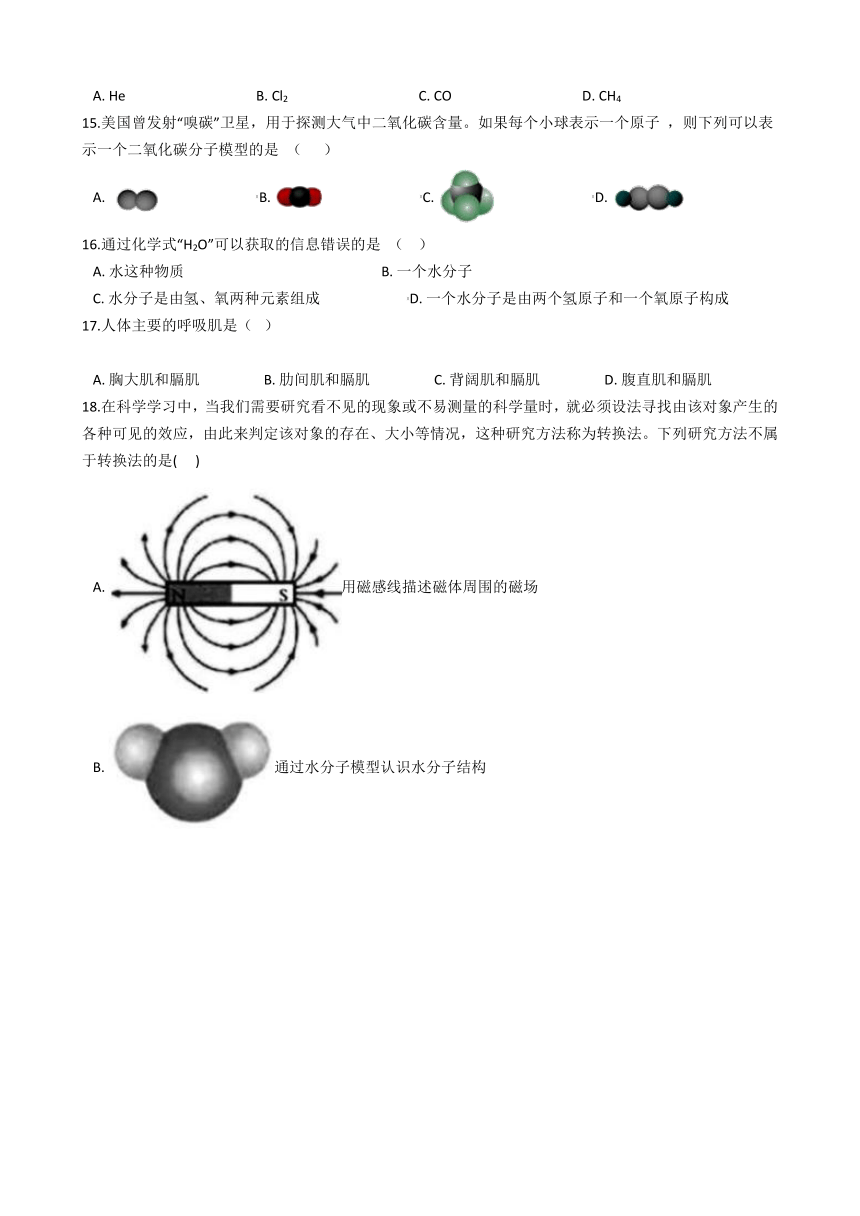
18.在科学学习中,当我们需要研究看不见的现象或不易测量的科学量时,就必须设法寻找由该对象产生的各种可见的效应,由此来判定该对象的存在、大小等情况,这种研究方法称为转换法。下列研究方法不属于转换法的是(??? )
A.?用磁感线描述磁体周围的磁场
B.?通过水分子模型认识水分子结构
C.?用红色水滴的移动来证明动物的呼吸作用
D.?通过两个塑料杯中的水温变化研究温室的保温原理
19.下列科学家的科学研究中,没有用到模型的是( ???)
A.?欧姆定律 ???????????????????????????B.?α粒子轰击原子
C.?DNA双螺旋结构 ???????????????????????????????D.?磷元素
20.二氧化硫,氧化钙,二氧化碳,氧气中都含(??? )
A.?氧气?????????????????????????????????B.?氧元素?????????????????????????????????C.?氧原子?????????????????????????????????D.?氧分子
二、填空题(共10题;共22分)
21.砷(As)是一种非金属元素,它有+3价和+5价,因此可以形成两种含氧酸——砷酸和亚砷酸。砷酸的化学式为________。
22.化学用语可准确简洁地表达和交流化学信息。请用化学符号填写:
(1)氮气________
(2)2个硫酸根离子________
(3)五个水分子________。
23.?已知镁可以在某种气体中燃烧,用化学方程式表达为:2Mg+X2MgO+C,则X的化学式为________?;该反应属于四种基本反应类型中的________?反应.标出氧化镁中镁元素的化合价________?.
24.????? 绣绣利用长柄 W 形玻璃管,完成了燃烧条件的探究与空气中氧气含量的粗略测定。
(1)燃烧条件的探究:在如图所示装置(省略夹持仪器,下同)中,向W 形玻璃管中放入足量红磷和白磷,塞好橡皮塞, 关闭活塞,然后将其放入 80℃的热水中,观察到红磷不燃烧而白磷燃烧,说明可燃物发生燃烧应具备的条件是________。
(2)空气中氧气含量的粗略测定:为减小测量误差,待火焰熄灭后,等玻璃管________ , 再打开活塞。
25.?根据下列示意图提供的信息回答问题:
(1)在化学反应中钠原子易________(填“得”或“失”)1个电子;
(2)氯元素属于________(填“金属”或“非金属”)元素;
(3)上述过程中形成化合物的化学式为________?.
26.写出下列物质的元素符号或元素名称:
碳________;??? 镁________;??? 氮________;??
Al________;??? Ca________
27.?如图所示,A是金属氧化物,B是一种金属单质,C是黄色溶液,D是浅绿色溶液,反应③是物质E与氧气、水发生的一个化合反应,请回答下列问题:
(1)写出试剂甲可能的化学式: ________? .
(2)试剂乙中一定含有的离子: ________?.
(3)写出化学变化①和②的化学方程式:
①________ ;
②________? .
28.20世纪初科学家发现,原子的核式结构与太阳系十分相似。它的中心是原子核,原子核是由 ________?和 ________?组成的。
29.能源、环境与人类的生活和社会发展密切相关.酒精(C2H5OH)是一种可再生能源,请写出酒精充分燃烧的化学方程式:________.
30.化学上用 ________?来表示元素原子之间相互化合的数目。一般情况下,在化合物里,氧元素通常显 ________?价;氢元素通常显________? 价;金属元素通常显________? ,非金属元素与氧化合时显 ________ 。在化合物中,各元素正负化合价的代数和为________? 。在单质中,元素的化合价为________? 。
三、解答题(共8题;共43分)
31.?某氢氧化钙粉末中含有碳酸钙杂质.现取样品15g于锥形瓶中并加适量水搅拌得悬浊液,然后向锥形瓶中滴加稀盐酸,充分反应,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示.
(1)生成二氧化碳的质量是________?g;
(2)加入60g稀盐酸后所得溶液中含有的溶质是 ________?、 ________?(填化学式);
(3)计算样品中碳酸钙的质量分数(写出计算过程,结果精确到0.1%).
32.?通过学习化学,你会发现化学就在身边,可以运用化学知识解释生活中一些现象.
(1)墙内开花墙外香主要体现分子的什么基本性质?
(2)油锅着火用锅盖盖灭应用什么灭火原理?
(3)冰箱里放活性炭除异味主要利用活性炭的什么性质?
33.新装修房间中往往会含有较多的甲醛,人体长期摄人超标的甲醛会对健康造成影响。甲醛的化学式为HCHO,请回答下列问题:
(1)甲醛由________种元素组成。
(2)甲醛中碳、氢、氧元素的质量比为________。(写最简整数比)
(3)计算甲醛中氢元素的质量分数。(保留两位小数)
34.头孢氨苄是一种常用的口服抗生素,它能抑制细菌细胞壁的合成,杀死细菌。
(1)头孢氨苄的化学式为C16H17N3O4S,完全燃烧生成CO2和H2O的质量比为________。
(2)头孢氨苄注射前要进行皮试,以免发生过敏反应。如用0.5克头孢氨苄粉末配制质量分数为0.05%的皮试药液,则可配得皮试药液的质量为________克。
(3)针对目前滥用抗生素的现象,医学界提出“能吃药不打针,能打针不输液”。下列有关抗生素使用的观点,其中合理的有?? ?????。??????
A.某次感冒时,服用头孢氨苄胶囊后很快痊愈,如果以后再感冒,坚持用头孢氨苄胶囊
B.感冒的致病原因有多种,不是所有的感冒都要使用抗生素进行治疗
C.为了避免浪费,感冒时应先服用以前用剩的头孢氨苄胶囊,若无效再寻医就诊
D.抗生素的治疗效果与用药量有关,为了早日痊愈,应尽量增加用药量
E.某种抗生素的治疗效果较好,也不应长期使用,避免使病菌产生耐药性
35.维生素C(化学式:C6H8O6)对人体皮肤和牙龈健康有重要作用,缺乏维生素C,会引起坏血病,中学生每天需要补充60mg维生素C,请阅读信息后回答:
(1)维生素C中有________种元素组成
(2)维生素C分子的相对分子质量是________。
36.?低钠盐是一种健康食盐,以普通钠盐为基础添加一定量氯化钠(氯化钠70%左右,氯化钾30%左右),有助于人体钠、钾平衡,降低高血压、心血管疾病的患病风险.另外,由于食盐中导致咸味的是氯离子,因此,低钠盐能较好实现减钠补钾不减咸味的目的.
课外探究小组为调查市场售低钠盐是否合格,选用一种常见低钠盐进行实验分析:
步骤一:用电子天平准确称取低钠盐样品2.00g,放入洁净小烧杯中加水,搅拌至样品充分溶解;
步骤二:向上述小烧杯中逐滴加入足量的硝酸银溶液,边滴边搅拌至不再生成沉淀为止;
步骤三:将沉淀经过滤、干燥后,称得沉淀质量为4.51g.
(1)某同学参照样品配比,计算出2.00g低钠盐样品中氯化钠(氯化钠70%)与硝酸银反应所得沉淀的质量为3.43g,请你计算出样品中氯化钾与硝酸银反应所得沉淀的质量;(简单写出计算过程,计算结果精确到0.01)
(2)经计算,你认为样品是否合格?________.
(3)可我探究小组在教师指导下,取同质量样品再次精确实验,最终得到沉淀的质量为4.56g,比较两次实验所得沉淀的质量.请分析造成误差的主要原因________ .
37.?一定质量的碳酸钠和氯化钠固体混合物,加入101克水完全溶解后,再往其中加入100g氯化钙溶液,恰好完全反应.过滤,将滤渣干燥,称得其质量为10g,测得滤液中溶质的质量分数为10%.试计算:
(1)100g氯化钙溶液中溶质的质量;
(2)原固体混合物中碳酸钠的质量分数.
38.下图是某包装袋上的部分文字说明。
(1)这里的钙、铁、磷、锌指的是________(选填“分子”、“原子”或“元素”)。
(2)这袋奶粉中含蛋白质的质量为________g。
(3)蛋白质是人体重要营养物质之一,在消化道中的________进行初步消化。
四、实验探究题(共2题;共7分)
39.卢瑟福用a粒子(α粒子是带两个单位正电荷的氦原子核)轰击金箔的实验,推翻了汤姆生在1903年提出的原子结构模型,为建立现代原子理论打下了基础,但通过该实验的下述三种现象(如图),不能获得核外电子带有负电荷的结论。
现象1:大多数α粒子能穿透金箔而不改变原来运动方向。
现象2:一小部分α粒子改变原来的运动方向。
现象3:极少数α粒子被弹了回来。
(1)请你根据原子结构知识分析以上现象产生的原因。
①现象1的原因: ________
②现象2的原因:________?
(2)1919年,卢瑟福用加速了的高能α粒子轰击氮原子,结果有种微粒从氮原子被打出,而α粒子留在了氮原子中,使氮原子变成了氧原子,从现代观点看,被打出的微粒一定是________?。
40.我国科学家屠呦呦因为“发现青蒿素(化学式为C15H22O5)﹣一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获得2015年诺贝尔生理学或医学奖。磺胺(化学式为C6H8N2O2S)是青蒿素之前最热门的抗疟药物之一。?
青蒿素是由________构成的,一个青蒿素分子是由________?构成的。
答案解析部分
一、单选题
1.【答案】 D
2.【答案】 B
3.【答案】 C
4.【答案】 C
5.【答案】 A
6.【答案】 D
7.【答案】 A
8.【答案】 C
9.【答案】 C
10.【答案】 A
11.【答案】 D
12.【答案】 C
13.【答案】 A
14.【答案】 C
15.【答案】 B
16.【答案】 C
17.【答案】 B
18.【答案】 B
19.【答案】 D
20.【答案】 B
二、填空题
21.【答案】 H3AsO4
22.【答案】 (1)N2
(2)2 SO42?
(3)5H2O
23.【答案】 CO2;置换;Mg+2O
24.【答案】 (1)温度达到着火点
(2)充分冷却
25.【答案】 失;非金属;NaCl
26.【答案】 C;Mg;N;铝;钙
27.【答案】 HCl或H2SO4;OH﹣;3CO+Fe2O32Fe+3CO2(合理即可);Fe+2HCl═FeCl2+H2↑或 Fe+H2SO4═FeSO4+H2↑(注:第1问填HCl,该题要写前面一个方程,第1问填H2SO4 , 则该题要填写后面一个方程).
28.【答案】 质子;中子
29.【答案】 C2H5OH+3O22CO2+3H2O
30.【答案】 数值;-2;+1;正价;正价;零;零
三、解答题
31.【答案】 (1)2.2
(2)CaCl2;HCl
(3)解:设样品中碳酸钙的质量分数为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100??????????????? ? ? ? ? ? ? ? ? ? ? ? ?? 44
15g×x????????????? ? ? ? ? ? ? ? ? ? ? ? 2.2g
10015gx=442.2g
解之得:x=33.3%
答:样品中碳酸钙的质量分数为33.3%.
32.【答案】 (1)答:分子在不断运动
(2)答:隔绝空气
(3)答:吸附性
33.【答案】 (1)3
(2)6:1:8
(3)H%= 1×21×2+12+16 ×100%=6.67%
34.【答案】 (1)704: 153
(2)1000
(3)B,E
35.【答案】 (1)3
(2)176
36.【答案】 (1)解:设样品中氯化钾生成沉淀的质量为x
样品中氯化钾的质量是:2.00g×30%=0.6g
KCl+AgNO3═AgCl↓+KNO3
74.5 ? ? ? ? ? ? ?? 143.5
0.6g ? ? ? ? ? ? ? ? ? x
74.50.6g=143.5x? x≈1.16g
答:反应所得沉淀的质量约为1.16g.
(2)不合格
(3)第一次进行过滤时,滤纸上的沉淀没有全部被称量
37.【答案】 (1)解:设恰好完全反应时参加反应的碳酸钠的质量为x,氯化钙溶液中氯化钙的质量为y,生成氯化钠的质量为Z,
Na2CO3+CaCl2═CaCO3↓+2NaCl
?106? 111??? 100??? 117
?x?? ? y???? 10g??? ? Z
106x=111y=10010g=117z
?? 解得:X=10.6g?? y=11.1g?? Z=11.7g
答:氯化钙溶液中溶质的质量为11.1g
(2)解:由题意可知,设原混合物中氯化钠的质量为a,则
a+11.7g10.6g+a+101g+100g?10g×100%=10%
解得:a=9.4g
纯碱样品中碳酸钠的质量分数为:10.6g9.4g+10.6g×100%=53%
答:纯碱样品中碳酸钠的质量分数为53%.
38.【答案】 (1)元素
(2)150
(3)胃
四、实验探究题
39.【答案】 (1)原子核很小, 原子内部有很大空间;α粒子离带正电的原子核较近,受到斥力
(2)质子
40.【答案】 青蒿素分子;15个碳原子、22个氢原子和5个氧原子构成
一、单选题(共20题;共40分)
1.“丹砂烧之成水银”中的“丹砂”指的是硫化汞,该反应的微观示意图如下。有关说法错误的是(?? )
A.?是一种氧化物???????????????????????????????????????B.?此反应遵循质量守恒定律
C.?反应前后分子的种类发生改变?????????????????????????????D.?反应前后各元素的化合价都不变
2.构成人体骨骼和牙齿的无机盐称为骨盐,其中含有氟化钙(CaF2)。氟化钙中氟(F)元素的化合价为(? )
A.??2????????????????????????????????????????B.??1????????????????????????????????????????C.?+1????????????????????????????????????????D.?+2
3.某化工厂以石灰石(CaCO3)和水为主要原料制取熟石灰[Ca(OH)2]。其制取过程中的变化关系可表示为CaCO3 →高温 CaO →+H2O Ca(OH)2。
上述两步变化过程中依次涉及到的化学反应类型是(??? )
A.?分解反应和氧化反应???????????????????????????????????????????B.?化合反应和分解反应
C.?分解反应和化合反应???????????????????????????????????????????D.?氧化反应和化合反应
4.?下列物质中所含氮元素化合价最低的是( )
A.?NO2???????????????????????????????????B.?N2???????????????????????????????????C.?NH4Cl???????????????????????????????????D.?HNO3
5.碳一12是指含6个中子的碳原子,下列对氧一16和氧一18两种氧原子的说法正确的是(?? )
A.?质子数相同??????????????????B.?质量相同??????????????????C.?电子数不相同??????????????????D.?16和18表示原子个数
6.?科学家最新发现,通过简单的化学反应,可以将树木纤维素转变成超级储能装置,如图是该反应的微观示意图,下列说法错误的是( )
A.?化学反应前后原子的种类、个数、质量均保持不变?????B.?W物质中碳元素的质量分数为75%
C.?参加反应的X、Y两物质的粒子个数比为3:4??????????????D.??该反应不属于置换反应
7.?根据下面的实验过程和提供的数据,可知样品中碳的质量分数为( )
A.?44% ????????????????????????????????????B.?46% ????????????????????????????????????C.?54% ????????????????????????????????????D.?64%
8.下列有关物质用途的描述中,错误的是( )
A.?氢气作清洁燃料??????????????????????????????????????????????????B.?氮气用作焊接金属的保护气
C.?O2做气体燃料????????????????????????????????????????????????????D.?稀有气体用于制作霓虹灯
9.人体吸入的 O2 有 2%转化为活性氧,它加速人体衰老,被称为“夺命杀手”。我国科学家尝试用 Na2SeO3 清除人体内的活性氧,Na2SeO3 中 Se(硒)元素的化合价是(?? )
A.?+2????????????????????????????????????????B.?+6????????????????????????????????????????C.?+4????????????????????????????????????????D.?-2
10.?下列说法正确的是( )
A.?空气的成分按体积计算氮气最多?????????????????????????B.?催化剂只能加快化学反应速率
C.?植物叶片发黄应施加磷肥????????????????????????????????????D.??碳酸氢钠俗称苏打,是发酵粉成分之一
11.?中科院广州化学研究所采用最新的纳米技术,成功地开发了“用二氧化碳制取全降解塑料”的新技术。下列说法错误的是( )
A.?该技术有助于减少“白色污染”?????????????????????????B.?该技术有助于缓解“温室效应”
C.?该技术开辟了利用二氧化碳的新途径??????????????????D.?全降解塑料不属于有机合成材料
12.下图为某化学反应的微观示意图,图中“●”表示硫原子,“○”表示氧原子。下列说法中错误的是(?? )
A.?甲是 SO2????????????????????????????????????????????????????????????B.?该反应属于化合反应
C.?反应前后,分子、原子种类均不变??????????????????????D.?反应中,甲、乙、丙三种物质的分子个数比为2∶1∶2
13.如图为空气成分示意图(按体积计算),其中“c”代表的是(??? )
A.?氧气????????????????????????????????B.?氮气????????????????????????????????C.?二氧化碳????????????????????????????????D.?稀有气体
14.“ ”示意图可表示的分子是(?? )
A.?He??????????????????????????????????????B.?Cl2??????????????????????????????????????C.?CO??????????????????????????????????????D.?CH4
15.美国曾发射“嗅碳”卫星,用于探测大气中二氧化碳含量。如果每个小球表示一个原子 ,则下列可以表示一个二氧化碳分子模型的是 ( ????)
A.?????????????????????????????B.?????????????????????????????C.?????????????????????????????D.?
16.通过化学式“H2O”可以获取的信息错误的是 (?? )
A.?水这种物质?????????????????????????????????????????????????????????B.?一个水分子
C.?水分子是由氢、氧两种元素组成?????????????????????????D.?一个水分子是由两个氢原子和一个氧原子构成
17.人体主要的呼吸肌是(? )
A.?胸大肌和膈肌??????????????????B.?肋间肌和膈肌??????????????????C.?背阔肌和膈肌??????????????????D.?腹直肌和膈肌
18.在科学学习中,当我们需要研究看不见的现象或不易测量的科学量时,就必须设法寻找由该对象产生的各种可见的效应,由此来判定该对象的存在、大小等情况,这种研究方法称为转换法。下列研究方法不属于转换法的是(??? )
A.?用磁感线描述磁体周围的磁场
B.?通过水分子模型认识水分子结构
C.?用红色水滴的移动来证明动物的呼吸作用
D.?通过两个塑料杯中的水温变化研究温室的保温原理
19.下列科学家的科学研究中,没有用到模型的是( ???)
A.?欧姆定律 ???????????????????????????B.?α粒子轰击原子
C.?DNA双螺旋结构 ???????????????????????????????D.?磷元素
20.二氧化硫,氧化钙,二氧化碳,氧气中都含(??? )
A.?氧气?????????????????????????????????B.?氧元素?????????????????????????????????C.?氧原子?????????????????????????????????D.?氧分子
二、填空题(共10题;共22分)
21.砷(As)是一种非金属元素,它有+3价和+5价,因此可以形成两种含氧酸——砷酸和亚砷酸。砷酸的化学式为________。
22.化学用语可准确简洁地表达和交流化学信息。请用化学符号填写:
(1)氮气________
(2)2个硫酸根离子________
(3)五个水分子________。
23.?已知镁可以在某种气体中燃烧,用化学方程式表达为:2Mg+X2MgO+C,则X的化学式为________?;该反应属于四种基本反应类型中的________?反应.标出氧化镁中镁元素的化合价________?.
24.????? 绣绣利用长柄 W 形玻璃管,完成了燃烧条件的探究与空气中氧气含量的粗略测定。
(1)燃烧条件的探究:在如图所示装置(省略夹持仪器,下同)中,向W 形玻璃管中放入足量红磷和白磷,塞好橡皮塞, 关闭活塞,然后将其放入 80℃的热水中,观察到红磷不燃烧而白磷燃烧,说明可燃物发生燃烧应具备的条件是________。
(2)空气中氧气含量的粗略测定:为减小测量误差,待火焰熄灭后,等玻璃管________ , 再打开活塞。
25.?根据下列示意图提供的信息回答问题:
(1)在化学反应中钠原子易________(填“得”或“失”)1个电子;
(2)氯元素属于________(填“金属”或“非金属”)元素;
(3)上述过程中形成化合物的化学式为________?.
26.写出下列物质的元素符号或元素名称:
碳________;??? 镁________;??? 氮________;??
Al________;??? Ca________
27.?如图所示,A是金属氧化物,B是一种金属单质,C是黄色溶液,D是浅绿色溶液,反应③是物质E与氧气、水发生的一个化合反应,请回答下列问题:
(1)写出试剂甲可能的化学式: ________? .
(2)试剂乙中一定含有的离子: ________?.
(3)写出化学变化①和②的化学方程式:
①________ ;
②________? .
28.20世纪初科学家发现,原子的核式结构与太阳系十分相似。它的中心是原子核,原子核是由 ________?和 ________?组成的。
29.能源、环境与人类的生活和社会发展密切相关.酒精(C2H5OH)是一种可再生能源,请写出酒精充分燃烧的化学方程式:________.
30.化学上用 ________?来表示元素原子之间相互化合的数目。一般情况下,在化合物里,氧元素通常显 ________?价;氢元素通常显________? 价;金属元素通常显________? ,非金属元素与氧化合时显 ________ 。在化合物中,各元素正负化合价的代数和为________? 。在单质中,元素的化合价为________? 。
三、解答题(共8题;共43分)
31.?某氢氧化钙粉末中含有碳酸钙杂质.现取样品15g于锥形瓶中并加适量水搅拌得悬浊液,然后向锥形瓶中滴加稀盐酸,充分反应,测得加入稀盐酸的质量与反应生成气体的质量关系如图所示.
(1)生成二氧化碳的质量是________?g;
(2)加入60g稀盐酸后所得溶液中含有的溶质是 ________?、 ________?(填化学式);
(3)计算样品中碳酸钙的质量分数(写出计算过程,结果精确到0.1%).
32.?通过学习化学,你会发现化学就在身边,可以运用化学知识解释生活中一些现象.
(1)墙内开花墙外香主要体现分子的什么基本性质?
(2)油锅着火用锅盖盖灭应用什么灭火原理?
(3)冰箱里放活性炭除异味主要利用活性炭的什么性质?
33.新装修房间中往往会含有较多的甲醛,人体长期摄人超标的甲醛会对健康造成影响。甲醛的化学式为HCHO,请回答下列问题:
(1)甲醛由________种元素组成。
(2)甲醛中碳、氢、氧元素的质量比为________。(写最简整数比)
(3)计算甲醛中氢元素的质量分数。(保留两位小数)
34.头孢氨苄是一种常用的口服抗生素,它能抑制细菌细胞壁的合成,杀死细菌。
(1)头孢氨苄的化学式为C16H17N3O4S,完全燃烧生成CO2和H2O的质量比为________。
(2)头孢氨苄注射前要进行皮试,以免发生过敏反应。如用0.5克头孢氨苄粉末配制质量分数为0.05%的皮试药液,则可配得皮试药液的质量为________克。
(3)针对目前滥用抗生素的现象,医学界提出“能吃药不打针,能打针不输液”。下列有关抗生素使用的观点,其中合理的有?? ?????。??????
A.某次感冒时,服用头孢氨苄胶囊后很快痊愈,如果以后再感冒,坚持用头孢氨苄胶囊
B.感冒的致病原因有多种,不是所有的感冒都要使用抗生素进行治疗
C.为了避免浪费,感冒时应先服用以前用剩的头孢氨苄胶囊,若无效再寻医就诊
D.抗生素的治疗效果与用药量有关,为了早日痊愈,应尽量增加用药量
E.某种抗生素的治疗效果较好,也不应长期使用,避免使病菌产生耐药性
35.维生素C(化学式:C6H8O6)对人体皮肤和牙龈健康有重要作用,缺乏维生素C,会引起坏血病,中学生每天需要补充60mg维生素C,请阅读信息后回答:
(1)维生素C中有________种元素组成
(2)维生素C分子的相对分子质量是________。
36.?低钠盐是一种健康食盐,以普通钠盐为基础添加一定量氯化钠(氯化钠70%左右,氯化钾30%左右),有助于人体钠、钾平衡,降低高血压、心血管疾病的患病风险.另外,由于食盐中导致咸味的是氯离子,因此,低钠盐能较好实现减钠补钾不减咸味的目的.
课外探究小组为调查市场售低钠盐是否合格,选用一种常见低钠盐进行实验分析:
步骤一:用电子天平准确称取低钠盐样品2.00g,放入洁净小烧杯中加水,搅拌至样品充分溶解;
步骤二:向上述小烧杯中逐滴加入足量的硝酸银溶液,边滴边搅拌至不再生成沉淀为止;
步骤三:将沉淀经过滤、干燥后,称得沉淀质量为4.51g.
(1)某同学参照样品配比,计算出2.00g低钠盐样品中氯化钠(氯化钠70%)与硝酸银反应所得沉淀的质量为3.43g,请你计算出样品中氯化钾与硝酸银反应所得沉淀的质量;(简单写出计算过程,计算结果精确到0.01)
(2)经计算,你认为样品是否合格?________.
(3)可我探究小组在教师指导下,取同质量样品再次精确实验,最终得到沉淀的质量为4.56g,比较两次实验所得沉淀的质量.请分析造成误差的主要原因________ .
37.?一定质量的碳酸钠和氯化钠固体混合物,加入101克水完全溶解后,再往其中加入100g氯化钙溶液,恰好完全反应.过滤,将滤渣干燥,称得其质量为10g,测得滤液中溶质的质量分数为10%.试计算:
(1)100g氯化钙溶液中溶质的质量;
(2)原固体混合物中碳酸钠的质量分数.
38.下图是某包装袋上的部分文字说明。
(1)这里的钙、铁、磷、锌指的是________(选填“分子”、“原子”或“元素”)。
(2)这袋奶粉中含蛋白质的质量为________g。
(3)蛋白质是人体重要营养物质之一,在消化道中的________进行初步消化。
四、实验探究题(共2题;共7分)
39.卢瑟福用a粒子(α粒子是带两个单位正电荷的氦原子核)轰击金箔的实验,推翻了汤姆生在1903年提出的原子结构模型,为建立现代原子理论打下了基础,但通过该实验的下述三种现象(如图),不能获得核外电子带有负电荷的结论。
现象1:大多数α粒子能穿透金箔而不改变原来运动方向。
现象2:一小部分α粒子改变原来的运动方向。
现象3:极少数α粒子被弹了回来。
(1)请你根据原子结构知识分析以上现象产生的原因。
①现象1的原因: ________
②现象2的原因:________?
(2)1919年,卢瑟福用加速了的高能α粒子轰击氮原子,结果有种微粒从氮原子被打出,而α粒子留在了氮原子中,使氮原子变成了氧原子,从现代观点看,被打出的微粒一定是________?。
40.我国科学家屠呦呦因为“发现青蒿素(化学式为C15H22O5)﹣一种用于治疗疟疾的药物,挽救了全球特别是发展中国家的数百万人的生命”而获得2015年诺贝尔生理学或医学奖。磺胺(化学式为C6H8N2O2S)是青蒿素之前最热门的抗疟药物之一。?
青蒿素是由________构成的,一个青蒿素分子是由________?构成的。
答案解析部分
一、单选题
1.【答案】 D
2.【答案】 B
3.【答案】 C
4.【答案】 C
5.【答案】 A
6.【答案】 D
7.【答案】 A
8.【答案】 C
9.【答案】 C
10.【答案】 A
11.【答案】 D
12.【答案】 C
13.【答案】 A
14.【答案】 C
15.【答案】 B
16.【答案】 C
17.【答案】 B
18.【答案】 B
19.【答案】 D
20.【答案】 B
二、填空题
21.【答案】 H3AsO4
22.【答案】 (1)N2
(2)2 SO42?
(3)5H2O
23.【答案】 CO2;置换;Mg+2O
24.【答案】 (1)温度达到着火点
(2)充分冷却
25.【答案】 失;非金属;NaCl
26.【答案】 C;Mg;N;铝;钙
27.【答案】 HCl或H2SO4;OH﹣;3CO+Fe2O32Fe+3CO2(合理即可);Fe+2HCl═FeCl2+H2↑或 Fe+H2SO4═FeSO4+H2↑(注:第1问填HCl,该题要写前面一个方程,第1问填H2SO4 , 则该题要填写后面一个方程).
28.【答案】 质子;中子
29.【答案】 C2H5OH+3O22CO2+3H2O
30.【答案】 数值;-2;+1;正价;正价;零;零
三、解答题
31.【答案】 (1)2.2
(2)CaCl2;HCl
(3)解:设样品中碳酸钙的质量分数为x,
CaCO3+2HCl═CaCl2+H2O+CO2↑
100??????????????? ? ? ? ? ? ? ? ? ? ? ? ?? 44
15g×x????????????? ? ? ? ? ? ? ? ? ? ? ? 2.2g
10015gx=442.2g
解之得:x=33.3%
答:样品中碳酸钙的质量分数为33.3%.
32.【答案】 (1)答:分子在不断运动
(2)答:隔绝空气
(3)答:吸附性
33.【答案】 (1)3
(2)6:1:8
(3)H%= 1×21×2+12+16 ×100%=6.67%
34.【答案】 (1)704: 153
(2)1000
(3)B,E
35.【答案】 (1)3
(2)176
36.【答案】 (1)解:设样品中氯化钾生成沉淀的质量为x
样品中氯化钾的质量是:2.00g×30%=0.6g
KCl+AgNO3═AgCl↓+KNO3
74.5 ? ? ? ? ? ? ?? 143.5
0.6g ? ? ? ? ? ? ? ? ? x
74.50.6g=143.5x? x≈1.16g
答:反应所得沉淀的质量约为1.16g.
(2)不合格
(3)第一次进行过滤时,滤纸上的沉淀没有全部被称量
37.【答案】 (1)解:设恰好完全反应时参加反应的碳酸钠的质量为x,氯化钙溶液中氯化钙的质量为y,生成氯化钠的质量为Z,
Na2CO3+CaCl2═CaCO3↓+2NaCl
?106? 111??? 100??? 117
?x?? ? y???? 10g??? ? Z
106x=111y=10010g=117z
?? 解得:X=10.6g?? y=11.1g?? Z=11.7g
答:氯化钙溶液中溶质的质量为11.1g
(2)解:由题意可知,设原混合物中氯化钠的质量为a,则
a+11.7g10.6g+a+101g+100g?10g×100%=10%
解得:a=9.4g
纯碱样品中碳酸钠的质量分数为:10.6g9.4g+10.6g×100%=53%
答:纯碱样品中碳酸钠的质量分数为53%.
38.【答案】 (1)元素
(2)150
(3)胃
四、实验探究题
39.【答案】 (1)原子核很小, 原子内部有很大空间;α粒子离带正电的原子核较近,受到斥力
(2)质子
40.【答案】 青蒿素分子;15个碳原子、22个氢原子和5个氧原子构成
