初中化学人教版九年级下册第十一单元课题1 生活中常见的盐 同步练习(含解析)
文档属性
| 名称 | 初中化学人教版九年级下册第十一单元课题1 生活中常见的盐 同步练习(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-10 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
初中化学人教版九年级下册第十一单元课题1 生活中常见的盐
一、单选题
1.有关复分解反应的说法,一定正确的是(?? )
A.?反应物均为化合物?????????????????B.?产生沉淀?????????????????C.?元素存在形态改变?????????????????D.?生成盐和水
2.下列鉴别或区分物质的方法错误的是(?? )
A.?用肥皂水鉴别硬水和软水????????????????????????????????????B.?用紫色石蕊溶液区分一氧化碳和二氧化碳
C.?用白醋鉴别贝壳粉和面粉????????????????????????????????????D.?通过观察颜色区分二氧化锰和氧化铜
3.下列四个图像中,能正确反映对应变化关系的是(?? )
A.?向氯化钠饱和溶液中加入硝酸钾
B.?用CuFe2O4-x作催化剂,光分解水制氢气与氧气
C.?向稀硫酸中加入水
D.?向一定质量的硫酸铜溶液中加氢氧化钠溶液21·cn·jy·com
4.某化学兴趣小组对A、B、C、D四种未知溶液的成分进行了检验,检验结果见下表。其中检验结果错误的是(?? ) 2·1·c·n·j·y
组别 溶液中检验出的离子
A K+、Na+、OH-、
B Ba2+、Na+、Cl-、OH-
C Cu2+、Mg2+、 、Cl-
D H+、 、 、
A.?A???????????????????????????????????????????B.?B???????????????????????????????????????????C.?C???????????????????????????????????????????D.?D
5.下列各组离子在溶液中能大量共存的是( ??)
A.?K+、 、 、OH-?????????????????????????????????B.?H+、Ba2+、Cl-、OH-
C.?Fe3+、Na+、 、 ???????????????????????????????D.?Ag+、Na+、Cl-、 21世纪教育网版权所有
6.下列物质的鉴别和除杂方案正确的是( ??)
选项 实验目的 实验方案
A 鉴别 CH4和 H2 点燃后分别在火焰上方罩一个冷而干燥的烧杯
B 鉴别羊毛和涤纶 分别取样,灼烧,闻气味
C 除去 KNO3溶液中的 KCl 加入过量 AgNO3溶液,过滤
D 除去铁粉中的少量铜粉 加入足量稀盐酸,充分反应后过滤、洗涤、干燥
A.?A???????????????????????????????????????????B.?B???????????????????????????????????????????C.?C???????????????????????????????????????????D.?D
7.如图是初中化学中_???è§????è?¨é?????_转化关系,其中A、B、C、D为氧化物,C是使地球产生温室效应的一种气体,丙是一种紫红色金属。(图中部分生成物已略去)下列叙述错误的是( ???)
A.?A的化学式是H2_O
B.?????_生成丙的化学反应类型为置换反应
C.?A与C反应的化学方程式为:CO2+H2O=H2CO3
D.?在A生成甲和乙的化学反应中,所得甲乙两种气体的质量比是2:121教育网
8.已知①中盛有一定量的Na2CO3溶液,根据图示的实验过程,下列说法错误的是(??? )
A.?烧杯②中溶液呈红色
B.?若步骤b中恰好完全反应,则静置后③中上层清液仍为红色
C.?取上述静置后③中上层清液加入过量稀盐酸,无气泡生成
D.?烧杯④中大量存在的离子有:Na+、 Ca2+ . 、H+、Cl2、 21·世纪*教育网
9.能鉴别盐酸、氢氧化钠溶液、蒸馏水三种无色溶液的试剂是(?? )
A.?石蕊溶液???????????????????????????B.?BaCl2溶液???????????????????????????C.?澄清石灰水???????????????????????????D.?生石灰
10.从海水中得到_??????????????????_含有可溶性杂质(主要有Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能使用。粗盐提纯的部分流程如图。有关该流程说法错误的是( ??)
A.?不溶性杂质主要是泥沙
B._??è????¤?????????_棒的作用是搅拌,以便加快过滤速度
C.?蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干
D.?操作①②③依次加入的试剂可以为BaCl2溶液、NaOH溶液、Na2CO3溶液21*cnjy*com
二、填空题
11.某白色固体A可能含有碳酸钠、氧化钙、氯化钠中的一种或几种,进行如下实验:
完成下列问题:
①操作I的名称是_________??????_据上述实验流程分析,A中一定含有的物质是________(填化学式),A中加足量的水后发生反应的化学方程式________,________。21教育名师原创作品
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表。
实验操作 现象 结论
用一支洁净的试管取适量滤液C,________。 ________ A中有氯化钠
12.下列各_??????è?¨??????N_a2CO3溶液和盐酸 ②稀盐酸和KOH溶液 ③NaOH溶液和KCl溶液④硫酸铜溶液和氯化钡溶液,能发生复分解反应的是________(填序号),其中盐和盐反应的化学方程式是________。
13.A?E_????????????è§????_五种物质,它们有如图所示的转化关系。已知A、C是无色液体,B、F是无色气体,其中D、G是黑色固体,E在纯净的B中燃烧火星四射。B转化为G的反应的文字表达式为________,该反应属于________反应(填基本反应类型)。 【来源:21·世纪·教育·网】
三、综合题
14.我国制碱工业先驱侯德榜发明了“侯氏制碱法”。其模拟流程如下:
(1)操作a的名称是________。
(2)NH3中氮元素的化合价为________。
(3)反应②的基本反应类型为________。
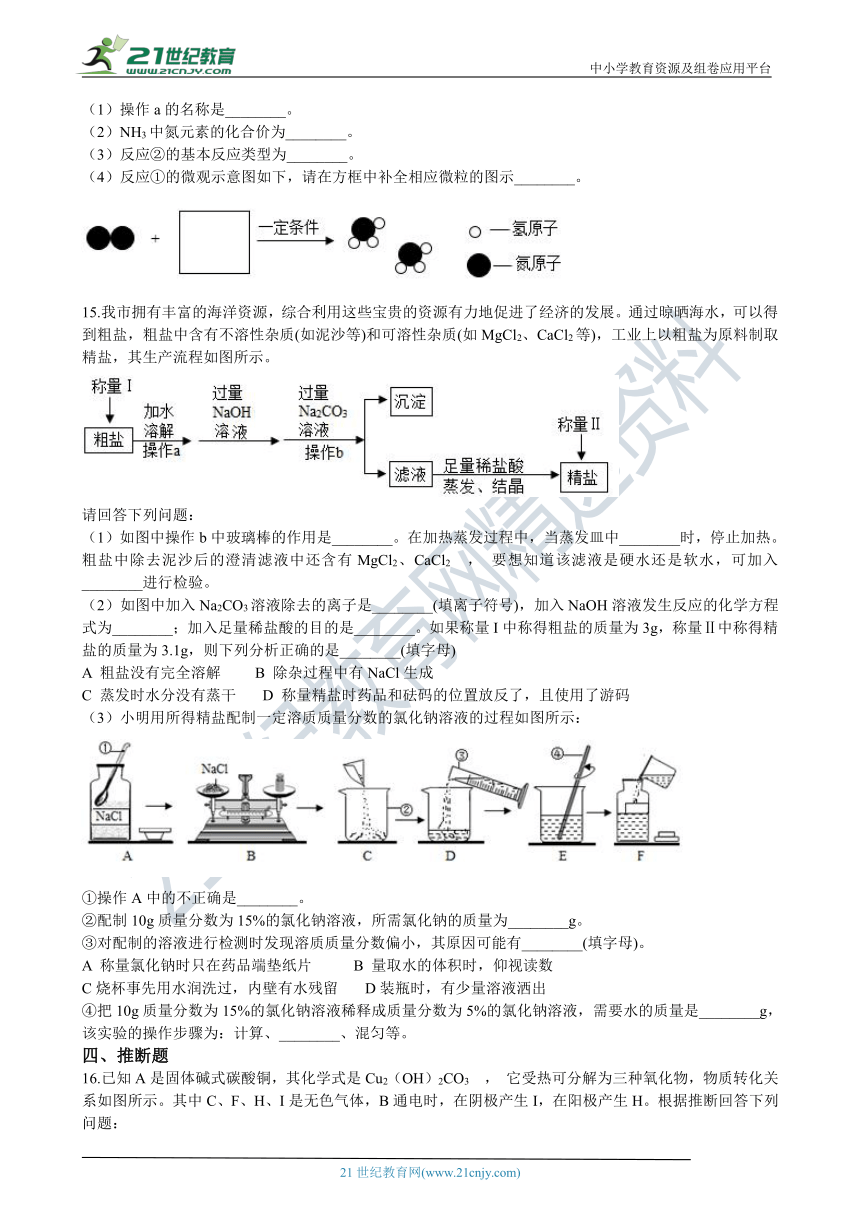
(4)反应①的微观示意图如下,请在方框中补全相应微粒的图示________。
15.我市拥有丰富的海洋_è?????????????????_用这些宝贵的资源有力地促进了经济的发展。通过晾晒海水,可以得到粗盐,粗盐中含有不溶性杂质(如泥沙等)和可溶性杂质(如MgCl2、CaCl2等),工业上以粗盐为原料制取精盐,其生产流程如图所示。 21*cnjy*com
请回答下列问题:
(1)如图中操作b中玻璃棒_????????¨???_________。在加热蒸发过程中,当蒸发皿中________时,停止加热。粗盐中除去泥沙后的澄清滤液中还含有MgCl2、CaCl2 , 要想知道该滤液是硬水还是软水,可加入________进行检验。 【版权所有:21教育】
(2)如图中加入Na2CO3_??????é?¤?????????_子是________(填离子符号),加入NaOH溶液发生反应的化学方程式为________;加入足量稀盐酸的目的是________。如果称量I中称得粗盐的质量为3g,称量Ⅱ中称得精盐的质量为3.1g,则下列分析正确的是________(填字母)
A 粗盐没有完全溶解??????? B 除杂过程中有NaCl生成
C 蒸发时水分没有蒸干????? D 称量精盐时药品和砝码的位置放反了,且使用了游码
(3)小明用所得精盐配制一定溶质质量分数的氯化钠溶液的过程如图所示:
①操作A中的不正确是________。
②配制10g质量分数为15%的氯化钠溶液,所需氯化钠的质量为________g。
③对配制的溶液进行检测时发现溶质质量分数偏小,其原因可能有________(填字母)。
A 称量氯化钠时只在药品端垫纸片????????? B 量取水的体积时,仰视读数
C烧杯事先用水润洗过,内壁有水残留????? D装瓶时,有少量溶液洒出
④把10g质量分数为15%_????°????é????????_稀释成质量分数为5%的氯化钠溶液,需要水的质量是________g,该实验的操作步骤为:计算、________、混匀等。【来源:21cnj*y.co*m】
四、推断题
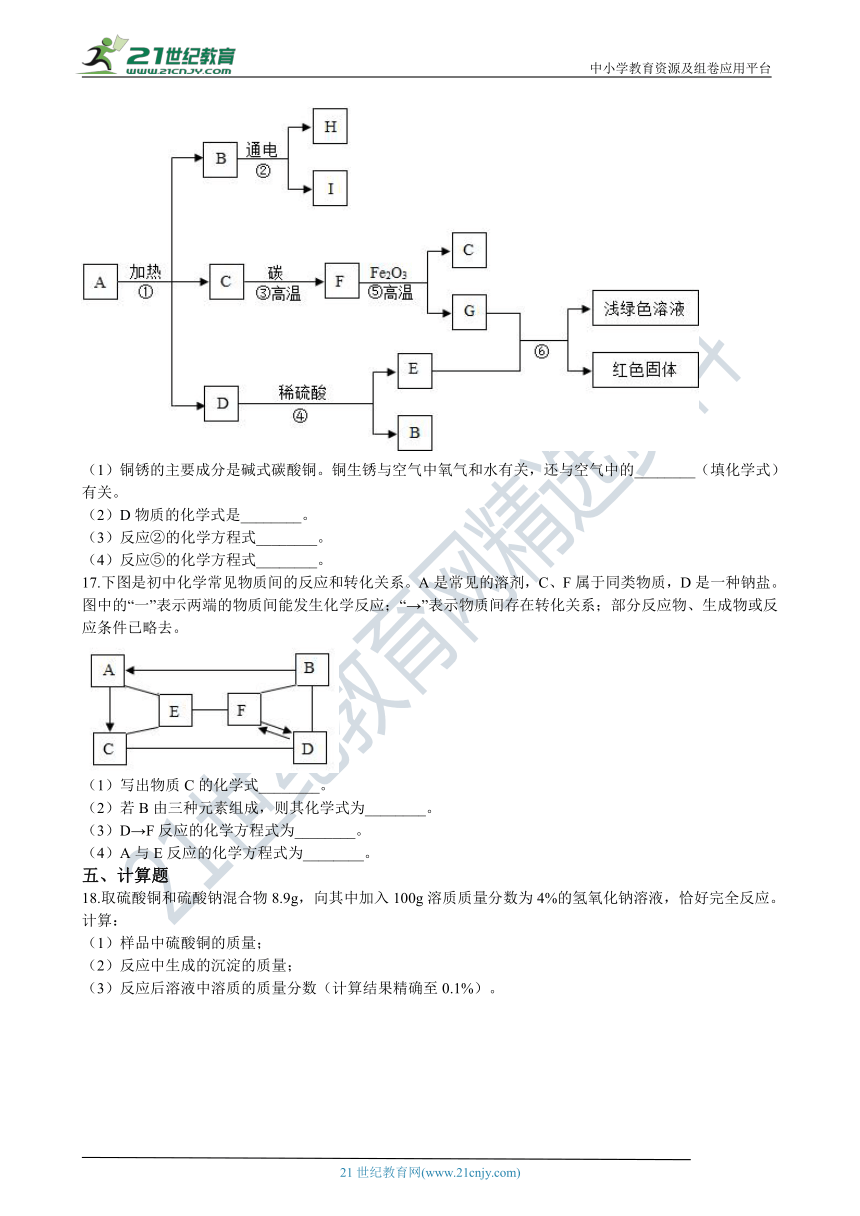
16.已知A是固体碱式碳酸铜,其_????????????Cu_2(OH)2CO3 , 它受热可分解为三种氧化物,物质转化关系如图所示。其中C、F、H、I是无色气体,B通电时,在阴极产生I,在阳极产生H。根据推断回答下列问题:
(1)铜锈的主要成分是碱式碳酸铜。铜生锈与空气中氧气和水有关,还与空气中的________(填化学式)有关。
(2)D物质的化学式是________。
(3)反应②的化学方程式________。
(4)反应⑤的化学方程式________。
17.下图是初中化_??????è§????è?¨é??_的反应和转化关系。A是常见的溶剂,C、F属于同类物质,D是一种钠盐。图中的“一”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。 www-2-1-cnjy-com
(1)写出物质C的化学式________。
(2)若B由三种元素组成,则其化学式为________。
(3)D→F反应的化学方程式为________。
(4)A与E反应的化学方程式为________。
五、计算题
18.取硫酸铜和硫酸钠混合物8.9g,向其中加入100g溶质质量分数为4%的氢氧化钠溶液,恰好完全反应。计算:
(1)样品中硫酸铜的质量;
(2)反应中生成的沉淀的质量;
(3)反应后溶液中溶质的质量分数(计算结果精确至0.1%)。
答案解析部分
一、单选题
1.答案: A
解析:A、两种化合物交换成分生成另外两种化合物的反应属于复分解反应,复分解反应反应物均为化合物,故说法符合题意; 2-1-c-n-j-y
B、有的复分解反应不一定非有沉淀生成,也可能有水或气体生成,故说法不符合题意;
C、复分解反应中元素的存在形态不发生变化,化合物和化合物的反应生成新的化合物,故说法不符合题意;
D、碱和盐的反应属于复分解反应,碱和盐生成新碱和新盐就没有生成盐和水,故说法不符合题意。
故答案为:A。
分析:根据复分解反应是两种化合物交换成分生成另外两种化合物的反应分析。
2.答案: D
解析:A、区分硬水和软水的方法是:加入肥皂水,泡沫多的是软水,泡沫少的是硬水,故方法不符合题意;
B、二氧化碳能与水反应_?????????é?????è??_使紫色的石蕊溶液变红色,一氧化碳不与水反应,不能使紫色的石蕊溶液,可用紫色的石蕊溶液区分一氧化碳和二氧化碳,故方法不符合题意;
C、白醋能与贝壳粉的碳酸钙反应生成二氧化碳气体,有气泡冒出,白醋不与面粉反应,无明显现象,现象不同,可以鉴别,故方法不符合题意;
D、通过观察颜色不可区分二氧化锰和氧化铜,因为两者都是黑色的固体,故方法符合题意。
故答案为:D。
分析:区_??????è?¨?????????_:1.物理方法 ??“看、闻、摸、溶、吸”等方式进行鉴别。
2.化学方法就是通过不同的物质在与同一种物质发生化学反应时,所产生的现象不同,把它们鉴别开的方法,它是鉴别物质的常用方法。
3.答案: D
解析:A. 向氯化钠的_é?±???????????????_入硝酸钾时,硝酸钾能够继续溶解,硝酸钾溶解过程中氯化钠的质量分数减小,该选项对应关系不正确,故错误;
B. 电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2,质量比是8:1,故错误;
C. 稀释稀硫酸溶液,酸性减弱,pH 增大,最终接近7,但是不能等于7,故错误;
D. 向一定质量的硫酸铜溶液中_???????°??°§???é??_溶液,氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,一开始反应就有沉淀产生,硫酸铜溶液完全耗尽后,沉淀不再增加,故正确。
故选D。
分析:A、硝酸钾溶解,会使溶液的质量增大,根据溶质质量分数=分析;
B、在电解水的过程中,生成氧气和氢气的体积比为1:2,而质量之比等于相对分子质量与个数的乘积之比;
C、将酸稀释,pH增大,但是肯定不能等于7;
D、根据氢氧化钠和硫酸铜的反应过程和产物判断。
4.答案: D
解析:A. 钾离子、钠离子、氢氧根离子、硫酸根离子不能形成沉淀、气体和水,可以大量共存,故不符合题意; www.21-cn-jy.com
B. 钡离子、钠离子、氯离子、氢氧根离子,不能形成沉淀、气体和水,可以大量共存,故不符合题意;
C. 铜离子、镁离子、硝酸根离子、氯离子,不能形成沉淀、气体和水,可以大量共存,故不符合题意;
D. 氢离子能与碳酸根离子结合生成二氧化碳和水,不能大量共存,故符合题意。
故答案为:D。
分析:所谓离子共存实质上就是看离子间是否发生反应。若离子在溶液中发生反应,生成气体,或沉淀,或水,就不能共存。
5.答案: C
解析:A、铵根离子能与氢氧根离子结合生成氨气和水,不能大量共存,不符合题意;
B、氢离子能与氢氧根离子结合生成水,不能大量共存,不符合题意;
C、铁离子、钠离子、硝酸根离子、铵根离子,不能形成沉淀、气体和水,可以大量共存,符合题意;
D、银离子能与氯离子结合生成氯化银沉淀,不能大量共存,不符合题意。
故答案为:C。
分析:共存问题即为各物质_??????è???????????_应,能发生反应则不能共存,不能发生反应则能共存。解题的关键是复分解反应条件的掌握,若各物质或离子交换成分后生成物中有气体或沉淀或水生成,则能反应,即不能共存。
6.答案: B
解析:A. 甲烷和氢气燃烧都会产生水, 点燃后分别在火焰上方罩一个冷而干燥的烧杯 不能鉴别,不符合题意;
B. 羊毛主要成分为蛋白质,灼烧有烧焦羽毛气味,可用灼烧的方法鉴别羊毛和涤纶,符合题意;
C. 加过量硝酸银溶液,能除去原杂质,但会引入新杂质硝酸银,不符合题意;
D. 加入足量稀盐酸,铁能与盐酸反应,而杂质铜不反应,不符合题意;
故答案为:B
分析:根据_???è?¨???é?¤??????_则和鉴别方法分析,物质除杂时选择的药品要只与杂质发生反应,不与原物质反应,且在除杂时不能引入新杂质,而鉴别则需利用不同现象区分。
7.答案: D
解析: A、B、C、D_????°§?????????C_是使地球产生温室效应的一种气体,则C为二氧化碳,丙是一种紫红色金属,丙为铜,A通电发生分解生成甲和乙,A为水,甲能与B反应生成丙,则甲为氢气,乙为氧气,B为氧化铜,D为一氧化碳,
A. A的化学式是H2O ,不符合题意;
B. 甲生成丙为氢气与氧化铜的反应,属于置换反应 ,不符合题意;
C. A与C反应的化学方程式为:CO2+H2O=H2CO3 ,不符合题意;
D. 在A生成甲和乙的化学反应中,所得甲乙两种气体的质量比是1:8,符合题意;
故答案为:D
分析:_?????????é????????_给信息及框图中物质间的反应关系推导出各物质,再结合置换反应定义、化学方程式书写及电解水时产生氢气、氧气质量关系分析。
8.答案: D
解析:A.碳酸钠溶液是碱性的,能使酚酞变红色,故A不符合题意
B.氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,因此溶液还是红色,故B不符合题意
C.氢氧化钠和稀盐酸反应生成氯化钠和水,无现象,故C不符合题意
D.根据碳酸根离子和氢离子结合生成二氧化碳和水,故D不符合题意
故答案为:D
分析:A、_?????????é??é?????_液是碱性的分析
B、根据反应的产物进行分析
C、根据溶液中的物质分析
D、根据氢离子和碳酸根离子结合生成二氧化碳分析
9.答案: A
解析:A、石蕊试液滴入三种溶液试样中,石蕊变成红色的是盐酸,变成蓝色的是氢氧化钠溶液,不变色的是蒸馏水,说法符合题意;
B、氯化钡溶液滴入三种溶液试样中,都没有明显现象,无法鉴别,说法不符合题意;
C、澄清石灰水滴入三种溶液试样中,都没有明显现象,无法鉴别,说法不符合题意;
D、生石灰加入三种溶液试样中,生石灰溶解掉的是盐酸,无法鉴别氢氧化钠溶液和蒸馏水,说法不符合题意;
故答案为:A。
分析:根据盐酸呈酸性、氢氧化钠溶液呈碱性、蒸馏水呈中性分析。
10.答案: B
解析:A、由题意,粗盐中含有不溶性杂质(泥沙等),则不溶性杂质主要就是泥沙,故不符合题意;
B、过滤时玻璃棒的作用是引流,故符合题意;
C、蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干,故不符合题意;
D、镁离子用氢氧根离子沉_?·??????????è??é??_的氢氧化钠可溶液以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都可以;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡;操作①②③依次加入的试剂可以为BaCl2溶液、NaOH溶液、Na2CO3溶液,故不符合题意。
故答案为:B。
分析:根据粗盐提纯时_????????????è?¨?°?_杂质全部转化为沉淀,再连同泥沙过滤除去分析,注意转化时所加入试剂均为过量,最后要保证将引入的新杂质也一同除去。
二、填空题
11.答案: 过滤;_Na2CO3_和CaO;CaO+H2O=Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;加入足量的稀硝酸和硝酸银溶液;产生白色沉淀
解析:①过滤_???????°?????????§_固体和液体分离,所以操作Ⅰ是过滤,根据上述实验分析,白色固体加水溶解,会生成白色沉淀,所以混合物中一定含有Na2CO3和 CaO。A中加入足量水,氧化钙与水反应生成氢氧化钙,碳酸钠和氢氧化钙会生成白色的碳酸钙沉淀和氢氧化钠。反应的化学方程式为:CaO+H2O=Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。
②进一步确定固体_A??????è???????¨_的物质,即确定是否含有氯化钠,C中一定含有的溶质是氢氧化钠,还可能含有碳酸钠,故检验氯化钠需要首先加入足量的稀硝酸除去氢氧化钠以及可能存在的碳酸钠,然后加入硝酸银,利用硝酸银可以和氯化钠反应生成氯化银的白色沉淀,检验氯离子。
实验操作 现象 结论
用一支洁净的试管取适量滤液C,加入足量的稀硝酸和硝酸银溶液。 产生白色沉淀 A中有氯化钠
分析:根据过滤操作原理、氧化钙和水反应生成氢氧化钙、碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠、氯离子的验证方法分析。
12.答案: ①②④;
解析:①N_a2CO3???_液和盐酸反应生成氯化钠、二氧化碳和水,该反应符合“两种化合物互相交换成分生成另外两种化合物的反应” 属于复分解反应,碳酸钠属于盐,盐酸属于酸,是盐与酸发生的反应;
②稀盐酸和KOH溶液反应_???????°????é?????_水,该反应符合“两种化合物互相交换成分生成另外两种化合物的反应” 属于复分解反应,稀盐酸是酸,氢氧化钾是碱,是酸与碱的反应;
?③NaOH溶液和KCl溶液不能形成沉淀、气体和水,不能发生复分解反应;
④硫酸铜溶液和氯化钡溶液_???????????????é??_钡和氯化铜,该反应符合“两种化合物互相交换成分生成另外两种化合物的反应” 属于复分解反应,硫酸铜和氯化钡都属于盐。
故能发生复分解反应的是①②④;
盐和盐反应的化学方程式为 。
分析:根据物质的性质,结合复分解反应的特点,进行分析。
13.答案: ;化合
解析:B转化为G的反应是铁在氧气中点燃生成四氧化三铁,故反应的文字表达式为 ,反应符合多变一,则该反应属于化合反应
分析:A、C是无色液_??????A??¨????°§_化锰作用下生成B和C,A是过氧化氢溶液,C是水,B、F是无色气体,B是氧气,D、G是黑色固体,E在纯净的B中燃烧火星四射,E是铁,G是四氧化三铁,D是碳,F是二氧化碳。
三、综合题
14.答案: (1)过滤
(2)-3价
(3)分解反应
(4)
解析:(1)操_???a???è????¤???_分离固体和液体;
(2)化合物中正负化合价代数和为零,氢为+1价,故氮元素是-3价;
(3)反应②是加热NaHCO3生成纯碱、水和二氧化碳,符合“一变多”的特征,属于分解反应;
(4)根据质量守恒定律,化学反应前后原子的种类和数目不变,生成物中含有2个氮原子,6个氢原子,反应物中方框中应有6个氢原子,2个氢原子构成1个氢分子,故方框中应有3个氢分子:
?。
分析:(1)过_??¤???????????????_和液体的方法。
(2)在化合物中,元素的正负化合价代数和为零,进行计算。
(3)根据分解反应的特点,进行分析。
(4)根据质量守恒定律,化学反应前后原子的种类和数目不变,进行推导。21cnjy.com
15.答案: (1)引流;出现较多固体;肥皂水
(2)Ca2+;;除尽剩余的氢氧化钠和碳酸钠;BCD
(3)瓶塞没有倒放;1.5;ABC;20;量取
解析:_???1??????_中操作b能实现固液分离,是过滤操作,过滤操作中玻璃棒的作用是:引流。为了防止蒸发出来的固体受热溅出蒸发皿,在加热蒸发过程中不能蒸干,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使少量水分蒸发。水样中加入肥皂水,搅拌或振荡后,如果泡沫多浮渣少,则是软水,如果泡沫少浮渣多,则是硬水,因此要想知道该滤液是硬水还是软水,可加入肥皂水进行检验。
(2)流程中加入过量氢氧化钠溶液,氯化镁和氢氧化钠溶液反应生成氢氧化镁沉淀,除去镁离子,加入Na2CO3溶液,氯化钙和碳酸钠反应生成碳酸钙沉淀,除去的离子是:Ca2+。氯化镁和加入的NaOH反应生成氢氧化镁和氯化钠,反应的化学方程式为: ;因为在除去氯化镁和氯化钙时加入了过量的氢氧化钠和碳酸钠,所以在滤液中加入足量稀盐酸的目的是:除尽剩余的氢氧化钠和碳酸钠。
如果称量I中称得粗盐的质量为3g,称量Ⅱ中称得精盐的质量为3.1g,则下列分析正确的是:BCD。
A、粗盐没有完全溶解,其后果应该是得到的氯化钠偏少,不正确;
B、因为除杂过_?¨??????????????°?_氧化钠溶液和氯化镁反应有氯化钠生成,加入的碳酸钠溶液和氯化钙反应有氯化钠生成,过量的氢氧化钠、碳酸钠和盐酸反应也有NaCl生成,所以得到的氯化钠质量偏大,正确;
C、如果蒸发时水分没有蒸干,得到的固体质量也偏大,正确;
D、如果称量精盐时药_??????????????????_置放反了,且使用了游码,则砝码质量为3g,游码质量为:0.1g,精盐的实际质量应该是:3g-0.1g=2.9g,正确。
(3)①操作A是氯化钠的取用,图中的不正确是:瓶塞没有倒放。
②配制10g质量分数为15%的氯化钠溶液,所需氯化钠的质量为:10g×15%=1.5g。
③对配制的溶液进行检测时发现溶质质量分数偏小,其原因可能有:ABC。
A、称量氯化钠时只在药品端垫纸片,砝码端没有垫纸片,会导致氯化钠质量偏小,配制的溶液溶质质量分数偏小,正确;
B、量取水的体积时,仰视读数,溶剂水的实际体积偏大,配制的溶液溶质质量分数偏小,正确;
C、烧杯事先用水润洗过,内壁有水残留,会导致溶液中水的质量偏大,配制的溶液溶质质量分数偏小,正确;
D、因为溶液是均一的,所以装瓶时,有少量溶液洒出,不会导致溶液溶质质量分数变化,不正确。
④把10g质量分数为1_5%????°????é??_溶液稀释成质量分数为5%的氯化钠溶液,假设需要水的质量是x , 根据溶液稀释前后溶质的质量不变,则10g ×15%=(10g+x) ×5%,x=20g。溶液稀释实验的操作步骤为:计算、量取、混匀等。
分析:(1)根据过滤操作中玻璃棒的作用,蒸发操作的注意事项,硬水与软水的区别,进行分析。
(2)碳酸钠与氯化钙反应_?????????é??é?????_淀和氯化钠。
氢氧化钠与氯化镁反应生成氢氧化镁沉淀和氯化钠。
盐酸与碳酸钠反应生成氯化钠和二氧化碳、水。
盐酸与氢氧化钠反应生成氯化钠和水。
(3)读取量筒的示数时,如果俯视, 读出的示数比实际值偏大;如果仰视,读出的示数比实际值偏小,因此正确的方法是视线与凹液面的最低处相平。
?四、推断题
16.答案: (1)CO2
(2)CuO
(3)
(4)
解析:已知A_???????????±??????_酸铜,其化学式是Cu2(OH)2CO3 , 可以将A视为Cu(OH)2+CuCO3 , 所以其受热会产生CuO、H2O、和CO2 , B通电可以生成两种无色气体H和I,所以B为H2O,在阴极产生I,在阳极产生H,则I为H2 , H为O2 , C为无色气体,则C为CO2 , 所以D是CuO,CO2与碳高温下生产无色气体F:CO,然后CO高温还原Fe2O3生成CO2和Fe,则G为Fe,D:CuO与稀硫酸反应B:H2O和E:CuSO4 , 综上,A:Cu2(OH)2CO3、B:H2O、C:CO2、D:CuO、E:CuSO4、F: CO、G:Fe、H:O2、I: H2; 【出处:21教育名师】
(1)、铜锈的主要成分是碱式碳酸铜,含有碳酸根,所以铜生锈还与空气中的CO2有关;
(2)、已知A是固体碱式碳_é??é??????????????_式是Cu2(OH)2CO3 , 可以将A视为Cu(OH)2+CuCO3 , 所以其受热会产生CuO、H2O、和CO2 , 而H2O、和CO2都不与稀硫酸反应,所以D为CuO;
(3)、反应②就是水被电解生成氢气和氧气,其化学方程式为: ;
(4)、反应⑤即一氧化碳高温下还原氧化铁生产二氧化碳和铁单质,其化学反应方程式为: 。
分析:根据题中有特_?????????è?¨é?????_推出,结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证,经过验证,推导正确,最后解答各个小题。
17.答案: (1)Ca(OH)2
(2)H2SO4(答案合理即可)
(3)
(4)
解析:(1)由分析可知,物质C为氢氧化钙,其化学式为Ca(OH)2 , 故填:Ca(OH)2;
(2)由分析可知,若B由三种元素组成,则B可以为硫酸,其化学式为H2SO4 , 故填:H2SO4(答案合理即可);
(3)D→F,即碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为: ;
(4)A为水,E为二氧化碳,二氧化碳与水反应生成碳酸,反应的化学方程式为: 。
分析:根据_A_??????è§????_溶剂,推断A 是水;
根据C、F属于同类物质,D是一种钠盐,水与氧化钙反应生成氢氧化钙,氢氧化钠与碳酸钠可以相互转化,所以推断D 是碳酸钠,F 是氢氧化钠,C 是氢氧化钙;
根据E可以与水、氢氧化钙反应,二氧化碳与氢氧化钠反应生成碳酸钠和水,所以推断E 是二氧化碳;
根据B可以与碳酸钠、氢氧化钠反应,B是一种酸。
五、计算题
18.答案: (1)解:氢氧化钠溶液中溶质质量为100g×4%=4g,设样品中硫酸铜的质量为x
,x=8g
答:样品中硫酸铜的质量为8g;
(2)解:设反应中生成的沉淀的质量为y。
?y=4.9g。
答:反应中生成的沉淀的质量为4.9g;
(3)解:设:生成硫酸钠质量为z
,z=7.1g。
反应后溶液中溶质的质量分数为:
答:反应后溶液中溶质的质量分数为7.7%。
解析:先设未知数,_???????????????é??_铜与氢氧化钠反应的化学方程式;再找准有关物质,已知量是氢氧化钠的质量,未知量是硫酸铜、生成氢氧化铜、硫酸钠的质量;列比例式计算。?
_21?????????è?????(www.21cnjy.com)_
初中化学人教版九年级下册第十一单元课题1 生活中常见的盐
一、单选题
1.有关复分解反应的说法,一定正确的是(?? )
A.?反应物均为化合物?????????????????B.?产生沉淀?????????????????C.?元素存在形态改变?????????????????D.?生成盐和水
2.下列鉴别或区分物质的方法错误的是(?? )
A.?用肥皂水鉴别硬水和软水????????????????????????????????????B.?用紫色石蕊溶液区分一氧化碳和二氧化碳
C.?用白醋鉴别贝壳粉和面粉????????????????????????????????????D.?通过观察颜色区分二氧化锰和氧化铜
3.下列四个图像中,能正确反映对应变化关系的是(?? )
A.?向氯化钠饱和溶液中加入硝酸钾
B.?用CuFe2O4-x作催化剂,光分解水制氢气与氧气
C.?向稀硫酸中加入水
D.?向一定质量的硫酸铜溶液中加氢氧化钠溶液21·cn·jy·com
4.某化学兴趣小组对A、B、C、D四种未知溶液的成分进行了检验,检验结果见下表。其中检验结果错误的是(?? ) 2·1·c·n·j·y
组别 溶液中检验出的离子
A K+、Na+、OH-、
B Ba2+、Na+、Cl-、OH-
C Cu2+、Mg2+、 、Cl-
D H+、 、 、
A.?A???????????????????????????????????????????B.?B???????????????????????????????????????????C.?C???????????????????????????????????????????D.?D
5.下列各组离子在溶液中能大量共存的是( ??)
A.?K+、 、 、OH-?????????????????????????????????B.?H+、Ba2+、Cl-、OH-
C.?Fe3+、Na+、 、 ???????????????????????????????D.?Ag+、Na+、Cl-、 21世纪教育网版权所有
6.下列物质的鉴别和除杂方案正确的是( ??)
选项 实验目的 实验方案
A 鉴别 CH4和 H2 点燃后分别在火焰上方罩一个冷而干燥的烧杯
B 鉴别羊毛和涤纶 分别取样,灼烧,闻气味
C 除去 KNO3溶液中的 KCl 加入过量 AgNO3溶液,过滤
D 除去铁粉中的少量铜粉 加入足量稀盐酸,充分反应后过滤、洗涤、干燥
A.?A???????????????????????????????????????????B.?B???????????????????????????????????????????C.?C???????????????????????????????????????????D.?D
7.如图是初中化学中_???è§????è?¨é?????_转化关系,其中A、B、C、D为氧化物,C是使地球产生温室效应的一种气体,丙是一种紫红色金属。(图中部分生成物已略去)下列叙述错误的是( ???)
A.?A的化学式是H2_O
B.?????_生成丙的化学反应类型为置换反应
C.?A与C反应的化学方程式为:CO2+H2O=H2CO3
D.?在A生成甲和乙的化学反应中,所得甲乙两种气体的质量比是2:121教育网
8.已知①中盛有一定量的Na2CO3溶液,根据图示的实验过程,下列说法错误的是(??? )
A.?烧杯②中溶液呈红色
B.?若步骤b中恰好完全反应,则静置后③中上层清液仍为红色
C.?取上述静置后③中上层清液加入过量稀盐酸,无气泡生成
D.?烧杯④中大量存在的离子有:Na+、 Ca2+ . 、H+、Cl2、 21·世纪*教育网
9.能鉴别盐酸、氢氧化钠溶液、蒸馏水三种无色溶液的试剂是(?? )
A.?石蕊溶液???????????????????????????B.?BaCl2溶液???????????????????????????C.?澄清石灰水???????????????????????????D.?生石灰
10.从海水中得到_??????????????????_含有可溶性杂质(主要有Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能使用。粗盐提纯的部分流程如图。有关该流程说法错误的是( ??)
A.?不溶性杂质主要是泥沙
B._??è????¤?????????_棒的作用是搅拌,以便加快过滤速度
C.?蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干
D.?操作①②③依次加入的试剂可以为BaCl2溶液、NaOH溶液、Na2CO3溶液21*cnjy*com
二、填空题
11.某白色固体A可能含有碳酸钠、氧化钙、氯化钠中的一种或几种,进行如下实验:
完成下列问题:
①操作I的名称是_________??????_据上述实验流程分析,A中一定含有的物质是________(填化学式),A中加足量的水后发生反应的化学方程式________,________。21教育名师原创作品
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成下表。
实验操作 现象 结论
用一支洁净的试管取适量滤液C,________。 ________ A中有氯化钠
12.下列各_??????è?¨??????N_a2CO3溶液和盐酸 ②稀盐酸和KOH溶液 ③NaOH溶液和KCl溶液④硫酸铜溶液和氯化钡溶液,能发生复分解反应的是________(填序号),其中盐和盐反应的化学方程式是________。
13.A?E_????????????è§????_五种物质,它们有如图所示的转化关系。已知A、C是无色液体,B、F是无色气体,其中D、G是黑色固体,E在纯净的B中燃烧火星四射。B转化为G的反应的文字表达式为________,该反应属于________反应(填基本反应类型)。 【来源:21·世纪·教育·网】
三、综合题
14.我国制碱工业先驱侯德榜发明了“侯氏制碱法”。其模拟流程如下:
(1)操作a的名称是________。
(2)NH3中氮元素的化合价为________。
(3)反应②的基本反应类型为________。
(4)反应①的微观示意图如下,请在方框中补全相应微粒的图示________。
15.我市拥有丰富的海洋_è?????????????????_用这些宝贵的资源有力地促进了经济的发展。通过晾晒海水,可以得到粗盐,粗盐中含有不溶性杂质(如泥沙等)和可溶性杂质(如MgCl2、CaCl2等),工业上以粗盐为原料制取精盐,其生产流程如图所示。 21*cnjy*com
请回答下列问题:
(1)如图中操作b中玻璃棒_????????¨???_________。在加热蒸发过程中,当蒸发皿中________时,停止加热。粗盐中除去泥沙后的澄清滤液中还含有MgCl2、CaCl2 , 要想知道该滤液是硬水还是软水,可加入________进行检验。 【版权所有:21教育】
(2)如图中加入Na2CO3_??????é?¤?????????_子是________(填离子符号),加入NaOH溶液发生反应的化学方程式为________;加入足量稀盐酸的目的是________。如果称量I中称得粗盐的质量为3g,称量Ⅱ中称得精盐的质量为3.1g,则下列分析正确的是________(填字母)
A 粗盐没有完全溶解??????? B 除杂过程中有NaCl生成
C 蒸发时水分没有蒸干????? D 称量精盐时药品和砝码的位置放反了,且使用了游码
(3)小明用所得精盐配制一定溶质质量分数的氯化钠溶液的过程如图所示:
①操作A中的不正确是________。
②配制10g质量分数为15%的氯化钠溶液,所需氯化钠的质量为________g。
③对配制的溶液进行检测时发现溶质质量分数偏小,其原因可能有________(填字母)。
A 称量氯化钠时只在药品端垫纸片????????? B 量取水的体积时,仰视读数
C烧杯事先用水润洗过,内壁有水残留????? D装瓶时,有少量溶液洒出
④把10g质量分数为15%_????°????é????????_稀释成质量分数为5%的氯化钠溶液,需要水的质量是________g,该实验的操作步骤为:计算、________、混匀等。【来源:21cnj*y.co*m】
四、推断题
16.已知A是固体碱式碳酸铜,其_????????????Cu_2(OH)2CO3 , 它受热可分解为三种氧化物,物质转化关系如图所示。其中C、F、H、I是无色气体,B通电时,在阴极产生I,在阳极产生H。根据推断回答下列问题:
(1)铜锈的主要成分是碱式碳酸铜。铜生锈与空气中氧气和水有关,还与空气中的________(填化学式)有关。
(2)D物质的化学式是________。
(3)反应②的化学方程式________。
(4)反应⑤的化学方程式________。
17.下图是初中化_??????è§????è?¨é??_的反应和转化关系。A是常见的溶剂,C、F属于同类物质,D是一种钠盐。图中的“一”表示两端的物质间能发生化学反应;“→”表示物质间存在转化关系;部分反应物、生成物或反应条件已略去。 www-2-1-cnjy-com
(1)写出物质C的化学式________。
(2)若B由三种元素组成,则其化学式为________。
(3)D→F反应的化学方程式为________。
(4)A与E反应的化学方程式为________。
五、计算题
18.取硫酸铜和硫酸钠混合物8.9g,向其中加入100g溶质质量分数为4%的氢氧化钠溶液,恰好完全反应。计算:
(1)样品中硫酸铜的质量;
(2)反应中生成的沉淀的质量;
(3)反应后溶液中溶质的质量分数(计算结果精确至0.1%)。
答案解析部分
一、单选题
1.答案: A
解析:A、两种化合物交换成分生成另外两种化合物的反应属于复分解反应,复分解反应反应物均为化合物,故说法符合题意; 2-1-c-n-j-y
B、有的复分解反应不一定非有沉淀生成,也可能有水或气体生成,故说法不符合题意;
C、复分解反应中元素的存在形态不发生变化,化合物和化合物的反应生成新的化合物,故说法不符合题意;
D、碱和盐的反应属于复分解反应,碱和盐生成新碱和新盐就没有生成盐和水,故说法不符合题意。
故答案为:A。
分析:根据复分解反应是两种化合物交换成分生成另外两种化合物的反应分析。
2.答案: D
解析:A、区分硬水和软水的方法是:加入肥皂水,泡沫多的是软水,泡沫少的是硬水,故方法不符合题意;
B、二氧化碳能与水反应_?????????é?????è??_使紫色的石蕊溶液变红色,一氧化碳不与水反应,不能使紫色的石蕊溶液,可用紫色的石蕊溶液区分一氧化碳和二氧化碳,故方法不符合题意;
C、白醋能与贝壳粉的碳酸钙反应生成二氧化碳气体,有气泡冒出,白醋不与面粉反应,无明显现象,现象不同,可以鉴别,故方法不符合题意;
D、通过观察颜色不可区分二氧化锰和氧化铜,因为两者都是黑色的固体,故方法符合题意。
故答案为:D。
分析:区_??????è?¨?????????_:1.物理方法 ??“看、闻、摸、溶、吸”等方式进行鉴别。
2.化学方法就是通过不同的物质在与同一种物质发生化学反应时,所产生的现象不同,把它们鉴别开的方法,它是鉴别物质的常用方法。
3.答案: D
解析:A. 向氯化钠的_é?±???????????????_入硝酸钾时,硝酸钾能够继续溶解,硝酸钾溶解过程中氯化钠的质量分数减小,该选项对应关系不正确,故错误;
B. 电解水时,正极产生的是氧气,负极产生的是氢气,氧气和氢气的体积比约为1:2,质量比是8:1,故错误;
C. 稀释稀硫酸溶液,酸性减弱,pH 增大,最终接近7,但是不能等于7,故错误;
D. 向一定质量的硫酸铜溶液中_???????°??°§???é??_溶液,氢氧化钠与硫酸铜反应生成氢氧化铜沉淀和硫酸钠,一开始反应就有沉淀产生,硫酸铜溶液完全耗尽后,沉淀不再增加,故正确。
故选D。
分析:A、硝酸钾溶解,会使溶液的质量增大,根据溶质质量分数=分析;
B、在电解水的过程中,生成氧气和氢气的体积比为1:2,而质量之比等于相对分子质量与个数的乘积之比;
C、将酸稀释,pH增大,但是肯定不能等于7;
D、根据氢氧化钠和硫酸铜的反应过程和产物判断。
4.答案: D
解析:A. 钾离子、钠离子、氢氧根离子、硫酸根离子不能形成沉淀、气体和水,可以大量共存,故不符合题意; www.21-cn-jy.com
B. 钡离子、钠离子、氯离子、氢氧根离子,不能形成沉淀、气体和水,可以大量共存,故不符合题意;
C. 铜离子、镁离子、硝酸根离子、氯离子,不能形成沉淀、气体和水,可以大量共存,故不符合题意;
D. 氢离子能与碳酸根离子结合生成二氧化碳和水,不能大量共存,故符合题意。
故答案为:D。
分析:所谓离子共存实质上就是看离子间是否发生反应。若离子在溶液中发生反应,生成气体,或沉淀,或水,就不能共存。
5.答案: C
解析:A、铵根离子能与氢氧根离子结合生成氨气和水,不能大量共存,不符合题意;
B、氢离子能与氢氧根离子结合生成水,不能大量共存,不符合题意;
C、铁离子、钠离子、硝酸根离子、铵根离子,不能形成沉淀、气体和水,可以大量共存,符合题意;
D、银离子能与氯离子结合生成氯化银沉淀,不能大量共存,不符合题意。
故答案为:C。
分析:共存问题即为各物质_??????è???????????_应,能发生反应则不能共存,不能发生反应则能共存。解题的关键是复分解反应条件的掌握,若各物质或离子交换成分后生成物中有气体或沉淀或水生成,则能反应,即不能共存。
6.答案: B
解析:A. 甲烷和氢气燃烧都会产生水, 点燃后分别在火焰上方罩一个冷而干燥的烧杯 不能鉴别,不符合题意;
B. 羊毛主要成分为蛋白质,灼烧有烧焦羽毛气味,可用灼烧的方法鉴别羊毛和涤纶,符合题意;
C. 加过量硝酸银溶液,能除去原杂质,但会引入新杂质硝酸银,不符合题意;
D. 加入足量稀盐酸,铁能与盐酸反应,而杂质铜不反应,不符合题意;
故答案为:B
分析:根据_???è?¨???é?¤??????_则和鉴别方法分析,物质除杂时选择的药品要只与杂质发生反应,不与原物质反应,且在除杂时不能引入新杂质,而鉴别则需利用不同现象区分。
7.答案: D
解析: A、B、C、D_????°§?????????C_是使地球产生温室效应的一种气体,则C为二氧化碳,丙是一种紫红色金属,丙为铜,A通电发生分解生成甲和乙,A为水,甲能与B反应生成丙,则甲为氢气,乙为氧气,B为氧化铜,D为一氧化碳,
A. A的化学式是H2O ,不符合题意;
B. 甲生成丙为氢气与氧化铜的反应,属于置换反应 ,不符合题意;
C. A与C反应的化学方程式为:CO2+H2O=H2CO3 ,不符合题意;
D. 在A生成甲和乙的化学反应中,所得甲乙两种气体的质量比是1:8,符合题意;
故答案为:D
分析:_?????????é????????_给信息及框图中物质间的反应关系推导出各物质,再结合置换反应定义、化学方程式书写及电解水时产生氢气、氧气质量关系分析。
8.答案: D
解析:A.碳酸钠溶液是碱性的,能使酚酞变红色,故A不符合题意
B.氢氧化钙和碳酸钠反应生成碳酸钙沉淀和氢氧化钠,因此溶液还是红色,故B不符合题意
C.氢氧化钠和稀盐酸反应生成氯化钠和水,无现象,故C不符合题意
D.根据碳酸根离子和氢离子结合生成二氧化碳和水,故D不符合题意
故答案为:D
分析:A、_?????????é??é?????_液是碱性的分析
B、根据反应的产物进行分析
C、根据溶液中的物质分析
D、根据氢离子和碳酸根离子结合生成二氧化碳分析
9.答案: A
解析:A、石蕊试液滴入三种溶液试样中,石蕊变成红色的是盐酸,变成蓝色的是氢氧化钠溶液,不变色的是蒸馏水,说法符合题意;
B、氯化钡溶液滴入三种溶液试样中,都没有明显现象,无法鉴别,说法不符合题意;
C、澄清石灰水滴入三种溶液试样中,都没有明显现象,无法鉴别,说法不符合题意;
D、生石灰加入三种溶液试样中,生石灰溶解掉的是盐酸,无法鉴别氢氧化钠溶液和蒸馏水,说法不符合题意;
故答案为:A。
分析:根据盐酸呈酸性、氢氧化钠溶液呈碱性、蒸馏水呈中性分析。
10.答案: B
解析:A、由题意,粗盐中含有不溶性杂质(泥沙等),则不溶性杂质主要就是泥沙,故不符合题意;
B、过滤时玻璃棒的作用是引流,故符合题意;
C、蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干,故不符合题意;
D、镁离子用氢氧根离子沉_?·??????????è??é??_的氢氧化钠可溶液以将镁离子沉淀;硫酸根离子用钡离子沉淀,加入过量的氯化钡溶液可以将硫酸根离子沉淀;至于先除镁离子,还是先除硫酸根离子都可以;钙离子用碳酸根离子沉淀,除钙离子加入过量的碳酸钠溶液转化为沉淀,但是加入碳酸钠溶液要放在加入的氯化钡溶液之后,这样碳酸钠会除去反应剩余的氯化钡;操作①②③依次加入的试剂可以为BaCl2溶液、NaOH溶液、Na2CO3溶液,故不符合题意。
故答案为:B。
分析:根据粗盐提纯时_????????????è?¨?°?_杂质全部转化为沉淀,再连同泥沙过滤除去分析,注意转化时所加入试剂均为过量,最后要保证将引入的新杂质也一同除去。
二、填空题
11.答案: 过滤;_Na2CO3_和CaO;CaO+H2O=Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;加入足量的稀硝酸和硝酸银溶液;产生白色沉淀
解析:①过滤_???????°?????????§_固体和液体分离,所以操作Ⅰ是过滤,根据上述实验分析,白色固体加水溶解,会生成白色沉淀,所以混合物中一定含有Na2CO3和 CaO。A中加入足量水,氧化钙与水反应生成氢氧化钙,碳酸钠和氢氧化钙会生成白色的碳酸钙沉淀和氢氧化钠。反应的化学方程式为:CaO+H2O=Ca(OH)2;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH。
②进一步确定固体_A??????è???????¨_的物质,即确定是否含有氯化钠,C中一定含有的溶质是氢氧化钠,还可能含有碳酸钠,故检验氯化钠需要首先加入足量的稀硝酸除去氢氧化钠以及可能存在的碳酸钠,然后加入硝酸银,利用硝酸银可以和氯化钠反应生成氯化银的白色沉淀,检验氯离子。
实验操作 现象 结论
用一支洁净的试管取适量滤液C,加入足量的稀硝酸和硝酸银溶液。 产生白色沉淀 A中有氯化钠
分析:根据过滤操作原理、氧化钙和水反应生成氢氧化钙、碳酸钠和氢氧化钙反应生成碳酸钙和氢氧化钠、氯离子的验证方法分析。
12.答案: ①②④;
解析:①N_a2CO3???_液和盐酸反应生成氯化钠、二氧化碳和水,该反应符合“两种化合物互相交换成分生成另外两种化合物的反应” 属于复分解反应,碳酸钠属于盐,盐酸属于酸,是盐与酸发生的反应;
②稀盐酸和KOH溶液反应_???????°????é?????_水,该反应符合“两种化合物互相交换成分生成另外两种化合物的反应” 属于复分解反应,稀盐酸是酸,氢氧化钾是碱,是酸与碱的反应;
?③NaOH溶液和KCl溶液不能形成沉淀、气体和水,不能发生复分解反应;
④硫酸铜溶液和氯化钡溶液_???????????????é??_钡和氯化铜,该反应符合“两种化合物互相交换成分生成另外两种化合物的反应” 属于复分解反应,硫酸铜和氯化钡都属于盐。
故能发生复分解反应的是①②④;
盐和盐反应的化学方程式为 。
分析:根据物质的性质,结合复分解反应的特点,进行分析。
13.答案: ;化合
解析:B转化为G的反应是铁在氧气中点燃生成四氧化三铁,故反应的文字表达式为 ,反应符合多变一,则该反应属于化合反应
分析:A、C是无色液_??????A??¨????°§_化锰作用下生成B和C,A是过氧化氢溶液,C是水,B、F是无色气体,B是氧气,D、G是黑色固体,E在纯净的B中燃烧火星四射,E是铁,G是四氧化三铁,D是碳,F是二氧化碳。
三、综合题
14.答案: (1)过滤
(2)-3价
(3)分解反应
(4)
解析:(1)操_???a???è????¤???_分离固体和液体;
(2)化合物中正负化合价代数和为零,氢为+1价,故氮元素是-3价;
(3)反应②是加热NaHCO3生成纯碱、水和二氧化碳,符合“一变多”的特征,属于分解反应;
(4)根据质量守恒定律,化学反应前后原子的种类和数目不变,生成物中含有2个氮原子,6个氢原子,反应物中方框中应有6个氢原子,2个氢原子构成1个氢分子,故方框中应有3个氢分子:
?。
分析:(1)过_??¤???????????????_和液体的方法。
(2)在化合物中,元素的正负化合价代数和为零,进行计算。
(3)根据分解反应的特点,进行分析。
(4)根据质量守恒定律,化学反应前后原子的种类和数目不变,进行推导。21cnjy.com
15.答案: (1)引流;出现较多固体;肥皂水
(2)Ca2+;;除尽剩余的氢氧化钠和碳酸钠;BCD
(3)瓶塞没有倒放;1.5;ABC;20;量取
解析:_???1??????_中操作b能实现固液分离,是过滤操作,过滤操作中玻璃棒的作用是:引流。为了防止蒸发出来的固体受热溅出蒸发皿,在加热蒸发过程中不能蒸干,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使少量水分蒸发。水样中加入肥皂水,搅拌或振荡后,如果泡沫多浮渣少,则是软水,如果泡沫少浮渣多,则是硬水,因此要想知道该滤液是硬水还是软水,可加入肥皂水进行检验。
(2)流程中加入过量氢氧化钠溶液,氯化镁和氢氧化钠溶液反应生成氢氧化镁沉淀,除去镁离子,加入Na2CO3溶液,氯化钙和碳酸钠反应生成碳酸钙沉淀,除去的离子是:Ca2+。氯化镁和加入的NaOH反应生成氢氧化镁和氯化钠,反应的化学方程式为: ;因为在除去氯化镁和氯化钙时加入了过量的氢氧化钠和碳酸钠,所以在滤液中加入足量稀盐酸的目的是:除尽剩余的氢氧化钠和碳酸钠。
如果称量I中称得粗盐的质量为3g,称量Ⅱ中称得精盐的质量为3.1g,则下列分析正确的是:BCD。
A、粗盐没有完全溶解,其后果应该是得到的氯化钠偏少,不正确;
B、因为除杂过_?¨??????????????°?_氧化钠溶液和氯化镁反应有氯化钠生成,加入的碳酸钠溶液和氯化钙反应有氯化钠生成,过量的氢氧化钠、碳酸钠和盐酸反应也有NaCl生成,所以得到的氯化钠质量偏大,正确;
C、如果蒸发时水分没有蒸干,得到的固体质量也偏大,正确;
D、如果称量精盐时药_??????????????????_置放反了,且使用了游码,则砝码质量为3g,游码质量为:0.1g,精盐的实际质量应该是:3g-0.1g=2.9g,正确。
(3)①操作A是氯化钠的取用,图中的不正确是:瓶塞没有倒放。
②配制10g质量分数为15%的氯化钠溶液,所需氯化钠的质量为:10g×15%=1.5g。
③对配制的溶液进行检测时发现溶质质量分数偏小,其原因可能有:ABC。
A、称量氯化钠时只在药品端垫纸片,砝码端没有垫纸片,会导致氯化钠质量偏小,配制的溶液溶质质量分数偏小,正确;
B、量取水的体积时,仰视读数,溶剂水的实际体积偏大,配制的溶液溶质质量分数偏小,正确;
C、烧杯事先用水润洗过,内壁有水残留,会导致溶液中水的质量偏大,配制的溶液溶质质量分数偏小,正确;
D、因为溶液是均一的,所以装瓶时,有少量溶液洒出,不会导致溶液溶质质量分数变化,不正确。
④把10g质量分数为1_5%????°????é??_溶液稀释成质量分数为5%的氯化钠溶液,假设需要水的质量是x , 根据溶液稀释前后溶质的质量不变,则10g ×15%=(10g+x) ×5%,x=20g。溶液稀释实验的操作步骤为:计算、量取、混匀等。
分析:(1)根据过滤操作中玻璃棒的作用,蒸发操作的注意事项,硬水与软水的区别,进行分析。
(2)碳酸钠与氯化钙反应_?????????é??é?????_淀和氯化钠。
氢氧化钠与氯化镁反应生成氢氧化镁沉淀和氯化钠。
盐酸与碳酸钠反应生成氯化钠和二氧化碳、水。
盐酸与氢氧化钠反应生成氯化钠和水。
(3)读取量筒的示数时,如果俯视, 读出的示数比实际值偏大;如果仰视,读出的示数比实际值偏小,因此正确的方法是视线与凹液面的最低处相平。
?四、推断题
16.答案: (1)CO2
(2)CuO
(3)
(4)
解析:已知A_???????????±??????_酸铜,其化学式是Cu2(OH)2CO3 , 可以将A视为Cu(OH)2+CuCO3 , 所以其受热会产生CuO、H2O、和CO2 , B通电可以生成两种无色气体H和I,所以B为H2O,在阴极产生I,在阳极产生H,则I为H2 , H为O2 , C为无色气体,则C为CO2 , 所以D是CuO,CO2与碳高温下生产无色气体F:CO,然后CO高温还原Fe2O3生成CO2和Fe,则G为Fe,D:CuO与稀硫酸反应B:H2O和E:CuSO4 , 综上,A:Cu2(OH)2CO3、B:H2O、C:CO2、D:CuO、E:CuSO4、F: CO、G:Fe、H:O2、I: H2; 【出处:21教育名师】
(1)、铜锈的主要成分是碱式碳酸铜,含有碳酸根,所以铜生锈还与空气中的CO2有关;
(2)、已知A是固体碱式碳_é??é??????????????_式是Cu2(OH)2CO3 , 可以将A视为Cu(OH)2+CuCO3 , 所以其受热会产生CuO、H2O、和CO2 , 而H2O、和CO2都不与稀硫酸反应,所以D为CuO;
(3)、反应②就是水被电解生成氢气和氧气,其化学方程式为: ;
(4)、反应⑤即一氧化碳高温下还原氧化铁生产二氧化碳和铁单质,其化学反应方程式为: 。
分析:根据题中有特_?????????è?¨é?????_推出,结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证,经过验证,推导正确,最后解答各个小题。
17.答案: (1)Ca(OH)2
(2)H2SO4(答案合理即可)
(3)
(4)
解析:(1)由分析可知,物质C为氢氧化钙,其化学式为Ca(OH)2 , 故填:Ca(OH)2;
(2)由分析可知,若B由三种元素组成,则B可以为硫酸,其化学式为H2SO4 , 故填:H2SO4(答案合理即可);
(3)D→F,即碳酸钠与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,反应的化学方程式为: ;
(4)A为水,E为二氧化碳,二氧化碳与水反应生成碳酸,反应的化学方程式为: 。
分析:根据_A_??????è§????_溶剂,推断A 是水;
根据C、F属于同类物质,D是一种钠盐,水与氧化钙反应生成氢氧化钙,氢氧化钠与碳酸钠可以相互转化,所以推断D 是碳酸钠,F 是氢氧化钠,C 是氢氧化钙;
根据E可以与水、氢氧化钙反应,二氧化碳与氢氧化钠反应生成碳酸钠和水,所以推断E 是二氧化碳;
根据B可以与碳酸钠、氢氧化钠反应,B是一种酸。
五、计算题
18.答案: (1)解:氢氧化钠溶液中溶质质量为100g×4%=4g,设样品中硫酸铜的质量为x
,x=8g
答:样品中硫酸铜的质量为8g;
(2)解:设反应中生成的沉淀的质量为y。
?y=4.9g。
答:反应中生成的沉淀的质量为4.9g;
(3)解:设:生成硫酸钠质量为z
,z=7.1g。
反应后溶液中溶质的质量分数为:
答:反应后溶液中溶质的质量分数为7.7%。
解析:先设未知数,_???????????????é??_铜与氢氧化钠反应的化学方程式;再找准有关物质,已知量是氢氧化钠的质量,未知量是硫酸铜、生成氢氧化铜、硫酸钠的质量;列比例式计算。?
_21?????????è?????(www.21cnjy.com)_
同课章节目录
