云南省镇雄县第四高中2020-2021学年高一下学期6月第二次月考化学试题 PDF版含答案
文档属性
| 名称 | 云南省镇雄县第四高中2020-2021学年高一下学期6月第二次月考化学试题 PDF版含答案 |

|
|
| 格式 | |||
| 文件大小 | 747.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-15 00:00:00 | ||
图片预览



文档简介
秘 密 ★ 启 用 前 4. 实 验 室 中 洗 涤 试 管 内 壁 附 着 的 杂 质 ,试 剂 正 确 的 是
A.
镇 雄 四 中 高 一 年 级 春 季 学 期 第 二 次 月 考 卷 用 稀 盐 酸 清 洗 久 置 石 灰 水 的 试 管
化 学 B. 用 稀 盐 酸 清 洗 附 着 的 二 氧 化 锰
本 试 卷 分 第 Ⅰ 卷 (选 择 题 )和 第 Ⅱ 卷 (非 选 择 题 )两 部 分 。第 Ⅰ 卷 第 1页 至 第 4页 ,第 Ⅱ 卷 第 5页 至 第 8 C. 用 酒 精 清 洗 附 着 的 硫 单 质
页 。考 试 结 束 后 ,请 将 本 试 卷 和 答 题 卡 一 并 交 回 。满 分 100分 ,考 试 用 时 90分 钟 。
D. 用 稀 硝 酸 清 洗 附 着 的 铁 粉
以 下 数 据 可 供 解 题 时 参 考 。
可 能 用 到 的 相 对 原 子 质 量 :H—1 C—12 N—14 O—16 Na—23 Al—27 S—32 Fe—56 Cu—64 5. 下 列 物 质 既 能 与 金 属 钠 作 用 放 出 气 体 ,又 能 与 纯 碱 作 用 放 出 气 体 的 是
第 Ⅰ 卷 (选 择 题 ,共 48分 ) A. C2H5OH B. H2O
注 意 事 项 :
1? 答 题 前 ,考 生 务 必 用 黑 色 碳 素 笔 将 自 己 的 姓 名 、准 考 证 号 、考 场 号 、座 位 号 在 答 题 卡 上 填 写 清 楚 。
2? C. CH COOH D. CH CHO
每 小 题 选 出 答 案 后 ,用 2B铅 笔 把 答 题 卡 上 对 应 题 目 的 答 案 标 号 涂 黑 。如 需 改 动 ,用 橡 皮 擦 干 净 后 ,再 3 3
选 涂 其 他 答 案 标 号 。在 试 题 卷 上 作 答 无 效 。 6. 下 列 说 法 正 确 的 是
一 、选 择 题 (本 大 题 共 16题 ,每 小 题 3分 ,共 48分 。在 每 小 题 给 出 的 四 个 选 项 中 ,只 有 一 项 是 符 合 题 目 要 求 A. 等 体 积 的 甲 烷 与 氯 气 混 合 ,在 光 照 下 反 应 只 生 成 一 氯 甲 烷 和 氯 化 氢
的 )
B. 相 同 质 量 的 烷 烃 完 全 燃 烧 时 ,甲 烷 的 耗 氧 量 最 少
1. 能 够 用 来 检 验 某 糖 尿 病 病 人 的 尿 液 中 是 否 含 葡 萄 糖 的 试 剂 是
A. C.
氨 水 B. 金 属 钠 通 常 情 况 下 ,烷 烃 能 够 使 高 锰 酸 钾 溶 液 褪 色
C. 新 制 Cu(OH)2 悬 浊 液 D. 硝 酸 银 溶 液 D. 烷 烃 的 熔 、沸 点 一 般 随 着 分 子 中 碳 原 子 数 的 增 加 而 升 高
2. 下 列 有 机 物 和 乙 醇 具 有 相 同 官 能 团 的 是 7. 要 将 在 酯 化 反 应 的 实 验 中 制 得 的 乙 酸 乙 酯 中 混 有 的 少 量 CH3COOH洗 涤 除 去 ,应 选 用 的 试 剂 是
A. 苯 乙 烯 ( ) B. 丙 三 醇 ( ) A. 乙 醇 B. 饱 和 Na2CO3 溶 液
C. 乙 醛 (CH3CHO) D. 乙 烷 (CH3CH3) C. 水 D. NaOH溶 液
3. 下 列 对 烃 的 分 类 不 正 确 的 是 8. 下 列 关 于 糖 类 、蛋 白 质 的 说 法 正 确 的 是
A. CH4、CH2 ?? CH2、CH2 ?? CHCH?? CH2 均 属 于 饱 和 烃 A. 葡 萄 糖 能 与 银 氨 溶 液 反 应 生 成 光 亮 的 “银 镜 ”
B. CH3CH2CH3、CH3CH?? CH2、CH3CH?? CHCH2CH?? CH2 均 属 于 链 状 烃
B. 糖 类 物 质 在 一 定 条 件 下 都 能 发 生 水 解 反 应
C. CH3CH3、 、C18H38均 属 于 饱 和 烃 C. 氨 基 酸 能 发 生 水 解 反 应 ,最 终 转 化 为 蛋 白 质
D. 均 属 于 芳 香 烃 D. 蛋 白 质 遇 到 硫 酸 铵 发 生 盐 析 ,并 失 去 生 理 活 性
化 学 ZX4·第 1页 (共 8页 ) 化 学 ZX4·第 2页 (共 8页 )
书书书
9. 下 列 说 法 不 正 确 的 是 14. 下 列 关 于 影 响 化 学 反 应 速 率 的 条 件 的 说 法 正 确 的 是
A. 淀 粉 、蛋 白 质 和 油 脂 都 能 发 生 水 解 反 应 A. 增 大 压 强 一 定 能 加 快 化 学 反 应 速 率
B. 猪 油 、奶 油 、花 生 油 、大 豆 油 都 属 于 油 脂 B. 使 用 催 化 剂 不 会 改 变 反 应 速 率
C. 利 用 植 物 秸 秆 等 物 质 中 的 纤 维 素 可 以 生 产 酒 精 ,用 作 燃 料 C. 反 应 物 浓 度 是 决 定 化 学 反 应 速 率 的 主 要 因 素
D. 向 鸡 蛋 清 的 水 溶 液 中 加 入 硝 酸 银 溶 液 可 能 产 生 沉 淀 ,加 水 后 沉 淀 又 会 溶 解
D. 升 高 温 度 ,一 般 能 加 快 化 学 反 应 速 率
10. 下 列 关 于 有 机 化 合 物 的 说 法 正 确 的 是
A. 塑 料 、天 然 橡 胶 都 是 天 然 高 分 子 化 合 物 15. 某 有 机 物 的 结 构 简 式 为 。下 列 关 于 该 有 机 物 的 叙 述 不 正 确 的 是
B. 乙 烯 、聚 乙 烯 和 苯 分 子 中 均 含 有 碳 碳 双 键 A. 能 与 NaHCO3 发 生 反 应 并 放 出 二 氧 化 碳
C. 棉 花 、羊 毛 、涤 纶 的 成 分 均 属 于 天 然 纤 维
B. 能 在 催 化 剂 作 用 下 与 HCl发 生 加 成 反 应
D. 乙 酸 和 乙 醇 可 用 Na2CO3 溶 液 加 以 区 别
C. 不 能 使 酸 性 KMnO4 溶 液 和 溴 水 褪 色
11. 下 列 物 质 转 化 常 通 过 加 成 反 应 实 现 的 是
A. CH4→ CH2Cl2 B. CH3CH2OH→ CH3COOCH2CH3 D. 在 浓 硫 酸 作 催 化 剂 条 件 下 能 和 乙 醇 发 生 酯 化 反 应 生 成 酯
C. CH3CH2OH→ CH3CHO D. CH2 ?? CH2→ CH3CH2Br 16. 下 列 对 图 2所 示 实 验 的 描 述 及 相 应 结 论 正 确 的 是
12. 可 以 用 来 鉴 别 甲 烷 和 乙 烯 的 试 剂 是
A. 水 B. 溴 水
C. 紫 色 石 蕊 溶 液 D. NaOH溶 液
13. 碳 原 子 成 键 的 多 样 性 、同 分 异 构 现 象 等 是 有 机 物 种 类 繁 多 的 原 因 。丁 烷 和 2-甲 基 丙 烷 的 结 构 式 如 图 1,下
图 2
列 关 于 上 述 两 种 物 质 的 说 法 不 正 确 的 是 A. 图 甲 :用 水 稀 释 浓 硫 酸 ,触 摸 烧 杯 外 壁 发 热 ,则 该 过 程 为 放 热 反 应
A. 分 子 式 相 同 B. 图 乙 :反 应 开 始 后 ,针 筒 活 塞 向 右 移 动 ,仅 凭 此 现 象 不 能 判 断 该 反 应 为 放 热 反 应
B. 互 为 同 分 异 构 体 C. 图 丙 :a电 极 质 量 减 小 ,b电 极 上 有 气 泡 生 成 ,则 金 属 活 泼 性 a>b
C. C H 图 1
等 物 质 的 量 的 两 物 质 中 碳 氢 键 (—)数 目 相 同
D. 图 丁 :等 质 量 两 份 锌 粉 分 别 加 入 过 量 稀 硫 酸 中 ,由 V(H2)-t关 系 图 推 测 a可 能 还 加 了 少 量 铜 粉
D. 物 理 性 质 、化 学 性 质 完 全 相 同
化 学 ZX4·第 3页 (共 8页 ) 化 学 ZX4·第 4页 (共 8页 )
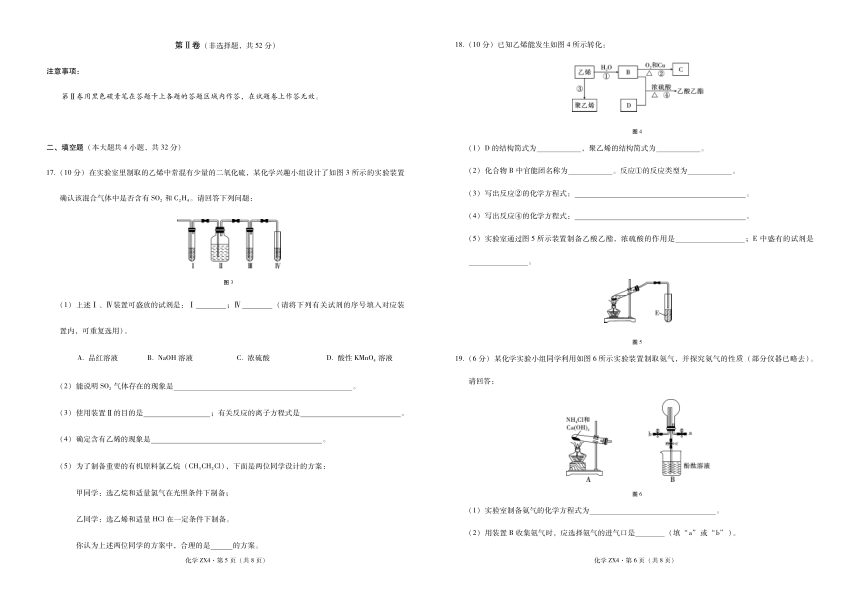
第 Ⅱ 卷 (非 选 择 题 ,共 52分 ) 18. (10分 )已 知 乙 烯 能 发 生 如 图 4所 示 转 化 :
注 意 事 项 :
第 Ⅱ 卷 用 黑 色 碳 素 笔 在 答 题 卡 上 各 题 的 答 题 区 域 内 作 答 ,在 试 题 卷 上 作 答 无 效 。
图 4
二 、填 空 题 (本 大 题 共 4小 题 ,共 32分 ) (1)D的 结 构 简 式 为 ,聚 乙 烯 的 结 构 简 式 为 。
17. (10 2 B
分 )在 实 验 室 里 制 取 的 乙 烯 中 常 混 有 少 量 的 二 氧 化 硫 ,某 化 学 兴 趣 小 组 设 计 了 如 图 3 所 示 的 实 验 装 置 ()化 合 物 中 官 能 团 名 称 为 。反 应 ① 的 反 应 类 型 为 。
(3)写 出 反 应 ② 的 化 学 方 程 式 : 。
确 认 该 混 合 气 体 中 是 否 含 有 SO2 和 C2H4。请 回 答 下 列 问 题 :
(4)写 出 反 应 ④ 的 化 学 方 程 式 : 。
(5)实 验 室 通 过 图 5所 示 装 置 制 备 乙 酸 乙 酯 ,浓 硫 酸 的 作 用 是 ;E 中 盛 有 的 试 剂 是
。
图 3
(1)上 述 Ⅰ 、Ⅳ 装 置 可 盛 放 的 试 剂 是 :Ⅰ ;Ⅳ (请 将 下 列 有 关 试 剂 的 序 号 填 入 对 应 装
置 内 ,可 重 复 选 用 )。
图 5
A. 品 红 溶 液 B. NaOH溶 液 C. 浓 硫 酸 D. 酸 性 KMnO4 溶 液 19. (6分 )某 化 学 实 验 小 组 同 学 利 用 如 图 6所 示 实 验 装 置 制 取 氨 气 ,并 探 究 氨 气 的 性 质 (部 分 仪 器 已 略 去 )。
请 回 答 :
(2)能 说 明 SO2 气 体 存 在 的 现 象 是 。
(3)使 用 装 置 Ⅱ 的 目 的 是 ;有 关 反 应 的 离 子 方 程 式 是 。
(4)确 定 含 有 乙 烯 的 现 象 是 。
(5)为 了 制 备 重 要 的 有 机 原 料 氯 乙 烷 (CH3CH2Cl),下 面 是 两 位 同 学 设 计 的 方 案 :
甲 同 学 :选 乙 烷 和 适 量 氯 气 在 光 照 条 件 下 制 备 ; 图 6
(1)实 验 室 制 备 氨 气 的 化 学 方 程 式 为 。
乙 同 学 :选 乙 烯 和 适 量 HCl在 一 定 条 件 下 制 备 。
(2)用 装 置 B收 集 氨 气 时 ,应 选 择 氨 气 的 进 气 口 是 (填 “a”或 “b”)。
你 认 为 上 述 两 位 同 学 的 方 案 中 ,合 理 的 是 的 方 案 。
化 学 ZX4·第 5页 (共 8页 ) 化 学 ZX4·第 6页 (共 8页 )
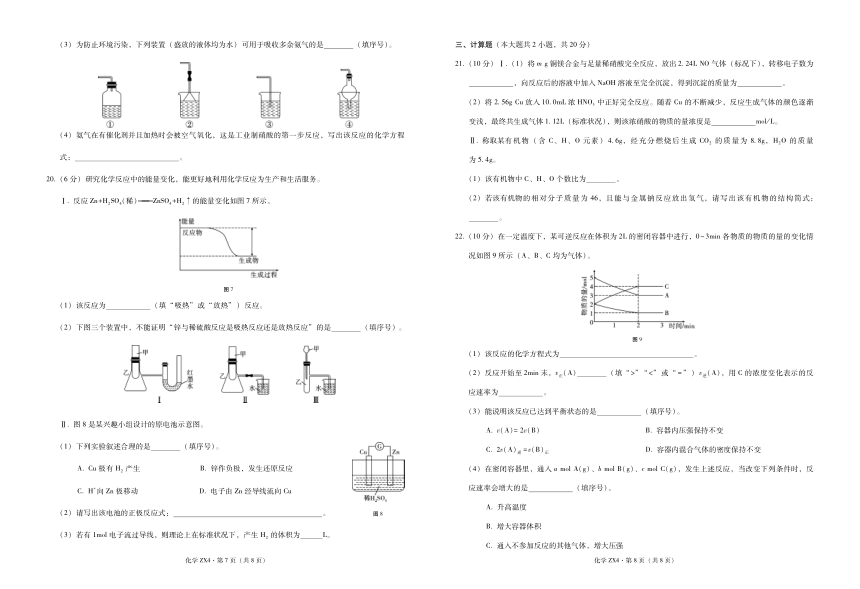
(3)为 防 止 环 境 污 染 ,下 列 装 置 (盛 放 的 液 体 均 为 水 )可 用 于 吸 收 多 余 氨 气 的 是 (填 序 号 )。 三 、计 算 题 (本 大 题 共 2小 题 ,共 20分 )
21. (10分 )Ⅰ . (1)将 m g铜 镁 合 金 与 足 量 稀 硝 酸 完 全 反 应 ,放 出 2?24L NO 气 体 (标 况 下 ),转 移 电 子 数 为
,向 反 应 后 的 溶 液 中 加 入 NaOH溶 液 至 完 全 沉 淀 ,得 到 沉 淀 的 质 量 为 。
(2)将 2?56g Cu放 入 10?0mL浓 HNO3 中 正 好 完 全 反 应 。随 着 Cu 的 不 断 减 少 ,反 应 生 成 气 体 的 颜 色 逐 渐
变 浅 ,最 终 共 生 成 气 体 1?12L (标 准 状 况 ),则 该 浓 硝 酸 的 物 质 的 量 浓 度 是 mol/L。
(4)氨 气 在 有 催 化 剂 并 且 加 热 时 会 被 空 气 氧 化 ,这 是 工 业 制 硝 酸 的 第 一 步 反 应 ,写 出 该 反 应 的 化 学 方 程 Ⅱ . 称 取 某 有 机 物 (含 C、H、O 元 素 )4?6g,经 充 分 燃 烧 后 生 成 CO2 的 质 量 为 8?8g,H2O 的 质 量
式 : 。 为 5?4g。
20. (6分 )研 究 化 学 反 应 中 的 能 量 变 化 ,能 更 好 地 利 用 化 学 反 应 为 生 产 和 生 活 服 务 。 (1)该 有 机 物 中 C、H、O个 数 比 为 。
Ⅰ . 2 46
反 应 Zn+H2SO4(稀 )? ? ? ZnSO4+H2↑ 的 能 量 变 化 如 图 7所 示 。 ()若 该 有 机 物 的 相 对 分 子 质 量 为 ,且 能 与 金 属 钠 反 应 放 出 氢 气 ,请 写 出 该 有 机 物 的 结 构 简 式 :
。
22. (10分 )在 一 定 温 度 下 ,某 可 逆 反 应 在 体 积 为 2L的 密 闭 容 器 中 进 行 ,0~3min 各 物 质 的 物 质 的 量 的 变 化 情
况 如 图 9所 示 (A、B、C均 为 气 体 )。
图 7
(1)该 反 应 为 (填 “吸 热 ”或 “放 热 ”)反 应 。
(2)下 图 三 个 装 置 中 ,不 能 证 明 “锌 与 稀 硫 酸 反 应 是 吸 热 反 应 还 是 放 热 反 应 ”的 是 (填 序 号 )。
图 9
(1)该 反 应 的 化 学 方 程 式 为 。
(2)反 应 开 始 至 2min末 ,v正 (A) (填 “>”“<”或 “=”)v逆 (A),用 C 的 浓 度 变 化 表 示 的 反
应 速 率 为 。
(3)能 说 明 该 反 应 已 达 到 平 衡 状 态 的 是 (填 序 号 )。
Ⅱ . 图 8是 某 兴 趣 小 组 设 计 的 原 电 池 示 意 图 。 A. v(A)= 2v(B) B. 容 器 内 压 强 保 持 不 变
(1)下 列 实 验 叙 述 合 理 的 是 (填 序 号 )。 C. 2v(A)逆 =v(B)正 D. 容 器 内 混 合 气 体 的 密 度 保 持 不 变
A. Cu极 有 H2 产 生 B. 锌 作 负 极 ,发 生 还 原 反 应 (4)在 密 闭 容 器 里 ,通 入 a mol A(g)、b mol B(g)、c mol C(g),发 生 上 述 反 应 ,当 改 变 下 列 条 件 时 ,反
+
C. H 向 Zn极 移 动 D. 电 子 由 Zn
经 导 线 流 向 Cu 应 速 率 会 增 大 的 是 (填 序 号 )。
A. 升 高 温 度
(2)请 写 出 该 电 池 的 正 极 反 应 式 : 。 图 8
B. 增 大 容 器 体 积
(3)若 有 1mol电 子 流 过 导 线 ,则 理 论 上 在 标 准 状 况 下 ,产 生 H2 的 体 积 为 L。 C. 通 入 不 参 加 反 应 的 其 他 气 体 ,增 大 压 强
化 学 ZX4·第 7页 (共 8页 ) 化 学 ZX4·第 8页 (共 8页 )
镇雄四中高一年级春季学期第二次月考卷
化学参考答案
第 Ⅰ 卷 (选择题,共 48 分)
一、选择题 (本大题共 16 小题,每小题 3 分,共 48
题号 9 10 11 12 13 14 15 16
答案 D D D B D D C B
【解析】
3. CH2 CH2、 CH CHCH CH2分子中含有碳碳双键,属于不饱和烃, A 错误。链状烃指
的是分子中无环状结构的烃, B正确。 CH3CH3、 、 C
化学 ZX4参考答案·第 1页(共 6页)
7. A项,乙酸乙酯的制备为可逆反应,用乙醇不能除去乙酸乙酯中的少量乙酸,并且还引入
了新的杂质。 B 项,乙酸的酸性比碳酸强,能与碳酸钠反应生成二氧化碳而被吸收,乙酸
乙酯不溶于饱和碳酸钠溶液,然后分液可得到纯净的乙酸乙酯。 C 项,虽然乙酸能溶于水
而除去,但乙酸乙酯也有部分溶于水,依据除杂原则,不能选用水洗。 D项,乙酸乙酯在
氢氧化钠溶液中能够完全水解,反应方程式为 CH3COOCH2CH3+NaOH CH3COONa
+CH3CH2OH。故选 B。
8.葡萄糖分子中含有醛基,能与银氨溶液发生银镜反应生成光亮的“银镜”, A正确。糖类
中的单糖不能水解,二糖、多糖均可水解, B 错误。氨基酸脱水缩合作用形成蛋白质, C
错误。硫酸铵是轻金属盐,蛋白质遇到硫酸铵发生盐析,但不会失去生理活性, D错误。
9.淀粉属于多糖,在酶催化下能水解生成葡萄糖;蛋白质可以水解生成氨基酸;油脂水解生
成高级脂肪酸和甘油, A正确。呈液态的油脂都称为油,如植物油,呈固态的称为脂肪如
动物油, B 正确。纤维素在一定条件下可以发生水解,水解产物葡萄糖和果糖在一定条件
下会转化为酒精, C 正确。鸡蛋清的主要成分是蛋白质,加入硝酸盐是重金属盐,重金属
盐会使蛋白质变性,变性是不可逆过程, D不正确。
11.甲烷与氯气在光照条件下发生取代反应转化。乙醇通过与 CH3COOH 发生取代反应转化
为 CH3COOCH2CH3。乙醇通过氧化反应转化为乙醛。乙烯含有双键,可通过与 HBr发生
加成反应转化为 CH3CH2Br。答案为 D。
12.甲烷和乙烯都不能与水反应,则不能用水鉴别甲烷和乙烯, A错误。甲烷不能与溴水反应,
而乙烯能与溴水发生加成反应,使溴水褪色,则能用溴水鉴别甲烷和乙烯, B正确。甲烷
和乙烯都不能与紫色石蕊溶液反应,则不能用紫色石蕊溶液鉴别甲烷和乙烯, C错误。甲
烷和乙烯都不能与氢氧化钠溶液反应,则不能用氢氧化钠溶液鉴别甲烷和乙烯, D错误。
13.分子式相同,均是 C4H10, A正确。二者分子式相同,结构不同,互为同分异构体, B正
确。每个分子中碳氢键( C— H)数目相同,均含有 10个, C正确。二者互为同分异构体,
物理性质不同,均是烷烃,化学性质相似, D错误。
14.压强对反应速率的影响只适用于有气体参与的反应,即改变压强,反应速率不一定改变,
A错误。催化剂可以改变反应速率, B错误。物质本身的性质是决定化学反应速率的主要
因素, C错误。升高温度,活化分子数增多,化学反应速率加快, D正确。
化学 ZX4参考答案·第 2页(共 6页)
15.该有机物分子中含有 、 —COOH 两种官能团,其中— COOH 能和 NaHCO3反应
放出 CO2, A正确。分子中的 可在催化剂作用下与 HCl发生加成反应, B正确。
分子中的 能使酸性 KMnO4溶液和溴水褪色, C错误。分子中含— COOH,在浓
硫酸作催化剂条件下能和乙醇发生酯化反应生成酯和水, D正确。
16.浓硫酸的稀释过程不是化学反应,属于放热过程,不属于放热反应, A错误。碳酸钙和稀
盐酸反应生成氯化钙、二氧化碳和水,生成的二氧化碳气体能使针筒活塞向右移动,则
针筒活塞向右移动不一定是反应放出热量导致, B正确。若 a为金属铝, b为金属镁,铝、
镁在氢氧化钠溶液中构成原电池,能与氢氧化钠溶液反应的铝作原电池的负极,镁作正
极,正极上有气泡生成,但金属活泼性铝小于镁, C错误。由于稀硫酸过量,两份锌等量,
若 a中加了少量铜粉,锌铜在稀硫酸中构成原电池,会加快反应速率,同时生成氢气的量
会减少, D错误。
第 Ⅱ 卷 (非选择题,共 52 分)
二、填空题 (本大题共 4小题,共 32分)
17. (除特殊标注外,每空 1分,共 10分)
( 1) A D
( 2) Ⅰ 中品红溶液褪色( 2分)
? 2
( 3)除去二氧化硫 SO2+2OH = ?
SO3 ( 2分)
( 4) Ⅲ 中品红溶液不褪色, Ⅳ 中酸性 KMnO4溶液褪色( 2分)
( 5)乙同学
【解析】 实验室用电石与饱和食盐水制备乙烯,乙烯具有碳碳双键,能与溴水发生加成反
应,与酸性高锰酸钾发生氧化反应。副产物二氧化硫具有还原性和漂白性,能使品红溶
液褪色,能与酸性高锰酸钾反应使其褪色。
( 1)根据产物性质,首先应检验二氧化硫的存在并彻底吸收后检验乙烯的存在。 Ⅰ 装置
可盛放品红溶液, Ⅱ 装置可盛放氢氧化钠, Ⅲ 装置可盛放品红溶液,检验是否除尽二氧
化硫, Ⅳ 装置可盛放酸性高锰酸钾,最终检验乙烯的存在。
( 2)二氧化硫具有漂白性,能说明 SO2气体存在的现象是 Ⅰ 中品红溶液褪色。
( 3)装置 Ⅱ 中为氢氧化钠,目的是除去二氧化硫。有关反应的离子方程式是
? 2
SO2+2OH = ?
SO3 +H2O。
化学 ZX4参考答案·第 3页(共 6页)
( 4)确定含有乙烯要保证二氧化硫全部除尽,即现象是 Ⅲ 中品红溶液不褪色, Ⅳ 中酸性
KMnO4溶液褪色。
( 5)制备氯乙烷( CH3CH2Cl) ,甲同学:选乙烷和适量氯气在光照条件下制备,产物多样,
难以控制反应产物为一氯代物。乙同学:选乙烯和适量 HCl 在一定条件下制备,发生加
成反应,产物唯一,产率高。上述两位同学的方案中,合理的是乙同学的方案。
18. (除特殊标注外,每空 1分,共 10分)
( 1) CH3COOH
( 2)羟基 加成反应
( 3) 2CH3CH2OH+O2 2CH3CHO+2H2O( 2分)
( 4) CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O( 2分)
( 5)催化剂、吸水剂 饱和 Na2CO3溶液
【解析】 乙烯和水反应生成乙醇,乙醇在催化剂作用下与氧气反应生成乙醛,乙烯发生加
聚反应生成聚乙烯,乙醇和乙酸在浓硫酸加热作用下反应生成乙酸乙酯。
( 1) D为乙酸,其结构简式为 CH3COOH,聚乙烯的结构简式为 。
( 2)化合物 B 是乙醇,其官能团名称为羟基。反应①是乙烯和水在催化剂作用下发生加
成反应。
( 3)反应②的化学方程式为 2CH3CH2OH+O2 2CH3CHO+2H2O。
( 4)反应④是乙醇和乙酸在浓硫酸催化剂作用下发生酯化反应生成乙酸乙酯,其化学方
程式为 CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O。
( 5)浓硫酸的作用是催化剂、吸水剂。 E中盛有的试剂是饱和 Na2CO3溶液。
19. (除特殊标注外,每空 1分,共 6分)
( 1) 2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O( 2分)
( 2) b
( 3)②④
催化剂
( 4) 4NH3+5O2===== ( 分)
△ 4NO+6H2O 2
【解析】 ( 1)实验室制备氨气的化学方程式为 2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O。
( 2)用装置 B 收集氨气时,由于氨气的密度比空气小,可用向下排空气法收集,导气管
要伸入烧瓶底部,所以应选择氨气的进气口是 b。
( 3)①不能使 NH3进入瓶中,②④能防止倒吸,③会发生倒吸,故答案为②④。
化学 ZX4参考答案·第 4页(共 6页)
20. (除特殊标注外,每空 1分,共 6分)
Ⅰ. ( 1)放热
( 2) Ⅲ
Ⅱ. ( 1) AD
+ ?
( 2) 2H +2e =H2↑( 2分)
( 3) 11.2
三、计算题 (本大题共 2小题,共 20分)
21. (每空 2分,共 10分)
Ⅰ. ( 1) 0.3NA (m+5.1)g
( 2) 13
Ⅱ. ( 1) 2∶ 6∶ 1
( 2) CH3CH2OH
V 2.24L
【解析】 Ⅰ. ( 1) n(NO)= = =0.1mol,则转移的电子数为 (5?2)×0.1mol=0.3mol,
Vm 22.4L/mol
即 0.3NA; Mg、 Cu混合物与硝酸反应生成 Mg(NO3)2、 Cu(NO3)2,部分硝酸被还原为 NO
气体,反应后的溶液加入 NaOH溶液使金属恰好沉淀完全,沉淀为 Cu(OH)2、 Mg(OH)2,
? ?
结合得失电子守恒可知 n(OH )=0.3mol,则 m(OH )=17g/mol×0.3mol=5.1g,故得到沉淀的
质量为 5.1g+m g=(m+5.1)g。
( 2)铜和 10mL浓硝酸反应,随着浓度的减少,硝酸的还原产物的价态越低,铜和浓硝酸
反应生成 NO2,而与稀硝酸反应时则生成 NO,故生成的气体有 NO2 和 NO,则
1.12L
n(NO2)+n(NO)= =0.05mol ,即被还原的硝酸的物质的量为 0.05mol,
22.4L/mol
2.56g
n(Cu)= =0.04mol,则生成 n[Cu(NO3)2]=0.04mol,可知表现酸性的硝酸的物质的
64g/mol
量为 0.04mol×2=0.08mol,则参加反应的硝酸的物质的量为 0.05mol+0.08mol=0.13mol,则
0.13mol
物质的量浓度为 =13mol/L。
0.01L
8.8g
Ⅱ.( 1 )根据反应前后元素守恒,可知 n(C)=n(CO2)= =0.2mol ,
44g/mol
5.4g 4.6g0.2mol12g/mol0.6mol1g/mol? ???
n(H)=2n(H2O)=2× =0.6mol, n(O)=
18g/mol 16g/mol
=0.1mol, n(C)∶ n(H)∶ n(O)=0.2mol∶ 0.6mol∶ 0.1mol=2∶ 6∶ 1。
化学 ZX4参考答案·第 5页(共 6页)
( 2)根据( 1)计算可知该有机物中 C、 H、 O三种元素的原子个数比是 2∶ 6∶ 1,则其最
简式是 C2H6O,最简式的式量是 46,而该有机物的相对分子质量为 46,因此其最简式就
是其分子式,符合该分子式的物质可能是 CH3CH2OH、 CH3OCH3,该有机物能与金属钠
反应放出氢气,说明分子中含有— OH,则该有机物的结构简式是 CH3CH2OH。
22. (每空 2分,共 10分)
( 1) 2A(g)+B(g) 2C(g)
( 2) = 0.5mol/(L· min)
( 3) B
( 4) A
【解析】 ( 1)由图像可知, A、 B为反应物, C为生成物,当反应进行到 2min时, A、 B、
C 三种物质的量变化量之比为 (5?3)mol∶ (2?1)mol∶ (4?2)mol=2∶ 1∶ 2。由各物质的物质
的量的变化量之比等于化学计量数之比可知,反应的化学方程式为
2A(g)+B(g) 2C(g)。
( 2)反应开始至 2min 末,反应达平衡状态,正逆反应速率相等。 C 的浓度变化
(42)mol? 1mol/L
?c= =1mol/L。用 C的浓度变化表示的反应速率为 =0.5mol/(L· min)。
2L 2min
( 3)反应的化学方程式为 2A(g)+B(g) 2C(g)。 A. v(A)=2v(B)不能说明正反应和逆反
应的关系,故不能判断反应是否达到平衡状态。 B.该反应为前后气体体积变小的反应,
随着反应的进行,气体的物质的量不断减小,压强也减小,当容器内压强保持不变时,
说明正逆反应速率相等,反应达到平衡状态。 C. v(A)逆 =2v(B)正 说明正逆反应速率相等,
则 2v(A)逆 =v(B)正 说明正反应速率大于逆反应速率,反应未达平衡状态。 D.该反应中各物
质均为气态,反应前后气体的总质量保持不变,容器的体积也保持不变,因此容器内混
合气体的密度始终保持不变,不能判断反应是否达到平衡状态。故选 B。
( 4) A.升高温度,活化分子数增多,化学反应速率加快。 B.增大容器体积,各物质的
浓度减小,化学反应速率减小。 C.容器的容积不变,通入不参加反应的其他气体,虽然
增大了压强,但是各物质的浓度不变,反应速率不变。故选 A。
化学 ZX4参考答案·第 6页(共 6页)
A.
镇 雄 四 中 高 一 年 级 春 季 学 期 第 二 次 月 考 卷 用 稀 盐 酸 清 洗 久 置 石 灰 水 的 试 管
化 学 B. 用 稀 盐 酸 清 洗 附 着 的 二 氧 化 锰
本 试 卷 分 第 Ⅰ 卷 (选 择 题 )和 第 Ⅱ 卷 (非 选 择 题 )两 部 分 。第 Ⅰ 卷 第 1页 至 第 4页 ,第 Ⅱ 卷 第 5页 至 第 8 C. 用 酒 精 清 洗 附 着 的 硫 单 质
页 。考 试 结 束 后 ,请 将 本 试 卷 和 答 题 卡 一 并 交 回 。满 分 100分 ,考 试 用 时 90分 钟 。
D. 用 稀 硝 酸 清 洗 附 着 的 铁 粉
以 下 数 据 可 供 解 题 时 参 考 。
可 能 用 到 的 相 对 原 子 质 量 :H—1 C—12 N—14 O—16 Na—23 Al—27 S—32 Fe—56 Cu—64 5. 下 列 物 质 既 能 与 金 属 钠 作 用 放 出 气 体 ,又 能 与 纯 碱 作 用 放 出 气 体 的 是
第 Ⅰ 卷 (选 择 题 ,共 48分 ) A. C2H5OH B. H2O
注 意 事 项 :
1? 答 题 前 ,考 生 务 必 用 黑 色 碳 素 笔 将 自 己 的 姓 名 、准 考 证 号 、考 场 号 、座 位 号 在 答 题 卡 上 填 写 清 楚 。
2? C. CH COOH D. CH CHO
每 小 题 选 出 答 案 后 ,用 2B铅 笔 把 答 题 卡 上 对 应 题 目 的 答 案 标 号 涂 黑 。如 需 改 动 ,用 橡 皮 擦 干 净 后 ,再 3 3
选 涂 其 他 答 案 标 号 。在 试 题 卷 上 作 答 无 效 。 6. 下 列 说 法 正 确 的 是
一 、选 择 题 (本 大 题 共 16题 ,每 小 题 3分 ,共 48分 。在 每 小 题 给 出 的 四 个 选 项 中 ,只 有 一 项 是 符 合 题 目 要 求 A. 等 体 积 的 甲 烷 与 氯 气 混 合 ,在 光 照 下 反 应 只 生 成 一 氯 甲 烷 和 氯 化 氢
的 )
B. 相 同 质 量 的 烷 烃 完 全 燃 烧 时 ,甲 烷 的 耗 氧 量 最 少
1. 能 够 用 来 检 验 某 糖 尿 病 病 人 的 尿 液 中 是 否 含 葡 萄 糖 的 试 剂 是
A. C.
氨 水 B. 金 属 钠 通 常 情 况 下 ,烷 烃 能 够 使 高 锰 酸 钾 溶 液 褪 色
C. 新 制 Cu(OH)2 悬 浊 液 D. 硝 酸 银 溶 液 D. 烷 烃 的 熔 、沸 点 一 般 随 着 分 子 中 碳 原 子 数 的 增 加 而 升 高
2. 下 列 有 机 物 和 乙 醇 具 有 相 同 官 能 团 的 是 7. 要 将 在 酯 化 反 应 的 实 验 中 制 得 的 乙 酸 乙 酯 中 混 有 的 少 量 CH3COOH洗 涤 除 去 ,应 选 用 的 试 剂 是
A. 苯 乙 烯 ( ) B. 丙 三 醇 ( ) A. 乙 醇 B. 饱 和 Na2CO3 溶 液
C. 乙 醛 (CH3CHO) D. 乙 烷 (CH3CH3) C. 水 D. NaOH溶 液
3. 下 列 对 烃 的 分 类 不 正 确 的 是 8. 下 列 关 于 糖 类 、蛋 白 质 的 说 法 正 确 的 是
A. CH4、CH2 ?? CH2、CH2 ?? CHCH?? CH2 均 属 于 饱 和 烃 A. 葡 萄 糖 能 与 银 氨 溶 液 反 应 生 成 光 亮 的 “银 镜 ”
B. CH3CH2CH3、CH3CH?? CH2、CH3CH?? CHCH2CH?? CH2 均 属 于 链 状 烃
B. 糖 类 物 质 在 一 定 条 件 下 都 能 发 生 水 解 反 应
C. CH3CH3、 、C18H38均 属 于 饱 和 烃 C. 氨 基 酸 能 发 生 水 解 反 应 ,最 终 转 化 为 蛋 白 质
D. 均 属 于 芳 香 烃 D. 蛋 白 质 遇 到 硫 酸 铵 发 生 盐 析 ,并 失 去 生 理 活 性
化 学 ZX4·第 1页 (共 8页 ) 化 学 ZX4·第 2页 (共 8页 )
书书书
9. 下 列 说 法 不 正 确 的 是 14. 下 列 关 于 影 响 化 学 反 应 速 率 的 条 件 的 说 法 正 确 的 是
A. 淀 粉 、蛋 白 质 和 油 脂 都 能 发 生 水 解 反 应 A. 增 大 压 强 一 定 能 加 快 化 学 反 应 速 率
B. 猪 油 、奶 油 、花 生 油 、大 豆 油 都 属 于 油 脂 B. 使 用 催 化 剂 不 会 改 变 反 应 速 率
C. 利 用 植 物 秸 秆 等 物 质 中 的 纤 维 素 可 以 生 产 酒 精 ,用 作 燃 料 C. 反 应 物 浓 度 是 决 定 化 学 反 应 速 率 的 主 要 因 素
D. 向 鸡 蛋 清 的 水 溶 液 中 加 入 硝 酸 银 溶 液 可 能 产 生 沉 淀 ,加 水 后 沉 淀 又 会 溶 解
D. 升 高 温 度 ,一 般 能 加 快 化 学 反 应 速 率
10. 下 列 关 于 有 机 化 合 物 的 说 法 正 确 的 是
A. 塑 料 、天 然 橡 胶 都 是 天 然 高 分 子 化 合 物 15. 某 有 机 物 的 结 构 简 式 为 。下 列 关 于 该 有 机 物 的 叙 述 不 正 确 的 是
B. 乙 烯 、聚 乙 烯 和 苯 分 子 中 均 含 有 碳 碳 双 键 A. 能 与 NaHCO3 发 生 反 应 并 放 出 二 氧 化 碳
C. 棉 花 、羊 毛 、涤 纶 的 成 分 均 属 于 天 然 纤 维
B. 能 在 催 化 剂 作 用 下 与 HCl发 生 加 成 反 应
D. 乙 酸 和 乙 醇 可 用 Na2CO3 溶 液 加 以 区 别
C. 不 能 使 酸 性 KMnO4 溶 液 和 溴 水 褪 色
11. 下 列 物 质 转 化 常 通 过 加 成 反 应 实 现 的 是
A. CH4→ CH2Cl2 B. CH3CH2OH→ CH3COOCH2CH3 D. 在 浓 硫 酸 作 催 化 剂 条 件 下 能 和 乙 醇 发 生 酯 化 反 应 生 成 酯
C. CH3CH2OH→ CH3CHO D. CH2 ?? CH2→ CH3CH2Br 16. 下 列 对 图 2所 示 实 验 的 描 述 及 相 应 结 论 正 确 的 是
12. 可 以 用 来 鉴 别 甲 烷 和 乙 烯 的 试 剂 是
A. 水 B. 溴 水
C. 紫 色 石 蕊 溶 液 D. NaOH溶 液
13. 碳 原 子 成 键 的 多 样 性 、同 分 异 构 现 象 等 是 有 机 物 种 类 繁 多 的 原 因 。丁 烷 和 2-甲 基 丙 烷 的 结 构 式 如 图 1,下
图 2
列 关 于 上 述 两 种 物 质 的 说 法 不 正 确 的 是 A. 图 甲 :用 水 稀 释 浓 硫 酸 ,触 摸 烧 杯 外 壁 发 热 ,则 该 过 程 为 放 热 反 应
A. 分 子 式 相 同 B. 图 乙 :反 应 开 始 后 ,针 筒 活 塞 向 右 移 动 ,仅 凭 此 现 象 不 能 判 断 该 反 应 为 放 热 反 应
B. 互 为 同 分 异 构 体 C. 图 丙 :a电 极 质 量 减 小 ,b电 极 上 有 气 泡 生 成 ,则 金 属 活 泼 性 a>b
C. C H 图 1
等 物 质 的 量 的 两 物 质 中 碳 氢 键 (—)数 目 相 同
D. 图 丁 :等 质 量 两 份 锌 粉 分 别 加 入 过 量 稀 硫 酸 中 ,由 V(H2)-t关 系 图 推 测 a可 能 还 加 了 少 量 铜 粉
D. 物 理 性 质 、化 学 性 质 完 全 相 同
化 学 ZX4·第 3页 (共 8页 ) 化 学 ZX4·第 4页 (共 8页 )
第 Ⅱ 卷 (非 选 择 题 ,共 52分 ) 18. (10分 )已 知 乙 烯 能 发 生 如 图 4所 示 转 化 :
注 意 事 项 :
第 Ⅱ 卷 用 黑 色 碳 素 笔 在 答 题 卡 上 各 题 的 答 题 区 域 内 作 答 ,在 试 题 卷 上 作 答 无 效 。
图 4
二 、填 空 题 (本 大 题 共 4小 题 ,共 32分 ) (1)D的 结 构 简 式 为 ,聚 乙 烯 的 结 构 简 式 为 。
17. (10 2 B
分 )在 实 验 室 里 制 取 的 乙 烯 中 常 混 有 少 量 的 二 氧 化 硫 ,某 化 学 兴 趣 小 组 设 计 了 如 图 3 所 示 的 实 验 装 置 ()化 合 物 中 官 能 团 名 称 为 。反 应 ① 的 反 应 类 型 为 。
(3)写 出 反 应 ② 的 化 学 方 程 式 : 。
确 认 该 混 合 气 体 中 是 否 含 有 SO2 和 C2H4。请 回 答 下 列 问 题 :
(4)写 出 反 应 ④ 的 化 学 方 程 式 : 。
(5)实 验 室 通 过 图 5所 示 装 置 制 备 乙 酸 乙 酯 ,浓 硫 酸 的 作 用 是 ;E 中 盛 有 的 试 剂 是
。
图 3
(1)上 述 Ⅰ 、Ⅳ 装 置 可 盛 放 的 试 剂 是 :Ⅰ ;Ⅳ (请 将 下 列 有 关 试 剂 的 序 号 填 入 对 应 装
置 内 ,可 重 复 选 用 )。
图 5
A. 品 红 溶 液 B. NaOH溶 液 C. 浓 硫 酸 D. 酸 性 KMnO4 溶 液 19. (6分 )某 化 学 实 验 小 组 同 学 利 用 如 图 6所 示 实 验 装 置 制 取 氨 气 ,并 探 究 氨 气 的 性 质 (部 分 仪 器 已 略 去 )。
请 回 答 :
(2)能 说 明 SO2 气 体 存 在 的 现 象 是 。
(3)使 用 装 置 Ⅱ 的 目 的 是 ;有 关 反 应 的 离 子 方 程 式 是 。
(4)确 定 含 有 乙 烯 的 现 象 是 。
(5)为 了 制 备 重 要 的 有 机 原 料 氯 乙 烷 (CH3CH2Cl),下 面 是 两 位 同 学 设 计 的 方 案 :
甲 同 学 :选 乙 烷 和 适 量 氯 气 在 光 照 条 件 下 制 备 ; 图 6
(1)实 验 室 制 备 氨 气 的 化 学 方 程 式 为 。
乙 同 学 :选 乙 烯 和 适 量 HCl在 一 定 条 件 下 制 备 。
(2)用 装 置 B收 集 氨 气 时 ,应 选 择 氨 气 的 进 气 口 是 (填 “a”或 “b”)。
你 认 为 上 述 两 位 同 学 的 方 案 中 ,合 理 的 是 的 方 案 。
化 学 ZX4·第 5页 (共 8页 ) 化 学 ZX4·第 6页 (共 8页 )
(3)为 防 止 环 境 污 染 ,下 列 装 置 (盛 放 的 液 体 均 为 水 )可 用 于 吸 收 多 余 氨 气 的 是 (填 序 号 )。 三 、计 算 题 (本 大 题 共 2小 题 ,共 20分 )
21. (10分 )Ⅰ . (1)将 m g铜 镁 合 金 与 足 量 稀 硝 酸 完 全 反 应 ,放 出 2?24L NO 气 体 (标 况 下 ),转 移 电 子 数 为
,向 反 应 后 的 溶 液 中 加 入 NaOH溶 液 至 完 全 沉 淀 ,得 到 沉 淀 的 质 量 为 。
(2)将 2?56g Cu放 入 10?0mL浓 HNO3 中 正 好 完 全 反 应 。随 着 Cu 的 不 断 减 少 ,反 应 生 成 气 体 的 颜 色 逐 渐
变 浅 ,最 终 共 生 成 气 体 1?12L (标 准 状 况 ),则 该 浓 硝 酸 的 物 质 的 量 浓 度 是 mol/L。
(4)氨 气 在 有 催 化 剂 并 且 加 热 时 会 被 空 气 氧 化 ,这 是 工 业 制 硝 酸 的 第 一 步 反 应 ,写 出 该 反 应 的 化 学 方 程 Ⅱ . 称 取 某 有 机 物 (含 C、H、O 元 素 )4?6g,经 充 分 燃 烧 后 生 成 CO2 的 质 量 为 8?8g,H2O 的 质 量
式 : 。 为 5?4g。
20. (6分 )研 究 化 学 反 应 中 的 能 量 变 化 ,能 更 好 地 利 用 化 学 反 应 为 生 产 和 生 活 服 务 。 (1)该 有 机 物 中 C、H、O个 数 比 为 。
Ⅰ . 2 46
反 应 Zn+H2SO4(稀 )? ? ? ZnSO4+H2↑ 的 能 量 变 化 如 图 7所 示 。 ()若 该 有 机 物 的 相 对 分 子 质 量 为 ,且 能 与 金 属 钠 反 应 放 出 氢 气 ,请 写 出 该 有 机 物 的 结 构 简 式 :
。
22. (10分 )在 一 定 温 度 下 ,某 可 逆 反 应 在 体 积 为 2L的 密 闭 容 器 中 进 行 ,0~3min 各 物 质 的 物 质 的 量 的 变 化 情
况 如 图 9所 示 (A、B、C均 为 气 体 )。
图 7
(1)该 反 应 为 (填 “吸 热 ”或 “放 热 ”)反 应 。
(2)下 图 三 个 装 置 中 ,不 能 证 明 “锌 与 稀 硫 酸 反 应 是 吸 热 反 应 还 是 放 热 反 应 ”的 是 (填 序 号 )。
图 9
(1)该 反 应 的 化 学 方 程 式 为 。
(2)反 应 开 始 至 2min末 ,v正 (A) (填 “>”“<”或 “=”)v逆 (A),用 C 的 浓 度 变 化 表 示 的 反
应 速 率 为 。
(3)能 说 明 该 反 应 已 达 到 平 衡 状 态 的 是 (填 序 号 )。
Ⅱ . 图 8是 某 兴 趣 小 组 设 计 的 原 电 池 示 意 图 。 A. v(A)= 2v(B) B. 容 器 内 压 强 保 持 不 变
(1)下 列 实 验 叙 述 合 理 的 是 (填 序 号 )。 C. 2v(A)逆 =v(B)正 D. 容 器 内 混 合 气 体 的 密 度 保 持 不 变
A. Cu极 有 H2 产 生 B. 锌 作 负 极 ,发 生 还 原 反 应 (4)在 密 闭 容 器 里 ,通 入 a mol A(g)、b mol B(g)、c mol C(g),发 生 上 述 反 应 ,当 改 变 下 列 条 件 时 ,反
+
C. H 向 Zn极 移 动 D. 电 子 由 Zn
经 导 线 流 向 Cu 应 速 率 会 增 大 的 是 (填 序 号 )。
A. 升 高 温 度
(2)请 写 出 该 电 池 的 正 极 反 应 式 : 。 图 8
B. 增 大 容 器 体 积
(3)若 有 1mol电 子 流 过 导 线 ,则 理 论 上 在 标 准 状 况 下 ,产 生 H2 的 体 积 为 L。 C. 通 入 不 参 加 反 应 的 其 他 气 体 ,增 大 压 强
化 学 ZX4·第 7页 (共 8页 ) 化 学 ZX4·第 8页 (共 8页 )
镇雄四中高一年级春季学期第二次月考卷
化学参考答案
第 Ⅰ 卷 (选择题,共 48 分)
一、选择题 (本大题共 16 小题,每小题 3 分,共 48
题号 9 10 11 12 13 14 15 16
答案 D D D B D D C B
【解析】
3. CH2 CH2、 CH CHCH CH2分子中含有碳碳双键,属于不饱和烃, A 错误。链状烃指
的是分子中无环状结构的烃, B正确。 CH3CH3、 、 C
化学 ZX4参考答案·第 1页(共 6页)
7. A项,乙酸乙酯的制备为可逆反应,用乙醇不能除去乙酸乙酯中的少量乙酸,并且还引入
了新的杂质。 B 项,乙酸的酸性比碳酸强,能与碳酸钠反应生成二氧化碳而被吸收,乙酸
乙酯不溶于饱和碳酸钠溶液,然后分液可得到纯净的乙酸乙酯。 C 项,虽然乙酸能溶于水
而除去,但乙酸乙酯也有部分溶于水,依据除杂原则,不能选用水洗。 D项,乙酸乙酯在
氢氧化钠溶液中能够完全水解,反应方程式为 CH3COOCH2CH3+NaOH CH3COONa
+CH3CH2OH。故选 B。
8.葡萄糖分子中含有醛基,能与银氨溶液发生银镜反应生成光亮的“银镜”, A正确。糖类
中的单糖不能水解,二糖、多糖均可水解, B 错误。氨基酸脱水缩合作用形成蛋白质, C
错误。硫酸铵是轻金属盐,蛋白质遇到硫酸铵发生盐析,但不会失去生理活性, D错误。
9.淀粉属于多糖,在酶催化下能水解生成葡萄糖;蛋白质可以水解生成氨基酸;油脂水解生
成高级脂肪酸和甘油, A正确。呈液态的油脂都称为油,如植物油,呈固态的称为脂肪如
动物油, B 正确。纤维素在一定条件下可以发生水解,水解产物葡萄糖和果糖在一定条件
下会转化为酒精, C 正确。鸡蛋清的主要成分是蛋白质,加入硝酸盐是重金属盐,重金属
盐会使蛋白质变性,变性是不可逆过程, D不正确。
11.甲烷与氯气在光照条件下发生取代反应转化。乙醇通过与 CH3COOH 发生取代反应转化
为 CH3COOCH2CH3。乙醇通过氧化反应转化为乙醛。乙烯含有双键,可通过与 HBr发生
加成反应转化为 CH3CH2Br。答案为 D。
12.甲烷和乙烯都不能与水反应,则不能用水鉴别甲烷和乙烯, A错误。甲烷不能与溴水反应,
而乙烯能与溴水发生加成反应,使溴水褪色,则能用溴水鉴别甲烷和乙烯, B正确。甲烷
和乙烯都不能与紫色石蕊溶液反应,则不能用紫色石蕊溶液鉴别甲烷和乙烯, C错误。甲
烷和乙烯都不能与氢氧化钠溶液反应,则不能用氢氧化钠溶液鉴别甲烷和乙烯, D错误。
13.分子式相同,均是 C4H10, A正确。二者分子式相同,结构不同,互为同分异构体, B正
确。每个分子中碳氢键( C— H)数目相同,均含有 10个, C正确。二者互为同分异构体,
物理性质不同,均是烷烃,化学性质相似, D错误。
14.压强对反应速率的影响只适用于有气体参与的反应,即改变压强,反应速率不一定改变,
A错误。催化剂可以改变反应速率, B错误。物质本身的性质是决定化学反应速率的主要
因素, C错误。升高温度,活化分子数增多,化学反应速率加快, D正确。
化学 ZX4参考答案·第 2页(共 6页)
15.该有机物分子中含有 、 —COOH 两种官能团,其中— COOH 能和 NaHCO3反应
放出 CO2, A正确。分子中的 可在催化剂作用下与 HCl发生加成反应, B正确。
分子中的 能使酸性 KMnO4溶液和溴水褪色, C错误。分子中含— COOH,在浓
硫酸作催化剂条件下能和乙醇发生酯化反应生成酯和水, D正确。
16.浓硫酸的稀释过程不是化学反应,属于放热过程,不属于放热反应, A错误。碳酸钙和稀
盐酸反应生成氯化钙、二氧化碳和水,生成的二氧化碳气体能使针筒活塞向右移动,则
针筒活塞向右移动不一定是反应放出热量导致, B正确。若 a为金属铝, b为金属镁,铝、
镁在氢氧化钠溶液中构成原电池,能与氢氧化钠溶液反应的铝作原电池的负极,镁作正
极,正极上有气泡生成,但金属活泼性铝小于镁, C错误。由于稀硫酸过量,两份锌等量,
若 a中加了少量铜粉,锌铜在稀硫酸中构成原电池,会加快反应速率,同时生成氢气的量
会减少, D错误。
第 Ⅱ 卷 (非选择题,共 52 分)
二、填空题 (本大题共 4小题,共 32分)
17. (除特殊标注外,每空 1分,共 10分)
( 1) A D
( 2) Ⅰ 中品红溶液褪色( 2分)
? 2
( 3)除去二氧化硫 SO2+2OH = ?
SO3 ( 2分)
( 4) Ⅲ 中品红溶液不褪色, Ⅳ 中酸性 KMnO4溶液褪色( 2分)
( 5)乙同学
【解析】 实验室用电石与饱和食盐水制备乙烯,乙烯具有碳碳双键,能与溴水发生加成反
应,与酸性高锰酸钾发生氧化反应。副产物二氧化硫具有还原性和漂白性,能使品红溶
液褪色,能与酸性高锰酸钾反应使其褪色。
( 1)根据产物性质,首先应检验二氧化硫的存在并彻底吸收后检验乙烯的存在。 Ⅰ 装置
可盛放品红溶液, Ⅱ 装置可盛放氢氧化钠, Ⅲ 装置可盛放品红溶液,检验是否除尽二氧
化硫, Ⅳ 装置可盛放酸性高锰酸钾,最终检验乙烯的存在。
( 2)二氧化硫具有漂白性,能说明 SO2气体存在的现象是 Ⅰ 中品红溶液褪色。
( 3)装置 Ⅱ 中为氢氧化钠,目的是除去二氧化硫。有关反应的离子方程式是
? 2
SO2+2OH = ?
SO3 +H2O。
化学 ZX4参考答案·第 3页(共 6页)
( 4)确定含有乙烯要保证二氧化硫全部除尽,即现象是 Ⅲ 中品红溶液不褪色, Ⅳ 中酸性
KMnO4溶液褪色。
( 5)制备氯乙烷( CH3CH2Cl) ,甲同学:选乙烷和适量氯气在光照条件下制备,产物多样,
难以控制反应产物为一氯代物。乙同学:选乙烯和适量 HCl 在一定条件下制备,发生加
成反应,产物唯一,产率高。上述两位同学的方案中,合理的是乙同学的方案。
18. (除特殊标注外,每空 1分,共 10分)
( 1) CH3COOH
( 2)羟基 加成反应
( 3) 2CH3CH2OH+O2 2CH3CHO+2H2O( 2分)
( 4) CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O( 2分)
( 5)催化剂、吸水剂 饱和 Na2CO3溶液
【解析】 乙烯和水反应生成乙醇,乙醇在催化剂作用下与氧气反应生成乙醛,乙烯发生加
聚反应生成聚乙烯,乙醇和乙酸在浓硫酸加热作用下反应生成乙酸乙酯。
( 1) D为乙酸,其结构简式为 CH3COOH,聚乙烯的结构简式为 。
( 2)化合物 B 是乙醇,其官能团名称为羟基。反应①是乙烯和水在催化剂作用下发生加
成反应。
( 3)反应②的化学方程式为 2CH3CH2OH+O2 2CH3CHO+2H2O。
( 4)反应④是乙醇和乙酸在浓硫酸催化剂作用下发生酯化反应生成乙酸乙酯,其化学方
程式为 CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O。
( 5)浓硫酸的作用是催化剂、吸水剂。 E中盛有的试剂是饱和 Na2CO3溶液。
19. (除特殊标注外,每空 1分,共 6分)
( 1) 2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O( 2分)
( 2) b
( 3)②④
催化剂
( 4) 4NH3+5O2===== ( 分)
△ 4NO+6H2O 2
【解析】 ( 1)实验室制备氨气的化学方程式为 2NH4Cl+Ca(OH)2 2NH3↑+CaCl2+2H2O。
( 2)用装置 B 收集氨气时,由于氨气的密度比空气小,可用向下排空气法收集,导气管
要伸入烧瓶底部,所以应选择氨气的进气口是 b。
( 3)①不能使 NH3进入瓶中,②④能防止倒吸,③会发生倒吸,故答案为②④。
化学 ZX4参考答案·第 4页(共 6页)
20. (除特殊标注外,每空 1分,共 6分)
Ⅰ. ( 1)放热
( 2) Ⅲ
Ⅱ. ( 1) AD
+ ?
( 2) 2H +2e =H2↑( 2分)
( 3) 11.2
三、计算题 (本大题共 2小题,共 20分)
21. (每空 2分,共 10分)
Ⅰ. ( 1) 0.3NA (m+5.1)g
( 2) 13
Ⅱ. ( 1) 2∶ 6∶ 1
( 2) CH3CH2OH
V 2.24L
【解析】 Ⅰ. ( 1) n(NO)= = =0.1mol,则转移的电子数为 (5?2)×0.1mol=0.3mol,
Vm 22.4L/mol
即 0.3NA; Mg、 Cu混合物与硝酸反应生成 Mg(NO3)2、 Cu(NO3)2,部分硝酸被还原为 NO
气体,反应后的溶液加入 NaOH溶液使金属恰好沉淀完全,沉淀为 Cu(OH)2、 Mg(OH)2,
? ?
结合得失电子守恒可知 n(OH )=0.3mol,则 m(OH )=17g/mol×0.3mol=5.1g,故得到沉淀的
质量为 5.1g+m g=(m+5.1)g。
( 2)铜和 10mL浓硝酸反应,随着浓度的减少,硝酸的还原产物的价态越低,铜和浓硝酸
反应生成 NO2,而与稀硝酸反应时则生成 NO,故生成的气体有 NO2 和 NO,则
1.12L
n(NO2)+n(NO)= =0.05mol ,即被还原的硝酸的物质的量为 0.05mol,
22.4L/mol
2.56g
n(Cu)= =0.04mol,则生成 n[Cu(NO3)2]=0.04mol,可知表现酸性的硝酸的物质的
64g/mol
量为 0.04mol×2=0.08mol,则参加反应的硝酸的物质的量为 0.05mol+0.08mol=0.13mol,则
0.13mol
物质的量浓度为 =13mol/L。
0.01L
8.8g
Ⅱ.( 1 )根据反应前后元素守恒,可知 n(C)=n(CO2)= =0.2mol ,
44g/mol
5.4g 4.6g0.2mol12g/mol0.6mol1g/mol? ???
n(H)=2n(H2O)=2× =0.6mol, n(O)=
18g/mol 16g/mol
=0.1mol, n(C)∶ n(H)∶ n(O)=0.2mol∶ 0.6mol∶ 0.1mol=2∶ 6∶ 1。
化学 ZX4参考答案·第 5页(共 6页)
( 2)根据( 1)计算可知该有机物中 C、 H、 O三种元素的原子个数比是 2∶ 6∶ 1,则其最
简式是 C2H6O,最简式的式量是 46,而该有机物的相对分子质量为 46,因此其最简式就
是其分子式,符合该分子式的物质可能是 CH3CH2OH、 CH3OCH3,该有机物能与金属钠
反应放出氢气,说明分子中含有— OH,则该有机物的结构简式是 CH3CH2OH。
22. (每空 2分,共 10分)
( 1) 2A(g)+B(g) 2C(g)
( 2) = 0.5mol/(L· min)
( 3) B
( 4) A
【解析】 ( 1)由图像可知, A、 B为反应物, C为生成物,当反应进行到 2min时, A、 B、
C 三种物质的量变化量之比为 (5?3)mol∶ (2?1)mol∶ (4?2)mol=2∶ 1∶ 2。由各物质的物质
的量的变化量之比等于化学计量数之比可知,反应的化学方程式为
2A(g)+B(g) 2C(g)。
( 2)反应开始至 2min 末,反应达平衡状态,正逆反应速率相等。 C 的浓度变化
(42)mol? 1mol/L
?c= =1mol/L。用 C的浓度变化表示的反应速率为 =0.5mol/(L· min)。
2L 2min
( 3)反应的化学方程式为 2A(g)+B(g) 2C(g)。 A. v(A)=2v(B)不能说明正反应和逆反
应的关系,故不能判断反应是否达到平衡状态。 B.该反应为前后气体体积变小的反应,
随着反应的进行,气体的物质的量不断减小,压强也减小,当容器内压强保持不变时,
说明正逆反应速率相等,反应达到平衡状态。 C. v(A)逆 =2v(B)正 说明正逆反应速率相等,
则 2v(A)逆 =v(B)正 说明正反应速率大于逆反应速率,反应未达平衡状态。 D.该反应中各物
质均为气态,反应前后气体的总质量保持不变,容器的体积也保持不变,因此容器内混
合气体的密度始终保持不变,不能判断反应是否达到平衡状态。故选 B。
( 4) A.升高温度,活化分子数增多,化学反应速率加快。 B.增大容器体积,各物质的
浓度减小,化学反应速率减小。 C.容器的容积不变,通入不参加反应的其他气体,虽然
增大了压强,但是各物质的浓度不变,反应速率不变。故选 A。
化学 ZX4参考答案·第 6页(共 6页)
同课章节目录
