2020-2021学年人教版高一化学必修二4.2《资源的综合利用 环境保护》过关训练试题(含解析)
文档属性
| 名称 | 2020-2021学年人教版高一化学必修二4.2《资源的综合利用 环境保护》过关训练试题(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 537.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-17 00:00:00 | ||
图片预览




文档简介
(人教版必修2)4.2资源的综合利用 环境保护》过关训练试题
(原卷版)
(时间45分钟 满分100分)
一、单项选择题:本题包括13小题,每小题4分,共52分。
1.化学与生活、社会密切相关。下列说法不正确的是( )
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.提倡人们购物时不用塑料袋,是为了防止白色污染
2.石油和煤都是重要的化石能源,下列有关石油和煤的叙述正确的是( )
A.都是纯净物 B.都含有碳元素
C.都是可再生能源 D.都有固定的沸点
3.下列关于煤和石油的说法正确的是
A.石油裂解的目的主要是为了得到更多的汽油
B.石油的分馏和煤的干馏都是物理变化
C.煤的气化就是将煤在高温条件由固态转化为气态的物理变化过程
D.工业上可以从煤的干馏产物中提取苯、甲苯等芳香烃
4.化学与科技、社会、环境密切相关。下列有关说法正确的是( )
A.pH小于7的雨水被称为酸雨
B.明矾溶于水可产生具有吸附性的胶体粒子,常用于饮用水的杀菌消毒
C.推广使用燃煤脱硫技术,主要是为了防治SO2污染
D.PM2.5是指大气中直径小于或等于2.5微米(2.5×10-6m)的细小可吸入颗粒物,其与空气形成的分散系属于胶体
5.化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是( )
A.为提高农作物的产量和质量,应大量使用化肥和农药
B.绿色化学的核心是应用化学原理对环境污染进行治理
C.实现化石燃料清洁利用,就无需开发新能源
D.垃圾是放错地方的资源,应分类回收利用
6.常见的大气污染物分一次污染和二次污染。二次污染是排入环境中的一次污染物在物理、化学因素或生物作用下发生了变化,或与环境中的其他物质发生反应生成的新污染物;如2NO+O2=2NO2,则NO2就是二次污染物,由NO2导致的污染就是NO的二次污染。下列物质中:①SO2,②NO,③NO2,④HCl,⑤CO2。不易导致二次污染的是 ( )
A.①②③④⑤ B.①③⑤
C.④⑤ D.④
7.下列说法正确的是
A.煤的气化、液化和干馏都是物理变化
B.加热能杀死病毒,是因为蛋白质受热发生变性
C.石油裂解可以得到更多的汽油,这种汽油是一种纯净物
D.动物脂肪和稀硫酸混合加热,可得到肥皂的主要成分和甘油
8.下列说法正确的是( )
A.利用化石燃料燃烧放出的热量使水分解产生氢气,是氢能开发的研究方向
B.光合作用是将光能转化为化学能的有效途径
C.石油、煤、天然气属于二次能源
D.绿色化学最显著的特征是在生产化工产品过程中必须以绿色植物为原料
9.对煤干馏并检验其中部分产物,装置(夹持装置已略)如图所示。下列说法不正确的是( )
A.煤的干馏过程发生复杂的物理、化学变化
B.向b装置的水层中滴入紫色石蕊溶液,溶液变蓝
C.c装置可检验产生的气体中一定含有H2S
D.e装置中产生的现象是固体由黑色变为红色
10.我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下。下列说法不正确的是( )
A.反应①的产物中含有水
B.汽油主要是C5~C11的烃类混合物
C.反应②中只有碳碳键形成
D.图中a的名称是2?甲基丁烷
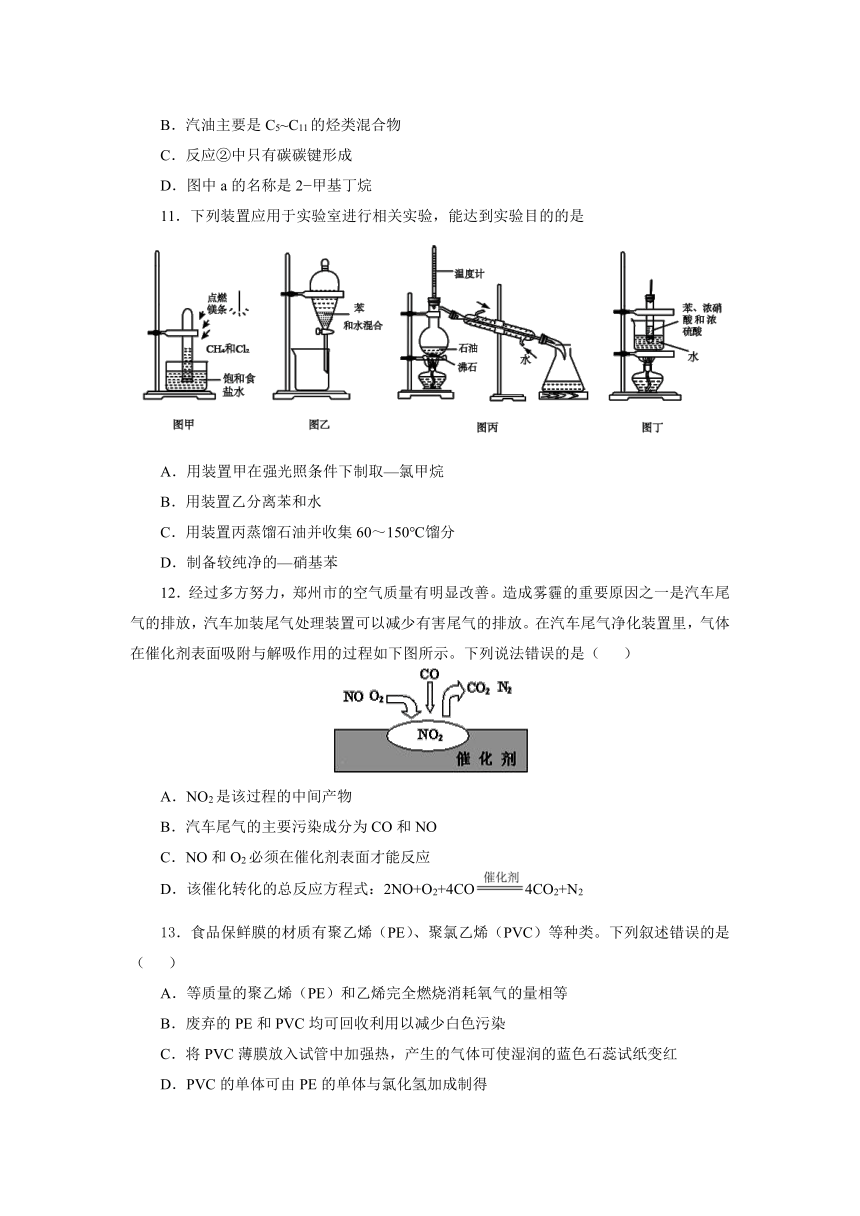
11.下列装置应用于实验室进行相关实验,能达到实验目的的是
A.用装置甲在强光照条件下制取—氯甲烷
B.用装置乙分离苯和水
C.用装置丙蒸馏石油并收集60~150℃馏分
D.制备较纯净的—硝基苯
12.经过多方努力,郑州市的空气质量有明显改善。造成雾霾的重要原因之一是汽车尾气的排放,汽车加装尾气处理装置可以减少有害尾气的排放。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如下图所示。下列说法错误的是( )
A.NO2是该过程的中间产物
B.汽车尾气的主要污染成分为CO和NO
C.NO和O2必须在催化剂表面才能反应
D.该催化转化的总反应方程式:2NO+O2+4CO4CO2+N2
13.食品保鲜膜的材质有聚乙烯(PE)、聚氯乙烯(PVC)等种类。下列叙述错误的是( )
A.等质量的聚乙烯(PE)和乙烯完全燃烧消耗氧气的量相等
B.废弃的PE和PVC均可回收利用以减少白色污染
C.将PVC薄膜放入试管中加强热,产生的气体可使湿润的蓝色石蕊试纸变红
D.PVC的单体可由PE的单体与氯化氢加成制得
二、非选择题:本题包括4小题,共48分。
14.(12分)以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息回答下列问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是________(填字母)。
A.CH2===CH2+HClCH3CH2Cl
B.CH3CH2OH+HClCH3CH2Cl+H2O
C.CH3CH3+Cl2CH3CH2Cl+HCl
D.CH2===CHCl+H2CH3CH2Cl
由上述四个反应可归纳出,原子经济性最高的是______(填反应类型)。
(2)有毒物质的无害化处理也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,它可将废水中少量的CN-等有毒的酸根离子氧化而除去。请写出用ClO2将废水中的CN-氧化成无毒气体的离子方程式:__________________________________________________,
该方法的优点是___________________________________________________。
(3)某饮用水厂由天然水制备纯净水(去离子水)的工艺流程示意图如下:
活性炭的作用是_______________________________________________________;
O3消毒的优点是_______________________________________________________。
15.(10分)硫酸型酸雨的形成原理可简化表示如下:
回答下列问题:
(1)D物质的化学式__________________。
(2)反应②的化学方程式为______________________________________________。该反应___________(填“属于”或“不属于”)可逆反应。
(3)反应④的化学方程式为_________________________________________________。
(4)你认为减少酸雨产生可采用的措施是___________(填序号)。
①少用煤做燃料;②把工厂烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新能源
16.(14分)“环境就是民生,青山就是美丽,蓝天也是幸福。“拥有天蓝、地绿、水净的美好家园,是每个中国人的梦想。回答下列问题:
(1)排放到大气中的氮的氧化物,会造成___________污染。
(2)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。氨氨废水是造成河流及湖泊富营养化的主要因素。某氮肥厂产生的氨氮废水中的氮元素多以NH4+和NH3·H2O形式存在,为达到变废为宝回收利用的目的,某团队设计处理流程如下:
过程Ⅱ为硝化过程,在微生物的作用下实现NH4+→NO2—→NO3—的转化,在碱性条件下NH4+被氧气氧化成NO3—的总反应离子方程式为__________________________________。
过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇(CH3OH)实现HNO3→NO2—→N2的转化,将lmol NO2—完全转化为N2,转移的电子数为___________。
(3)磷酸生产及煤燃烧产生的废气SO2等会对大气造成污染。防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏。脱硫反应的化学方程式为___________________________________________。某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸___________吨(假设生产过程中96%SO2转化为SO3)。
17.(12分)可持续发展需要注意“环境保护”和“节约能源”。
(1)以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的主要气体是________;
(2)氮氧化物(NOx)是大气中的主要气态污染物之一、汽车尾气中含有NOx、CO和碳氢化合物等。汽车尾气净化装置里装有Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用韵机理如图所示。
尾气净纯装置中发生的总反应化学方程式为_____________________________________;
(3)工业废承需处理达标后才能排放,下列处理方法合理的是___________(填字母);
A.用中和法除去废水中的酸
B.用絮凝剂除去废水中的重金属离子
C.用氯气除去废水中的悬浮物
(4)饮用水钓消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一、漂白粉是常用的消毒剂,其有效成分是___________。Cl2是传统的自来水消毒剂,而ClO2是新型的自来水消毒剂,这两种消毒剂消毒完成后,氯元素均以Cl-形式存在。现要消毒1m3生活污水,分别用Cl2和ClO2来消毒处理,所耗这两种消毒剂的质量比为___________。(保留小数点后2位)
(人教版必修2)4.2资源的综合利用 环境保护》过关训练试题
(解析版)
(时间45分钟 满分100分)
一、单项选择题:本题包括13小题,每小题4分,共52分。
1.化学与生活、社会密切相关。下列说法不正确的是( )
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.提倡人们购物时不用塑料袋,是为了防止白色污染
【答案】B
【解析】A.用太阳能等清洁能源代替化石燃料,有利于节约能源,减少污染物的排放,有利于环境保护,所以A选项是正确的;B.食品添加剂不全对人体有害,但对人体有害的应严格控制用量,并不是一盖杜绝,故B错误;C.废旧电池中含有汞、镉和铅等重金属元素,对人体有害,应积极开发废电池的综合利用技术,充分回收利用,所以C选项是正确的;D.塑料袋的主要分成为聚乙烯,难以降解,易导致白色污染,应控制使用,所以D选项是正确的。答案选B。
2.石油和煤都是重要的化石能源,下列有关石油和煤的叙述正确的是( )
A.都是纯净物 B.都含有碳元素
C.都是可再生能源 D.都有固定的沸点
【答案】B
【解析】煤、石油都属于不可再生能源,是混合物,没有固定的沸点,故B项正确。
3.下列关于煤和石油的说法正确的是
A.石油裂解的目的主要是为了得到更多的汽油
B.石油的分馏和煤的干馏都是物理变化
C.煤的气化就是将煤在高温条件由固态转化为气态的物理变化过程
D.工业上可以从煤的干馏产物中提取苯、甲苯等芳香烃
【答案】D
【解析】A.石油裂解的目的主要是为了获得乙烯、丙烯等基本化工原料,A错误;B.石油的分馏是物理变化,而煤的干馏是化学变化,B错误;C.煤的气化就是将煤在高温条件下与水蒸气反应转化为水煤气的化学变化过程,C错误;D.工业上可以从煤的干馏产物煤焦油中分离提取苯、甲苯等芳香烃,D正确;故答案为:D。
4.化学与科技、社会、环境密切相关。下列有关说法正确的是( )
A.pH小于7的雨水被称为酸雨
B.明矾溶于水可产生具有吸附性的胶体粒子,常用于饮用水的杀菌消毒
C.推广使用燃煤脱硫技术,主要是为了防治SO2污染
D.PM2.5是指大气中直径小于或等于2.5微米(2.5×10-6m)的细小可吸入颗粒物,其与空气形成的分散系属于胶体
【答案】C
【解析】A. pH小于5.6的雨水被称为酸雨,故A错误;B. 明矾常用于饮用水的净化,不能消毒,故B错误;C. 推广使用燃煤脱硫技术,减少SO2的排放,故C正确;D. PM2.5的直径大于胶体的直径,不属于胶体,故D错误;答案选C。
5.化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是( )
A.为提高农作物的产量和质量,应大量使用化肥和农药
B.绿色化学的核心是应用化学原理对环境污染进行治理
C.实现化石燃料清洁利用,就无需开发新能源
D.垃圾是放错地方的资源,应分类回收利用
【答案】D
【解析】A.化肥和农药虽然能提高农作物产量和质量,但会污染环境、影响人体健康,不能大量使用,A错误;B.绿色化学的核心是利用化学原理从源头上减少和消除对环境的污染,B错误;C.化石燃料属于不可再生能源,故仍需开发新能源缓解能源缺乏的问题,C错误;D.垃圾可分类回收利用,节约能源,D正确。答案选D。
6.常见的大气污染物分一次污染和二次污染。二次污染是排入环境中的一次污染物在物理、化学因素或生物作用下发生了变化,或与环境中的其他物质发生反应生成的新污染物;如2NO+O2=2NO2,则NO2就是二次污染物,由NO2导致的污染就是NO的二次污染。下列物质中:①SO2,②NO,③NO2,④HCl,⑤CO2。不易导致二次污染的是 ( )
A.①②③④⑤ B.①③⑤
C.④⑤ D.④
【答案】C
7.下列说法正确的是
A.煤的气化、液化和干馏都是物理变化
B.加热能杀死病毒,是因为蛋白质受热发生变性
C.石油裂解可以得到更多的汽油,这种汽油是一种纯净物
D.动物脂肪和稀硫酸混合加热,可得到肥皂的主要成分和甘油
【答案】B
【解析】A.煤的气化、液化和干馏过程中都产生了新的物质,因此发生的变化属于化学变化,A错误;B.加热能杀死病毒,是因为病毒主要是由蛋白质构成,蛋白质受热时会失去其生理活性而发生变性,B正确;C.石油裂解可以得到更多的汽油,这种汽油中含有多种烷烃和烯烃,因此是一种混合物,C错误;D.动物脂肪在碱性条件下加热会发生水解反应产生高级脂肪酸盐和甘油,高级脂肪酸盐是肥皂的主要成分,故油脂在碱性条件下的水解反应为皂化反应。而在酸性条件下水解产生的是高级脂肪酸和甘油,D错误;故合理选项是B。
8.下列说法正确的是( )
A.利用化石燃料燃烧放出的热量使水分解产生氢气,是氢能开发的研究方向
B.光合作用是将光能转化为化学能的有效途径
C.石油、煤、天然气属于二次能源
D.绿色化学最显著的特征是在生产化工产品过程中必须以绿色植物为原料
【答案】B
【解析】利用化石燃料燃烧法使水分解制氢气需要消耗大量的能源,A错误;光合作用是将光能转化为化学能的有效途径,B正确;石油、煤、天然气属于一次能源,C错误;绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染,反应物的原子全部转化为期望的最终产物,D错误。
9.对煤干馏并检验其中部分产物,装置(夹持装置已略)如图所示。下列说法不正确的是( )
A.煤的干馏过程发生复杂的物理、化学变化
B.向b装置的水层中滴入紫色石蕊溶液,溶液变蓝
C.c装置可检验产生的气体中一定含有H2S
D.e装置中产生的现象是固体由黑色变为红色
【答案】C
【解析】煤干馏得到焦炉气、粗氨水、粗苯、煤焦油、焦炭,据此分析;A.煤的干馏是指将煤隔绝空气加强热使之分解的过程,发生复杂的物理、化学变化,得到焦炉气、粗氨水、粗苯、煤焦油、焦炭,故A说法正确;B.煤的干馏得到产物中含有NH3,氨水显碱性,能使紫色石蕊溶液变蓝,故B说法正确;C.焦炉气中含有乙烯,乙烯也能使酸性KMnO4溶液褪色,故C说法错误;D.焦炉气中含有H2、CH4、CO都能还原CuO,使黑色变为红色,故D说法正确;答案:C。
10.我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下。下列说法不正确的是( )
A.反应①的产物中含有水
B.汽油主要是C5~C11的烃类混合物
C.反应②中只有碳碳键形成
D.图中a的名称是2?甲基丁烷
【答案】C
【解析】A. 反应①为二氧化碳和氢气反应生成一氧化碳和水,产物中含有水,故正确;B. 汽油是石油的分馏产物,主要是C5~C11的烃类混合物,故正确;C. 反应②中不仅有碳碳键形成,还有碳氢键形成,故错误;D. 图中a主链有4个碳原子,2号碳上有一个甲基,所以名称是2?甲基丁烷,故正确。故选C。
11.下列装置应用于实验室进行相关实验,能达到实验目的的是
A.用装置甲在强光照条件下制取—氯甲烷
B.用装置乙分离苯和水
C.用装置丙蒸馏石油并收集60~150℃馏分
D.制备较纯净的—硝基苯
【答案】B
【解析】A.甲在强光照条件下会爆炸,且制取可能为一氯甲烷、二氯甲烷等物质,A不能达到实验目的;B.苯不溶于水,苯与水的混合液有明显的分层,可以用分液漏斗分离苯和水,B能达到实验目的;C.石油分馏实验中,温度计测量蒸气的温度,因此温度计的水银球应在蒸馏烧瓶支管口处,C不能达到实验目的;D.苯、硝基苯相互溶解,则不能制备纯净的硝基苯,D不能达到实验目的;答案为B。
12.经过多方努力,郑州市的空气质量有明显改善。造成雾霾的重要原因之一是汽车尾气的排放,汽车加装尾气处理装置可以减少有害尾气的排放。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如下图所示。下列说法错误的是( )
A.NO2是该过程的中间产物
B.汽车尾气的主要污染成分为CO和NO
C.NO和O2必须在催化剂表面才能反应
D.该催化转化的总反应方程式:2NO+O2+4CO4CO2+N2
【答案】C
【解析】A. 由题目提供的图可知:2NO+O2===2NO2,2NO2+4CO4CO2+N2,NO2是该过程的中间产物,故A正确;B. 汽油不完全燃烧可生成CO,空气中的氮气在气缸中放电条件下可生成NO,汽车尾气的主要污染成分是CO、NO、NO2等,故B正确;C. NO和O2在常温下就能反应生成NO2,故C错误;D. 该反应的反应物是NO、O2、CO,生成物是CO2、N2,反应条件是催化剂,所以该反应方程式2NO+O2+4CO4CO2+N2,故D正确。故选C。
13.食品保鲜膜的材质有聚乙烯(PE)、聚氯乙烯(PVC)等种类。下列叙述错误的是( )
A.等质量的聚乙烯(PE)和乙烯完全燃烧消耗氧气的量相等
B.废弃的PE和PVC均可回收利用以减少白色污染
C.将PVC薄膜放入试管中加强热,产生的气体可使湿润的蓝色石蕊试纸变红
D.PVC的单体可由PE的单体与氯化氢加成制得
【答案】D
【解析】乙烯、聚乙烯含碳量相同,等质量的聚乙烯(PE)和乙烯完全燃烧消耗氧气的量相等,故A正确;废弃的塑料回收利用以减少白色污染,故B正确;聚氯乙烯放入试管中加强热,产生的气体可生成氯化氢,故C正确;PE的单体是乙烯,乙烯与氯化氢加成生成一氯乙烷,PVC的单体是氯乙烯,故D错误。
二、非选择题:本题包括4小题,共48分。
14.(12分)以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息回答下列问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是________(填字母)。
A.CH2===CH2+HClCH3CH2Cl
B.CH3CH2OH+HClCH3CH2Cl+H2O
C.CH3CH3+Cl2CH3CH2Cl+HCl
D.CH2===CHCl+H2CH3CH2Cl
由上述四个反应可归纳出,原子经济性最高的是______(填反应类型)。
(2)有毒物质的无害化处理也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,它可将废水中少量的CN-等有毒的酸根离子氧化而除去。请写出用ClO2将废水中的CN-氧化成无毒气体的离子方程式:__________________________________________________,
该方法的优点是___________________________________________________。
(3)某饮用水厂由天然水制备纯净水(去离子水)的工艺流程示意图如下:
活性炭的作用是_______________________________________________________;
O3消毒的优点是_______________________________________________________。
【答案】(1)AD 加成反应
(2)2ClO2+2CN-===2CO2+N2+2Cl- 产物为无毒无害的Cl-、CO2和N2
(3)吸附水中的有机物(或除去水中的异味) 反应产物无毒无害
【解析】 (1)原子经济性高,即理论上原子的利用率尽可能达到100%,没有副产物。A、D两项中的原子利用率都是100%。(2)把CN-氧化成无毒气体,说明C、N分别生成了CO2、N2,ClO2的还原产物应该是无毒的Cl-。(3)活性炭能吸附水中的有机物,从而除去异味。用O3消毒时,其产物为无毒无害的O2。
15.(10分)硫酸型酸雨的形成原理可简化表示如下:
回答下列问题:
(1)D物质的化学式__________________。
(2)反应②的化学方程式为______________________________________________。该反应___________(填“属于”或“不属于”)可逆反应。
(3)反应④的化学方程式为_________________________________________________。
(4)你认为减少酸雨产生可采用的措施是___________(填序号)。
①少用煤做燃料;②把工厂烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新能源
【答案】(1)H2SO3 (2)2SO2+O22SO3 属于
(3)SO2+H2OH2SO3 (4)①③⑤
【解析】硫酸型酸雨的形成原理:含硫燃料燃烧生成A物质主要成分为二氧化硫,二氧化硫在空气中被进一步氧化生成B为三氧化硫,三氧化硫与水反应生成C为硫酸,为酸雨成分之一;二氧化硫与水反应生成D为亚硫酸,亚硫酸在空气中被氧化生成硫酸。(1)D物质为亚硫酸,其化学式为H2SO3;(2)反应②是二氧化硫被空气中的氧气氧化生成三氧化硫,反应的化学方程式为2SO2+O22SO3;该反应属于可逆反应;(3)反应④是二氧化硫与水反应生成亚硫酸,反应的化学方程式为SO2+H2OH2SO3;(4) 少用煤作燃料、燃料脱硫、开发新的能源等措施可以减少二氧化硫气体的排放,从而减少酸雨的形成;
答案为①③⑤。
16.(14分)“环境就是民生,青山就是美丽,蓝天也是幸福。“拥有天蓝、地绿、水净的美好家园,是每个中国人的梦想。回答下列问题:
(1)排放到大气中的氮的氧化物,会造成___________污染。
(2)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。氨氨废水是造成河流及湖泊富营养化的主要因素。某氮肥厂产生的氨氮废水中的氮元素多以NH4+和NH3·H2O形式存在,为达到变废为宝回收利用的目的,某团队设计处理流程如下:
过程Ⅱ为硝化过程,在微生物的作用下实现NH4+→NO2—→NO3—的转化,在碱性条件下NH4+被氧气氧化成NO3—的总反应离子方程式为__________________________________。
过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇(CH3OH)实现HNO3→NO2—→N2的转化,将lmol NO2—完全转化为N2,转移的电子数为___________。
(3)磷酸生产及煤燃烧产生的废气SO2等会对大气造成污染。防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏。脱硫反应的化学方程式为___________________________________________。某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸___________吨(假设生产过程中96%SO2转化为SO3)。
【答案】(1)光化学烟雾 (2)NH4++2OH-+2O2 NO3—+3H2O (3)3NA (4)2SO2+O2+2CaCO3=2CaSO4+2CO2 (5) 2.4
【解析】(1)排放到大气中的氮的氧化物,会造成光化学烟雾污染;(2)在碱性条件下 NH4+被氧气氧化成NO3—的总反应离子方程式为: NH4++2OH-+2O2 NO3—+3H2O;将lmol完全转化为N2时,NO2—的氮元素由为+3价转化为N2中的 0价,根据原子守恒可知转移的电子数为3mol,即转移的电子数为3NA,(3)①向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏,说明煤燃烧产生SO2和CaCO3反应生成了石膏CaSO4,反应的方程式为:2SO2+O2+2CaCO3=2CaSO4+2CO2;②依据反应前后硫元素质量不变可知:FeS2~2SO2~2SO3~2H2SO4,设制备浓硫酸的质量为m,生产过程中96%SO2转化为SO3,则
,
,解得。
17.(12分)可持续发展需要注意“环境保护”和“节约能源”。
(1)以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的主要气体是________;
(2)氮氧化物(NOx)是大气中的主要气态污染物之一、汽车尾气中含有NOx、CO和碳氢化合物等。汽车尾气净化装置里装有Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用韵机理如图所示。
尾气净纯装置中发生的总反应化学方程式为_____________________________________;
(3)工业废承需处理达标后才能排放,下列处理方法合理的是___________(填字母);
A.用中和法除去废水中的酸
B.用絮凝剂除去废水中的重金属离子
C.用氯气除去废水中的悬浮物
(4)饮用水钓消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一、漂白粉是常用的消毒剂,其有效成分是___________。Cl2是传统的自来水消毒剂,而ClO2是新型的自来水消毒剂,这两种消毒剂消毒完成后,氯元素均以Cl-形式存在。现要消毒1m3生活污水,分别用Cl2和ClO2来消毒处理,所耗这两种消毒剂的质量比为___________。(保留小数点后2位)
【答案】(1)SO2 (2)2NO+O2+4CON2+4CO2 (3) A
(4) Ca(ClO)2 2.63∶1
【解析】(1)煤炭中的硫燃烧会生成二氧化硫,空气中的二氧化硫气体会在粉尘作催化剂的条件下反应生成三氧化硫,三氧化硫再与雨水形成酸雨,形成这类酸雨的主要气体是SO2;(2)由图可知,反应Ⅰ为2NO+O2=2NO2,反应Ⅱ为2NO2+4CON2+4CO2,Ⅰ+Ⅱ得到2NO+O2+4CON2+4CO2;(3)A.中和法适用于除去废水中的酸,所以用中和法除去废水中的酸,故A符合题意;B.用混凝剂如明矾等除去废水中的悬浮物,用沉淀法除去废水中的重金属离子,故B不符合题意;C.用混凝剂如明矾等除去废水中的悬浮物,氯气能消毒杀菌,但不能除去悬浮物,故C不符合题意;答案为A;(4)漂白粉的主要成分是CaCl2、Ca(ClO)2,有效成分是Ca(ClO)2;用Cl2消毒处理,转移2mol电子时消耗消毒剂Cl2的质量为71g,转移1mol电子时消耗消毒剂Cl2的质量为35.5g,ClO2来消毒处理,转移5mol电子时消耗消毒剂Cl2的质量为67.5g,转移1mol电子时消耗消毒剂ClO2的质量为13.5g,要消毒1m3生活污水,转移相同物质的量的电子消耗消毒剂Cl2和ClO2的质量比为:35.5g∶13.5g=2.63∶1。
(原卷版)
(时间45分钟 满分100分)
一、单项选择题:本题包括13小题,每小题4分,共52分。
1.化学与生活、社会密切相关。下列说法不正确的是( )
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.提倡人们购物时不用塑料袋,是为了防止白色污染
2.石油和煤都是重要的化石能源,下列有关石油和煤的叙述正确的是( )
A.都是纯净物 B.都含有碳元素
C.都是可再生能源 D.都有固定的沸点
3.下列关于煤和石油的说法正确的是
A.石油裂解的目的主要是为了得到更多的汽油
B.石油的分馏和煤的干馏都是物理变化
C.煤的气化就是将煤在高温条件由固态转化为气态的物理变化过程
D.工业上可以从煤的干馏产物中提取苯、甲苯等芳香烃
4.化学与科技、社会、环境密切相关。下列有关说法正确的是( )
A.pH小于7的雨水被称为酸雨
B.明矾溶于水可产生具有吸附性的胶体粒子,常用于饮用水的杀菌消毒
C.推广使用燃煤脱硫技术,主要是为了防治SO2污染
D.PM2.5是指大气中直径小于或等于2.5微米(2.5×10-6m)的细小可吸入颗粒物,其与空气形成的分散系属于胶体
5.化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是( )
A.为提高农作物的产量和质量,应大量使用化肥和农药
B.绿色化学的核心是应用化学原理对环境污染进行治理
C.实现化石燃料清洁利用,就无需开发新能源
D.垃圾是放错地方的资源,应分类回收利用
6.常见的大气污染物分一次污染和二次污染。二次污染是排入环境中的一次污染物在物理、化学因素或生物作用下发生了变化,或与环境中的其他物质发生反应生成的新污染物;如2NO+O2=2NO2,则NO2就是二次污染物,由NO2导致的污染就是NO的二次污染。下列物质中:①SO2,②NO,③NO2,④HCl,⑤CO2。不易导致二次污染的是 ( )
A.①②③④⑤ B.①③⑤
C.④⑤ D.④
7.下列说法正确的是
A.煤的气化、液化和干馏都是物理变化
B.加热能杀死病毒,是因为蛋白质受热发生变性
C.石油裂解可以得到更多的汽油,这种汽油是一种纯净物
D.动物脂肪和稀硫酸混合加热,可得到肥皂的主要成分和甘油
8.下列说法正确的是( )
A.利用化石燃料燃烧放出的热量使水分解产生氢气,是氢能开发的研究方向
B.光合作用是将光能转化为化学能的有效途径
C.石油、煤、天然气属于二次能源
D.绿色化学最显著的特征是在生产化工产品过程中必须以绿色植物为原料
9.对煤干馏并检验其中部分产物,装置(夹持装置已略)如图所示。下列说法不正确的是( )
A.煤的干馏过程发生复杂的物理、化学变化
B.向b装置的水层中滴入紫色石蕊溶液,溶液变蓝
C.c装置可检验产生的气体中一定含有H2S
D.e装置中产生的现象是固体由黑色变为红色
10.我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下。下列说法不正确的是( )
A.反应①的产物中含有水
B.汽油主要是C5~C11的烃类混合物
C.反应②中只有碳碳键形成
D.图中a的名称是2?甲基丁烷
11.下列装置应用于实验室进行相关实验,能达到实验目的的是
A.用装置甲在强光照条件下制取—氯甲烷
B.用装置乙分离苯和水
C.用装置丙蒸馏石油并收集60~150℃馏分
D.制备较纯净的—硝基苯
12.经过多方努力,郑州市的空气质量有明显改善。造成雾霾的重要原因之一是汽车尾气的排放,汽车加装尾气处理装置可以减少有害尾气的排放。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如下图所示。下列说法错误的是( )
A.NO2是该过程的中间产物
B.汽车尾气的主要污染成分为CO和NO
C.NO和O2必须在催化剂表面才能反应
D.该催化转化的总反应方程式:2NO+O2+4CO4CO2+N2
13.食品保鲜膜的材质有聚乙烯(PE)、聚氯乙烯(PVC)等种类。下列叙述错误的是( )
A.等质量的聚乙烯(PE)和乙烯完全燃烧消耗氧气的量相等
B.废弃的PE和PVC均可回收利用以减少白色污染
C.将PVC薄膜放入试管中加强热,产生的气体可使湿润的蓝色石蕊试纸变红
D.PVC的单体可由PE的单体与氯化氢加成制得
二、非选择题:本题包括4小题,共48分。
14.(12分)以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息回答下列问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是________(填字母)。
A.CH2===CH2+HClCH3CH2Cl
B.CH3CH2OH+HClCH3CH2Cl+H2O
C.CH3CH3+Cl2CH3CH2Cl+HCl
D.CH2===CHCl+H2CH3CH2Cl
由上述四个反应可归纳出,原子经济性最高的是______(填反应类型)。
(2)有毒物质的无害化处理也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,它可将废水中少量的CN-等有毒的酸根离子氧化而除去。请写出用ClO2将废水中的CN-氧化成无毒气体的离子方程式:__________________________________________________,
该方法的优点是___________________________________________________。
(3)某饮用水厂由天然水制备纯净水(去离子水)的工艺流程示意图如下:
活性炭的作用是_______________________________________________________;
O3消毒的优点是_______________________________________________________。
15.(10分)硫酸型酸雨的形成原理可简化表示如下:
回答下列问题:
(1)D物质的化学式__________________。
(2)反应②的化学方程式为______________________________________________。该反应___________(填“属于”或“不属于”)可逆反应。
(3)反应④的化学方程式为_________________________________________________。
(4)你认为减少酸雨产生可采用的措施是___________(填序号)。
①少用煤做燃料;②把工厂烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新能源
16.(14分)“环境就是民生,青山就是美丽,蓝天也是幸福。“拥有天蓝、地绿、水净的美好家园,是每个中国人的梦想。回答下列问题:
(1)排放到大气中的氮的氧化物,会造成___________污染。
(2)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。氨氨废水是造成河流及湖泊富营养化的主要因素。某氮肥厂产生的氨氮废水中的氮元素多以NH4+和NH3·H2O形式存在,为达到变废为宝回收利用的目的,某团队设计处理流程如下:
过程Ⅱ为硝化过程,在微生物的作用下实现NH4+→NO2—→NO3—的转化,在碱性条件下NH4+被氧气氧化成NO3—的总反应离子方程式为__________________________________。
过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇(CH3OH)实现HNO3→NO2—→N2的转化,将lmol NO2—完全转化为N2,转移的电子数为___________。
(3)磷酸生产及煤燃烧产生的废气SO2等会对大气造成污染。防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏。脱硫反应的化学方程式为___________________________________________。某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸___________吨(假设生产过程中96%SO2转化为SO3)。
17.(12分)可持续发展需要注意“环境保护”和“节约能源”。
(1)以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的主要气体是________;
(2)氮氧化物(NOx)是大气中的主要气态污染物之一、汽车尾气中含有NOx、CO和碳氢化合物等。汽车尾气净化装置里装有Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用韵机理如图所示。
尾气净纯装置中发生的总反应化学方程式为_____________________________________;
(3)工业废承需处理达标后才能排放,下列处理方法合理的是___________(填字母);
A.用中和法除去废水中的酸
B.用絮凝剂除去废水中的重金属离子
C.用氯气除去废水中的悬浮物
(4)饮用水钓消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一、漂白粉是常用的消毒剂,其有效成分是___________。Cl2是传统的自来水消毒剂,而ClO2是新型的自来水消毒剂,这两种消毒剂消毒完成后,氯元素均以Cl-形式存在。现要消毒1m3生活污水,分别用Cl2和ClO2来消毒处理,所耗这两种消毒剂的质量比为___________。(保留小数点后2位)
(人教版必修2)4.2资源的综合利用 环境保护》过关训练试题
(解析版)
(时间45分钟 满分100分)
一、单项选择题:本题包括13小题,每小题4分,共52分。
1.化学与生活、社会密切相关。下列说法不正确的是( )
A.利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境
B.凡含有食品添加剂的食物对人体健康均有害,不可食用
C.为防止电池中的重金属等污染土壤和水体,应积极开发废电池的综合利用技术
D.提倡人们购物时不用塑料袋,是为了防止白色污染
【答案】B
【解析】A.用太阳能等清洁能源代替化石燃料,有利于节约能源,减少污染物的排放,有利于环境保护,所以A选项是正确的;B.食品添加剂不全对人体有害,但对人体有害的应严格控制用量,并不是一盖杜绝,故B错误;C.废旧电池中含有汞、镉和铅等重金属元素,对人体有害,应积极开发废电池的综合利用技术,充分回收利用,所以C选项是正确的;D.塑料袋的主要分成为聚乙烯,难以降解,易导致白色污染,应控制使用,所以D选项是正确的。答案选B。
2.石油和煤都是重要的化石能源,下列有关石油和煤的叙述正确的是( )
A.都是纯净物 B.都含有碳元素
C.都是可再生能源 D.都有固定的沸点
【答案】B
【解析】煤、石油都属于不可再生能源,是混合物,没有固定的沸点,故B项正确。
3.下列关于煤和石油的说法正确的是
A.石油裂解的目的主要是为了得到更多的汽油
B.石油的分馏和煤的干馏都是物理变化
C.煤的气化就是将煤在高温条件由固态转化为气态的物理变化过程
D.工业上可以从煤的干馏产物中提取苯、甲苯等芳香烃
【答案】D
【解析】A.石油裂解的目的主要是为了获得乙烯、丙烯等基本化工原料,A错误;B.石油的分馏是物理变化,而煤的干馏是化学变化,B错误;C.煤的气化就是将煤在高温条件下与水蒸气反应转化为水煤气的化学变化过程,C错误;D.工业上可以从煤的干馏产物煤焦油中分离提取苯、甲苯等芳香烃,D正确;故答案为:D。
4.化学与科技、社会、环境密切相关。下列有关说法正确的是( )
A.pH小于7的雨水被称为酸雨
B.明矾溶于水可产生具有吸附性的胶体粒子,常用于饮用水的杀菌消毒
C.推广使用燃煤脱硫技术,主要是为了防治SO2污染
D.PM2.5是指大气中直径小于或等于2.5微米(2.5×10-6m)的细小可吸入颗粒物,其与空气形成的分散系属于胶体
【答案】C
【解析】A. pH小于5.6的雨水被称为酸雨,故A错误;B. 明矾常用于饮用水的净化,不能消毒,故B错误;C. 推广使用燃煤脱硫技术,减少SO2的排放,故C正确;D. PM2.5的直径大于胶体的直径,不属于胶体,故D错误;答案选C。
5.化学与能源开发、环境保护、资源利用等密切相关。下列说法正确的是( )
A.为提高农作物的产量和质量,应大量使用化肥和农药
B.绿色化学的核心是应用化学原理对环境污染进行治理
C.实现化石燃料清洁利用,就无需开发新能源
D.垃圾是放错地方的资源,应分类回收利用
【答案】D
【解析】A.化肥和农药虽然能提高农作物产量和质量,但会污染环境、影响人体健康,不能大量使用,A错误;B.绿色化学的核心是利用化学原理从源头上减少和消除对环境的污染,B错误;C.化石燃料属于不可再生能源,故仍需开发新能源缓解能源缺乏的问题,C错误;D.垃圾可分类回收利用,节约能源,D正确。答案选D。
6.常见的大气污染物分一次污染和二次污染。二次污染是排入环境中的一次污染物在物理、化学因素或生物作用下发生了变化,或与环境中的其他物质发生反应生成的新污染物;如2NO+O2=2NO2,则NO2就是二次污染物,由NO2导致的污染就是NO的二次污染。下列物质中:①SO2,②NO,③NO2,④HCl,⑤CO2。不易导致二次污染的是 ( )
A.①②③④⑤ B.①③⑤
C.④⑤ D.④
【答案】C
7.下列说法正确的是
A.煤的气化、液化和干馏都是物理变化
B.加热能杀死病毒,是因为蛋白质受热发生变性
C.石油裂解可以得到更多的汽油,这种汽油是一种纯净物
D.动物脂肪和稀硫酸混合加热,可得到肥皂的主要成分和甘油
【答案】B
【解析】A.煤的气化、液化和干馏过程中都产生了新的物质,因此发生的变化属于化学变化,A错误;B.加热能杀死病毒,是因为病毒主要是由蛋白质构成,蛋白质受热时会失去其生理活性而发生变性,B正确;C.石油裂解可以得到更多的汽油,这种汽油中含有多种烷烃和烯烃,因此是一种混合物,C错误;D.动物脂肪在碱性条件下加热会发生水解反应产生高级脂肪酸盐和甘油,高级脂肪酸盐是肥皂的主要成分,故油脂在碱性条件下的水解反应为皂化反应。而在酸性条件下水解产生的是高级脂肪酸和甘油,D错误;故合理选项是B。
8.下列说法正确的是( )
A.利用化石燃料燃烧放出的热量使水分解产生氢气,是氢能开发的研究方向
B.光合作用是将光能转化为化学能的有效途径
C.石油、煤、天然气属于二次能源
D.绿色化学最显著的特征是在生产化工产品过程中必须以绿色植物为原料
【答案】B
【解析】利用化石燃料燃烧法使水分解制氢气需要消耗大量的能源,A错误;光合作用是将光能转化为化学能的有效途径,B正确;石油、煤、天然气属于一次能源,C错误;绿色化学的核心是利用化学原理从源头上减少和消除工业生产对环境的污染,反应物的原子全部转化为期望的最终产物,D错误。
9.对煤干馏并检验其中部分产物,装置(夹持装置已略)如图所示。下列说法不正确的是( )
A.煤的干馏过程发生复杂的物理、化学变化
B.向b装置的水层中滴入紫色石蕊溶液,溶液变蓝
C.c装置可检验产生的气体中一定含有H2S
D.e装置中产生的现象是固体由黑色变为红色
【答案】C
【解析】煤干馏得到焦炉气、粗氨水、粗苯、煤焦油、焦炭,据此分析;A.煤的干馏是指将煤隔绝空气加强热使之分解的过程,发生复杂的物理、化学变化,得到焦炉气、粗氨水、粗苯、煤焦油、焦炭,故A说法正确;B.煤的干馏得到产物中含有NH3,氨水显碱性,能使紫色石蕊溶液变蓝,故B说法正确;C.焦炉气中含有乙烯,乙烯也能使酸性KMnO4溶液褪色,故C说法错误;D.焦炉气中含有H2、CH4、CO都能还原CuO,使黑色变为红色,故D说法正确;答案:C。
10.我国在CO2催化加氢制取汽油方面取得突破性进展,CO2转化过程示意图如下。下列说法不正确的是( )
A.反应①的产物中含有水
B.汽油主要是C5~C11的烃类混合物
C.反应②中只有碳碳键形成
D.图中a的名称是2?甲基丁烷
【答案】C
【解析】A. 反应①为二氧化碳和氢气反应生成一氧化碳和水,产物中含有水,故正确;B. 汽油是石油的分馏产物,主要是C5~C11的烃类混合物,故正确;C. 反应②中不仅有碳碳键形成,还有碳氢键形成,故错误;D. 图中a主链有4个碳原子,2号碳上有一个甲基,所以名称是2?甲基丁烷,故正确。故选C。
11.下列装置应用于实验室进行相关实验,能达到实验目的的是
A.用装置甲在强光照条件下制取—氯甲烷
B.用装置乙分离苯和水
C.用装置丙蒸馏石油并收集60~150℃馏分
D.制备较纯净的—硝基苯
【答案】B
【解析】A.甲在强光照条件下会爆炸,且制取可能为一氯甲烷、二氯甲烷等物质,A不能达到实验目的;B.苯不溶于水,苯与水的混合液有明显的分层,可以用分液漏斗分离苯和水,B能达到实验目的;C.石油分馏实验中,温度计测量蒸气的温度,因此温度计的水银球应在蒸馏烧瓶支管口处,C不能达到实验目的;D.苯、硝基苯相互溶解,则不能制备纯净的硝基苯,D不能达到实验目的;答案为B。
12.经过多方努力,郑州市的空气质量有明显改善。造成雾霾的重要原因之一是汽车尾气的排放,汽车加装尾气处理装置可以减少有害尾气的排放。在汽车尾气净化装置里,气体在催化剂表面吸附与解吸作用的过程如下图所示。下列说法错误的是( )
A.NO2是该过程的中间产物
B.汽车尾气的主要污染成分为CO和NO
C.NO和O2必须在催化剂表面才能反应
D.该催化转化的总反应方程式:2NO+O2+4CO4CO2+N2
【答案】C
【解析】A. 由题目提供的图可知:2NO+O2===2NO2,2NO2+4CO4CO2+N2,NO2是该过程的中间产物,故A正确;B. 汽油不完全燃烧可生成CO,空气中的氮气在气缸中放电条件下可生成NO,汽车尾气的主要污染成分是CO、NO、NO2等,故B正确;C. NO和O2在常温下就能反应生成NO2,故C错误;D. 该反应的反应物是NO、O2、CO,生成物是CO2、N2,反应条件是催化剂,所以该反应方程式2NO+O2+4CO4CO2+N2,故D正确。故选C。
13.食品保鲜膜的材质有聚乙烯(PE)、聚氯乙烯(PVC)等种类。下列叙述错误的是( )
A.等质量的聚乙烯(PE)和乙烯完全燃烧消耗氧气的量相等
B.废弃的PE和PVC均可回收利用以减少白色污染
C.将PVC薄膜放入试管中加强热,产生的气体可使湿润的蓝色石蕊试纸变红
D.PVC的单体可由PE的单体与氯化氢加成制得
【答案】D
【解析】乙烯、聚乙烯含碳量相同,等质量的聚乙烯(PE)和乙烯完全燃烧消耗氧气的量相等,故A正确;废弃的塑料回收利用以减少白色污染,故B正确;聚氯乙烯放入试管中加强热,产生的气体可生成氯化氢,故C正确;PE的单体是乙烯,乙烯与氯化氢加成生成一氯乙烷,PVC的单体是氯乙烯,故D错误。
二、非选择题:本题包括4小题,共48分。
14.(12分)以下是与绿色化学、环境保护和人类健康息息相关的三个主题,请根据已知信息回答下列问题:
(1)下列制备氯乙烷的反应中原子经济性最高的是________(填字母)。
A.CH2===CH2+HClCH3CH2Cl
B.CH3CH2OH+HClCH3CH2Cl+H2O
C.CH3CH3+Cl2CH3CH2Cl+HCl
D.CH2===CHCl+H2CH3CH2Cl
由上述四个反应可归纳出,原子经济性最高的是______(填反应类型)。
(2)有毒物质的无害化处理也是绿色化学研究的内容之一。ClO2是一种性能优良的消毒剂,它可将废水中少量的CN-等有毒的酸根离子氧化而除去。请写出用ClO2将废水中的CN-氧化成无毒气体的离子方程式:__________________________________________________,
该方法的优点是___________________________________________________。
(3)某饮用水厂由天然水制备纯净水(去离子水)的工艺流程示意图如下:
活性炭的作用是_______________________________________________________;
O3消毒的优点是_______________________________________________________。
【答案】(1)AD 加成反应
(2)2ClO2+2CN-===2CO2+N2+2Cl- 产物为无毒无害的Cl-、CO2和N2
(3)吸附水中的有机物(或除去水中的异味) 反应产物无毒无害
【解析】 (1)原子经济性高,即理论上原子的利用率尽可能达到100%,没有副产物。A、D两项中的原子利用率都是100%。(2)把CN-氧化成无毒气体,说明C、N分别生成了CO2、N2,ClO2的还原产物应该是无毒的Cl-。(3)活性炭能吸附水中的有机物,从而除去异味。用O3消毒时,其产物为无毒无害的O2。
15.(10分)硫酸型酸雨的形成原理可简化表示如下:
回答下列问题:
(1)D物质的化学式__________________。
(2)反应②的化学方程式为______________________________________________。该反应___________(填“属于”或“不属于”)可逆反应。
(3)反应④的化学方程式为_________________________________________________。
(4)你认为减少酸雨产生可采用的措施是___________(填序号)。
①少用煤做燃料;②把工厂烟囱造高;③燃料脱硫;④在已酸化的土壤中加石灰;⑤开发新能源
【答案】(1)H2SO3 (2)2SO2+O22SO3 属于
(3)SO2+H2OH2SO3 (4)①③⑤
【解析】硫酸型酸雨的形成原理:含硫燃料燃烧生成A物质主要成分为二氧化硫,二氧化硫在空气中被进一步氧化生成B为三氧化硫,三氧化硫与水反应生成C为硫酸,为酸雨成分之一;二氧化硫与水反应生成D为亚硫酸,亚硫酸在空气中被氧化生成硫酸。(1)D物质为亚硫酸,其化学式为H2SO3;(2)反应②是二氧化硫被空气中的氧气氧化生成三氧化硫,反应的化学方程式为2SO2+O22SO3;该反应属于可逆反应;(3)反应④是二氧化硫与水反应生成亚硫酸,反应的化学方程式为SO2+H2OH2SO3;(4) 少用煤作燃料、燃料脱硫、开发新的能源等措施可以减少二氧化硫气体的排放,从而减少酸雨的形成;
答案为①③⑤。
16.(14分)“环境就是民生,青山就是美丽,蓝天也是幸福。“拥有天蓝、地绿、水净的美好家园,是每个中国人的梦想。回答下列问题:
(1)排放到大气中的氮的氧化物,会造成___________污染。
(2)化肥、炼油、稀土、钢铁等工业都会排放出高浓度的氨氮废水。氨氨废水是造成河流及湖泊富营养化的主要因素。某氮肥厂产生的氨氮废水中的氮元素多以NH4+和NH3·H2O形式存在,为达到变废为宝回收利用的目的,某团队设计处理流程如下:
过程Ⅱ为硝化过程,在微生物的作用下实现NH4+→NO2—→NO3—的转化,在碱性条件下NH4+被氧气氧化成NO3—的总反应离子方程式为__________________________________。
过程Ⅲ为反硝化过程,向一定条件下的废水中加入甲醇(CH3OH)实现HNO3→NO2—→N2的转化,将lmol NO2—完全转化为N2,转移的电子数为___________。
(3)磷酸生产及煤燃烧产生的废气SO2等会对大气造成污染。防止工业煤燃烧产生SO2,常向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏。脱硫反应的化学方程式为___________________________________________。某硫酸化工厂,使用一种含杂质为25%的黄铁矿石(FeS2)为原料。若取2吨该矿石,可制得98%的浓硫酸___________吨(假设生产过程中96%SO2转化为SO3)。
【答案】(1)光化学烟雾 (2)NH4++2OH-+2O2 NO3—+3H2O (3)3NA (4)2SO2+O2+2CaCO3=2CaSO4+2CO2 (5) 2.4
【解析】(1)排放到大气中的氮的氧化物,会造成光化学烟雾污染;(2)在碱性条件下 NH4+被氧气氧化成NO3—的总反应离子方程式为: NH4++2OH-+2O2 NO3—+3H2O;将lmol完全转化为N2时,NO2—的氮元素由为+3价转化为N2中的 0价,根据原子守恒可知转移的电子数为3mol,即转移的电子数为3NA,(3)①向燃煤中加入CaCO3浆状物进行脱硫,脱硫的产物用于制造石膏,说明煤燃烧产生SO2和CaCO3反应生成了石膏CaSO4,反应的方程式为:2SO2+O2+2CaCO3=2CaSO4+2CO2;②依据反应前后硫元素质量不变可知:FeS2~2SO2~2SO3~2H2SO4,设制备浓硫酸的质量为m,生产过程中96%SO2转化为SO3,则
,
,解得。
17.(12分)可持续发展需要注意“环境保护”和“节约能源”。
(1)以煤炭为主的能源结构易导致酸雨的形成,形成这类酸雨的主要气体是________;
(2)氮氧化物(NOx)是大气中的主要气态污染物之一、汽车尾气中含有NOx、CO和碳氢化合物等。汽车尾气净化装置里装有Pd等过渡元素的催化剂,气体在催化剂表面吸附与解吸作用韵机理如图所示。
尾气净纯装置中发生的总反应化学方程式为_____________________________________;
(3)工业废承需处理达标后才能排放,下列处理方法合理的是___________(填字母);
A.用中和法除去废水中的酸
B.用絮凝剂除去废水中的重金属离子
C.用氯气除去废水中的悬浮物
(4)饮用水钓消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一、漂白粉是常用的消毒剂,其有效成分是___________。Cl2是传统的自来水消毒剂,而ClO2是新型的自来水消毒剂,这两种消毒剂消毒完成后,氯元素均以Cl-形式存在。现要消毒1m3生活污水,分别用Cl2和ClO2来消毒处理,所耗这两种消毒剂的质量比为___________。(保留小数点后2位)
【答案】(1)SO2 (2)2NO+O2+4CON2+4CO2 (3) A
(4) Ca(ClO)2 2.63∶1
【解析】(1)煤炭中的硫燃烧会生成二氧化硫,空气中的二氧化硫气体会在粉尘作催化剂的条件下反应生成三氧化硫,三氧化硫再与雨水形成酸雨,形成这类酸雨的主要气体是SO2;(2)由图可知,反应Ⅰ为2NO+O2=2NO2,反应Ⅱ为2NO2+4CON2+4CO2,Ⅰ+Ⅱ得到2NO+O2+4CON2+4CO2;(3)A.中和法适用于除去废水中的酸,所以用中和法除去废水中的酸,故A符合题意;B.用混凝剂如明矾等除去废水中的悬浮物,用沉淀法除去废水中的重金属离子,故B不符合题意;C.用混凝剂如明矾等除去废水中的悬浮物,氯气能消毒杀菌,但不能除去悬浮物,故C不符合题意;答案为A;(4)漂白粉的主要成分是CaCl2、Ca(ClO)2,有效成分是Ca(ClO)2;用Cl2消毒处理,转移2mol电子时消耗消毒剂Cl2的质量为71g,转移1mol电子时消耗消毒剂Cl2的质量为35.5g,ClO2来消毒处理,转移5mol电子时消耗消毒剂Cl2的质量为67.5g,转移1mol电子时消耗消毒剂ClO2的质量为13.5g,要消毒1m3生活污水,转移相同物质的量的电子消耗消毒剂Cl2和ClO2的质量比为:35.5g∶13.5g=2.63∶1。
