云南省峨山县高中2020-2021学年高一下学期6月月考化学试题 Word版含答案
文档属性
| 名称 | 云南省峨山县高中2020-2021学年高一下学期6月月考化学试题 Word版含答案 |  | |
| 格式 | docx | ||
| 文件大小 | 152.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-18 06:36:00 | ||
图片预览


文档简介
峨山县高中12357100124587002020-2021学年高一年级下学期6月考试
化学试卷
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
共100分。考试时间90分钟。
注意事项:1.答卷Ⅰ前,考生务必将自己的姓名、考号、科目用2B铅笔填涂在答题卡上。
2.答卷Ⅰ时,每小题选出答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案。不能答在试题卷上。
第Ⅰ卷选择题(共56分)
一、选择题(本题包括28小题,每小题2分,共56分。每小题只有一个选项符合题意)
1. 下列做法会对人体健康造成危害的是
A. 用食醋清洗热水瓶胆内壁附着的水垢 B. 用硅胶作袋装食品的干燥剂
C. 食用由SO2漂白的银耳 D. 用碘酒对伤口进行消毒
2. 危险化学品往往在包装上贴有警告标志。下列物质应贴有“腐蚀品”的是
A. 天然气 B. 浓硫酸 C. 石灰石 D. 汽油
3. 当光束通过下列分散系时,能观察到丁达尔效应的是
A. 蒸馏水 B. 盐酸 C. NaCl 溶液 D. Fe (OH)3 胶体
4. 关于反应2Na+2H2O=2NaOH+H2↑的说法错误的是
A. Na失去电子被氧化 B. Na作还原剂
C. H2O得到电子被还原 D. H2O发生氧化反应
5. 在某人尿液中加入新制氢氧化铜,加热后产生砖红色沉淀,说明该人尿液中有
A. 葡萄糖 B. 油脂 C. 蛋白质 D. 氯化钠
6. 下列对物质的分类正确的是
A. 纯碱属于碱 B. CuSO4·5H2O属于盐
C. H2CO3属于有机物 D. 蔗糖属于电解质
7. 下列属于同位素的是
A. 金刚石和石墨 B. false和false
C. 14C和14N D. 异丁烷和正戊烷
8. “绿色化学”的核心是利用化学原理从源头上减少和消除工业生产对环境的污染。下列属于“绿色化学”的是
A. 废弃塑料的回收和利用 B. 污水的治理
C. 在已酸化的土壤中加熟石灰 D. 氢能源代替化石能源
9. 下列物质含有离子键的是
A. NaCl B. CO2 C. Cl2 D. Ar
10. 下列属于加成反应的是
A. 苯与溴反应生成溴苯 B. 甲烷与氯气反应生成一氯甲烷
C. 乙烯与氯化氢反应生成氯乙烷 D. 淀粉水解生成葡萄糖
11. 决定化学反应速率的主要因素是
A. 反应物本身的性质 B. 催化剂
C. 温度及反应物的状态 D. 反应物的浓度
12. 下图为铜锌原电池示意图。下列有关说法正确的是
A. 负极发生还原反应 B. 正极发生反应为Cu-2e-=Cu2+
C. 电流由锌片通过导线流向铜片 D. 锌是负极,其质量逐渐减小
13. 某溶液中存在大量的H+、Cl-、SOfalse,该溶液中还可能大量存在的是
A. HCOfalse B. Ba2+ C. Ag+ D. Al3+
14. 下列反应中,反应物总能量低于生成物总能量的是
A. 煤的燃烧 B. 铝粉和盐酸的反应
C. 盐酸和氢氧化钠的反应 D. 氢氧化钡晶体和氯化铵晶体的反应
15. 下列物质的变化,不能通过一步化学反应完成的是
A. S→SO2 B. SiO2→H2SiO3 C. Na2O2→Na2CO3 D. SiO2→Na2SiO3
16. 下列说法正确的是
A. 摩尔是一种物理量 B. CO2的摩尔质量是44 g
C. 500 mL0.1 mol/LNaOH溶液中含有溶质2 g D. 标准状况下的气体摩尔体积约为22.4 L
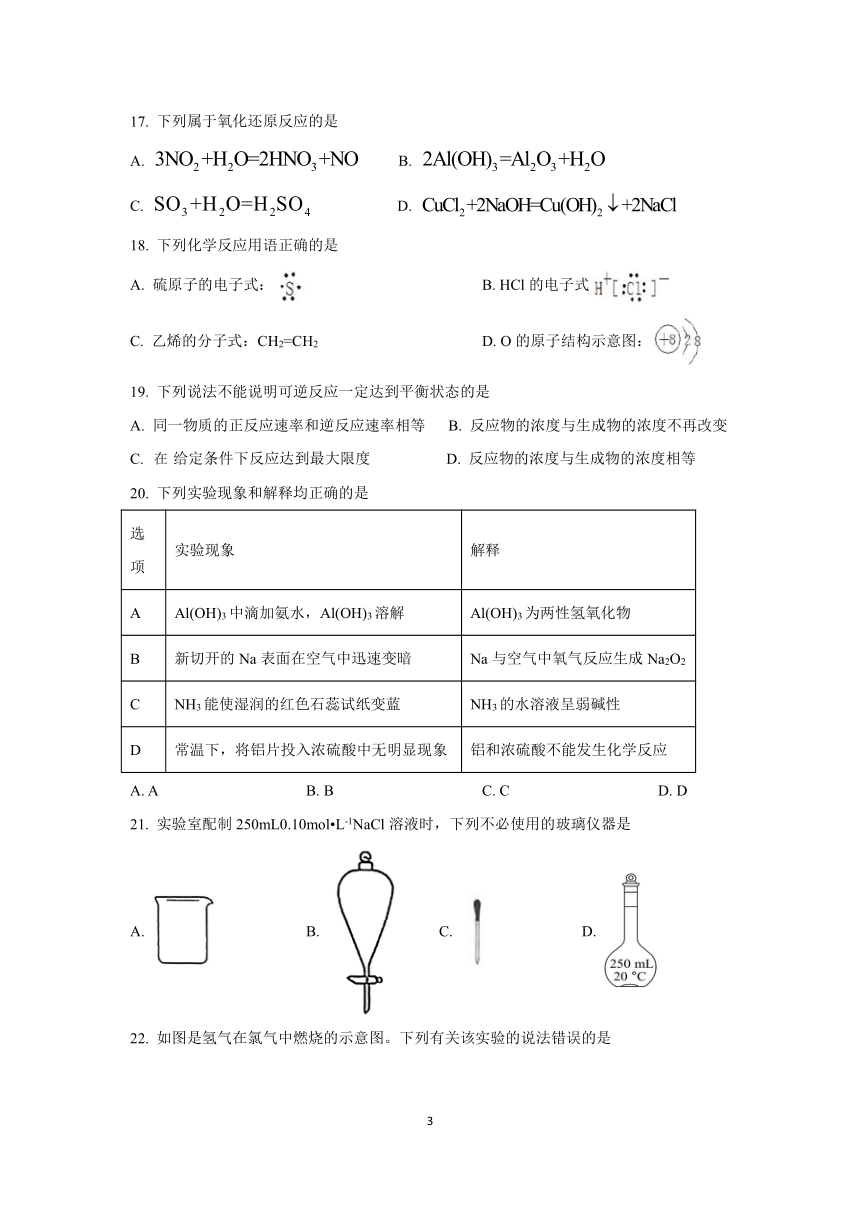
17. 下列属于氧化还原反应的是
A. false B. false
C. false D. false
18. 下列化学反应用语正确的是
A. 硫原子的电子式: B. HCl的电子式
C. 乙烯的分子式:CH2=CH2 D. O的原子结构示意图:
19. 下列说法不能说明可逆反应一定达到平衡状态的是
A. 同一物质的正反应速率和逆反应速率相等 B. 反应物的浓度与生成物的浓度不再改变
C. 给定条件下反应达到最大限度 D. 反应物的浓度与生成物的浓度相等
20. 下列实验现象和解释均正确的是
选项
实验现象
解释
A
Al(OH)3中滴加氨水,Al(OH)3溶解
Al(OH)3为两性氢氧化物
B
新切开的Na表面在空气中迅速变暗
Na与空气中氧气反应生成Na2O2
C
NH3能使湿润的红色石蕊试纸变蓝
NH3的水溶液呈弱碱性
D
常温下,将铝片投入浓硫酸中无明显现象
铝和浓硫酸不能发生化学反应
A. A B. B C. C D. D
21. 实验室配制250mL0.10mol?L-1NaCl溶液时,下列不必使用的玻璃仪器是
A. B. C. D.
22. 如图是氢气在氯气中燃烧的示意图。下列有关该实验的说法错误的是
A. 集气瓶中氯气呈黄绿色 B. 氧气在氯气中燃烧火焰呈淡蓝色
C. 燃烧过程中集气瓶口会产生大量白雾 D. 该实验能充分说明燃烧不一定有氧气参加
23. 考古时常利用falseC测定一些文物的年代。下列关于falseC的说法错误的是
A. 原子序数为6 B. 质量数为14
C. 核外电子数8 D. 中子数为8
24. “一带一路”分别指的是“丝绸之路经济带”和“21世纪海上丝绸之路”,丝绸的主要成分是
A. 糖类 B. 蛋白质 C. 油脂 D. 无机盐
25. 如图所示,将盛有甲烷和氯气混合气体的大试管倒立于饱和食盐水中,放置在光亮处(避免日光直射)。有关该实验的说法错误的是
A. 试管内的反应是加成反应 B. 试管内壁会产生油状液滴
C. 该反应的生成物是混合物 D. 试管内的液面会逐渐上升
26. 一定条件下,在一密闭容器中进行的反应3H2(g)+N2(g) ?2NH3(g)达到最大限度时,下列说法正确的是
A. 反应已经停止 B. H2和N2已经全部转化成NH3
C. 正反应速率和逆反应速率不相等 D. 反应混合物中各组分的浓度不再变化
27. 实验室现有已经配好的NH4Cl、AlCl3和Na2SO4三种无色溶液,因为没有及时贴上标签而无法使用,现在需要进行鉴别。下列试剂能将以上三种溶液一次性鉴别出来的是
A. NaOH B. H2SO4 C. AgNO3 D. BaCl2
28. 常温常压下,取下列四种有机物各1mol,分别在足量的氧气中燃烧,消耗氧气最多是
A.C2H5OH B.CH4 C.C2H4O D.C3H8
非选择题(共44分)
二、非选择题(本大题包括5小题,共44分)
29.(12分) 元素周期表的建立是化学发展史上重要的里程碑之一,它揭示了元素之间的内在联系。如图是元素周期表的短周期示意图,相应方格中每个序号代表处于该位置的一种元素。
请回答下列问题:
(1)元素①的名称为__ _。
(2)元素③的最高价氧化物的水化物为__ _(填化学式)
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是__ _(填化学式)。
(4)②和④两种元素形成的常见气态化合物中化学键类型为__ _。
(5)⑤和⑦两种元素形成的化合物的电子式为__ _。
(6) ⑦的单质与⑤的最高价氧化物对应水化物反应的化学方程式为 。
30. (8分)A,B,C,D是中学化学的常见物质。已知:①A为黄绿色气体,B为金属单质;②A与B化合生成C,C的水溶液遇KSCN溶液呈红色;③A与氢气反应生成D,请回答:
(1)C的化学式为___________;
(2)单质A可以用于制取漂白粉,漂白粉的有效成分为________ (填名称);
(3)D与NH3反应的化学方程式是_________ ;
(4)B与C的水溶液反应的离子方程式为_________ _。
31. (10分)A-F六种常见有机物的转化关系如图所示。其中A是一种植物生长调节剂,其产量可以衡量一个国家石油工业发展水平;F是一种高分子化合物,可以用来制造多种包装材料。
请回答下列问题:
(1)C的名称为__ _。
(2)E的结构简式为__ _。
(3)B与C反应生成D的反应类型为__ _。
(4)由A生成F的化学方程式为__ _。
(5)请写出物质B的一种用途:__ _。
32. (10分)某研究性学习小组为了探究温度对H2O2分解速率的影响,设计了如图所示的实验装置反应温度通过调节水浴温度来控制(导管体积忽略不计)。
请回答下列问题:
(1)仪器A的名称是___ 。
(2)实验开始时,需要先向A中滴加1-2滴FeCl3溶液,FeCl3溶液的作用是__ 。
(3)实验开始后装置A中发生反应的化学方程式为__ _。
(4)该实验中判断不同温度下H2O2分解速率快慢的依据是_ __。
(5)相同条件下进行该实验,反应速率总是随着时间的推移而逐渐减慢。速率减慢的原因是__ 。
33. (4分)一定量的Cu与足量浓硫酸混合加热,充分反应后生成2.24LSO2气体(标准状况下),反应后溶液体积为500mL。试计算:
(1)参加反应的Cu的质量?
(2)反应后溶液中CuSO4的物质的量浓度?
峨山县高中2020-2021学年高一年级下学期6月考试
化学试卷参考答案
第Ⅰ卷选择题(共56分)
一、选择题(本题包括28小题,每小题2分,共56分。每小题只有一个选项符合题意)
1. C 2. B 3. D 4. D 5. A 6. B 7. B 8. D 9. A 10. C 11. A 12. D 13. D 14. D 15. B 16. C 17. A 18. A 19. D 20. C 21. B 22. B 23. C 24. B 25. A 26. D 27. A 28. D
非选择题(共44分)
二、非选择题(本大题包括5小题,共44分)
29.(12分)
(1). 氢 (2). HNO3 (3). HCl (4). 极性共价键 (5).
(6) Cl2 + 2NaOHNaCl + NaClO + H2O
30. (8分)
(1). FeCl3 (2). 次氯酸钙 (3). HCl+NH3=NH4Cl (4). Fe+2Fe3+=3Fe2+
31.
(1). 乙酸 (2). CH3CHO (3). 取代反应(或酯化反应) (4). nCH2=CH2false (5). 杀菌消毒
32.
(1). 锥形瓶 (2). 作催化剂(或加快H2O2分解速率) (3). 2H2O2false2H2O+O2↑ (4). 单位时间内生成气体的体积(或A中产生气泡的速率) (5). H2O2浓度逐渐减小,分解速率逐渐减慢
33.
(1). 6.4g (2). 0.2mol/L
化学试卷
本试卷分第Ⅰ卷(选择题)和第Ⅱ卷(非选择题)两部分。
共100分。考试时间90分钟。
注意事项:1.答卷Ⅰ前,考生务必将自己的姓名、考号、科目用2B铅笔填涂在答题卡上。
2.答卷Ⅰ时,每小题选出答案后,用铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡皮擦干净后,再选涂其他答案。不能答在试题卷上。
第Ⅰ卷选择题(共56分)
一、选择题(本题包括28小题,每小题2分,共56分。每小题只有一个选项符合题意)
1. 下列做法会对人体健康造成危害的是
A. 用食醋清洗热水瓶胆内壁附着的水垢 B. 用硅胶作袋装食品的干燥剂
C. 食用由SO2漂白的银耳 D. 用碘酒对伤口进行消毒
2. 危险化学品往往在包装上贴有警告标志。下列物质应贴有“腐蚀品”的是
A. 天然气 B. 浓硫酸 C. 石灰石 D. 汽油
3. 当光束通过下列分散系时,能观察到丁达尔效应的是
A. 蒸馏水 B. 盐酸 C. NaCl 溶液 D. Fe (OH)3 胶体
4. 关于反应2Na+2H2O=2NaOH+H2↑的说法错误的是
A. Na失去电子被氧化 B. Na作还原剂
C. H2O得到电子被还原 D. H2O发生氧化反应
5. 在某人尿液中加入新制氢氧化铜,加热后产生砖红色沉淀,说明该人尿液中有
A. 葡萄糖 B. 油脂 C. 蛋白质 D. 氯化钠
6. 下列对物质的分类正确的是
A. 纯碱属于碱 B. CuSO4·5H2O属于盐
C. H2CO3属于有机物 D. 蔗糖属于电解质
7. 下列属于同位素的是
A. 金刚石和石墨 B. false和false
C. 14C和14N D. 异丁烷和正戊烷
8. “绿色化学”的核心是利用化学原理从源头上减少和消除工业生产对环境的污染。下列属于“绿色化学”的是
A. 废弃塑料的回收和利用 B. 污水的治理
C. 在已酸化的土壤中加熟石灰 D. 氢能源代替化石能源
9. 下列物质含有离子键的是
A. NaCl B. CO2 C. Cl2 D. Ar
10. 下列属于加成反应的是
A. 苯与溴反应生成溴苯 B. 甲烷与氯气反应生成一氯甲烷
C. 乙烯与氯化氢反应生成氯乙烷 D. 淀粉水解生成葡萄糖
11. 决定化学反应速率的主要因素是
A. 反应物本身的性质 B. 催化剂
C. 温度及反应物的状态 D. 反应物的浓度
12. 下图为铜锌原电池示意图。下列有关说法正确的是
A. 负极发生还原反应 B. 正极发生反应为Cu-2e-=Cu2+
C. 电流由锌片通过导线流向铜片 D. 锌是负极,其质量逐渐减小
13. 某溶液中存在大量的H+、Cl-、SOfalse,该溶液中还可能大量存在的是
A. HCOfalse B. Ba2+ C. Ag+ D. Al3+
14. 下列反应中,反应物总能量低于生成物总能量的是
A. 煤的燃烧 B. 铝粉和盐酸的反应
C. 盐酸和氢氧化钠的反应 D. 氢氧化钡晶体和氯化铵晶体的反应
15. 下列物质的变化,不能通过一步化学反应完成的是
A. S→SO2 B. SiO2→H2SiO3 C. Na2O2→Na2CO3 D. SiO2→Na2SiO3
16. 下列说法正确的是
A. 摩尔是一种物理量 B. CO2的摩尔质量是44 g
C. 500 mL0.1 mol/LNaOH溶液中含有溶质2 g D. 标准状况下的气体摩尔体积约为22.4 L
17. 下列属于氧化还原反应的是
A. false B. false
C. false D. false
18. 下列化学反应用语正确的是
A. 硫原子的电子式: B. HCl的电子式
C. 乙烯的分子式:CH2=CH2 D. O的原子结构示意图:
19. 下列说法不能说明可逆反应一定达到平衡状态的是
A. 同一物质的正反应速率和逆反应速率相等 B. 反应物的浓度与生成物的浓度不再改变
C. 给定条件下反应达到最大限度 D. 反应物的浓度与生成物的浓度相等
20. 下列实验现象和解释均正确的是
选项
实验现象
解释
A
Al(OH)3中滴加氨水,Al(OH)3溶解
Al(OH)3为两性氢氧化物
B
新切开的Na表面在空气中迅速变暗
Na与空气中氧气反应生成Na2O2
C
NH3能使湿润的红色石蕊试纸变蓝
NH3的水溶液呈弱碱性
D
常温下,将铝片投入浓硫酸中无明显现象
铝和浓硫酸不能发生化学反应
A. A B. B C. C D. D
21. 实验室配制250mL0.10mol?L-1NaCl溶液时,下列不必使用的玻璃仪器是
A. B. C. D.
22. 如图是氢气在氯气中燃烧的示意图。下列有关该实验的说法错误的是
A. 集气瓶中氯气呈黄绿色 B. 氧气在氯气中燃烧火焰呈淡蓝色
C. 燃烧过程中集气瓶口会产生大量白雾 D. 该实验能充分说明燃烧不一定有氧气参加
23. 考古时常利用falseC测定一些文物的年代。下列关于falseC的说法错误的是
A. 原子序数为6 B. 质量数为14
C. 核外电子数8 D. 中子数为8
24. “一带一路”分别指的是“丝绸之路经济带”和“21世纪海上丝绸之路”,丝绸的主要成分是
A. 糖类 B. 蛋白质 C. 油脂 D. 无机盐
25. 如图所示,将盛有甲烷和氯气混合气体的大试管倒立于饱和食盐水中,放置在光亮处(避免日光直射)。有关该实验的说法错误的是
A. 试管内的反应是加成反应 B. 试管内壁会产生油状液滴
C. 该反应的生成物是混合物 D. 试管内的液面会逐渐上升
26. 一定条件下,在一密闭容器中进行的反应3H2(g)+N2(g) ?2NH3(g)达到最大限度时,下列说法正确的是
A. 反应已经停止 B. H2和N2已经全部转化成NH3
C. 正反应速率和逆反应速率不相等 D. 反应混合物中各组分的浓度不再变化
27. 实验室现有已经配好的NH4Cl、AlCl3和Na2SO4三种无色溶液,因为没有及时贴上标签而无法使用,现在需要进行鉴别。下列试剂能将以上三种溶液一次性鉴别出来的是
A. NaOH B. H2SO4 C. AgNO3 D. BaCl2
28. 常温常压下,取下列四种有机物各1mol,分别在足量的氧气中燃烧,消耗氧气最多是
A.C2H5OH B.CH4 C.C2H4O D.C3H8
非选择题(共44分)
二、非选择题(本大题包括5小题,共44分)
29.(12分) 元素周期表的建立是化学发展史上重要的里程碑之一,它揭示了元素之间的内在联系。如图是元素周期表的短周期示意图,相应方格中每个序号代表处于该位置的一种元素。
请回答下列问题:
(1)元素①的名称为__ _。
(2)元素③的最高价氧化物的水化物为__ _(填化学式)
(3)⑥和⑦两种元素的气态氢化物中稳定性较强的是__ _(填化学式)。
(4)②和④两种元素形成的常见气态化合物中化学键类型为__ _。
(5)⑤和⑦两种元素形成的化合物的电子式为__ _。
(6) ⑦的单质与⑤的最高价氧化物对应水化物反应的化学方程式为 。
30. (8分)A,B,C,D是中学化学的常见物质。已知:①A为黄绿色气体,B为金属单质;②A与B化合生成C,C的水溶液遇KSCN溶液呈红色;③A与氢气反应生成D,请回答:
(1)C的化学式为___________;
(2)单质A可以用于制取漂白粉,漂白粉的有效成分为________ (填名称);
(3)D与NH3反应的化学方程式是_________ ;
(4)B与C的水溶液反应的离子方程式为_________ _。
31. (10分)A-F六种常见有机物的转化关系如图所示。其中A是一种植物生长调节剂,其产量可以衡量一个国家石油工业发展水平;F是一种高分子化合物,可以用来制造多种包装材料。
请回答下列问题:
(1)C的名称为__ _。
(2)E的结构简式为__ _。
(3)B与C反应生成D的反应类型为__ _。
(4)由A生成F的化学方程式为__ _。
(5)请写出物质B的一种用途:__ _。
32. (10分)某研究性学习小组为了探究温度对H2O2分解速率的影响,设计了如图所示的实验装置反应温度通过调节水浴温度来控制(导管体积忽略不计)。
请回答下列问题:
(1)仪器A的名称是___ 。
(2)实验开始时,需要先向A中滴加1-2滴FeCl3溶液,FeCl3溶液的作用是__ 。
(3)实验开始后装置A中发生反应的化学方程式为__ _。
(4)该实验中判断不同温度下H2O2分解速率快慢的依据是_ __。
(5)相同条件下进行该实验,反应速率总是随着时间的推移而逐渐减慢。速率减慢的原因是__ 。
33. (4分)一定量的Cu与足量浓硫酸混合加热,充分反应后生成2.24LSO2气体(标准状况下),反应后溶液体积为500mL。试计算:
(1)参加反应的Cu的质量?
(2)反应后溶液中CuSO4的物质的量浓度?
峨山县高中2020-2021学年高一年级下学期6月考试
化学试卷参考答案
第Ⅰ卷选择题(共56分)
一、选择题(本题包括28小题,每小题2分,共56分。每小题只有一个选项符合题意)
1. C 2. B 3. D 4. D 5. A 6. B 7. B 8. D 9. A 10. C 11. A 12. D 13. D 14. D 15. B 16. C 17. A 18. A 19. D 20. C 21. B 22. B 23. C 24. B 25. A 26. D 27. A 28. D
非选择题(共44分)
二、非选择题(本大题包括5小题,共44分)
29.(12分)
(1). 氢 (2). HNO3 (3). HCl (4). 极性共价键 (5).
(6) Cl2 + 2NaOHNaCl + NaClO + H2O
30. (8分)
(1). FeCl3 (2). 次氯酸钙 (3). HCl+NH3=NH4Cl (4). Fe+2Fe3+=3Fe2+
31.
(1). 乙酸 (2). CH3CHO (3). 取代反应(或酯化反应) (4). nCH2=CH2false (5). 杀菌消毒
32.
(1). 锥形瓶 (2). 作催化剂(或加快H2O2分解速率) (3). 2H2O2false2H2O+O2↑ (4). 单位时间内生成气体的体积(或A中产生气泡的速率) (5). H2O2浓度逐渐减小,分解速率逐渐减慢
33.
(1). 6.4g (2). 0.2mol/L
同课章节目录
