2012新课标同步导学高一化学练习:4.2.2(苏教版必修1)
文档属性
| 名称 | 2012新课标同步导学高一化学练习:4.2.2(苏教版必修1) |

|
|
| 格式 | zip | ||
| 文件大小 | 498.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-04-11 21:29:30 | ||
图片预览

文档简介
(本栏目内容,在学生用书中以活页形式分册装订!)
一、选择题
1.氨水中存在的粒子有( )
①NH3 ②NH3·H2O ③H2O ④OH- ⑤NH ⑥H+
A.①②③④ B.②④⑤⑥
C.①②③④⑤ D.①②③④⑤⑥
【解析】 NH3+H2O??NH3·H2O??NH+OH-,H2O??H++OH-。
【答案】 D
2.(2009年徐州质检)气体甲能使湿润的红色石蕊试纸变蓝,气体乙可在空气中产生白雾,当甲与乙相遇时可能生成( )
A.NH4Cl B.NH4HCO3
C.(NH4)2CO3 D.(NH4)2SO4
【解析】 使湿润的红色石蕊试纸变蓝的气体为氨气,可在空气中产生白雾的气体是HCl,氨气与HCl相遇时生成NH4Cl。
【答案】 A
3.能把NH4NO3、KCl、(NH4)2SO4三瓶无色溶液加以区别(必要时可以加热)的一种试剂是( )
A.BaCl2 B.Ba(NO3)2
C.Ba(OH)2 D.NaOH
【解析】 加入Ba(OH)2有刺激性气味的气体产生的是NH4NO3;无明显现象的是KCl;有刺激性气味的气体产生,且有白色沉淀生成的是(NH4)2SO4。
【答案】 C
4.在一定浓度的BaCl2溶液中通入SO2气体,未见沉淀生成。若先通入另一种气体,然后再通入SO2气体,可生成白色沉淀,该气体是( )
A.Cl2 B.NH3
C.HCl D.CO2
【解析】 先通入Cl2再通入SO2会发生反应:Cl2+SO2+2H2O===H2SO4+2HCl,H2SO4+BaCl2===BaSO4↓+2HCl,产生BaSO4沉淀。先通入NH3再通入SO2会发生反应NH3+H2O??NH3·H2O,2NH3·H2O+SO2===(NH4)2SO3+2H2O,SO+Ba2+===BaSO3↓,产生BaSO3白色沉淀。
【答案】 AB
5.同温同压下,在3支相同体积的试管中分别充有等体积混合的2种气体,它们是①NO和NO2,②NO2和O2,③NH3和N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是( )
A.V1>V2>V3 B.V1>V3>V2
C.V2>V3>V1 D.V3>V1>V2
【解析】 本题考查学生利用氮的氧化物与H2O反应进行有关化学计算的能力。
假定各试管的容积均为2 L,则每种成分的体积为1 L。
①3NO2+H2O===2HNO3+NO
V1=1 L+ L= L
②4NO2+O2+2H2O===4HNO3
经判断知O2过量,V2=1 L- L= L
③NH3极易溶于水,N2难溶于水,最后剩余N2,故V3=1 L。所以V1>V3>V2。
【答案】 B
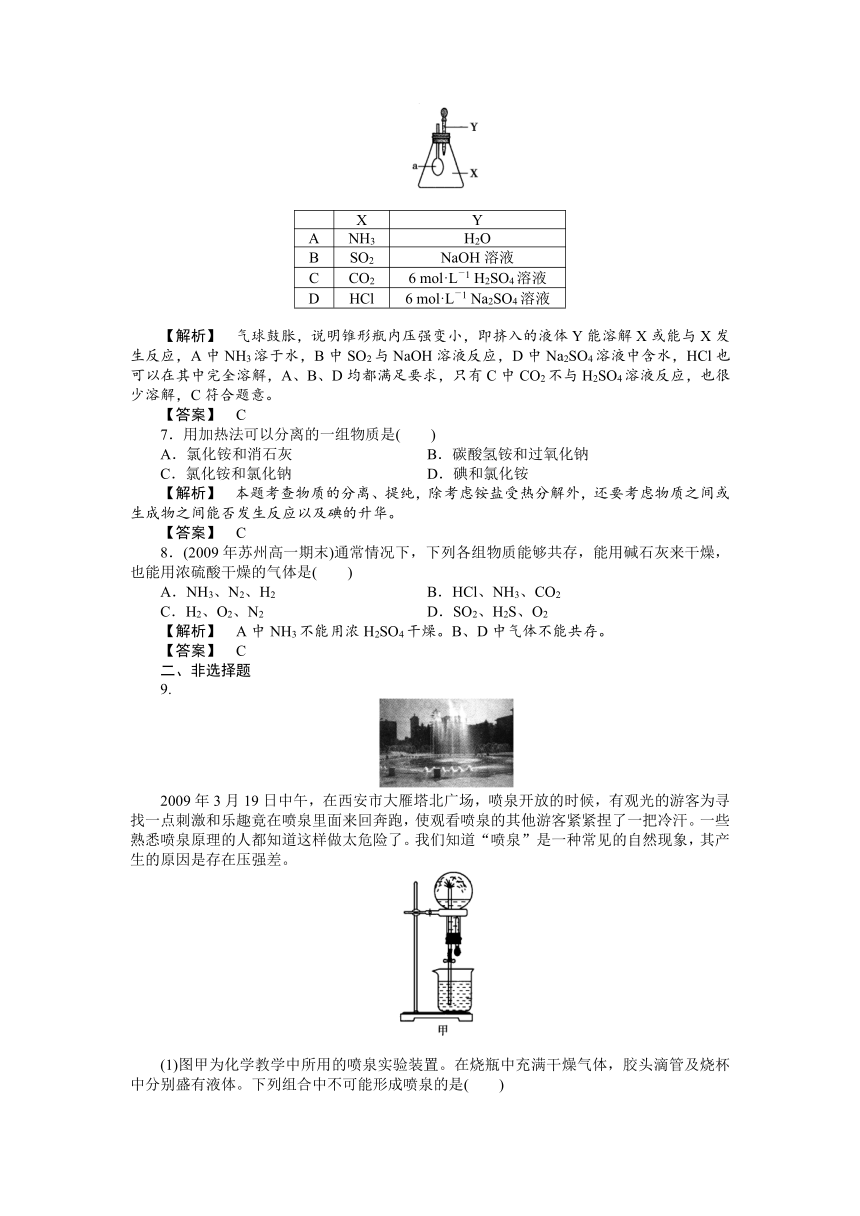
6.如下图所示,锥形瓶内盛有气体X,滴管内盛有液体Y。若挤压胶头滴管,使液体Y滴入锥形瓶中,振荡,过一会儿,可见小气球a鼓胀起来。气体X和液体Y不可能是( )
X Y
A NH3 H2O
B SO2 NaOH溶液
C CO2 6 mol·L-1 H2SO4溶液
D HCl 6 mol·L-1 Na2SO4溶液
【解析】 气球鼓胀,说明锥形瓶内压强变小,即挤入的液体Y能溶解X或能与X发生反应,A中NH3溶于水,B中SO2与NaOH溶液反应,D中Na2SO4溶液中含水,HCl也可以在其中完全溶解,A、B、D均都满足要求,只有C中CO2不与H2SO4溶液反应,也很少溶解,C符合题意。
【答案】 C
7.用加热法可以分离的一组物质是( )
A.氯化铵和消石灰 B.碳酸氢铵和过氧化钠
C.氯化铵和氯化钠 D.碘和氯化铵
【解析】 本题考查物质的分离、提纯,除考虑铵盐受热分解外,还要考虑物质之间或生成物之间能否发生反应以及碘的升华。
【答案】 C
8.(2009年苏州高一期末)通常情况下,下列各组物质能够共存,能用碱石灰来干燥,也能用浓硫酸干燥的气体是( )
A.NH3、N2、H2 B.HCl、NH3、CO2
C.H2、O2、N2 D.SO2、H2S、O2
【解析】 A中NH3不能用浓H2SO4干燥。B、D中气体不能共存。
【答案】 C
二、非选择题
9.
2009年3月19日中午,在西安市大雁塔北广场,喷泉开放的时候,有观光的游客为寻找一点刺激和乐趣竟在喷泉里面来回奔跑,使观看喷泉的其他游客紧紧捏了一把冷汗。一些熟悉喷泉原理的人都知道这样做太危险了。我们知道“喷泉”是一种常见的自然现象,其产生的原因是存在压强差。
(1)图甲为化学教学中所用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是( )
A.HCl和H2O B.O2和H2O
C.NH3和H2O D.CO2和NaOH溶液
(2)某学生积极思考产生喷泉的其他办法,并设计了如图乙所示装置。
在图乙的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是________。
A.Cu与稀盐酸
B.NaHCO3与NaOH溶液
C.CaCO3与稀硫酸
D.NH4HCO3与稀盐酸
【解析】 形成喷泉的可能原因或方法——烧瓶内压强减小而形成“喷泉”、锥形瓶中压强增大而产生压强差形成“喷泉”。
(1)
(2)
【答案】 (1)B (2)D
10.在标准状况下,用一定量的水吸收氨后制得浓度为12.0 mol/L、密度为0.915 g/cm3的氨水。试问1体积水吸收多少体积的氨才可制得上述氨水?
【解析】 1.00 L氨水中含NH3的质量为:12.0 mol/L×1.00 L×17.0 g/mol=204 g
则其在标准状况下的体积为:
12.0 mol×22.4 L/mol=268.8 L;
1.00 L该氨水中含水的质量为:
1.00 L×915 g/L-204 g=711 g;
则原来水的体积为=0.711 L
故==378,即1体积水吸收378体积的NH3(标准状况下)才可制得题给的氨水。
【答案】 378体积
11.某学生课外活动小组利用如下图所示装置分别做如下实验:
在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________溶液;加热时溶液由红色逐渐变浅的原因是:
________________________________________________________________________。
【解析】 解题的关键是要认真观察实验装置的特点:试管口上套有气球,说明加热时会有气体逸出(说明该物质不稳定),一下就使“红色溶液”的范围缩小:溶有酸性气体的石蕊溶液或溶有碱性气体的酚酞溶液。而前者在加热后,红色变为紫色,不符合“溶液颜色逐渐变浅”的条件,结论只有稀氨水和酚酞。
【答案】 稀氨水和酚酞 稀氨水中的NH3逸出,所以溶液的颜色变浅
12.(能力提高)(2009年全国理综Ⅱ)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
回答下列问题:
(1)A中加入的物质是________________________,发生反应的化学方程式是
________________________________________________________________________;
(2)B中加入的物质是____________,其作用是
________________________________________________________________________;
(3)实验时在C中观察到的现象是__________________,发生反应的化学方程式是________________________________________________________________________;
(4)实验时在D中观察到的现象是________________,D中收集到的物质是__________,检验该物质的方法和现象是
________________________________________________________________________。
【解析】 本题以氨气的实验室制法为载体,探究氨气还原氧化铜,并检验其产物。实验装置包括:气体发生装置→气体净化装置→氨气还原氧化铜装置→产物(1)收集装置→产物(2)收集装置。
(1)该制氨气装置属于“固(Ⅰ)+固(Ⅱ)气”装置,实验室选择氯化铵固体与消石灰反应,发生反应分别为:2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O。(2)装置中用干燥管干燥氨气,只能用固体干燥剂,干燥氨气用碱石灰、生石灰、固体氢氧化钠等碱性干燥剂,不能用酸性干燥剂五氧化二磷,也不能用氯化钙。(3)根据实验目的知,硬质试管C中的固体为氧化铜,发生反应:2NH3+3CuO3Cu+N2+3H2O,实验现象是黑色粉末逐渐变成红色粉末。(4)D装置中冰水温度保持在0 ℃,冷凝水蒸气,使试管D中的压强减小,E中的水倒吸进入D试管,氨气溶于水,故D装置收集到的是氨水。
【答案】 (1)固体NH4Cl和Ca(OH)2 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O(其他合理答案也可)
(2)碱石灰(或CaO) 除去NH3气流中的水蒸气
(3)黑色粉末部分逐渐变为红色 2NH3+3CuON2+3H2O+3Cu
(4)出现无色液体 氨水 用红色石蕊试纸检验、试纸变蓝,用无水硫酸铜检验、无水硫酸铜变蓝
.精品资料。欢迎使用。 ( http: / / www.21cnjy.com / " \o "欢迎登陆21世纪教育网 )
一、选择题
1.氨水中存在的粒子有( )
①NH3 ②NH3·H2O ③H2O ④OH- ⑤NH ⑥H+
A.①②③④ B.②④⑤⑥
C.①②③④⑤ D.①②③④⑤⑥
【解析】 NH3+H2O??NH3·H2O??NH+OH-,H2O??H++OH-。
【答案】 D
2.(2009年徐州质检)气体甲能使湿润的红色石蕊试纸变蓝,气体乙可在空气中产生白雾,当甲与乙相遇时可能生成( )
A.NH4Cl B.NH4HCO3
C.(NH4)2CO3 D.(NH4)2SO4
【解析】 使湿润的红色石蕊试纸变蓝的气体为氨气,可在空气中产生白雾的气体是HCl,氨气与HCl相遇时生成NH4Cl。
【答案】 A
3.能把NH4NO3、KCl、(NH4)2SO4三瓶无色溶液加以区别(必要时可以加热)的一种试剂是( )
A.BaCl2 B.Ba(NO3)2
C.Ba(OH)2 D.NaOH
【解析】 加入Ba(OH)2有刺激性气味的气体产生的是NH4NO3;无明显现象的是KCl;有刺激性气味的气体产生,且有白色沉淀生成的是(NH4)2SO4。
【答案】 C
4.在一定浓度的BaCl2溶液中通入SO2气体,未见沉淀生成。若先通入另一种气体,然后再通入SO2气体,可生成白色沉淀,该气体是( )
A.Cl2 B.NH3
C.HCl D.CO2
【解析】 先通入Cl2再通入SO2会发生反应:Cl2+SO2+2H2O===H2SO4+2HCl,H2SO4+BaCl2===BaSO4↓+2HCl,产生BaSO4沉淀。先通入NH3再通入SO2会发生反应NH3+H2O??NH3·H2O,2NH3·H2O+SO2===(NH4)2SO3+2H2O,SO+Ba2+===BaSO3↓,产生BaSO3白色沉淀。
【答案】 AB
5.同温同压下,在3支相同体积的试管中分别充有等体积混合的2种气体,它们是①NO和NO2,②NO2和O2,③NH3和N2。现将3支试管均倒置于水槽中,充分反应后,试管中剩余气体的体积分别为V1、V2、V3,则下列关系正确的是( )
A.V1>V2>V3 B.V1>V3>V2
C.V2>V3>V1 D.V3>V1>V2
【解析】 本题考查学生利用氮的氧化物与H2O反应进行有关化学计算的能力。
假定各试管的容积均为2 L,则每种成分的体积为1 L。
①3NO2+H2O===2HNO3+NO
V1=1 L+ L= L
②4NO2+O2+2H2O===4HNO3
经判断知O2过量,V2=1 L- L= L
③NH3极易溶于水,N2难溶于水,最后剩余N2,故V3=1 L。所以V1>V3>V2。
【答案】 B
6.如下图所示,锥形瓶内盛有气体X,滴管内盛有液体Y。若挤压胶头滴管,使液体Y滴入锥形瓶中,振荡,过一会儿,可见小气球a鼓胀起来。气体X和液体Y不可能是( )
X Y
A NH3 H2O
B SO2 NaOH溶液
C CO2 6 mol·L-1 H2SO4溶液
D HCl 6 mol·L-1 Na2SO4溶液
【解析】 气球鼓胀,说明锥形瓶内压强变小,即挤入的液体Y能溶解X或能与X发生反应,A中NH3溶于水,B中SO2与NaOH溶液反应,D中Na2SO4溶液中含水,HCl也可以在其中完全溶解,A、B、D均都满足要求,只有C中CO2不与H2SO4溶液反应,也很少溶解,C符合题意。
【答案】 C
7.用加热法可以分离的一组物质是( )
A.氯化铵和消石灰 B.碳酸氢铵和过氧化钠
C.氯化铵和氯化钠 D.碘和氯化铵
【解析】 本题考查物质的分离、提纯,除考虑铵盐受热分解外,还要考虑物质之间或生成物之间能否发生反应以及碘的升华。
【答案】 C
8.(2009年苏州高一期末)通常情况下,下列各组物质能够共存,能用碱石灰来干燥,也能用浓硫酸干燥的气体是( )
A.NH3、N2、H2 B.HCl、NH3、CO2
C.H2、O2、N2 D.SO2、H2S、O2
【解析】 A中NH3不能用浓H2SO4干燥。B、D中气体不能共存。
【答案】 C
二、非选择题
9.
2009年3月19日中午,在西安市大雁塔北广场,喷泉开放的时候,有观光的游客为寻找一点刺激和乐趣竟在喷泉里面来回奔跑,使观看喷泉的其他游客紧紧捏了一把冷汗。一些熟悉喷泉原理的人都知道这样做太危险了。我们知道“喷泉”是一种常见的自然现象,其产生的原因是存在压强差。
(1)图甲为化学教学中所用的喷泉实验装置。在烧瓶中充满干燥气体,胶头滴管及烧杯中分别盛有液体。下列组合中不可能形成喷泉的是( )
A.HCl和H2O B.O2和H2O
C.NH3和H2O D.CO2和NaOH溶液
(2)某学生积极思考产生喷泉的其他办法,并设计了如图乙所示装置。
在图乙的锥形瓶中,分别加入足量的下列物质,反应后可能产生喷泉的是________。
A.Cu与稀盐酸
B.NaHCO3与NaOH溶液
C.CaCO3与稀硫酸
D.NH4HCO3与稀盐酸
【解析】 形成喷泉的可能原因或方法——烧瓶内压强减小而形成“喷泉”、锥形瓶中压强增大而产生压强差形成“喷泉”。
(1)
(2)
【答案】 (1)B (2)D
10.在标准状况下,用一定量的水吸收氨后制得浓度为12.0 mol/L、密度为0.915 g/cm3的氨水。试问1体积水吸收多少体积的氨才可制得上述氨水?
【解析】 1.00 L氨水中含NH3的质量为:12.0 mol/L×1.00 L×17.0 g/mol=204 g
则其在标准状况下的体积为:
12.0 mol×22.4 L/mol=268.8 L;
1.00 L该氨水中含水的质量为:
1.00 L×915 g/L-204 g=711 g;
则原来水的体积为=0.711 L
故==378,即1体积水吸收378体积的NH3(标准状况下)才可制得题给的氨水。
【答案】 378体积
11.某学生课外活动小组利用如下图所示装置分别做如下实验:
在试管中注入某红色溶液,加热试管,溶液颜色逐渐变浅,冷却后恢复红色,则原溶液可能是________溶液;加热时溶液由红色逐渐变浅的原因是:
________________________________________________________________________。
【解析】 解题的关键是要认真观察实验装置的特点:试管口上套有气球,说明加热时会有气体逸出(说明该物质不稳定),一下就使“红色溶液”的范围缩小:溶有酸性气体的石蕊溶液或溶有碱性气体的酚酞溶液。而前者在加热后,红色变为紫色,不符合“溶液颜色逐渐变浅”的条件,结论只有稀氨水和酚酞。
【答案】 稀氨水和酚酞 稀氨水中的NH3逸出,所以溶液的颜色变浅
12.(能力提高)(2009年全国理综Ⅱ)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用示意图中的装置可以实现该反应。
回答下列问题:
(1)A中加入的物质是________________________,发生反应的化学方程式是
________________________________________________________________________;
(2)B中加入的物质是____________,其作用是
________________________________________________________________________;
(3)实验时在C中观察到的现象是__________________,发生反应的化学方程式是________________________________________________________________________;
(4)实验时在D中观察到的现象是________________,D中收集到的物质是__________,检验该物质的方法和现象是
________________________________________________________________________。
【解析】 本题以氨气的实验室制法为载体,探究氨气还原氧化铜,并检验其产物。实验装置包括:气体发生装置→气体净化装置→氨气还原氧化铜装置→产物(1)收集装置→产物(2)收集装置。
(1)该制氨气装置属于“固(Ⅰ)+固(Ⅱ)气”装置,实验室选择氯化铵固体与消石灰反应,发生反应分别为:2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O。(2)装置中用干燥管干燥氨气,只能用固体干燥剂,干燥氨气用碱石灰、生石灰、固体氢氧化钠等碱性干燥剂,不能用酸性干燥剂五氧化二磷,也不能用氯化钙。(3)根据实验目的知,硬质试管C中的固体为氧化铜,发生反应:2NH3+3CuO3Cu+N2+3H2O,实验现象是黑色粉末逐渐变成红色粉末。(4)D装置中冰水温度保持在0 ℃,冷凝水蒸气,使试管D中的压强减小,E中的水倒吸进入D试管,氨气溶于水,故D装置收集到的是氨水。
【答案】 (1)固体NH4Cl和Ca(OH)2 2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O(其他合理答案也可)
(2)碱石灰(或CaO) 除去NH3气流中的水蒸气
(3)黑色粉末部分逐渐变为红色 2NH3+3CuON2+3H2O+3Cu
(4)出现无色液体 氨水 用红色石蕊试纸检验、试纸变蓝,用无水硫酸铜检验、无水硫酸铜变蓝
.精品资料。欢迎使用。 ( http: / / www.21cnjy.com / " \o "欢迎登陆21世纪教育网 )
