人教版高中化学选修五2.1.3 炔烃 脂肪烃的来源及其应用 课件 (30张PPT)
文档属性
| 名称 | 人教版高中化学选修五2.1.3 炔烃 脂肪烃的来源及其应用 课件 (30张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 5.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-21 00:00:00 | ||
图片预览








文档简介
第二章 烃和卤代烃
2.1.3 炔烃
人教版 选修五
(一)炔烃的结构特点和通式
分子里含有碳碳三键的一类脂肪烃称为炔烃。
1. 概念:
2. 炔烃的通式:
(二)炔烃的物理性质:
CnH2n-2 (n≥2)
随着碳原子数的增多,沸点逐渐升高,液态时的密度逐渐增加,C原子数≤4时为气态。
炔烃
一
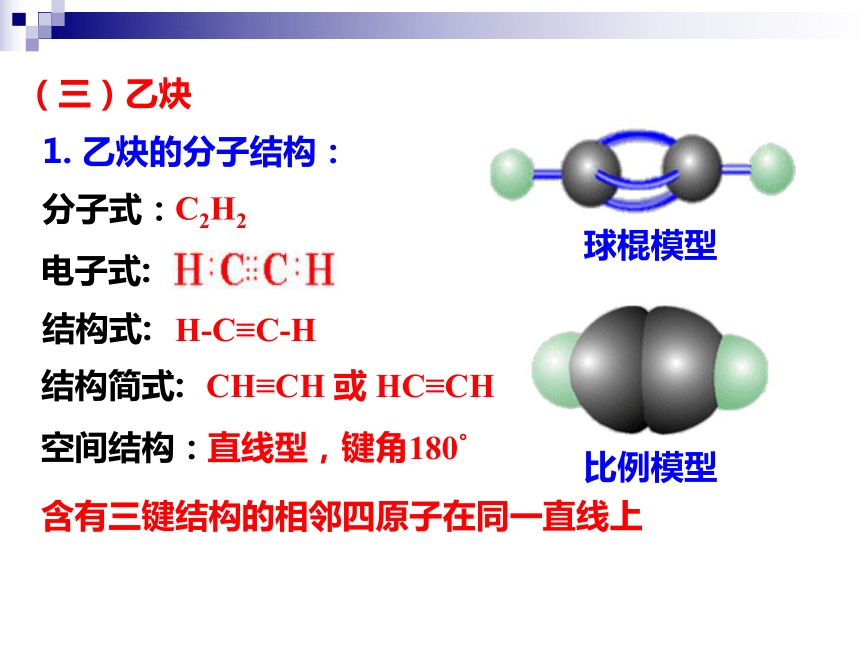
(三)乙炔
1. 乙炔的分子结构:
电子式:
H-C≡C-H
结构简式:
CH≡CH 或 HC≡CH
结构式:
直线型,键角180°
空间结构:
分子式:
C2H2
球棍模型
比例模型
含有三键结构的相邻四原子在同一直线上
在烯烃分子中如果双键碳上连接了两个不同的原子或原子团,将可以出现顺反异构,请问在炔烃分子中是否也存在顺反异构?
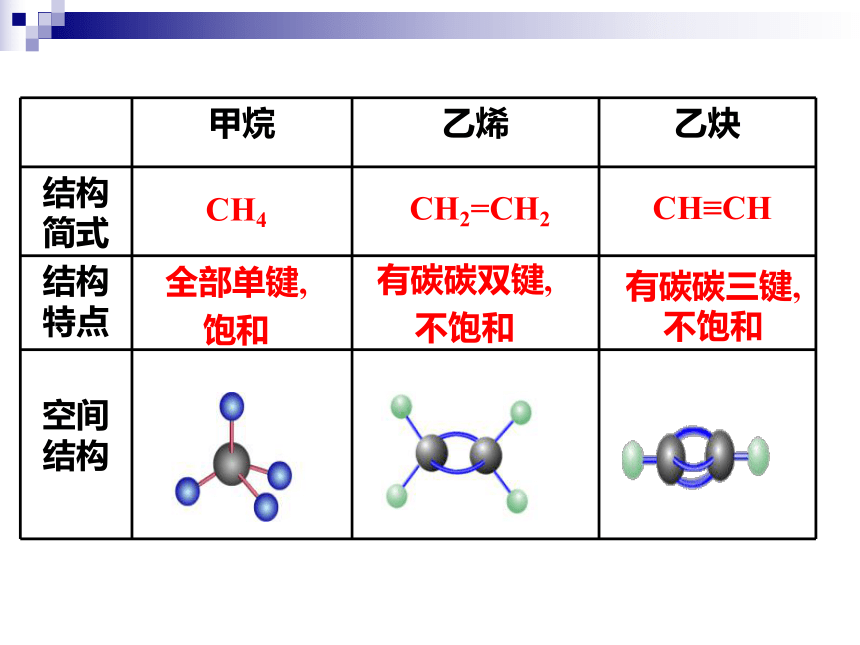
甲烷
乙烯
乙炔
结构简式
结构特点
空间结构
CH4
CH2=CH2
CH≡CH
全部单键,
饱和
有碳碳双键,
不饱和
有碳碳三键,不饱和
1. 描述CH3—CH=CH—C≡C—CF3分子结构的下列叙述中,正确的是( )
A、6个碳原子有可能在同一直线上
B、6个碳原子有可能在同一平面上
C、6个碳原子不可能在同一直线上
D、6个碳原子不可能在同一平面上
H
H
C=C
H3C
C = C— CF3
(2) 乙炔的实验室制法
CaC2+2H2O C2H2↑+Ca(OH)2
②反应原理:
① 原料:电石(CaC2)与 H2O
2. 乙炔的制法
(1) 工业制法
——甲烷裂解法
2CH4 CH≡CH +3H2
1500 ℃
碳化钙
反应装置
③装置特点:
i. 装置不能用启普发生器,改用分液漏斗
ii. 实验中常用饱和食盐水代替水
固体 +液体 气体
a. 碳化钙与水反应较剧烈,难以控反制应速率;
b. 放出的大量热量,操作不当会使启普发生器炸裂。
降低水的含量,得到平稳的乙炔气流。
启普发生器
c. 生成的Ca(OH)2呈糊状容易堵塞球型漏斗。
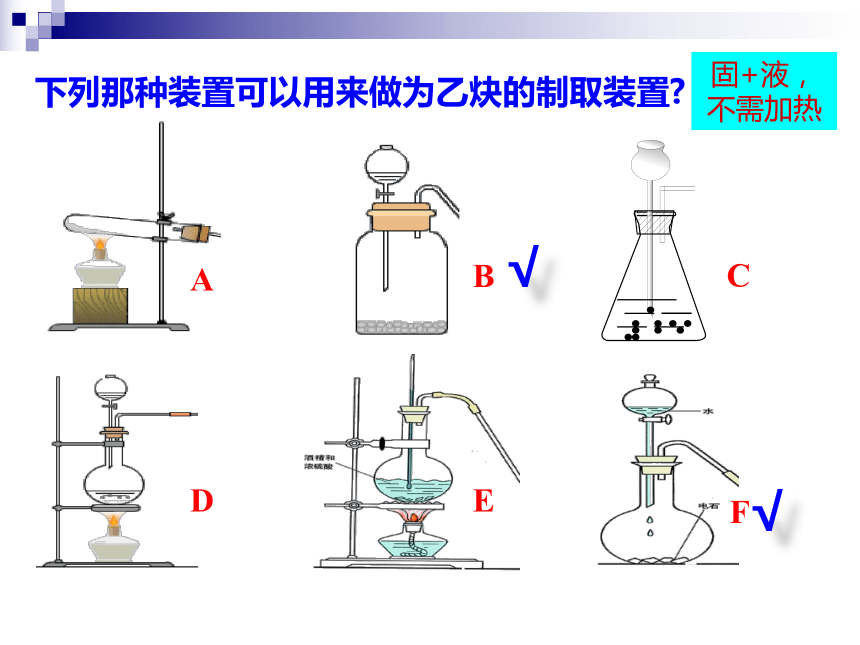
下列那种装置可以用来做为乙炔的制取装置?
A
B
C
D
E
F
固+液,
不需加热
A
B
C
D
E
F
√
√
④净化:
杂质——H2S、PH3、水蒸气等
通常将气体通过CuSO4溶液除去H2S和PH3,再通过碱石灰除去水蒸气。
H2S + CuSO4 = CuS↓ + H2SO4
⑤收集:
排水集气法
注意:
ii. 制取乙炔气体时在导气管口附近塞入少量棉花
i. 电石工业制法——
生石灰和焦炭在电炉中高温反应
目的:为防止产生的泡沫涌入导管。
CaO + 3C CaC2 + CO?
电炉
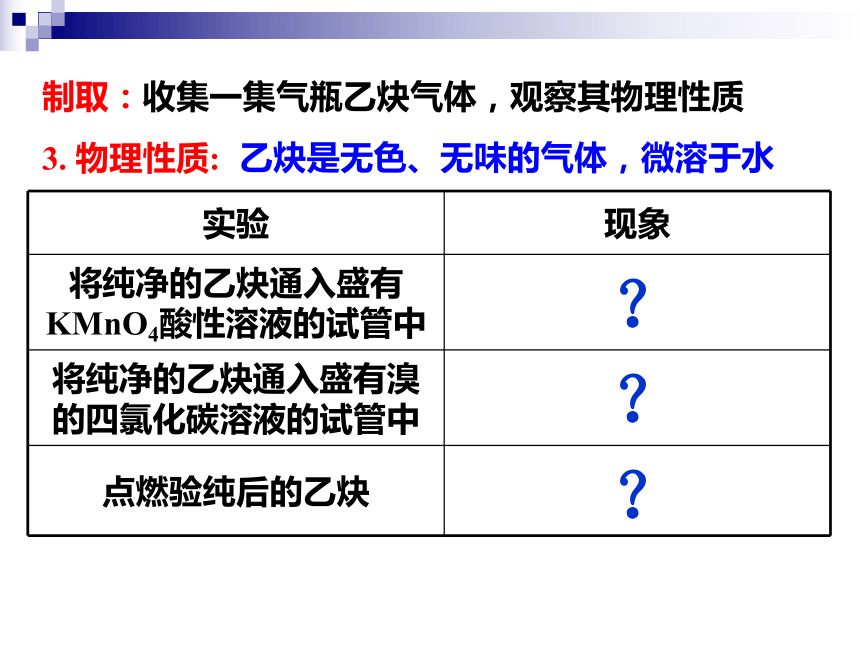
制取:收集一集气瓶乙炔气体,观察其物理性质
3. 物理性质:
实验
现象
将纯净的乙炔通入盛有KMnO4酸性溶液的试管中
将纯净的乙炔通入盛有溴的四氯化碳溶液的试管中
点燃验纯后的乙炔
乙炔是无色、无味的气体,微溶于水
?
?
?
碳碳三键属于不饱和键,且一强两弱,易断裂,化学性质较活泼
乙烷 乙烯 乙炔
348 KJ/mol
615 KJ/mol
812 KJ/mol
【结论】
C-C键键能对比
C≡C的键能和键长并不是C-C的三倍,也不是C=C和C—C之和。说明叁键中有二个键不稳定,容易断裂,有一个键较稳定。
【分析】
4. 乙炔的化学性质:
⑴ 氧化反应:
①可燃性
火焰明亮,并伴有浓烟
2C2H2+5O2 4CO2+2H2O(l)
点燃
乙炔跟空气的混合物遇火会发生爆炸,在生产和使用乙炔时,点燃前要验纯!
注意
甲烷、乙烯、乙炔的燃烧
C2H4
CH4
C2H2
(2)加成反应
2KMnO4+ 3H2SO4+ C2H2→2MnSO4+ K2SO4+2CO2↑+ 4H2O
②被氧化剂氧化
①催化加氢
使酸性KMnO4溶液褪色
CH≡CH+H2 CH2=CH2
催化剂
△
CH2=CH2+H2 CH3—CH3
催化剂
△
(2) 使溴水褪色
CH≡CH+Br2 CH=CH
Br
Br
CH=CH+Br2 CH—CH
Br
Br
Br
Br
Br
Br
1 , 2 —二溴乙烯
1 , 1 , 2 , 2 —四溴乙烷
使溴水褪色
△
CH≡CH+H2O CH3CHO
(3) 与HX等的反应
△
CH≡CH+HCl CH2=CHCl
催化剂
氯乙烯
乙醛
3. 加聚反应
nCH ≡ CH [ CH=CH ]n
催化剂
聚乙炔
(制导电高分子材料)
催化剂
实验
现象
将纯净的乙炔通入盛有KMnO4酸性溶液的试管中
将纯净的乙炔通入盛有溴的四氯化碳溶液的试管中
点燃验纯后的乙炔
溶液紫色逐渐褪去
溴的颜色逐渐褪去,生成无色易溶于四氯化碳的物质
火焰明亮,并伴有浓烟
(1) 乙炔是一种重要的基本有机原料,可以用来制备氯乙烯、聚氯乙烯和乙醛等。
(2) 乙炔燃烧时产生的氧炔焰可用来切割或焊接金属。
5. 乙炔的用途
(四)炔烃
化学性质(与乙炔相似)
(1)氧化反应
① 燃烧:
② 与酸性高锰酸钾溶液反应:
酸性高锰酸钾溶液褪色
(2)加成反应
使溴水褪色
火焰明亮,伴有大量黑烟
CH2=CHCl
CH?CH + HCl
催化剂
nCH2=CH
Cl
加温、加压
催化剂
CH2?CH
Cl
n
1、 乙炔是一种重要的基本有机原料,可以用来制备氯乙烯,写出乙炔制取聚氯乙烯的化学反应方程式。
氯乙烯
聚氯乙烯
2、某气态烃0.5mol能与1mol HCl氯化氢完全加成,加成产物分子上的氢原子又可被6molCl2取代,则气态烃可能是( )
A、CH ≡CH B、CH2=CH2
C、CH≡C—CH3 D、CH2=C(CH3)CH3
原油的分馏及裂化的产品和用途
五、脂肪烃的来源及其应用
石油分馏示意图
石油分馏塔
炼油设备
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
炼制方法
原理
主要产品
主要原料
分馏
催化裂化
催化重整
裂解
用蒸发冷凝的方法把石油分成不同沸点范围的蒸馏产物
在催化剂存在的条件下,把相对分子质量大,沸点高的烃断裂为相对分子量小,沸点低的烃
高温下,把长链分子烃断裂为各种短链的气态烃或液态烃
在催化剂条件下,把碳链的结构重新排列成新的分子结构
原油
汽油馏分中的烃类分子
直链烷烃分馏产品
重油
石油气、汽油、煤油、柴油和重油润滑油、凡士林、石蜡
提高汽油产量,短链烷烃和烯烃乙烷、丙烷、丁烯等
提高汽油的辛烷值和制取芳香烃
乙烯、丙烯、丁二烯
分子结构:
是含有C?C叁键的直线型分子
化学性质:
可燃性, 氧化反应、加成反应
主要用途:
焊接或切割金属, 化工原料
炔烃
脂肪烃来源:
石油的分馏、重油的催化裂化或裂解
本课时结束
人教版 选修五
2.1.3 炔烃
人教版 选修五
(一)炔烃的结构特点和通式
分子里含有碳碳三键的一类脂肪烃称为炔烃。
1. 概念:
2. 炔烃的通式:
(二)炔烃的物理性质:
CnH2n-2 (n≥2)
随着碳原子数的增多,沸点逐渐升高,液态时的密度逐渐增加,C原子数≤4时为气态。
炔烃
一
(三)乙炔
1. 乙炔的分子结构:
电子式:
H-C≡C-H
结构简式:
CH≡CH 或 HC≡CH
结构式:
直线型,键角180°
空间结构:
分子式:
C2H2
球棍模型
比例模型
含有三键结构的相邻四原子在同一直线上
在烯烃分子中如果双键碳上连接了两个不同的原子或原子团,将可以出现顺反异构,请问在炔烃分子中是否也存在顺反异构?
甲烷
乙烯
乙炔
结构简式
结构特点
空间结构
CH4
CH2=CH2
CH≡CH
全部单键,
饱和
有碳碳双键,
不饱和
有碳碳三键,不饱和
1. 描述CH3—CH=CH—C≡C—CF3分子结构的下列叙述中,正确的是( )
A、6个碳原子有可能在同一直线上
B、6个碳原子有可能在同一平面上
C、6个碳原子不可能在同一直线上
D、6个碳原子不可能在同一平面上
H
H
C=C
H3C
C = C— CF3
(2) 乙炔的实验室制法
CaC2+2H2O C2H2↑+Ca(OH)2
②反应原理:
① 原料:电石(CaC2)与 H2O
2. 乙炔的制法
(1) 工业制法
——甲烷裂解法
2CH4 CH≡CH +3H2
1500 ℃
碳化钙
反应装置
③装置特点:
i. 装置不能用启普发生器,改用分液漏斗
ii. 实验中常用饱和食盐水代替水
固体 +液体 气体
a. 碳化钙与水反应较剧烈,难以控反制应速率;
b. 放出的大量热量,操作不当会使启普发生器炸裂。
降低水的含量,得到平稳的乙炔气流。
启普发生器
c. 生成的Ca(OH)2呈糊状容易堵塞球型漏斗。
下列那种装置可以用来做为乙炔的制取装置?
A
B
C
D
E
F
固+液,
不需加热
A
B
C
D
E
F
√
√
④净化:
杂质——H2S、PH3、水蒸气等
通常将气体通过CuSO4溶液除去H2S和PH3,再通过碱石灰除去水蒸气。
H2S + CuSO4 = CuS↓ + H2SO4
⑤收集:
排水集气法
注意:
ii. 制取乙炔气体时在导气管口附近塞入少量棉花
i. 电石工业制法——
生石灰和焦炭在电炉中高温反应
目的:为防止产生的泡沫涌入导管。
CaO + 3C CaC2 + CO?
电炉
制取:收集一集气瓶乙炔气体,观察其物理性质
3. 物理性质:
实验
现象
将纯净的乙炔通入盛有KMnO4酸性溶液的试管中
将纯净的乙炔通入盛有溴的四氯化碳溶液的试管中
点燃验纯后的乙炔
乙炔是无色、无味的气体,微溶于水
?
?
?
碳碳三键属于不饱和键,且一强两弱,易断裂,化学性质较活泼
乙烷 乙烯 乙炔
348 KJ/mol
615 KJ/mol
812 KJ/mol
【结论】
C-C键键能对比
C≡C的键能和键长并不是C-C的三倍,也不是C=C和C—C之和。说明叁键中有二个键不稳定,容易断裂,有一个键较稳定。
【分析】
4. 乙炔的化学性质:
⑴ 氧化反应:
①可燃性
火焰明亮,并伴有浓烟
2C2H2+5O2 4CO2+2H2O(l)
点燃
乙炔跟空气的混合物遇火会发生爆炸,在生产和使用乙炔时,点燃前要验纯!
注意
甲烷、乙烯、乙炔的燃烧
C2H4
CH4
C2H2
(2)加成反应
2KMnO4+ 3H2SO4+ C2H2→2MnSO4+ K2SO4+2CO2↑+ 4H2O
②被氧化剂氧化
①催化加氢
使酸性KMnO4溶液褪色
CH≡CH+H2 CH2=CH2
催化剂
△
CH2=CH2+H2 CH3—CH3
催化剂
△
(2) 使溴水褪色
CH≡CH+Br2 CH=CH
Br
Br
CH=CH+Br2 CH—CH
Br
Br
Br
Br
Br
Br
1 , 2 —二溴乙烯
1 , 1 , 2 , 2 —四溴乙烷
使溴水褪色
△
CH≡CH+H2O CH3CHO
(3) 与HX等的反应
△
CH≡CH+HCl CH2=CHCl
催化剂
氯乙烯
乙醛
3. 加聚反应
nCH ≡ CH [ CH=CH ]n
催化剂
聚乙炔
(制导电高分子材料)
催化剂
实验
现象
将纯净的乙炔通入盛有KMnO4酸性溶液的试管中
将纯净的乙炔通入盛有溴的四氯化碳溶液的试管中
点燃验纯后的乙炔
溶液紫色逐渐褪去
溴的颜色逐渐褪去,生成无色易溶于四氯化碳的物质
火焰明亮,并伴有浓烟
(1) 乙炔是一种重要的基本有机原料,可以用来制备氯乙烯、聚氯乙烯和乙醛等。
(2) 乙炔燃烧时产生的氧炔焰可用来切割或焊接金属。
5. 乙炔的用途
(四)炔烃
化学性质(与乙炔相似)
(1)氧化反应
① 燃烧:
② 与酸性高锰酸钾溶液反应:
酸性高锰酸钾溶液褪色
(2)加成反应
使溴水褪色
火焰明亮,伴有大量黑烟
CH2=CHCl
CH?CH + HCl
催化剂
nCH2=CH
Cl
加温、加压
催化剂
CH2?CH
Cl
n
1、 乙炔是一种重要的基本有机原料,可以用来制备氯乙烯,写出乙炔制取聚氯乙烯的化学反应方程式。
氯乙烯
聚氯乙烯
2、某气态烃0.5mol能与1mol HCl氯化氢完全加成,加成产物分子上的氢原子又可被6molCl2取代,则气态烃可能是( )
A、CH ≡CH B、CH2=CH2
C、CH≡C—CH3 D、CH2=C(CH3)CH3
原油的分馏及裂化的产品和用途
五、脂肪烃的来源及其应用
石油分馏示意图
石油分馏塔
炼油设备
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A}
炼制方法
原理
主要产品
主要原料
分馏
催化裂化
催化重整
裂解
用蒸发冷凝的方法把石油分成不同沸点范围的蒸馏产物
在催化剂存在的条件下,把相对分子质量大,沸点高的烃断裂为相对分子量小,沸点低的烃
高温下,把长链分子烃断裂为各种短链的气态烃或液态烃
在催化剂条件下,把碳链的结构重新排列成新的分子结构
原油
汽油馏分中的烃类分子
直链烷烃分馏产品
重油
石油气、汽油、煤油、柴油和重油润滑油、凡士林、石蜡
提高汽油产量,短链烷烃和烯烃乙烷、丙烷、丁烯等
提高汽油的辛烷值和制取芳香烃
乙烯、丙烯、丁二烯
分子结构:
是含有C?C叁键的直线型分子
化学性质:
可燃性, 氧化反应、加成反应
主要用途:
焊接或切割金属, 化工原料
炔烃
脂肪烃来源:
石油的分馏、重油的催化裂化或裂解
本课时结束
人教版 选修五
