2020-2021学年科粤版九(下)第6章《金属》6.2金属的化学性质基础训练(word版有答案)
文档属性
| 名称 | 2020-2021学年科粤版九(下)第6章《金属》6.2金属的化学性质基础训练(word版有答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 148.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-21 00:00:00 | ||
图片预览

文档简介
科奥版九(下)第6章6.2金属的化学性质基础训练
附相对原子质量:H-1;C-12;N-14;O-16;Mg-24;Fe-56
一、选择题:
1、下列金属不能与稀盐酸反应的是( )
A.Ag B.Zn C.Fe D.Al
2、小明结合化学知识,给家中厨房用品的使用写了下列建议。其中不可取的是( )
A.燃气灶火焰呈现黄色,锅底出现黑色时,可增大灶具进风口
B.炒菜时油锅中的油着火了,可用锅盖盖灭
C.家里冰箱有异味时,可以放活性炭除臭
D.用钢刷擦洗铝锅表面污垢
3、同学们对金属N的活动性进行探究发现:将金属N放入稀盐酸中,有气泡产生(生成NCl2),将金属N放入ZnSO4溶液中无明显变化。下列化学方程式书写错误的是( )
A.N+H2SO4═NSO4+H2↑
B.N+MgSO4═Mg+NSO4
C.2Al+3NSO4═3N+Al2(SO4)3
D.N+CuSO4═Cu+NSO4
4、下列区分铜和黄铜的方法不正确的是( )
A.看颜色 B.用硝酸银溶液
C.用相互刻画的方法 D.用稀硫酸溶液
5、下列描述与事实相符合的是( )
A.细铁丝伸入盛有氧气的集气瓶中剧烈燃烧
B.铜丝插入稀硫酸中,溶液由无色变为蓝色
C.镁带在空气中燃烧,发出耀眼的白光,生成白色固体
D.电解水实验,电源正极产生的气体燃烧时会发出淡蓝色火焰
6、有X、Y、Z三种金属片,分别放入稀硫酸中,X、Z表面有气泡产生,Y没有明显现象,X放入ZCl2溶液,没有明显现象。判断这三种金属的活动性由强到弱的顺序是( )
A.X>Y>Z B.X>Z>Y C.Z>X>Y D.Y>X>Z
7、如图是金属活动性探究实验的部分,下列有关该实验的说法正确的是( )
A.实验③溶液变为蓝色
B.①②或②③都能得出金属活动性顺序为:Al>Cu>Ag
C.通过该实验能得出,金属活动性顺序为:A1>H>Cu>Ag
D.实验前常将金属片表面打磨,目的是增大接触面积,加快反应
8、归纳和推理是化学学习常用的思维方法。下列说法正确的是( )
A.金属铝的表面在空气中被氧化可以保护里层的铝,所以金属铁也有类似的性质
B.二氧化锰在氯酸钾分解反应中作催化剂,所以二氧化锰可作一切化学反应的催化剂
C.化学变化过程中常伴随着发光、放热现象,所以有发光、放热现象产生的一定是化学变化
D.合金是由一种金属跟其他金属(或非金属)熔合而成的具有金属特性的物质,所以合金一定是混合物
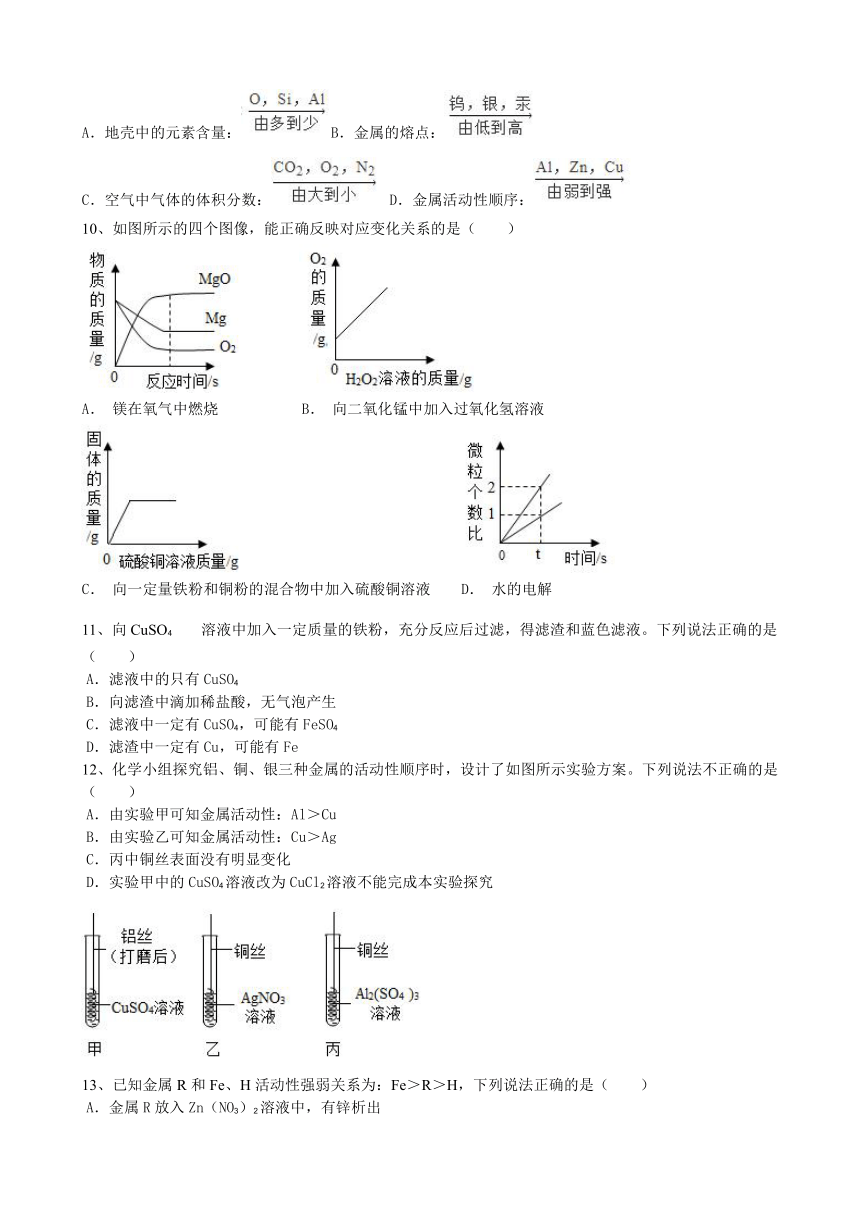
9、归纳总结是学习化学的重要方法之一。下列选项正确的是( )
A.地壳中的元素含量:B.金属的熔点:
C.空气中气体的体积分数: D.金属活动性顺序:
10、如图所示的四个图像,能正确反映对应变化关系的是( )
A. 镁在氧气中燃烧 B. 向二氧化锰中加入过氧化氢溶液
C. 向一定量铁粉和铜粉的混合物中加入硫酸铜溶液 D. 水的电解
11、向CuSO4溶液中加入一定质量的铁粉,充分反应后过滤,得滤渣和蓝色滤液。下列说法正确的是( )
A.滤液中的只有CuSO4
B.向滤渣中滴加稀盐酸,无气泡产生
C.滤液中一定有CuSO4,可能有FeSO4
D.滤渣中一定有Cu,可能有Fe
12、化学小组探究铝、铜、银三种金属的活动性顺序时,设计了如图所示实验方案。下列说法不正确的是( )
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.丙中铜丝表面没有明显变化
D.实验甲中的CuSO4溶液改为CuCl2溶液不能完成本实验探究
13、已知金属R和Fe、H活动性强弱关系为:Fe>R>H,下列说法正确的是( )
A.金属R放入Zn(NO3)2溶液中,有锌析出
B.金属铁放入AgNO3溶液中,一段时间后,固体的质量变小
C.金属铁(足量)放入R(NO3)2溶液中,溶液变黄色
D.金属R放入CuSO4溶液中,金属表面有红色固体析出
二、填空题:
1、2020年中国首次火星探测,利用火星车一次实现“环绕、着陆、巡视”三个目标,这是其他国家第一次实施火星探测从未有过的,面临的挑战也是前所未有的。(火星车模型如图)
(1)硅片太阳能电池板在日光照射下或跟空气、水分接触时都不容易发生反应,硅化学性质稳定的原因是 ,Si属于 (填“金属”或“非金属”)。
(2)火星车采用钛合金、铝合金、复合记忆纤维等材料制造,为保证火星车在火星上着陆并正常工作,钛、铝合金应具有密度、硬度大、耐腐蚀等优良性能;铝的化学性质很活泼,但铝制品却很耐腐蚀的原因是 (用化学方程式表示)。
(3)火星大气中二氧化碳含量高,二氧化碳在一定条件下能发生反应生成一氧化碳和氧气,该反应的化学方程式 ,所属的基本反应类型为 ,生成的一氧化碳可解决火星探测器的燃料问题。
2、某化学兴趣小组对某仿冒黄金(铜锌合金)进行如下处理,请回答有关问题:
(1)粉碎仿冒黄金的目的是 。
(2)操作A的名称是 。
(3)固体X为 。
(4)写出上述流程中加入过量稀盐酸发生反应的化学方程式 。
(5)区别真金和仿冒黄金的方法有很多,请另举一例 。
3、汽车是现代生活中重要的交通工具。请回答下列问题:
(1)图1材料中属于金属材料的是 。汽车电路中的导线一般为铜芯线,这是利用了金属铜的延展性和 性。
(2)将镁铝合金与铝片相互刻画,在铝片表面留下明显划痕,说明镁铝合金的硬度 铝的硬度(填“大于”或“小于”)。
(3)某汽修厂清洗汽车零件后的废液中常含有一定量的AgNO3和Cu(NO3)2.向一定质量的该废液中[假设溶质只含AgNO3和Cu(NO3)2]中加入Zn,充分反应。根据图2回答下列问题:
1)a点溶液中的溶质有 ,c点溶液中溶质为
2)若取a~b段溶液,滴加稀盐酸,发生反应的化学方程式
3)取d点的固体,加入稀盐酸,发生反应的化学方程式 。
4、金属制品与我们的日常生活密不可分。
(1)电动车是一类典型的新能源车,推广新能源汽车能有效减少有害气体的排放,目前我国计入空气污染指数的项目中除了可吸入颗粒物外,还包括下列物质中 (填序号)。
A.CO
B.CO2
C.SO2
D.NO2
电动车身及车轮采用铝合金,铝合金具有密度小、硬度 (填“大”或“小”)、耐腐蚀的优良性能。铝在地壳中的含量 (填“大于”或“小于”,下同)铁;钢和生铁都是合金,生铁的含碳量 钢的含碳量。
(2)铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动性顺序,某同学设计了如图实验,甲中铝丝表面会出现的现象是 ,实验甲能得出的结论是 的金属活动性更强。另一位同学认为实验乙、丙中均无明显现象,对完整的结论没有作用,都可以省去。你的看法是 (填序号)。
A.乙、丙都可以省去
B.乙、丙都不能省去
C.丙可以省去,乙不能省
D.乙可以省去,丙不能省
(3)非金属与金属类似,较活泼的非金属也能把较不活泼的非金属从它们化合物的溶液里置换出来。已知活泼性Cl2>Br2>I2,请写出将Cl2通入NaBr溶液中发生反应的化学方程式 。
参考答案
一、选择题:
1、A 2、D 3、B 4、B 5、C 6、C 7、A 8、D 9、A 10、D
11、B 12、D 13、D
二、填空题:
1、答案:(1)硅原子最外层电子数为4,既不容易得电子,也不容易失电子;非金属;
(2)4Al+3O2=2Al2O3;
(3)2CO22CO+O2↑;分解反应。
2、答案:(1)增大接触面积,使其充分反应。
(2)过滤。
(3)铜。
(4)Zn+2HCl═ZnCl2+H2↑。
(5)灼烧或加入硝酸银溶液等。
3、答案为:(1)镁铝合金,导电性;(2)大于;(3)1)硝酸银、硝酸铜和硝酸锌;硝酸锌;
2)HCl+AgNO3=AgCl↓+HNO3;3)Zn+2HCl=ZnCl2+H2↑。
4、解:(1)我国计入空气污染指数的项目除了可吸入颗粒物外,还有CO、SO2和氮的氧化物,则填ACD;合金比其组分金属硬度大,则铝合金具有密度小、硬度大、耐腐蚀的优良性能,铝是地壳中含量最多的金属元素,则铝在地壳中的含量大于铁;生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%,则生铁的含碳量析大于钢的含碳量;故填:ACD;大;大于;大于;
(2)Al、Mg、Cu的金属活性为Mg>Al>Cu,则甲中发生的反应为2Al+3CuSO4=Al2(SO4)3+2Al,甲中铝丝表面会出现的现象是有红色物质析出,实验甲能得出的结论是铝的金属活性更强,实验乙无明显现象说明铝的金属活性小于镁的金属活性,则通过甲、乙实验可得出Mg>Al>Cu,而丙实验无实际意义,故填:有红色物质析出;铝;C;
(3)依据题中信息非金属与金属类似,较活泼的非金属也能把较不活泼的非金属从它们化合物的溶液里置换出来,已知活泼性Cl2>Br2>I2,将Cl2通入NaBr溶液中发生反应的化学方程式为Cl2+2NaBr=2NaCl+Br2,故填:Cl2+2NaBr=2NaCl+Br2。
附相对原子质量:H-1;C-12;N-14;O-16;Mg-24;Fe-56
一、选择题:
1、下列金属不能与稀盐酸反应的是( )
A.Ag B.Zn C.Fe D.Al
2、小明结合化学知识,给家中厨房用品的使用写了下列建议。其中不可取的是( )
A.燃气灶火焰呈现黄色,锅底出现黑色时,可增大灶具进风口
B.炒菜时油锅中的油着火了,可用锅盖盖灭
C.家里冰箱有异味时,可以放活性炭除臭
D.用钢刷擦洗铝锅表面污垢
3、同学们对金属N的活动性进行探究发现:将金属N放入稀盐酸中,有气泡产生(生成NCl2),将金属N放入ZnSO4溶液中无明显变化。下列化学方程式书写错误的是( )
A.N+H2SO4═NSO4+H2↑
B.N+MgSO4═Mg+NSO4
C.2Al+3NSO4═3N+Al2(SO4)3
D.N+CuSO4═Cu+NSO4
4、下列区分铜和黄铜的方法不正确的是( )
A.看颜色 B.用硝酸银溶液
C.用相互刻画的方法 D.用稀硫酸溶液
5、下列描述与事实相符合的是( )
A.细铁丝伸入盛有氧气的集气瓶中剧烈燃烧
B.铜丝插入稀硫酸中,溶液由无色变为蓝色
C.镁带在空气中燃烧,发出耀眼的白光,生成白色固体
D.电解水实验,电源正极产生的气体燃烧时会发出淡蓝色火焰
6、有X、Y、Z三种金属片,分别放入稀硫酸中,X、Z表面有气泡产生,Y没有明显现象,X放入ZCl2溶液,没有明显现象。判断这三种金属的活动性由强到弱的顺序是( )
A.X>Y>Z B.X>Z>Y C.Z>X>Y D.Y>X>Z
7、如图是金属活动性探究实验的部分,下列有关该实验的说法正确的是( )
A.实验③溶液变为蓝色
B.①②或②③都能得出金属活动性顺序为:Al>Cu>Ag
C.通过该实验能得出,金属活动性顺序为:A1>H>Cu>Ag
D.实验前常将金属片表面打磨,目的是增大接触面积,加快反应
8、归纳和推理是化学学习常用的思维方法。下列说法正确的是( )
A.金属铝的表面在空气中被氧化可以保护里层的铝,所以金属铁也有类似的性质
B.二氧化锰在氯酸钾分解反应中作催化剂,所以二氧化锰可作一切化学反应的催化剂
C.化学变化过程中常伴随着发光、放热现象,所以有发光、放热现象产生的一定是化学变化
D.合金是由一种金属跟其他金属(或非金属)熔合而成的具有金属特性的物质,所以合金一定是混合物
9、归纳总结是学习化学的重要方法之一。下列选项正确的是( )
A.地壳中的元素含量:B.金属的熔点:
C.空气中气体的体积分数: D.金属活动性顺序:
10、如图所示的四个图像,能正确反映对应变化关系的是( )
A. 镁在氧气中燃烧 B. 向二氧化锰中加入过氧化氢溶液
C. 向一定量铁粉和铜粉的混合物中加入硫酸铜溶液 D. 水的电解
11、向CuSO4溶液中加入一定质量的铁粉,充分反应后过滤,得滤渣和蓝色滤液。下列说法正确的是( )
A.滤液中的只有CuSO4
B.向滤渣中滴加稀盐酸,无气泡产生
C.滤液中一定有CuSO4,可能有FeSO4
D.滤渣中一定有Cu,可能有Fe
12、化学小组探究铝、铜、银三种金属的活动性顺序时,设计了如图所示实验方案。下列说法不正确的是( )
A.由实验甲可知金属活动性:Al>Cu
B.由实验乙可知金属活动性:Cu>Ag
C.丙中铜丝表面没有明显变化
D.实验甲中的CuSO4溶液改为CuCl2溶液不能完成本实验探究
13、已知金属R和Fe、H活动性强弱关系为:Fe>R>H,下列说法正确的是( )
A.金属R放入Zn(NO3)2溶液中,有锌析出
B.金属铁放入AgNO3溶液中,一段时间后,固体的质量变小
C.金属铁(足量)放入R(NO3)2溶液中,溶液变黄色
D.金属R放入CuSO4溶液中,金属表面有红色固体析出
二、填空题:
1、2020年中国首次火星探测,利用火星车一次实现“环绕、着陆、巡视”三个目标,这是其他国家第一次实施火星探测从未有过的,面临的挑战也是前所未有的。(火星车模型如图)
(1)硅片太阳能电池板在日光照射下或跟空气、水分接触时都不容易发生反应,硅化学性质稳定的原因是 ,Si属于 (填“金属”或“非金属”)。
(2)火星车采用钛合金、铝合金、复合记忆纤维等材料制造,为保证火星车在火星上着陆并正常工作,钛、铝合金应具有密度、硬度大、耐腐蚀等优良性能;铝的化学性质很活泼,但铝制品却很耐腐蚀的原因是 (用化学方程式表示)。
(3)火星大气中二氧化碳含量高,二氧化碳在一定条件下能发生反应生成一氧化碳和氧气,该反应的化学方程式 ,所属的基本反应类型为 ,生成的一氧化碳可解决火星探测器的燃料问题。
2、某化学兴趣小组对某仿冒黄金(铜锌合金)进行如下处理,请回答有关问题:
(1)粉碎仿冒黄金的目的是 。
(2)操作A的名称是 。
(3)固体X为 。
(4)写出上述流程中加入过量稀盐酸发生反应的化学方程式 。
(5)区别真金和仿冒黄金的方法有很多,请另举一例 。
3、汽车是现代生活中重要的交通工具。请回答下列问题:
(1)图1材料中属于金属材料的是 。汽车电路中的导线一般为铜芯线,这是利用了金属铜的延展性和 性。
(2)将镁铝合金与铝片相互刻画,在铝片表面留下明显划痕,说明镁铝合金的硬度 铝的硬度(填“大于”或“小于”)。
(3)某汽修厂清洗汽车零件后的废液中常含有一定量的AgNO3和Cu(NO3)2.向一定质量的该废液中[假设溶质只含AgNO3和Cu(NO3)2]中加入Zn,充分反应。根据图2回答下列问题:
1)a点溶液中的溶质有 ,c点溶液中溶质为
2)若取a~b段溶液,滴加稀盐酸,发生反应的化学方程式
3)取d点的固体,加入稀盐酸,发生反应的化学方程式 。
4、金属制品与我们的日常生活密不可分。
(1)电动车是一类典型的新能源车,推广新能源汽车能有效减少有害气体的排放,目前我国计入空气污染指数的项目中除了可吸入颗粒物外,还包括下列物质中 (填序号)。
A.CO
B.CO2
C.SO2
D.NO2
电动车身及车轮采用铝合金,铝合金具有密度小、硬度 (填“大”或“小”)、耐腐蚀的优良性能。铝在地壳中的含量 (填“大于”或“小于”,下同)铁;钢和生铁都是合金,生铁的含碳量 钢的含碳量。
(2)铝合金中主要含有铝、铜、镁三种金属,为验证这三种金属的活动性顺序,某同学设计了如图实验,甲中铝丝表面会出现的现象是 ,实验甲能得出的结论是 的金属活动性更强。另一位同学认为实验乙、丙中均无明显现象,对完整的结论没有作用,都可以省去。你的看法是 (填序号)。
A.乙、丙都可以省去
B.乙、丙都不能省去
C.丙可以省去,乙不能省
D.乙可以省去,丙不能省
(3)非金属与金属类似,较活泼的非金属也能把较不活泼的非金属从它们化合物的溶液里置换出来。已知活泼性Cl2>Br2>I2,请写出将Cl2通入NaBr溶液中发生反应的化学方程式 。
参考答案
一、选择题:
1、A 2、D 3、B 4、B 5、C 6、C 7、A 8、D 9、A 10、D
11、B 12、D 13、D
二、填空题:
1、答案:(1)硅原子最外层电子数为4,既不容易得电子,也不容易失电子;非金属;
(2)4Al+3O2=2Al2O3;
(3)2CO22CO+O2↑;分解反应。
2、答案:(1)增大接触面积,使其充分反应。
(2)过滤。
(3)铜。
(4)Zn+2HCl═ZnCl2+H2↑。
(5)灼烧或加入硝酸银溶液等。
3、答案为:(1)镁铝合金,导电性;(2)大于;(3)1)硝酸银、硝酸铜和硝酸锌;硝酸锌;
2)HCl+AgNO3=AgCl↓+HNO3;3)Zn+2HCl=ZnCl2+H2↑。
4、解:(1)我国计入空气污染指数的项目除了可吸入颗粒物外,还有CO、SO2和氮的氧化物,则填ACD;合金比其组分金属硬度大,则铝合金具有密度小、硬度大、耐腐蚀的优良性能,铝是地壳中含量最多的金属元素,则铝在地壳中的含量大于铁;生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%,则生铁的含碳量析大于钢的含碳量;故填:ACD;大;大于;大于;
(2)Al、Mg、Cu的金属活性为Mg>Al>Cu,则甲中发生的反应为2Al+3CuSO4=Al2(SO4)3+2Al,甲中铝丝表面会出现的现象是有红色物质析出,实验甲能得出的结论是铝的金属活性更强,实验乙无明显现象说明铝的金属活性小于镁的金属活性,则通过甲、乙实验可得出Mg>Al>Cu,而丙实验无实际意义,故填:有红色物质析出;铝;C;
(3)依据题中信息非金属与金属类似,较活泼的非金属也能把较不活泼的非金属从它们化合物的溶液里置换出来,已知活泼性Cl2>Br2>I2,将Cl2通入NaBr溶液中发生反应的化学方程式为Cl2+2NaBr=2NaCl+Br2,故填:Cl2+2NaBr=2NaCl+Br2。
