人教版高中化学选修五3.3 羧酸 酯 课件 (22张PPT)
文档属性
| 名称 | 人教版高中化学选修五3.3 羧酸 酯 课件 (22张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 431.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-22 00:00:00 | ||
图片预览




文档简介
第三章 烃的含氧衍生物
3.3 羧酸 酯
人教版 选修五
蚁酸(甲酸)HCOOH
柠檬酸
HO—C—COOH
CH2—COOH
CH2—COOH
安息香酸(苯甲酸)
自然界中的有机酸
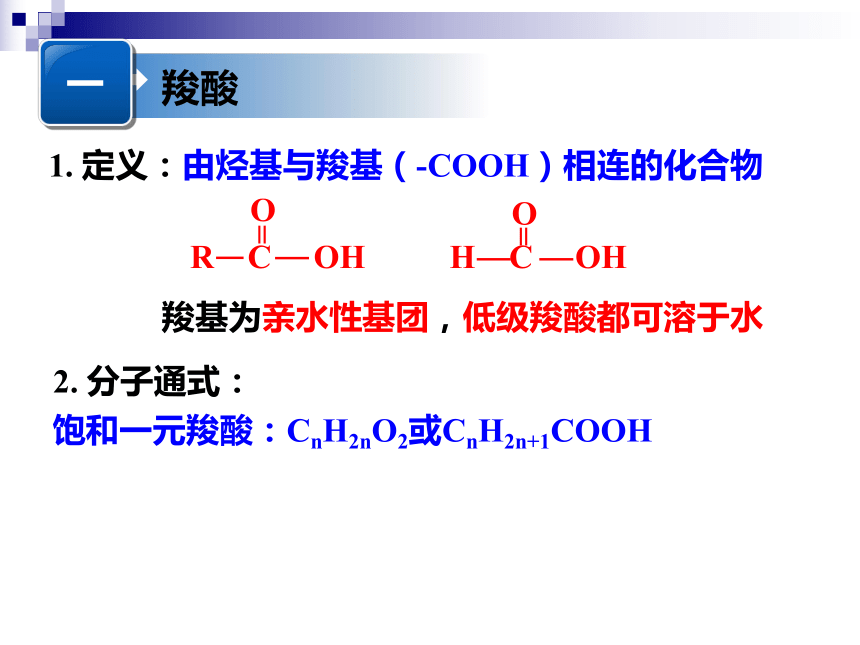
1. 定义:由烃基与羧基(-COOH)相连的化合物
R C OH
=
O
H C OH
=
O
2. 分子通式:
饱和一元羧酸:CnH2nO2或CnH2n+1COOH
羧酸
一
羧基为亲水性基团,低级羧酸都可溶于水
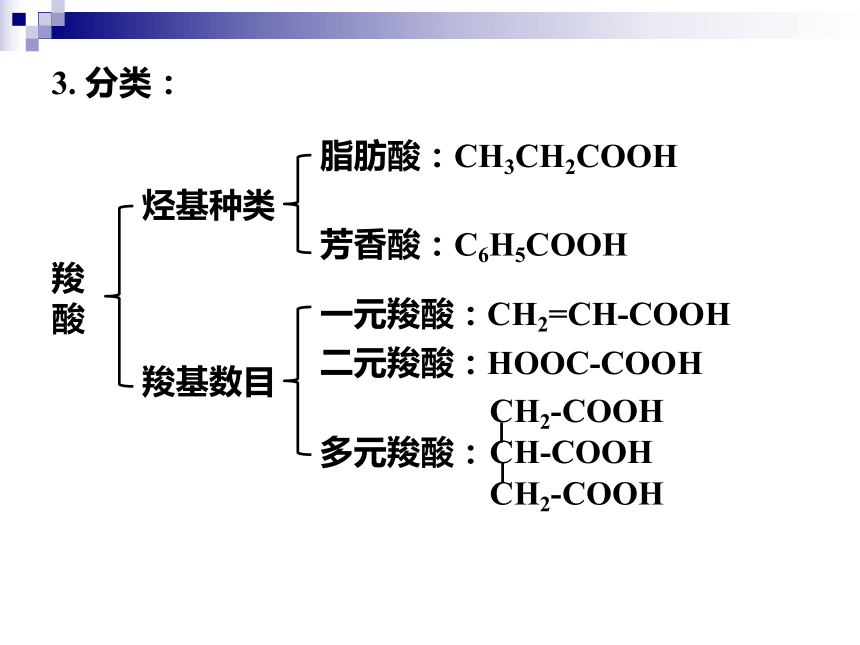
3. 分类:
羧
酸
烃基种类
羧基数目
脂肪酸:CH3CH2COOH
芳香酸:C6H5COOH
一元羧酸:CH2=CH-COOH
二元羧酸:HOOC-COOH
多元羧酸:
CH2-COOH
CH-COOH
CH2-COOH
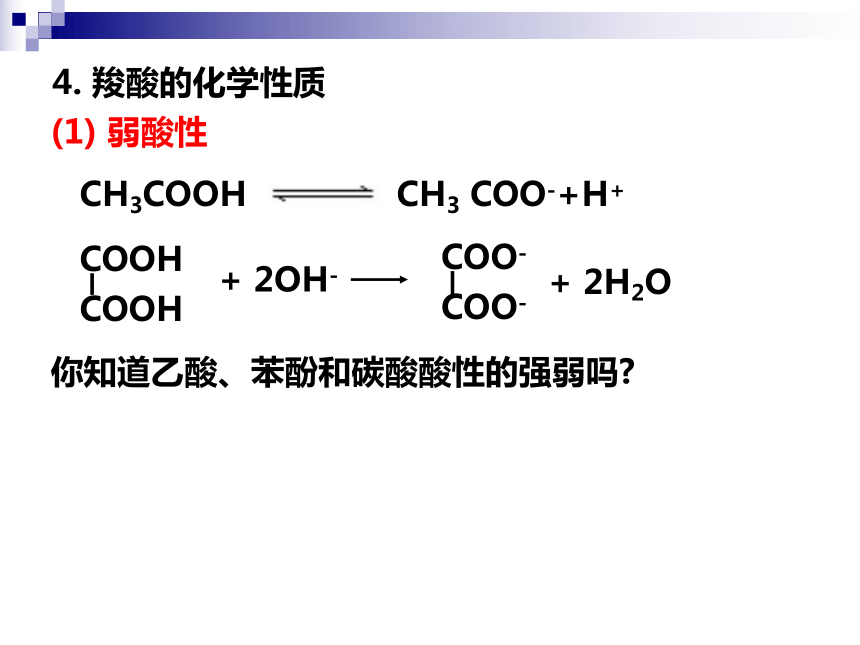
4. 羧酸的化学性质
(1) 弱酸性
CH3COOH CH3 COO-+H+
COOH
COOH
+ 2OH-
COO-
COO-
+ 2H2O
你知道乙酸、苯酚和碳酸酸性的强弱吗?
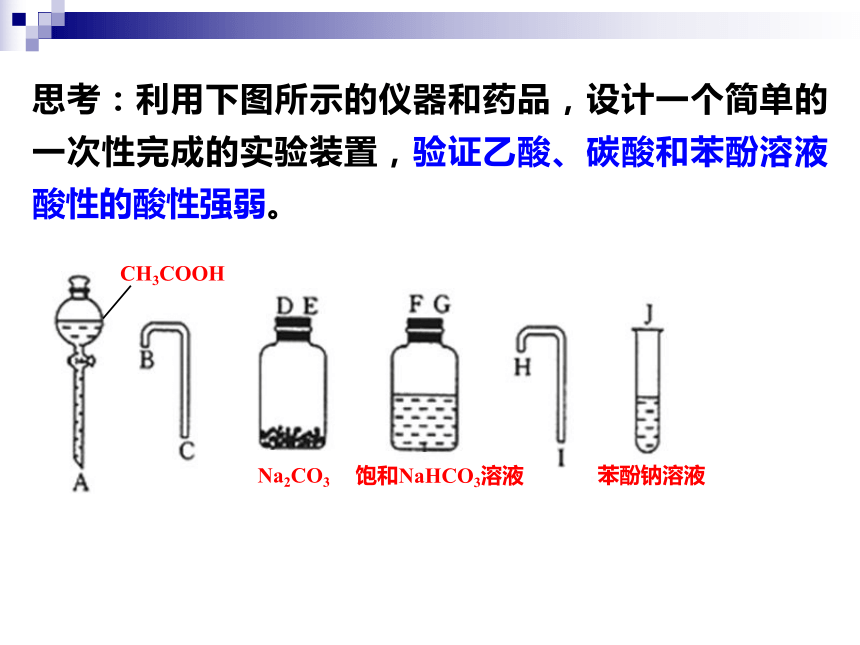
思考:利用下图所示的仪器和药品,设计一个简单的一次性完成的实验装置,验证乙酸、碳酸和苯酚溶液酸性的酸性强弱。
CH3COOH
Na2CO3
饱和NaHCO3溶液
苯酚钠溶液
① 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O
② C6H5ONa+CO2+H2O→C6H5OH+NaHCO3
实验装置图
①
②
乙酸酸性的具体表现:
① 使石蕊变红,能电离出H+
② 能与活泼金属反应产生H2
③ 能与碱发生中和反应
④ 能与碱性氧化物反应
⑤ 能与一些盐发生反应
2CH3COOH+CO32-→2CH3COO-+CO2↑+H2O
CH3COOH CH3COO- + H+
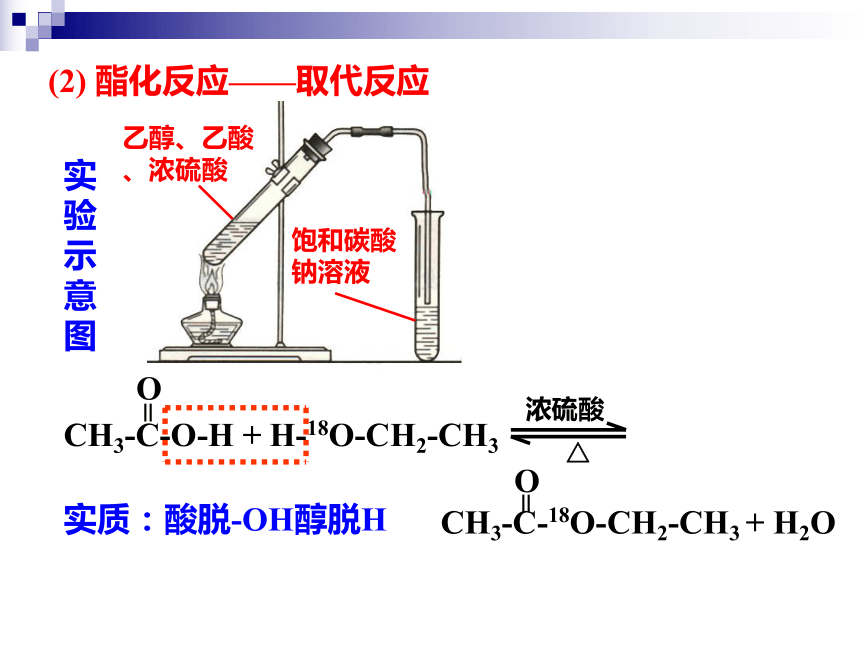
(2) 酯化反应——取代反应
CH3-C-O-H + H-18O-CH2-CH3
浓硫酸
△
=
O
CH3-C-18O-CH2-CH3 + H2O
=
O
实质:酸脱-OH醇脱H
饱和碳酸钠溶液
乙醇、乙酸、浓硫酸
实验示意图
实验分析:
1. 浓硫酸的作用是:
3. 得到的反应产物是否纯净?主要杂质有哪些?
4. 饱和Na2CO3溶液有什么作用?
催化剂、吸水剂
不纯净;主要含乙酸、乙醇。
③ 降低酯在水中的溶解度,以便使酯分层析出。
2. 试剂加入的顺序应该怎样:
无水乙醇→浓硫酸→乙酸
② 溶解乙醇
① 中和乙酸
5. 为什么导管不插入饱和Na2CO3溶液中?
防止受热不匀发生倒吸。
乙酸与乙醇的酯化反应是可逆的,在制取乙酸乙酯的实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?
(3) 使用浓H2SO4作吸水剂,提高反应转化率。
根据化学平衡原理,提高乙酸乙酯产率的措施有:
(1) 由于乙酸乙酯的沸点比乙酸、乙醇都低,因此从反应物中不断蒸出乙酸乙酯可提高其产率。
(2) 使用过量的乙醇,可提高乙酸转化率。
(4) 还原反应
(3) 羧酸α-H的取代反应
R-CH2COOH+Cl2
R-CH-COOH+HCl
Cl
催化剂
R-COOH
LiAlH4
R-CH2OH
预测化学性质:
俗名蚁酸,是具有刺激性气味的无色液体,有腐蚀性,除了具有羧酸的通性外,甲酸还可以具有醛的性质。
酸性(电离方程式): ;
酯化反应: ;
银镜反应: ;
与新制Cu(OH)2反应: 。
C
H
OH
=
O
5. 甲酸
酯
二
1.概念:酸与醇反应脱水后生成的一类化合物。
酸可以是无机酸吗?
【拓展】无机含氧酸和醇的酯化反应:
C2H5O-NO2 + H2O
C2H5OH + HO-NO2
浓H2SO4
硝酸乙酯
2. 酯的通式
(1) 一般通式:
饱和一元羧酸和饱和一元醇生成的酯
(2) 一元饱和羧酸酯通式:CnH2nO2
R-C-O-R′
=
O
RCOOR′
3. 酯的命名——某酸某酯
(1) HCOOCH2CH2CH3
(2) CH3COOCH2
CH3COOCH2
(3) CH2COOCH3
CH2COOCH3
3. 化学性质——水解反应
CH3-C-O-C2H5 + H2O
O
=
稀H2SO4
CH3COOH + CH3CH2OH
CH3-C-O-C2H5 +NaOH
O
=
CH3COONa + CH3CH2OH
酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的。
乙酸乙酯的水解
装置图
试 剂
现 象
结论
①乙酸乙酯+水
②乙酸乙酯+稀硫
酸
③乙酸乙酯+氢氧
化钠溶液
①酯层不变
②酯层变薄
③酯层消失
在硫酸作用下水解反应是可逆反应;
在NaOH作用下彻底水解
①②③
酯的水解反应在酸性条件好,还是碱性条件好?
1. 下列有关酯的叙述中,不正确的是( )
A.羧酸与醇在强酸的存在下加热可得到酯
B.乙酸和甲醇发生酯化反应生成甲酸乙酯
C.酯化反应的逆反应是水解反应
D.果类和花草中存在着芳香气味的低级酯
2. 0.1mol阿斯匹林(结构式为 )可跟足量的NaOH溶液反应,最多消耗NaOH的物质的量为( )
A.0.1mol B.0.2 mol
C.0.3 mol D.0.4 mol
3. 写出下列酯化反应方程式。
HCOOC2H5 + H2O
HCOOH + C2H5OH
浓H2SO4
(2) 足量乙酸与乙二醇酯化:
H-O-CH2
H-O-CH2
2CH3COOH +
CH3COO-CH2
CH3COO-CH2
浓H2SO4
+2H2O
(1) 甲酸与乙醇的酯化:
浓H2SO4
C-OH
C-OH
=
=
O
O
H-O-CH2
H-O-CH2
+
C
C
CH2
CH2
O
O
O
O
=
=
+ 2H2O
(3) 乙二酸与足量乙醇酯化:
(4) 乙二酸与乙二醇酯化生成环酯:
浓H2SO4
C-OH
C-OH
=
=
O
O
+ C2H5OH
C-OC2H5
C-OC2H5
=
=
O
O
+ 2H2O
本课时结束
人教版 选修五
3.3 羧酸 酯
人教版 选修五
蚁酸(甲酸)HCOOH
柠檬酸
HO—C—COOH
CH2—COOH
CH2—COOH
安息香酸(苯甲酸)
自然界中的有机酸
1. 定义:由烃基与羧基(-COOH)相连的化合物
R C OH
=
O
H C OH
=
O
2. 分子通式:
饱和一元羧酸:CnH2nO2或CnH2n+1COOH
羧酸
一
羧基为亲水性基团,低级羧酸都可溶于水
3. 分类:
羧
酸
烃基种类
羧基数目
脂肪酸:CH3CH2COOH
芳香酸:C6H5COOH
一元羧酸:CH2=CH-COOH
二元羧酸:HOOC-COOH
多元羧酸:
CH2-COOH
CH-COOH
CH2-COOH
4. 羧酸的化学性质
(1) 弱酸性
CH3COOH CH3 COO-+H+
COOH
COOH
+ 2OH-
COO-
COO-
+ 2H2O
你知道乙酸、苯酚和碳酸酸性的强弱吗?
思考:利用下图所示的仪器和药品,设计一个简单的一次性完成的实验装置,验证乙酸、碳酸和苯酚溶液酸性的酸性强弱。
CH3COOH
Na2CO3
饱和NaHCO3溶液
苯酚钠溶液
① 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O
② C6H5ONa+CO2+H2O→C6H5OH+NaHCO3
实验装置图
①
②
乙酸酸性的具体表现:
① 使石蕊变红,能电离出H+
② 能与活泼金属反应产生H2
③ 能与碱发生中和反应
④ 能与碱性氧化物反应
⑤ 能与一些盐发生反应
2CH3COOH+CO32-→2CH3COO-+CO2↑+H2O
CH3COOH CH3COO- + H+
(2) 酯化反应——取代反应
CH3-C-O-H + H-18O-CH2-CH3
浓硫酸
△
=
O
CH3-C-18O-CH2-CH3 + H2O
=
O
实质:酸脱-OH醇脱H
饱和碳酸钠溶液
乙醇、乙酸、浓硫酸
实验示意图
实验分析:
1. 浓硫酸的作用是:
3. 得到的反应产物是否纯净?主要杂质有哪些?
4. 饱和Na2CO3溶液有什么作用?
催化剂、吸水剂
不纯净;主要含乙酸、乙醇。
③ 降低酯在水中的溶解度,以便使酯分层析出。
2. 试剂加入的顺序应该怎样:
无水乙醇→浓硫酸→乙酸
② 溶解乙醇
① 中和乙酸
5. 为什么导管不插入饱和Na2CO3溶液中?
防止受热不匀发生倒吸。
乙酸与乙醇的酯化反应是可逆的,在制取乙酸乙酯的实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?
(3) 使用浓H2SO4作吸水剂,提高反应转化率。
根据化学平衡原理,提高乙酸乙酯产率的措施有:
(1) 由于乙酸乙酯的沸点比乙酸、乙醇都低,因此从反应物中不断蒸出乙酸乙酯可提高其产率。
(2) 使用过量的乙醇,可提高乙酸转化率。
(4) 还原反应
(3) 羧酸α-H的取代反应
R-CH2COOH+Cl2
R-CH-COOH+HCl
Cl
催化剂
R-COOH
LiAlH4
R-CH2OH
预测化学性质:
俗名蚁酸,是具有刺激性气味的无色液体,有腐蚀性,除了具有羧酸的通性外,甲酸还可以具有醛的性质。
酸性(电离方程式): ;
酯化反应: ;
银镜反应: ;
与新制Cu(OH)2反应: 。
C
H
OH
=
O
5. 甲酸
酯
二
1.概念:酸与醇反应脱水后生成的一类化合物。
酸可以是无机酸吗?
【拓展】无机含氧酸和醇的酯化反应:
C2H5O-NO2 + H2O
C2H5OH + HO-NO2
浓H2SO4
硝酸乙酯
2. 酯的通式
(1) 一般通式:
饱和一元羧酸和饱和一元醇生成的酯
(2) 一元饱和羧酸酯通式:CnH2nO2
R-C-O-R′
=
O
RCOOR′
3. 酯的命名——某酸某酯
(1) HCOOCH2CH2CH3
(2) CH3COOCH2
CH3COOCH2
(3) CH2COOCH3
CH2COOCH3
3. 化学性质——水解反应
CH3-C-O-C2H5 + H2O
O
=
稀H2SO4
CH3COOH + CH3CH2OH
CH3-C-O-C2H5 +NaOH
O
=
CH3COONa + CH3CH2OH
酯在无机酸、碱催化下,均能发生水解反应,其中在酸性条件下水解是可逆的,在碱性条件下水解是不可逆的。
乙酸乙酯的水解
装置图
试 剂
现 象
结论
①乙酸乙酯+水
②乙酸乙酯+稀硫
酸
③乙酸乙酯+氢氧
化钠溶液
①酯层不变
②酯层变薄
③酯层消失
在硫酸作用下水解反应是可逆反应;
在NaOH作用下彻底水解
①②③
酯的水解反应在酸性条件好,还是碱性条件好?
1. 下列有关酯的叙述中,不正确的是( )
A.羧酸与醇在强酸的存在下加热可得到酯
B.乙酸和甲醇发生酯化反应生成甲酸乙酯
C.酯化反应的逆反应是水解反应
D.果类和花草中存在着芳香气味的低级酯
2. 0.1mol阿斯匹林(结构式为 )可跟足量的NaOH溶液反应,最多消耗NaOH的物质的量为( )
A.0.1mol B.0.2 mol
C.0.3 mol D.0.4 mol
3. 写出下列酯化反应方程式。
HCOOC2H5 + H2O
HCOOH + C2H5OH
浓H2SO4
(2) 足量乙酸与乙二醇酯化:
H-O-CH2
H-O-CH2
2CH3COOH +
CH3COO-CH2
CH3COO-CH2
浓H2SO4
+2H2O
(1) 甲酸与乙醇的酯化:
浓H2SO4
C-OH
C-OH
=
=
O
O
H-O-CH2
H-O-CH2
+
C
C
CH2
CH2
O
O
O
O
=
=
+ 2H2O
(3) 乙二酸与足量乙醇酯化:
(4) 乙二酸与乙二醇酯化生成环酯:
浓H2SO4
C-OH
C-OH
=
=
O
O
+ C2H5OH
C-OC2H5
C-OC2H5
=
=
O
O
+ 2H2O
本课时结束
人教版 选修五
