2020-2021学年九年级化学鲁教版下册第七单元第二节 碱及其性质 课件(共21张PPT)
文档属性
| 名称 | 2020-2021学年九年级化学鲁教版下册第七单元第二节 碱及其性质 课件(共21张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-22 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
第二节 碱及其性质
NaOH
KOH
Ca(OH)2
Cu(OH)2
NaOH
KOH
Ca(OH)2
NaOH
KOH
Cu(OH)2
Ca(OH)2
NaOH
KOH
NaOH
KOH
Ca(OH)2
NaOH
KOH
Cu(OH)2
Ca(OH)2
NaOH
KOH
NaOH
KOH
NaOH
Ca(OH)2
KOH
NaOH
Cu(OH)2
Ca(OH)2
KOH
NaOH
Cu(OH)2
Ca(OH)2
KOH
NaOH
NaOH
KOH
NaOH
Ca(OH)2
KOH
NaOH
Cu(OH)2
Ca(OH)2
KOH
NaOH
KOH
NaOH
Ca(OH)2
KOH
NaOH
Cu(OH)2
Ca(OH)2
KOH
NaOH
NaOH
KOH
NaOH
Ca(OH)2
KOH
Cu(OH)2
Ca(OH)2
KOH
KOH
Cu(OH)2
Cu(OH)2
Cu(OH)2
上述几种碱在组成上有什么共同特点?
(都含有OH-)
碱:电离时电离出的阴离子全部是OH-的化合物
氢氧化钠 氢氧化钙
认识氢氧化钠和氢氧化钙
认识氢氧化钠和氢氧化钙
1、观察固体氢氧化钠和氢氧化钙的颜色、状态,在表面皿中放一些固体烧碱,露置在空气中一段时间,观察它发生什么变化。
2、在两只小烧杯中分别加一些固体氢氧化钠和氢氧化钙,加入水,振荡,观察它们的溶解过程,并摸一摸烧杯,感觉溶液温度的变化。
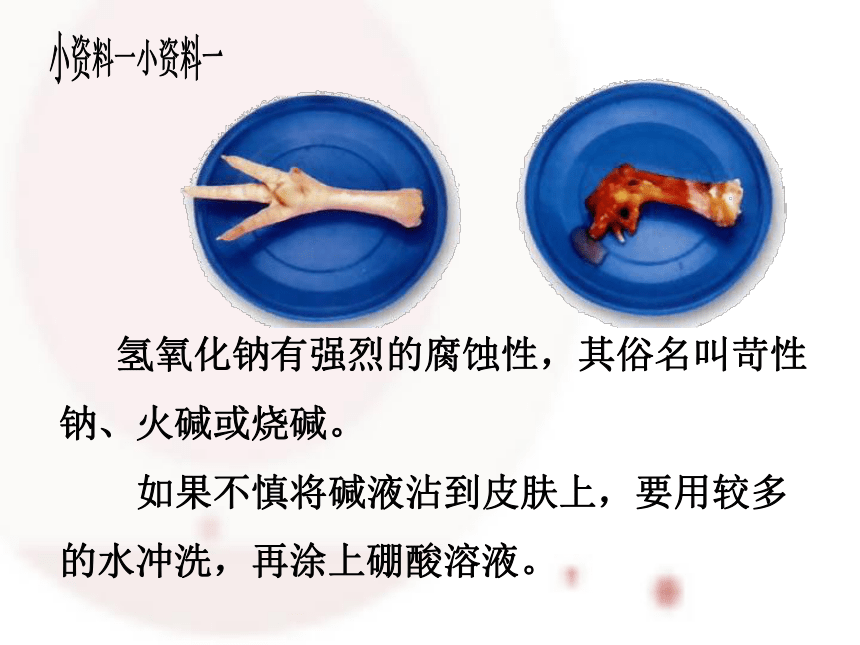
氢氧化钠有强烈的腐蚀性,其俗名叫苛性钠、火碱或烧碱。
如果不慎将碱液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液。
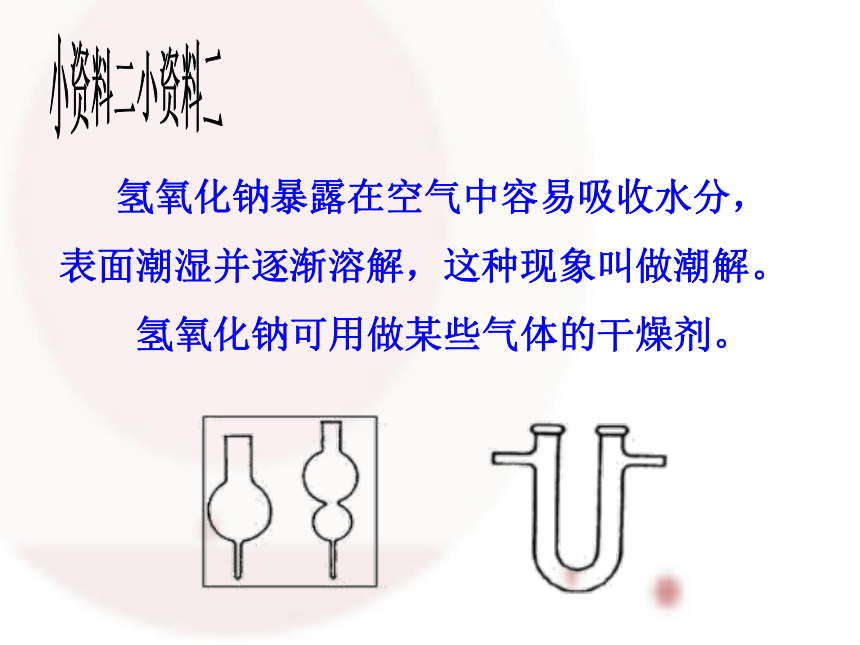
氢氧化钠暴露在空气中容易吸收水分,表面潮湿并逐渐溶解,这种现象叫做潮解。
氢氧化钠可用做某些气体的干燥剂。
(1)俗名:熟石灰、消石灰
(2)氢氧化钙的制备
CaO + H2O = Ca(OH)2
生石灰 熟石灰
反应过程中放出大量的热。
工业上通过高温煅烧石灰石生产生石灰:
氧化钙俗称生石灰,具有吸水性,常用作干燥剂。
CaCO3 CaO+CO2↑
CaCO3 CaO + CO2
高温
(1)俗名:熟石灰、消石灰
(2)氢氧化钙的制备
氢氧化钙
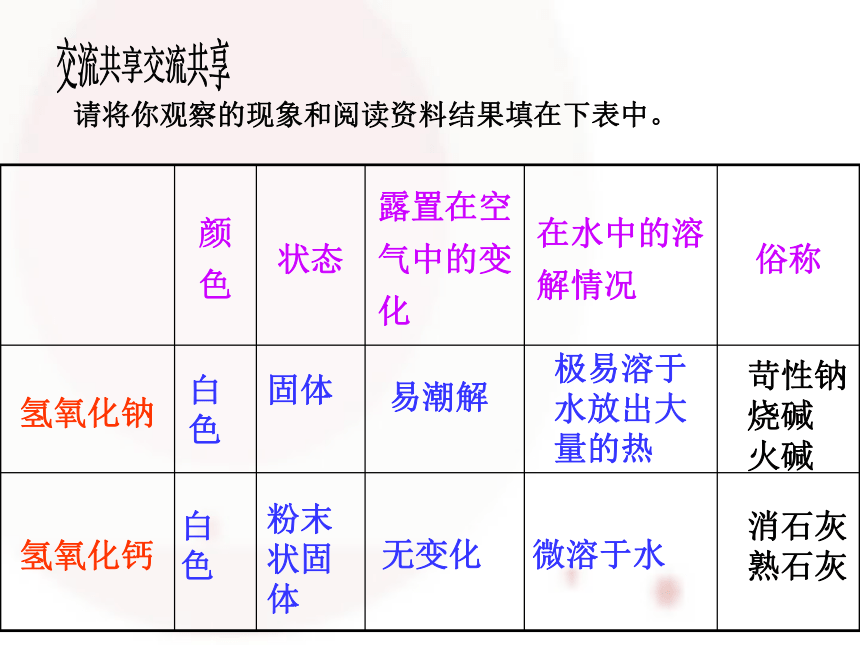
颜色 状态 露置在空气中的变化 在水中的溶解情况 俗称
氢氧化钠
氢氧化钙
白色
固体
粉末状固体
白色
微溶于水
极易溶于水放出大量的热
易潮解
无变化
请将你观察的现象和阅读资料结果填在下表中。
消石灰 熟石灰
苛性钠烧碱 火碱
合作完成下列实验
实验内容 反应现象 化学方程式
氢氧化钠的溶液 紫色石蕊试液
无色酚酞试液
生锈铁钉
氯化铜溶液
碳酸钠溶液
NaOH的化学性质
现象 化学方程式
试液变蓝
试液变红
无现象
有蓝色沉淀生成
2NaOH+CuCl2=Cu(OH)2
+2 NaCl
无现象
NaOH能否与CO2发生反应?
向盛有NaOH溶液的试管中吹入CO2,观察现象
怎样证明二者发生反应?你能否设计实验加以证明?
向两个装有CO2的矿泉水瓶中分别加入少量的NaOH溶液和水,立即盖紧瓶盖,振荡,观察现象
装有NaOH溶液的矿泉水瓶变瘪的厉害
CO2 + 2NaOH = Na2CO3 +H2O
1.若要吸收或除去二氧化碳可以用氢氧化钠溶液,可是它的反应方程式该如何写?
CO2 + 2NaOH = Na2CO3 +H2O
2.二氧化硫能污染大气,硫酸工业排放的废气里含有二氧化硫气体.工业上常用氢氧化钠溶液来吸收二氧化硫
SO2 + 2NaOH = Na2SO3+ H2O
1.若要吸收或除去二氧化碳可以用氢氧化钠溶液,可是它的反应方程式该如何写?
2.二氧化硫能污染大气,硫酸工业排放的废气里含有二氧化硫气体.工业上常用氢氧化钠溶液来吸收二氧化硫
1.若要吸收或除去二氧化碳可以用氢氧化钠溶液,可是它的反应方程式该如何写?
2.二氧化硫能污染大气,硫酸工业排放的废气里含有二氧化硫气体.工业上常用氢氧化钠溶液来吸收二氧化硫
1.若要吸收或除去二氧化碳可以用氢氧化钠溶液,可是它的反应方程式该如何写?
2.二氧化硫能污染大气,硫酸工业排放的废气里含有二氧化硫气体.工业上常用氢氧化钠溶液来吸收二氧化硫
1.若要吸收或除去二氧化碳可以用氢氧化钠溶液,可是它的反应方程式该如何写?
你能总结出NaOH的化学性质吗?
(1)与酸碱指示剂反应
(2)与非金属氧化物反应
(3)与某些盐反应
(4)与酸反应(见酸的性质)
合作完成下列实验
实验内容 反应现象 化学方程式
氢氧化钠的溶液 紫色石蕊试液
无色酚酞试液
生锈铁钉
氯化铜溶液
碳酸钠溶液
NaOH的化学性质
CO2 + 2NaOH = Na2CO3 +H2O
1.下列物质不属于碱类物质的是( )
A.纯碱(Na2CO3)
B.氢氧化铁[Fe(OH)3]
C.氢氧化钡[Ba(OH)2]
D.消石灰[Ca(OH)2]
A
2.下列说法正确的是( )
A.凡分子中含有氢氧根离子的化合物[Cu2(OH)2CO3]都属于碱类.
B.碱电离时产生的阴离子全部是氢氧根离子.
C.碱电离时生成的金属离子所带的正电荷数与氢氧根离子所带的负电荷数相等.
D.碱电离时生成的金属离子数和氢氧根离子数相等.
B
3.某溶液能使紫色石蕊试液变蓝色,则该溶液能使无色酚酞试液变( )
A.无色 B.蓝色
C.紫色 D.红色
D
4.以下是某化学探究的过程。请在下列横线上填写适当的内容。向NaOH溶液中滴入紫色石蕊试液,溶液显蓝色
(1)提出问题:是什么粒子使紫色石蕊试液蓝色呢?
(2)查找资料:NaOH溶液中存在的粒子有大量的H2O、 Na+ 、OH- 和极少量的H+ 。
(3)猜想:是大量的OH-使紫色石蕊试液蓝色。
(4)实验探究步骤及其说明:
①在一支干净试管中加入2mL蒸馏水,再滴入几滴紫色石蕊试液,溶液几平不变色,说明 ;
②在一支干净试管中加入2mL氯化钠溶液,再滴入几滴紫色石蕊试液,溶液几平不变色,说明 ;
③ 。
(5)结论:原假设 。(填“成立”或“不成立”)
第二节 碱及其性质
NaOH
KOH
Ca(OH)2
Cu(OH)2
NaOH
KOH
Ca(OH)2
NaOH
KOH
Cu(OH)2
Ca(OH)2
NaOH
KOH
NaOH
KOH
Ca(OH)2
NaOH
KOH
Cu(OH)2
Ca(OH)2
NaOH
KOH
NaOH
KOH
NaOH
Ca(OH)2
KOH
NaOH
Cu(OH)2
Ca(OH)2
KOH
NaOH
Cu(OH)2
Ca(OH)2
KOH
NaOH
NaOH
KOH
NaOH
Ca(OH)2
KOH
NaOH
Cu(OH)2
Ca(OH)2
KOH
NaOH
KOH
NaOH
Ca(OH)2
KOH
NaOH
Cu(OH)2
Ca(OH)2
KOH
NaOH
NaOH
KOH
NaOH
Ca(OH)2
KOH
Cu(OH)2
Ca(OH)2
KOH
KOH
Cu(OH)2
Cu(OH)2
Cu(OH)2
上述几种碱在组成上有什么共同特点?
(都含有OH-)
碱:电离时电离出的阴离子全部是OH-的化合物
氢氧化钠 氢氧化钙
认识氢氧化钠和氢氧化钙
认识氢氧化钠和氢氧化钙
1、观察固体氢氧化钠和氢氧化钙的颜色、状态,在表面皿中放一些固体烧碱,露置在空气中一段时间,观察它发生什么变化。
2、在两只小烧杯中分别加一些固体氢氧化钠和氢氧化钙,加入水,振荡,观察它们的溶解过程,并摸一摸烧杯,感觉溶液温度的变化。
氢氧化钠有强烈的腐蚀性,其俗名叫苛性钠、火碱或烧碱。
如果不慎将碱液沾到皮肤上,要用较多的水冲洗,再涂上硼酸溶液。
氢氧化钠暴露在空气中容易吸收水分,表面潮湿并逐渐溶解,这种现象叫做潮解。
氢氧化钠可用做某些气体的干燥剂。
(1)俗名:熟石灰、消石灰
(2)氢氧化钙的制备
CaO + H2O = Ca(OH)2
生石灰 熟石灰
反应过程中放出大量的热。
工业上通过高温煅烧石灰石生产生石灰:
氧化钙俗称生石灰,具有吸水性,常用作干燥剂。
CaCO3 CaO+CO2↑
CaCO3 CaO + CO2
高温
(1)俗名:熟石灰、消石灰
(2)氢氧化钙的制备
氢氧化钙
颜色 状态 露置在空气中的变化 在水中的溶解情况 俗称
氢氧化钠
氢氧化钙
白色
固体
粉末状固体
白色
微溶于水
极易溶于水放出大量的热
易潮解
无变化
请将你观察的现象和阅读资料结果填在下表中。
消石灰 熟石灰
苛性钠烧碱 火碱
合作完成下列实验
实验内容 反应现象 化学方程式
氢氧化钠的溶液 紫色石蕊试液
无色酚酞试液
生锈铁钉
氯化铜溶液
碳酸钠溶液
NaOH的化学性质
现象 化学方程式
试液变蓝
试液变红
无现象
有蓝色沉淀生成
2NaOH+CuCl2=Cu(OH)2
+2 NaCl
无现象
NaOH能否与CO2发生反应?
向盛有NaOH溶液的试管中吹入CO2,观察现象
怎样证明二者发生反应?你能否设计实验加以证明?
向两个装有CO2的矿泉水瓶中分别加入少量的NaOH溶液和水,立即盖紧瓶盖,振荡,观察现象
装有NaOH溶液的矿泉水瓶变瘪的厉害
CO2 + 2NaOH = Na2CO3 +H2O
1.若要吸收或除去二氧化碳可以用氢氧化钠溶液,可是它的反应方程式该如何写?
CO2 + 2NaOH = Na2CO3 +H2O
2.二氧化硫能污染大气,硫酸工业排放的废气里含有二氧化硫气体.工业上常用氢氧化钠溶液来吸收二氧化硫
SO2 + 2NaOH = Na2SO3+ H2O
1.若要吸收或除去二氧化碳可以用氢氧化钠溶液,可是它的反应方程式该如何写?
2.二氧化硫能污染大气,硫酸工业排放的废气里含有二氧化硫气体.工业上常用氢氧化钠溶液来吸收二氧化硫
1.若要吸收或除去二氧化碳可以用氢氧化钠溶液,可是它的反应方程式该如何写?
2.二氧化硫能污染大气,硫酸工业排放的废气里含有二氧化硫气体.工业上常用氢氧化钠溶液来吸收二氧化硫
1.若要吸收或除去二氧化碳可以用氢氧化钠溶液,可是它的反应方程式该如何写?
2.二氧化硫能污染大气,硫酸工业排放的废气里含有二氧化硫气体.工业上常用氢氧化钠溶液来吸收二氧化硫
1.若要吸收或除去二氧化碳可以用氢氧化钠溶液,可是它的反应方程式该如何写?
你能总结出NaOH的化学性质吗?
(1)与酸碱指示剂反应
(2)与非金属氧化物反应
(3)与某些盐反应
(4)与酸反应(见酸的性质)
合作完成下列实验
实验内容 反应现象 化学方程式
氢氧化钠的溶液 紫色石蕊试液
无色酚酞试液
生锈铁钉
氯化铜溶液
碳酸钠溶液
NaOH的化学性质
CO2 + 2NaOH = Na2CO3 +H2O
1.下列物质不属于碱类物质的是( )
A.纯碱(Na2CO3)
B.氢氧化铁[Fe(OH)3]
C.氢氧化钡[Ba(OH)2]
D.消石灰[Ca(OH)2]
A
2.下列说法正确的是( )
A.凡分子中含有氢氧根离子的化合物[Cu2(OH)2CO3]都属于碱类.
B.碱电离时产生的阴离子全部是氢氧根离子.
C.碱电离时生成的金属离子所带的正电荷数与氢氧根离子所带的负电荷数相等.
D.碱电离时生成的金属离子数和氢氧根离子数相等.
B
3.某溶液能使紫色石蕊试液变蓝色,则该溶液能使无色酚酞试液变( )
A.无色 B.蓝色
C.紫色 D.红色
D
4.以下是某化学探究的过程。请在下列横线上填写适当的内容。向NaOH溶液中滴入紫色石蕊试液,溶液显蓝色
(1)提出问题:是什么粒子使紫色石蕊试液蓝色呢?
(2)查找资料:NaOH溶液中存在的粒子有大量的H2O、 Na+ 、OH- 和极少量的H+ 。
(3)猜想:是大量的OH-使紫色石蕊试液蓝色。
(4)实验探究步骤及其说明:
①在一支干净试管中加入2mL蒸馏水,再滴入几滴紫色石蕊试液,溶液几平不变色,说明 ;
②在一支干净试管中加入2mL氯化钠溶液,再滴入几滴紫色石蕊试液,溶液几平不变色,说明 ;
③ 。
(5)结论:原假设 。(填“成立”或“不成立”)
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
