物质鉴定、提纯、推断
图片预览











文档简介
(共34张PPT)
·新课标
物质的检验与鉴别
物质的分离与提纯
物质的推断
盐的水溶液的颜色:
铜盐 溶液(Cu2+)一般 呈 蓝色
铁盐溶液(Fe3+)一般 呈 黄色
亚铁盐溶液(Fe2+)一般呈浅绿色
高锰酸钾溶液(MnO4-)呈紫红色
其它盐溶液一般为无色
盐的颜色:
固体时大多为白色晶体
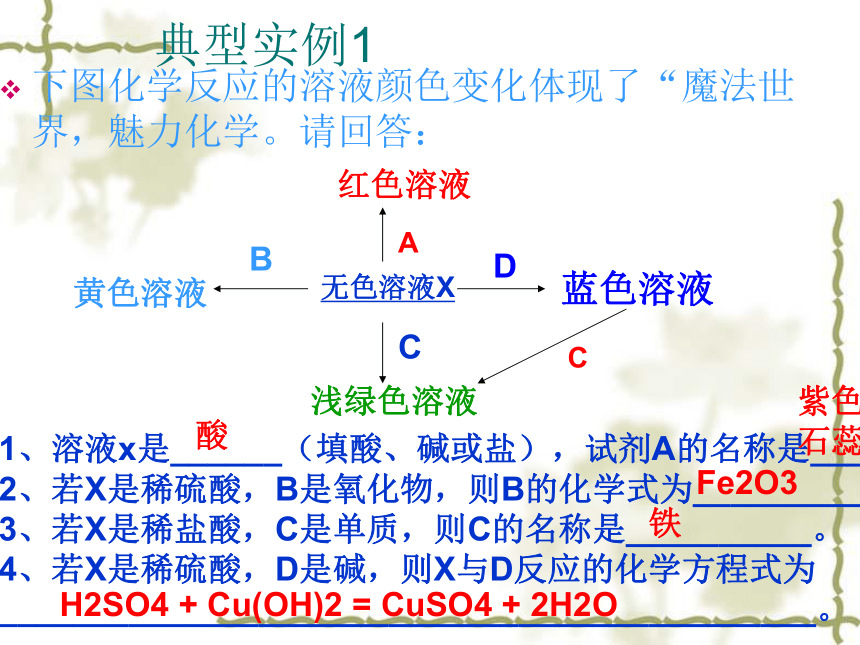
典型实例1
下图化学反应的溶液颜色变化体现了“魔法世界,魅力化学。请回答:
无色溶液X
A
红色溶液
B
黄色溶液
D
蓝色溶液
C
浅绿色溶液
C
1、溶液x是______(填酸、碱或盐),试剂A的名称是____。
2、若X是稀硫酸,B是氧化物,则B的化学式为_________。
3、若X是稀盐酸,C是单质,则C的名称是__________。
4、若X是稀硫酸,D是碱,则X与D反应的化学方程式为
____________________________________________。
酸
紫色
石蕊
Fe2O3
铁
H2SO4 + Cu(OH)2 = CuSO4 + 2H2O
判断复分解反应能否发生常涉及的沉淀有:
BaSO4(白色沉淀)
Cu(OH)2(蓝色沉淀)
1.判断复分解反应能否发生。
2.判断离子能否共存。
应 用
Mg(OH)2
BaCO3
CaCO3
AgCl(白色沉淀)
(白色沉淀)
(白色沉淀)
(白色沉淀)
Fe(OH)3(红褐色沉淀)
CuCO3(蓝色沉淀)
{
不溶酸
{
有色沉淀
典型实例2
下列各组离子能共存的是( )
A、 Ba2+、K+、NO3-、CO32-、H+
B、K+、Cl-、Mg2+、NO3-、H+
C、Fe3+、SO42-、OH-、Na+、Cu2+
D、Ag+、Ba2+、Cl-、NO3-、K+
B
·新课标
一、 物质的检验与鉴别
物质的检验 利用物质的特性(颜色、溶解性等)或反应特定的现象,证明物质的存在,如检验氧气利用______________,检验二氧化碳利用______________等
物质的鉴别 利用物质间反应的不同现象将物质区分开来
带火星的木条
澄清的石灰水
·新课标
│典例示范│
1.[2011·苏州] 下列有关物质的检验方法和结论都合理的是
A.加入稀盐酸,有无色气体产生的物质中一定含有碳酸盐
B.用燃着的木条伸入某气体中,火焰熄灭,则该气体一定是二氧化碳
C.经点燃,产生蓝色火焰的气体不一定是一氧化碳
D.尝一下,有咸味的白色固体一定是食盐
C
·新课标
│典例示范
[解析] 能与酸反应产生气体的有较活泼的金属、碳酸盐等,故A错误;氮气和二氧化碳气体一样,都不能燃烧,也不能支持燃烧,而且都能使燃着的木条熄灭,B错误;一氧化碳和甲烷燃烧都产生蓝色火焰,C正确;亚硝酸钠也有咸味,不是食盐。
·新课标
│典例示范
2.[2011·苏州] 下列区别两种不同物质的方法合理的是
A.用蒸馏水区别四氧化三铁与二氧化锰
B.用酚酞溶液区别氯化钠溶液与稀醋酸
C.用加热的方法区别碳酸氢铵与氯化钠
D.用石蕊溶液区别稀烧碱溶液与石灰水
C
·新课标
│典例示范
[解析] 四氧化三铁和二氧化锰都是不溶于水的黑色固体,A错误;氯化钠和稀醋酸都不能使酚酞溶液变色,B错误;碳酸氢铵受热分解产生有刺激性气味的气体,氯化钠受热没有明显现象,C正确;烧碱溶液和石灰水都会使石蕊溶液变蓝,D错误。
·新课标
│针对练习│
1.[2011·聊城] 下列区分物质的试剂或方法不正确的是
A.用水区分氯化钙和碳酸钙
B.用酚酞溶液区分盐酸和食盐水
C.用肥皂水区分硬水和软水
D.用闻气味的方法区分白醋和白酒
B
·新课标
│ 针对练习
[解析] 氯化钙可溶于水,碳酸钙不溶于水,A正确;盐酸和食盐水都不能使酚酞溶液变色,B错误;硬水降低肥皂的起泡能力,C正确;白醋有酸味,白酒有特殊香味,D正确。
·新课标
│ 针对练习
2.[2011·济南] 三瓶失去标签的无色溶液,已知分别是H2SO4溶液、Ba(OH)2溶液、KCl溶液中的各一种,下列四种试液中,能将上述三种溶液一次鉴别出来的是( )
A.Na2CO3溶液
B.NaOH溶液
C.MgCl2溶液
D.酚酞溶液
A
·新课标
│ 针对练习
[解析] 稀硫酸和碳酸钠反应产生气泡,氢氧化钡和碳酸钠反应产生白色沉淀,氯化钾与碳酸钠不反应。
|针对训练|
3、不用其它试剂,用最简捷的方法鉴别:①氢氧化钠②硫酸镁③硝酸钡④氯化铁⑤氯化钾五种溶液,则被鉴别出来的物质的正确的顺序是( )
A、①②③④⑤ B、④①②③⑤
C、④③①②⑤ D、②③①④⑤
B
|针对训练|
解析:先观察颜色,氯化铁为黄色,其余溶液为无色,首先鉴别出④;然后用其它物质与氯化铁反应,有红褐色沉淀的是氢氧化钠,再鉴别出 ;再用氢氧化钠与其它物质反应,有白色沉淀的是 硫酸镁;再用硫酸镁剩下的物质反应,有白色沉淀的是 硝酸钡。
·新课标
│典例示范│
1.下列除杂(括号内是杂质)所选试剂合理的是( )
A.Cu(Fe) 稀盐酸
B.CO2气体(HCl) 氢氧化钠溶液
C.CuO(Cu) 稀硫酸
D.Na2SO4溶液(Na2CO3) 氯化钡溶液
A
·新课标
│典例示范
[解析] 稀盐酸与铁反应使铁溶解,铜不与稀盐酸反应,A合理;氢氧化钠不但能与氯化氢气体反应,而且还能与二氧化碳反应,B不合理;稀硫酸只与被提纯物质氧化铜反应,不与杂质铜反应,C不合理;氯化钡与硫酸钠和碳酸钠都反应,D不合理。
·新课标
│典例示范
2.[2011·淄博] 除去下列物质中混有的少量杂质,所选用的试剂及操作方法不正确的是
序号 物质 杂质(少量) 试剂和操作方法
A O2 水蒸气 通过浓H2SO4
B 稀盐酸 稀硫酸 加入适量BaCl2
溶液,过滤
C Na2CO3粉末 NaHCO3粉末 加热
D KNO3溶液 Ba(NO3)2
溶液 加入适量的Na2SO4
溶液,过滤
D
·新课标
│典例示范
[解析] 浓硫酸具有吸水性,可以除去氧气中的水蒸气,A正确;氯化钡与稀硫酸反应生成沉淀和稀盐酸,可过滤除去沉淀,B正确;碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,C正确;硝酸钡与硫酸钠反应生成硫酸钡沉淀的同时产生硝酸钠新的杂质,D错误。
·新课标
│ 针对练习
3.[2011·达州] 下列各组括号内除杂质的方法或试剂错误的是
A.CO2中混有CO(点燃)
B.Cu粉中混有CuO(稀硫酸)
C.CO中混有CO2 (氢氧化钠溶液)
D.Cu粉中混有Fe粉(用磁铁吸引)
A
·新课标
│ 针对练习
[解析] 大量的二氧化碳中混有的少量一氧化碳无法被点燃。
·新课标
│ 针对练习
4.下列除杂试剂使用正确的是
选项 物质(括号内为杂质) 除杂试剂
A C(Fe) 盐酸
B CaCl2溶液(HCl) Ba(OH)2溶液
C CO2 (CO) 碱石灰(CaO和
NaOH 的混合物)
D NaOH 溶液[Ca(OH)2] K2CO3 溶液
A
·新课标
│ 针对练习
[解析] 盐酸只与铁反应,可过滤得到碳,A正确;氢氧化钡与盐酸反应产生新的杂质氯化钡,B错误;碱石灰与二氧化碳反应,C错误;碳酸钾与氢氧化钙反应引入新的杂质氢氧化钾,D错误。
·新课标
│考点梳理│
三、物质的推断
首先:利用物理性质(颜色、溶解性)
其次:根据特征的反应或现象——“题眼”,然后向正向或反向推理,得出每一结论。
最后:总结前面结论。
·新课标
│典例示范│
1.[2011·大庆] 现有一包白色粉末,可能含有NaCl、Na2CO3、Na2SO4、CuCl2、CaCl2中的一种或几种物质。取少量该粉末,加入水中溶解后得到无色透明的溶液,向所得的溶液加入足量的Ba(NO3)2溶液后,产生白色沉淀。取所产生的白色沉淀,加入足量的稀硝酸溶液,沉淀全部溶解。根据上述操作及现象,下列说中一定正确的是 ( )
A.原粉末中一定有Na2CO3、Na2SO4
B.原粉末中可能含有NaCl、CaCl2
C.原粉末中一定没有CuCl2、Na2SO4、CaCl2
D.原粉末中只有Na2CO3一种物质
C
·新课标
│典例示范
[解析] 溶于水得到无色透明溶液,说明一定不含有氯化铜,且碳酸钠和氯化钙最多只能含有一种;加入硝酸钡产生白色沉淀且沉淀全部可溶于稀硝酸,说明原物质中不含有硫酸钠,一定含有碳酸钠,则原物质中一定不含有氯化钙;原物质中是否含有氯化钠无法确定。
·新课标
│典例示范
2.[2011·宁波] A~E为初中化学中常见的物质,其中A能使带火星的木条复燃,E的浓溶液能使小木棒变黑。它们的反应转化关系如图K19-1所示(图中部分生成物未标出)。
·新课标
│典例示范
(1)金属单质B的化学式是__________;
(2)金属铁与蓝色溶液D反应的化学方程式为________________________________。
Fe+CuSO4===FeSO4+Cu
Cu
[解析] A能使带火星的木条复燃,则A是氧气;E的浓溶液能使小木棒变黑,则E为硫酸;蓝色溶液为硫酸铜,黑色固体为氧化铜,金属B为铜。
·新课标
│针对练习│
5.[2011·宜宾] 已知:①常温常压下,A为无色液体,A在二氧化锰的催化作用下分解为水和B,B是空气的组成成分之一。②C单质在足量的B中燃烧生成气体D,D能使澄清石灰水变浑浊。③C单质在不足量的B中燃烧生成有毒气体E,E与红色物质F的反应是工业炼铁的原理。请按要求填空:
(1)A的化学式为______________。
(2)请简述如何检验B?________________________________________________________________________。
H2O2
将带火星的木条伸入盛有B气体的集气瓶中,如果木条复燃,则说明该气体为氧气
·新课标
│ 针对练习
(3)B与C生成D的基本反应类型是____________反应。
(4)完成E与F反应的化学方程式______________________________。
化合
3CO+Fe2O3 2Fe+3CO2
高温
·新课标
│ 针对练习
6.根据下列发生的反应,推断A、B、C、D、E、F六种物质的化学式或名称(提示:难溶性碱加热可生成金属氧化物和水):
①A+B―→C+H2O;
②C+KOH―→D(蓝色)↓+E
③D A+H2O;
④E+AgNO3―→F↓(白色凝乳状不溶于硝酸的盐)+KNO3。
A是__________;B是________;
C是______________;D是______________;E是___________; F是__________。
CuO(氧化铜)
HCl(盐酸)
CuCl2(氯化铜)
Cu(OH)2(氢氧化铜)
KCl(氯化钾)
AgCl(氯化银)
·新课标
│ 针对练习
[解析] 该题的“突破口”为反应式②或④,因为与AgNO3溶液反应后生成的白色凝乳状且又不溶于稀硝酸的沉淀物必定为AgCl,根据复分解反应的规律可以推出E为KCl,蓝色沉淀D为氢氧化铜,可推出C为CuCl2,再结合反应①③可得出A为氧化铜,B为盐酸。
·新课标
物质的检验与鉴别
物质的分离与提纯
物质的推断
盐的水溶液的颜色:
铜盐 溶液(Cu2+)一般 呈 蓝色
铁盐溶液(Fe3+)一般 呈 黄色
亚铁盐溶液(Fe2+)一般呈浅绿色
高锰酸钾溶液(MnO4-)呈紫红色
其它盐溶液一般为无色
盐的颜色:
固体时大多为白色晶体
典型实例1
下图化学反应的溶液颜色变化体现了“魔法世界,魅力化学。请回答:
无色溶液X
A
红色溶液
B
黄色溶液
D
蓝色溶液
C
浅绿色溶液
C
1、溶液x是______(填酸、碱或盐),试剂A的名称是____。
2、若X是稀硫酸,B是氧化物,则B的化学式为_________。
3、若X是稀盐酸,C是单质,则C的名称是__________。
4、若X是稀硫酸,D是碱,则X与D反应的化学方程式为
____________________________________________。
酸
紫色
石蕊
Fe2O3
铁
H2SO4 + Cu(OH)2 = CuSO4 + 2H2O
判断复分解反应能否发生常涉及的沉淀有:
BaSO4(白色沉淀)
Cu(OH)2(蓝色沉淀)
1.判断复分解反应能否发生。
2.判断离子能否共存。
应 用
Mg(OH)2
BaCO3
CaCO3
AgCl(白色沉淀)
(白色沉淀)
(白色沉淀)
(白色沉淀)
Fe(OH)3(红褐色沉淀)
CuCO3(蓝色沉淀)
{
不溶酸
{
有色沉淀
典型实例2
下列各组离子能共存的是( )
A、 Ba2+、K+、NO3-、CO32-、H+
B、K+、Cl-、Mg2+、NO3-、H+
C、Fe3+、SO42-、OH-、Na+、Cu2+
D、Ag+、Ba2+、Cl-、NO3-、K+
B
·新课标
一、 物质的检验与鉴别
物质的检验 利用物质的特性(颜色、溶解性等)或反应特定的现象,证明物质的存在,如检验氧气利用______________,检验二氧化碳利用______________等
物质的鉴别 利用物质间反应的不同现象将物质区分开来
带火星的木条
澄清的石灰水
·新课标
│典例示范│
1.[2011·苏州] 下列有关物质的检验方法和结论都合理的是
A.加入稀盐酸,有无色气体产生的物质中一定含有碳酸盐
B.用燃着的木条伸入某气体中,火焰熄灭,则该气体一定是二氧化碳
C.经点燃,产生蓝色火焰的气体不一定是一氧化碳
D.尝一下,有咸味的白色固体一定是食盐
C
·新课标
│典例示范
[解析] 能与酸反应产生气体的有较活泼的金属、碳酸盐等,故A错误;氮气和二氧化碳气体一样,都不能燃烧,也不能支持燃烧,而且都能使燃着的木条熄灭,B错误;一氧化碳和甲烷燃烧都产生蓝色火焰,C正确;亚硝酸钠也有咸味,不是食盐。
·新课标
│典例示范
2.[2011·苏州] 下列区别两种不同物质的方法合理的是
A.用蒸馏水区别四氧化三铁与二氧化锰
B.用酚酞溶液区别氯化钠溶液与稀醋酸
C.用加热的方法区别碳酸氢铵与氯化钠
D.用石蕊溶液区别稀烧碱溶液与石灰水
C
·新课标
│典例示范
[解析] 四氧化三铁和二氧化锰都是不溶于水的黑色固体,A错误;氯化钠和稀醋酸都不能使酚酞溶液变色,B错误;碳酸氢铵受热分解产生有刺激性气味的气体,氯化钠受热没有明显现象,C正确;烧碱溶液和石灰水都会使石蕊溶液变蓝,D错误。
·新课标
│针对练习│
1.[2011·聊城] 下列区分物质的试剂或方法不正确的是
A.用水区分氯化钙和碳酸钙
B.用酚酞溶液区分盐酸和食盐水
C.用肥皂水区分硬水和软水
D.用闻气味的方法区分白醋和白酒
B
·新课标
│ 针对练习
[解析] 氯化钙可溶于水,碳酸钙不溶于水,A正确;盐酸和食盐水都不能使酚酞溶液变色,B错误;硬水降低肥皂的起泡能力,C正确;白醋有酸味,白酒有特殊香味,D正确。
·新课标
│ 针对练习
2.[2011·济南] 三瓶失去标签的无色溶液,已知分别是H2SO4溶液、Ba(OH)2溶液、KCl溶液中的各一种,下列四种试液中,能将上述三种溶液一次鉴别出来的是( )
A.Na2CO3溶液
B.NaOH溶液
C.MgCl2溶液
D.酚酞溶液
A
·新课标
│ 针对练习
[解析] 稀硫酸和碳酸钠反应产生气泡,氢氧化钡和碳酸钠反应产生白色沉淀,氯化钾与碳酸钠不反应。
|针对训练|
3、不用其它试剂,用最简捷的方法鉴别:①氢氧化钠②硫酸镁③硝酸钡④氯化铁⑤氯化钾五种溶液,则被鉴别出来的物质的正确的顺序是( )
A、①②③④⑤ B、④①②③⑤
C、④③①②⑤ D、②③①④⑤
B
|针对训练|
解析:先观察颜色,氯化铁为黄色,其余溶液为无色,首先鉴别出④;然后用其它物质与氯化铁反应,有红褐色沉淀的是氢氧化钠,再鉴别出 ;再用氢氧化钠与其它物质反应,有白色沉淀的是 硫酸镁;再用硫酸镁剩下的物质反应,有白色沉淀的是 硝酸钡。
·新课标
│典例示范│
1.下列除杂(括号内是杂质)所选试剂合理的是( )
A.Cu(Fe) 稀盐酸
B.CO2气体(HCl) 氢氧化钠溶液
C.CuO(Cu) 稀硫酸
D.Na2SO4溶液(Na2CO3) 氯化钡溶液
A
·新课标
│典例示范
[解析] 稀盐酸与铁反应使铁溶解,铜不与稀盐酸反应,A合理;氢氧化钠不但能与氯化氢气体反应,而且还能与二氧化碳反应,B不合理;稀硫酸只与被提纯物质氧化铜反应,不与杂质铜反应,C不合理;氯化钡与硫酸钠和碳酸钠都反应,D不合理。
·新课标
│典例示范
2.[2011·淄博] 除去下列物质中混有的少量杂质,所选用的试剂及操作方法不正确的是
序号 物质 杂质(少量) 试剂和操作方法
A O2 水蒸气 通过浓H2SO4
B 稀盐酸 稀硫酸 加入适量BaCl2
溶液,过滤
C Na2CO3粉末 NaHCO3粉末 加热
D KNO3溶液 Ba(NO3)2
溶液 加入适量的Na2SO4
溶液,过滤
D
·新课标
│典例示范
[解析] 浓硫酸具有吸水性,可以除去氧气中的水蒸气,A正确;氯化钡与稀硫酸反应生成沉淀和稀盐酸,可过滤除去沉淀,B正确;碳酸氢钠受热分解生成碳酸钠、水和二氧化碳,C正确;硝酸钡与硫酸钠反应生成硫酸钡沉淀的同时产生硝酸钠新的杂质,D错误。
·新课标
│ 针对练习
3.[2011·达州] 下列各组括号内除杂质的方法或试剂错误的是
A.CO2中混有CO(点燃)
B.Cu粉中混有CuO(稀硫酸)
C.CO中混有CO2 (氢氧化钠溶液)
D.Cu粉中混有Fe粉(用磁铁吸引)
A
·新课标
│ 针对练习
[解析] 大量的二氧化碳中混有的少量一氧化碳无法被点燃。
·新课标
│ 针对练习
4.下列除杂试剂使用正确的是
选项 物质(括号内为杂质) 除杂试剂
A C(Fe) 盐酸
B CaCl2溶液(HCl) Ba(OH)2溶液
C CO2 (CO) 碱石灰(CaO和
NaOH 的混合物)
D NaOH 溶液[Ca(OH)2] K2CO3 溶液
A
·新课标
│ 针对练习
[解析] 盐酸只与铁反应,可过滤得到碳,A正确;氢氧化钡与盐酸反应产生新的杂质氯化钡,B错误;碱石灰与二氧化碳反应,C错误;碳酸钾与氢氧化钙反应引入新的杂质氢氧化钾,D错误。
·新课标
│考点梳理│
三、物质的推断
首先:利用物理性质(颜色、溶解性)
其次:根据特征的反应或现象——“题眼”,然后向正向或反向推理,得出每一结论。
最后:总结前面结论。
·新课标
│典例示范│
1.[2011·大庆] 现有一包白色粉末,可能含有NaCl、Na2CO3、Na2SO4、CuCl2、CaCl2中的一种或几种物质。取少量该粉末,加入水中溶解后得到无色透明的溶液,向所得的溶液加入足量的Ba(NO3)2溶液后,产生白色沉淀。取所产生的白色沉淀,加入足量的稀硝酸溶液,沉淀全部溶解。根据上述操作及现象,下列说中一定正确的是 ( )
A.原粉末中一定有Na2CO3、Na2SO4
B.原粉末中可能含有NaCl、CaCl2
C.原粉末中一定没有CuCl2、Na2SO4、CaCl2
D.原粉末中只有Na2CO3一种物质
C
·新课标
│典例示范
[解析] 溶于水得到无色透明溶液,说明一定不含有氯化铜,且碳酸钠和氯化钙最多只能含有一种;加入硝酸钡产生白色沉淀且沉淀全部可溶于稀硝酸,说明原物质中不含有硫酸钠,一定含有碳酸钠,则原物质中一定不含有氯化钙;原物质中是否含有氯化钠无法确定。
·新课标
│典例示范
2.[2011·宁波] A~E为初中化学中常见的物质,其中A能使带火星的木条复燃,E的浓溶液能使小木棒变黑。它们的反应转化关系如图K19-1所示(图中部分生成物未标出)。
·新课标
│典例示范
(1)金属单质B的化学式是__________;
(2)金属铁与蓝色溶液D反应的化学方程式为________________________________。
Fe+CuSO4===FeSO4+Cu
Cu
[解析] A能使带火星的木条复燃,则A是氧气;E的浓溶液能使小木棒变黑,则E为硫酸;蓝色溶液为硫酸铜,黑色固体为氧化铜,金属B为铜。
·新课标
│针对练习│
5.[2011·宜宾] 已知:①常温常压下,A为无色液体,A在二氧化锰的催化作用下分解为水和B,B是空气的组成成分之一。②C单质在足量的B中燃烧生成气体D,D能使澄清石灰水变浑浊。③C单质在不足量的B中燃烧生成有毒气体E,E与红色物质F的反应是工业炼铁的原理。请按要求填空:
(1)A的化学式为______________。
(2)请简述如何检验B?________________________________________________________________________。
H2O2
将带火星的木条伸入盛有B气体的集气瓶中,如果木条复燃,则说明该气体为氧气
·新课标
│ 针对练习
(3)B与C生成D的基本反应类型是____________反应。
(4)完成E与F反应的化学方程式______________________________。
化合
3CO+Fe2O3 2Fe+3CO2
高温
·新课标
│ 针对练习
6.根据下列发生的反应,推断A、B、C、D、E、F六种物质的化学式或名称(提示:难溶性碱加热可生成金属氧化物和水):
①A+B―→C+H2O;
②C+KOH―→D(蓝色)↓+E
③D A+H2O;
④E+AgNO3―→F↓(白色凝乳状不溶于硝酸的盐)+KNO3。
A是__________;B是________;
C是______________;D是______________;E是___________; F是__________。
CuO(氧化铜)
HCl(盐酸)
CuCl2(氯化铜)
Cu(OH)2(氢氧化铜)
KCl(氯化钾)
AgCl(氯化银)
·新课标
│ 针对练习
[解析] 该题的“突破口”为反应式②或④,因为与AgNO3溶液反应后生成的白色凝乳状且又不溶于稀硝酸的沉淀物必定为AgCl,根据复分解反应的规律可以推出E为KCl,蓝色沉淀D为氢氧化铜,可推出C为CuCl2,再结合反应①③可得出A为氧化铜,B为盐酸。
