高中化学人教版(2019)必修第一册第三章第一节 铁的重要化合物(共19张ppt)
文档属性
| 名称 | 高中化学人教版(2019)必修第一册第三章第一节 铁的重要化合物(共19张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 6.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-25 00:00:00 | ||
图片预览






文档简介
(共19张PPT)
化学
·
必修1
铁是人体必需的微量元素中含量最多的一种(约4~5克),缺铁性贫血已成为仅次于结核病的全球患病率最高、耗资最大的公共卫生问题。
二价铁为人体的主要存在形式
铁在自然界中的含量居第四位,仅次于氧、硅和铝,主要以+2和+3价化合物的形式存在。
那铁元素在人体中又是以什么形式存在呢?
情景导入
动物肝脏
瘦肉
鸡蛋黄
黄豆
黑木耳
蘑菇
红枣
桂圆
葡萄
铁在自然界中分布极为广泛,为何人类发现和利用铁却比黄金和铜要迟?
黄铁矿
FeS2
问题探究
赤铁矿-Fe2O3
黄铁矿-FeS2
磁铁矿-Fe3O4
名称
氧化亚铁
氧化铁
四氧化三铁
俗称
化学式
色态
化合价
水溶性
类型
与酸
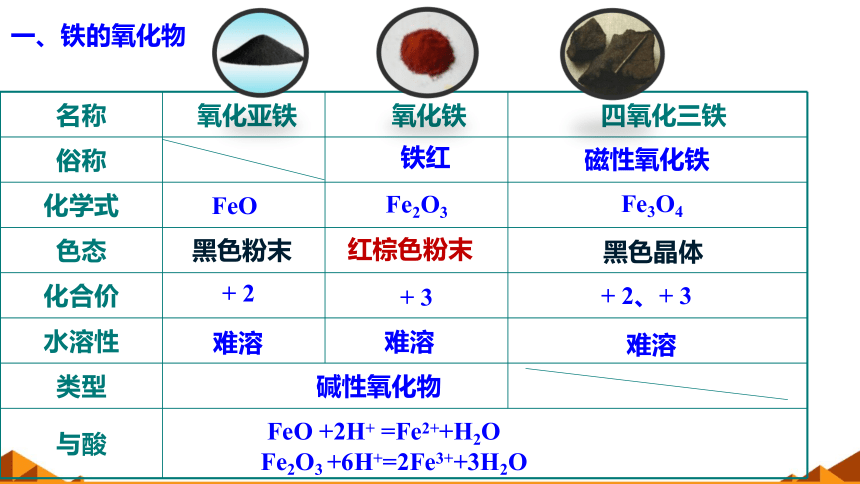
一、铁的氧化物
铁红
磁性氧化铁
FeO
Fe2O3
Fe3O4
黑色粉末
红棕色粉末
黑色晶体
+
2
+
3
+
2、+
3
难溶
难溶
难溶
FeO
+2H+
=Fe2++H2O
Fe2O3
+6H+=2Fe3++3H2O
碱性氧化物
用途:
Fe2O3
红色油漆和涂料,炼铁原料
氧化铁可做外墙涂料
一、铁的氧化物
在两支试管里分别加入少量FeCl3溶液和FeSO4溶液,然后滴入NaOH溶液。观察并描述发生的现象。
—FeSO4
溶液
—NaOH溶液
—FeCl3
溶液
—NaOH溶液
二、铁的氢氧化物
离子方程式
FeCl3溶液
FeSO4溶液
试管中产生红褐色沉淀
试管中先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色
加入NaOH溶液
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
4Fe(OH)2+O2+2H2O
=4Fe(OH)3
白色
灰绿色
红褐色
二、铁的氢氧化物
归纳总结
为什么在溶液中加入溶液时,生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色呢?
Fe(OH)2+O2+
H2O=
Fe(OH)3,
+2
+3
0
-2
化合价升高,失
1e-,被氧化
想一想
化合价降低,得
2e-,被还原
4
2
4
4×
2×
Fe(OH)2在空气中极易被氧化,实验室中如何采取一定措施制得白色的Fe(OH)2沉淀呢?
把胶头滴管插入溶液深处滴加NaOH溶液
用煮沸过的蒸馏水配制FeSO4
、NaOH溶液
液封:在配制好的FeSO4溶液上面滴加少量煤油
思考与交流
Fe(OH)2和Fe(OH)3都是不溶性碱,两者难溶于水,易溶于酸。你能写出它们与(盐酸)酸反应的化学/离子方程式吗?
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+=
Fe3++3H2O
Fe(OH)2+2HCl=FeCl2+2H2O/
Fe(OH)3+3HCl=FeCl3+3H2O/
二、铁的氢氧化物
学与问
加热Fe(OH)3,
能失去水生成红棕色的Fe2O3粉末
2Fe(OH)3==Fe2O3+H2O
?
二、铁的氢氧化物
化学式
Fe(OH)2
Fe(OH)3
色态
溶解性
稳定性
与O2反应
与酸反应
制备
白色固体
红褐色固体
难溶
难溶
不稳定,易被空气氧化
受热可分解
2Fe(OH)3
Fe2O3+H2O
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+=
Fe3++3H2O
4Fe(OH)2+2H2O+O2=4Fe(OH)3
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
白色→灰绿色→红褐色
总结感悟
?
切开的苹果在空气中很容易变黄,这是为什么呢?
1、Fe3+的检验
三、铁盐和亚铁盐
滴入KSCN溶液
FeCl2溶液
FeCl3溶液
无明显变化
棕黄色溶液变成血红色
Fe3++3SCN-
=
Fe(SCN)3
结论与应用:含有Fe3+的盐溶液遇到KSCN溶液时,变成血红色,可以利用该反应检验Fe3+的存在
实验3-10
2、Fe3+和Fe2+的转化
三、铁盐和亚铁盐
科学探究
加入
现象
反应的离子方程式
在FeCl3溶液中加入铁粉,KSCN溶液
上层清液加入氯水,振荡
2Fe3++Fe=3Fe2+
溶液不显血红色
溶液变成血红色
2Fe2++Cl2=2Fe3++2Cl-
结论
Fe3+遇到较强的还原剂时,会被还原成Fe2+
,而在较强的氧化剂的作用下会被氧化成Fe3+。
Fe3+
Fe2+
Fe3+
Fe2+
溶液颜色
与碱反应
检验
黄色
浅绿色
Fe(OH)2沉淀
Fe(OH)3沉淀
⑴观察溶液的颜色
⑵加OH-
⑶加KSCN溶液
⑴观察溶液的颜色
⑵加OH-,观察沉淀颜色变化
⑶加KSCN后再加氯水
总结感悟
三、铁盐和亚铁盐
Fe2+
Fe3+
氧化剂(Cl2
O2
HNO3
KMnO4)
浅绿色
棕黄色
Fe(OH)3
Fe(OH)2
红褐色
白色
空气中放置
OH-
H+
小结
OH-
H+
还原剂(Fe
Cu
I-
S2-
)
了解FeCl3制作印刷电路板,用化学方程式表示其所用的化学原理。
制作过程:
先在塑料板上镀上一层铜,然后在设计好的铜线路上涂上一层石蜡,把板浸到氯化铁溶液中,没有在线路上的铜即没有被石蜡覆盖住的铜就被反应掉。
活学活用
当堂巩固
1、为检验某FeCl2溶液是否变质可以向溶液中加入(
)
A、
NaOH
溶液
B、
铁片
C、
KSCN
溶液
D、石蕊试液
2、在含有1molFeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤,然后在空气中灼烧沉淀,得到的固体物质是(
)
A、Fe
B、
FeO
C、
Fe(OH)3
D、Fe2O3
C
D
化学
·
必修1
铁是人体必需的微量元素中含量最多的一种(约4~5克),缺铁性贫血已成为仅次于结核病的全球患病率最高、耗资最大的公共卫生问题。
二价铁为人体的主要存在形式
铁在自然界中的含量居第四位,仅次于氧、硅和铝,主要以+2和+3价化合物的形式存在。
那铁元素在人体中又是以什么形式存在呢?
情景导入
动物肝脏
瘦肉
鸡蛋黄
黄豆
黑木耳
蘑菇
红枣
桂圆
葡萄
铁在自然界中分布极为广泛,为何人类发现和利用铁却比黄金和铜要迟?
黄铁矿
FeS2
问题探究
赤铁矿-Fe2O3
黄铁矿-FeS2
磁铁矿-Fe3O4
名称
氧化亚铁
氧化铁
四氧化三铁
俗称
化学式
色态
化合价
水溶性
类型
与酸
一、铁的氧化物
铁红
磁性氧化铁
FeO
Fe2O3
Fe3O4
黑色粉末
红棕色粉末
黑色晶体
+
2
+
3
+
2、+
3
难溶
难溶
难溶
FeO
+2H+
=Fe2++H2O
Fe2O3
+6H+=2Fe3++3H2O
碱性氧化物
用途:
Fe2O3
红色油漆和涂料,炼铁原料
氧化铁可做外墙涂料
一、铁的氧化物
在两支试管里分别加入少量FeCl3溶液和FeSO4溶液,然后滴入NaOH溶液。观察并描述发生的现象。
—FeSO4
溶液
—NaOH溶液
—FeCl3
溶液
—NaOH溶液
二、铁的氢氧化物
离子方程式
FeCl3溶液
FeSO4溶液
试管中产生红褐色沉淀
试管中先生成白色絮状沉淀,迅速变成灰绿色,最后变成红褐色
加入NaOH溶液
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
4Fe(OH)2+O2+2H2O
=4Fe(OH)3
白色
灰绿色
红褐色
二、铁的氢氧化物
归纳总结
为什么在溶液中加入溶液时,生成的白色絮状沉淀迅速变成灰绿色,最后变成红褐色呢?
Fe(OH)2+O2+
H2O=
Fe(OH)3,
+2
+3
0
-2
化合价升高,失
1e-,被氧化
想一想
化合价降低,得
2e-,被还原
4
2
4
4×
2×
Fe(OH)2在空气中极易被氧化,实验室中如何采取一定措施制得白色的Fe(OH)2沉淀呢?
把胶头滴管插入溶液深处滴加NaOH溶液
用煮沸过的蒸馏水配制FeSO4
、NaOH溶液
液封:在配制好的FeSO4溶液上面滴加少量煤油
思考与交流
Fe(OH)2和Fe(OH)3都是不溶性碱,两者难溶于水,易溶于酸。你能写出它们与(盐酸)酸反应的化学/离子方程式吗?
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+=
Fe3++3H2O
Fe(OH)2+2HCl=FeCl2+2H2O/
Fe(OH)3+3HCl=FeCl3+3H2O/
二、铁的氢氧化物
学与问
加热Fe(OH)3,
能失去水生成红棕色的Fe2O3粉末
2Fe(OH)3==Fe2O3+H2O
?
二、铁的氢氧化物
化学式
Fe(OH)2
Fe(OH)3
色态
溶解性
稳定性
与O2反应
与酸反应
制备
白色固体
红褐色固体
难溶
难溶
不稳定,易被空气氧化
受热可分解
2Fe(OH)3
Fe2O3+H2O
Fe(OH)2+2H+=Fe2++2H2O
Fe(OH)3+3H+=
Fe3++3H2O
4Fe(OH)2+2H2O+O2=4Fe(OH)3
Fe3++3OH-=Fe(OH)3↓
Fe2++2OH-=Fe(OH)2↓
白色→灰绿色→红褐色
总结感悟
?
切开的苹果在空气中很容易变黄,这是为什么呢?
1、Fe3+的检验
三、铁盐和亚铁盐
滴入KSCN溶液
FeCl2溶液
FeCl3溶液
无明显变化
棕黄色溶液变成血红色
Fe3++3SCN-
=
Fe(SCN)3
结论与应用:含有Fe3+的盐溶液遇到KSCN溶液时,变成血红色,可以利用该反应检验Fe3+的存在
实验3-10
2、Fe3+和Fe2+的转化
三、铁盐和亚铁盐
科学探究
加入
现象
反应的离子方程式
在FeCl3溶液中加入铁粉,KSCN溶液
上层清液加入氯水,振荡
2Fe3++Fe=3Fe2+
溶液不显血红色
溶液变成血红色
2Fe2++Cl2=2Fe3++2Cl-
结论
Fe3+遇到较强的还原剂时,会被还原成Fe2+
,而在较强的氧化剂的作用下会被氧化成Fe3+。
Fe3+
Fe2+
Fe3+
Fe2+
溶液颜色
与碱反应
检验
黄色
浅绿色
Fe(OH)2沉淀
Fe(OH)3沉淀
⑴观察溶液的颜色
⑵加OH-
⑶加KSCN溶液
⑴观察溶液的颜色
⑵加OH-,观察沉淀颜色变化
⑶加KSCN后再加氯水
总结感悟
三、铁盐和亚铁盐
Fe2+
Fe3+
氧化剂(Cl2
O2
HNO3
KMnO4)
浅绿色
棕黄色
Fe(OH)3
Fe(OH)2
红褐色
白色
空气中放置
OH-
H+
小结
OH-
H+
还原剂(Fe
Cu
I-
S2-
)
了解FeCl3制作印刷电路板,用化学方程式表示其所用的化学原理。
制作过程:
先在塑料板上镀上一层铜,然后在设计好的铜线路上涂上一层石蜡,把板浸到氯化铁溶液中,没有在线路上的铜即没有被石蜡覆盖住的铜就被反应掉。
活学活用
当堂巩固
1、为检验某FeCl2溶液是否变质可以向溶液中加入(
)
A、
NaOH
溶液
B、
铁片
C、
KSCN
溶液
D、石蕊试液
2、在含有1molFeSO4的溶液中投入一小块金属钠,反应完全后,滤出沉淀并洗涤,然后在空气中灼烧沉淀,得到的固体物质是(
)
A、Fe
B、
FeO
C、
Fe(OH)3
D、Fe2O3
C
D
