浙江省2020-2021年中考科学试题分类——专题17 粒子的模型与符号(解析版)
文档属性
| 名称 | 浙江省2020-2021年中考科学试题分类——专题17 粒子的模型与符号(解析版) |

|
|
| 格式 | docx | ||
| 文件大小 | 543.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-06-24 00:00:00 | ||
图片预览



文档简介
2020-2021年浙江省中考科学试题分类——专题17粒子的模型与符号
一、单选题
1.(2021·宁波)如图是物质甲和乙反应生成丙的微观示意图。下列说法正确的是( ???)
A.?该反应属于化合反应
B.?甲、乙、丙都是有机物
C.?该反应中参加反应的甲和乙质量比为1:1
D.?该反应在反应前后原子的种类发生了改变
2.(2021·宁波)含硫元素的同类物质中硫元素的化合价可能不同,不同类物质中硫元素的化合价可能相同,如表所示。下列判断正确的是( ???)
类别
物质
化合价
单质
氧化物
酸
X
0
a
-
-
-
+4
-
b
d
Na2SO3等
+6
-
c
e
f
A.?X表示碱
B.?物质a在空气中燃烧会发出明亮的蓝紫色火焰
C.?物质b是二氧化硫,它是空气污染物之一
D.?物质d和NaOH溶液发生中和反应生成Na2SO4和H2O
3.(2021·温州)氮化锶(Sr3N2)是生产高端荧光粉的主要原料。已知Sr3N2中N的化合价为-3,则Sr的化合价为(??? )
A.?-3?????????????????????????????????????????B.?-2?????????????????????????????????????????C.?+2?????????????????????????????????????????D.?+3
4.(2021·温州)2021年4月,我国科学家首次合成的铀-214,是目前已知质量最小的铀原子。其相对原子质量为214,质子数是92。则铀-214原子的核外电子数为(??? )
A.?92???????????????????????????????????????B.?122???????????????????????????????????????C.?214???????????????????????????????????????D.?306
5.(2021·湖州)二氧化碳和二氧化硫都是由AB2型分子构成的物质,但分子中A原子和B原子的空间位置不同,其模型如右图所示。根据此模型,下列叙述错误的是( ??)
A.?两种物质都由两种元素组成????????????????????????????????B.?两种物质中碳元素和硫元素化合价相同
C.?两种物质的化学性质相同????????????????????????????????????D.?分子中原子空间位置不同是因为A原子种类不同
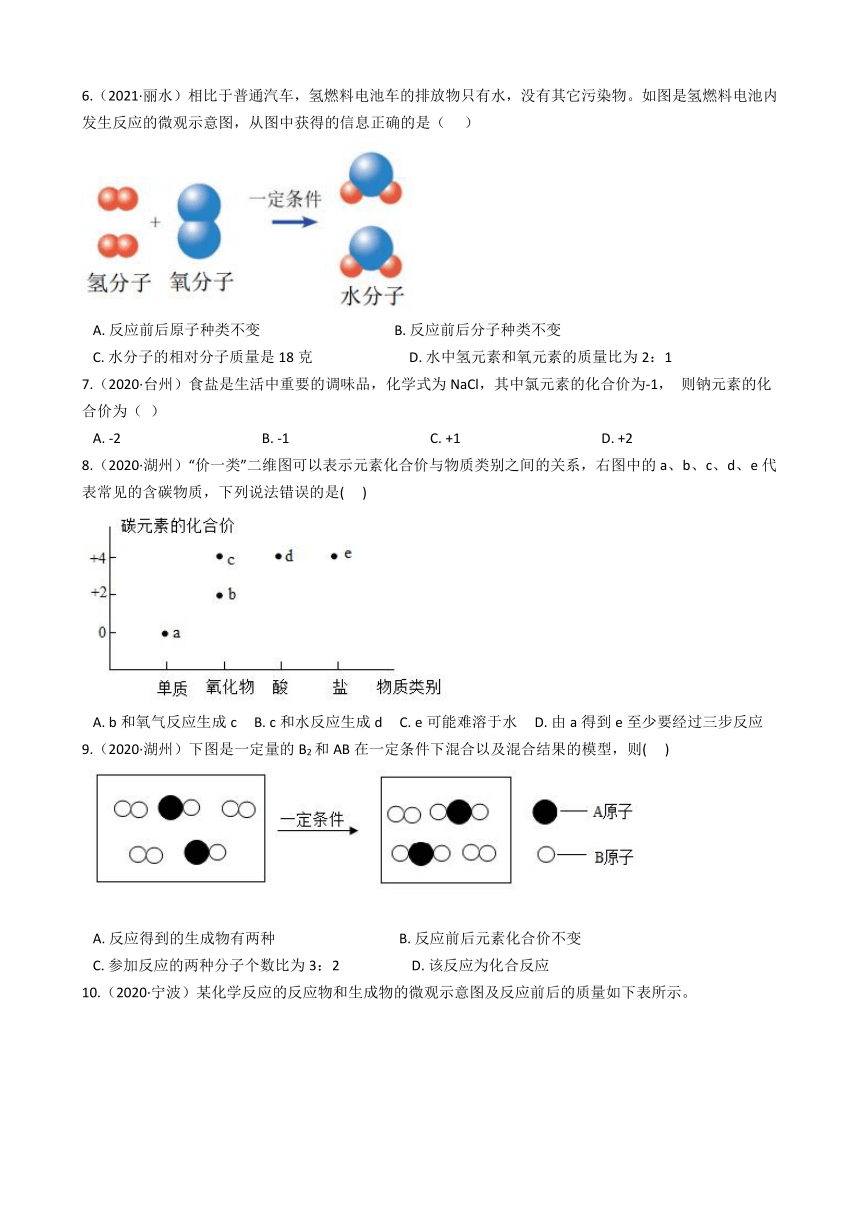
6.(2021·丽水)相比于普通汽车,氢燃料电池车的排放物只有水,没有其它污染物。如图是氢燃料电池内发生反应的微观示意图,从图中获得的信息正确的是( ???)
A.?反应前后原子种类不变???????????????????????????????????????B.?反应前后分子种类不变
C.?水分子的相对分子质量是18克????????????????????????????D.?水中氢元素和氧元素的质量比为2:1
7.(2020·台州)食盐是生活中重要的调味品,化学式为NaCl,其中氯元素的化合价为-1, 则钠元素的化合价为( )
A.?-2?????????????????????????????????????????B.?-1?????????????????????????????????????????C.?+1?????????????????????????????????????????D.?+2
8.(2020·湖州)“价一类”二维图可以表示元素化合价与物质类别之间的关系,右图中的a、b、c、d、e代表常见的含碳物质,下列说法错误的是(??? )
A.?b和氧气反应生成c?????B.?c和水反应生成d?????C.?e可能难溶于水?????D.?由a得到e至少要经过三步反应
9.(2020·湖州)下图是一定量的B2和AB在一定条件下混合以及混合结果的模型,则(??? )
?
A.?反应得到的生成物有两种????????????????????????????????????B.?反应前后元素化合价不变
C.?参加反应的两种分子个数比为3:2?????????????????????D.?该反应为化合反应
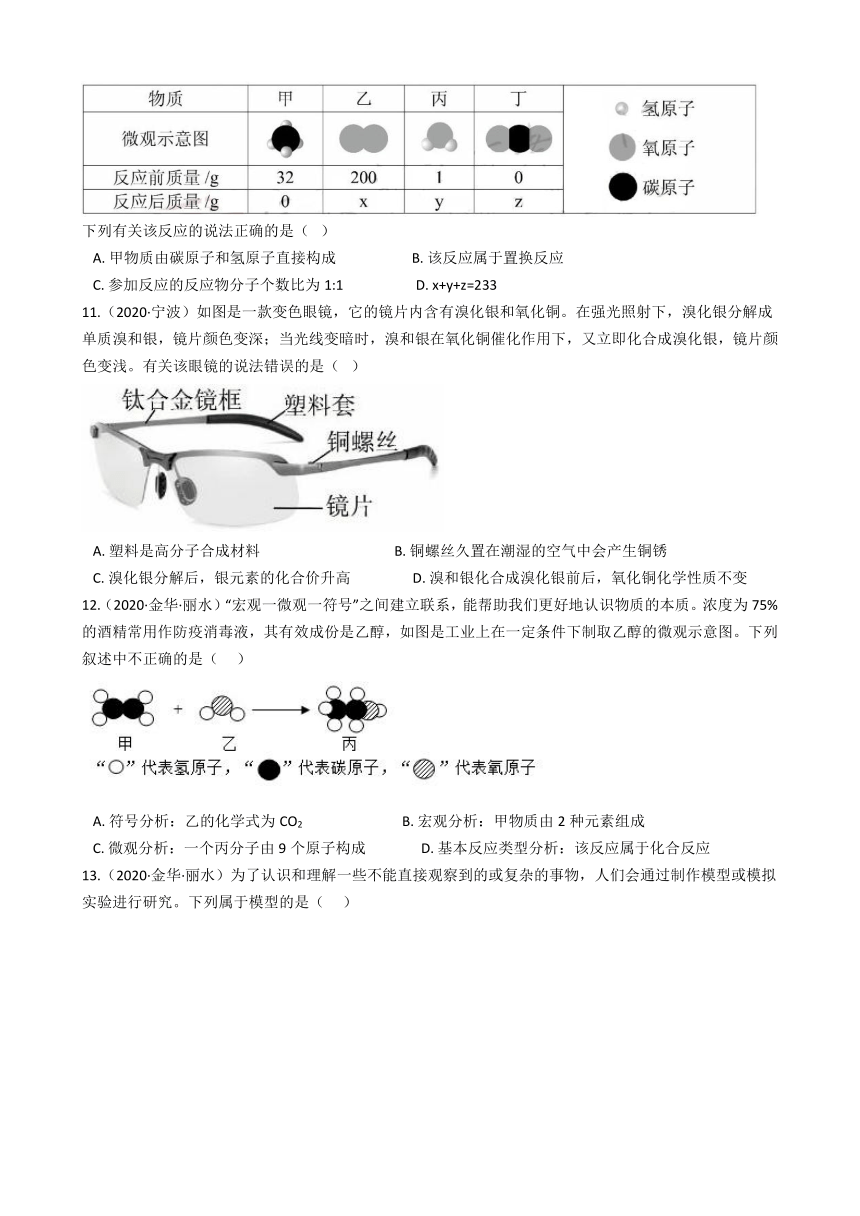
10.(2020·宁波)某化学反应的反应物和生成物的微观示意图及反应前后的质量如下表所示。
下列有关该反应的说法正确的是( ?)
A.?甲物质由碳原子和氢原子直接构成??????????????????????B.?该反应属于置换反应
C.?参加反应的反应物分子个数比为1:1?????????????????????D.?x+y+z=233
11.(2020·宁波)如图是一款变色眼镜,它的镜片内含有溴化银和氧化铜。在强光照射下,溴化银分解成单质溴和银,镜片颜色变深;当光线变暗时,溴和银在氧化铜催化作用下,又立即化合成溴化银,镜片颜色变浅。有关该眼镜的说法错误的是( ?)
A.?塑料是高分子合成材料???????????????????????????????????????B.?铜螺丝久置在潮湿的空气中会产生铜锈
C.?溴化银分解后,银元素的化合价升高??????????????????D.?溴和银化合成溴化银前后,氧化铜化学性质不变
12.(2020·金华·丽水)“宏观一微观一符号”之间建立联系,能帮助我们更好地认识物质的本质。浓度为75%的酒精常用作防疫消毒液,其有效成份是乙醇,如图是工业上在一定条件下制取乙醇的微观示意图。下列叙述中不正确的是( ???)
A.?符号分析:乙的化学式为CO2?????????????????????????????B.?宏观分析:甲物质由2种元素组成
C.?微观分析:一个丙分子由9个原子构成????????????????D.?基本反应类型分析:该反应属于化合反应
13.(2020·金华·丽水)为了认识和理解一些不能直接观察到的或复杂的事物,人们会通过制作模型或模拟实验进行研究。下列属于模型的是( ???)
A.?用力拉板使纸断裂 ??????????????????B.?向内推书使书隆起
C.?地球仪 ???????????????????????????????????????????D.?铅笔在篮球和木板上移动
14.(2020·温州)银器在使用过程中,因为发生化学反应:4Ag+O2+2H2S=2Ag2S+2H2O,产生的Ag2S使银器逐渐失去光泽。已知银的化合价为+1价,则Ag2S中S的化合价为(??? )
A.?+2?????????????????????????????????????????B.?-2?????????????????????????????????????????C.?+1?????????????????????????????????????????D.?-1
15.(2020·绍兴)与图示微观变化相符的化学反应是(??? )
A.?2CO+O2 点燃__ 2CO2????????????????????????????????????????B.?H2+CuO ? H2O+Cu
C.?2H2+O2 点燃__ 2H2O????????????????????????????????????????D.?H2CO3 ? H2O+CO2↑
16.(2020·嘉兴)某化合物在水中能完全电离,将该化合物配制成甲、乙、丙三种不同浓度的水溶液,对溶液中所含阴、阳离子数目进行测定,结果如图所示。由图可判断该化合物可能是( ?)
A.?CaCl2???????????????????????????????B.?Al(NO3)3? ???????????????????????????????C.?NaOH???????????????????????????????D.?H2SO4
二、填空题
17.(2021·温州)1783年,拉瓦锡利用如图装置探究水的组成:往A杯中滴加少量的水,水通过灼热的铁管时发生汽化,水蒸气与灼热的铁反应,生成了一种黑色固体(Fe3O4)和“可燃空气”,将气体通过放在冷水中的铜管,在B装置中收集到纯净的可燃空气。最终,拉瓦锡证明了水是由两种元素组成的。
(1)将气体通过放在冷水中的铜管,目的是除去________。
(2)将B装置收集到的可燃空气在氧气中点燃,生成了水。可燃空气的名称是________。
(3)若该实验中生成的黑色固体质量为m1 , 可燃空气的质量为m2 , 可燃空气完全燃烧生成水的质量为m3 , 如果水是由“氧元素”和“可燃空气元素”组成的,则m1、m2、m3三者应满足的关系是________。
18.(2021·绍兴)? 2021年3月,四川三星堆遗址进行了新一轮考古发掘。至今三星堆已出土了黄金面具、青铜纵目面具等一批珍贵文物,如图。
(1)出土的黄金面具仍金光灿灿,而青铜纵目面具已锈迹斑斑,这说明金的活动性比铜________(选填“强”或“弱”)。
(2)古代制作青铜器的铜来源于铜矿,如黄铜矿。黄铜矿的主要成分为二硫化亚铁铜 (CuFeS2),其中铁元素和铜元素均为+2价,硫元素的化合价为 ________。
(3)应用碳-14测出三星堆遗址距今3000年左右,碳-12和碳-14是碳元素的两种同位素原子,它们的主要区别是原子核中________?数不同。
19.(2021·丽水)“价类图”是以化合价为纵坐标、物质类别为横坐标绘制的图像,它能将散乱的科学知识联系在一起,有助于对科学问题的理解和整体认知。如图是含氯元素的物质的价类图,其中“一”表示物质间的转化关系。请回答;
(1)A和氢氧化钾反应得到D和水,则该反应属于基本反应类型中的化合价________;
(2)物质C的化学式为________;
(3)E在一定条件下得到D的化学方程式为________。
20.(2020·衢州)用高能粒子轰击原子核是研究微观粒子的一种方法。
1934年,意大利科学家费米用中子轰击铀原子(质子数为92,元素符号为U),得到了一种质量增加的原子,他公开宣布发现了93号元素,被科学界认可,从而获得了诺贝尔物理学奖。
1938年,德国科学家哈恩在重复费米的实验后,发现费米实验中得到的是56号钡元素,并用图示模型来定义这一变化。费米知道后,立即重复哈恩的实验,结果证实自己错了,费米坦率地检讨并纠正了错误。
(1)费米用中子轰击铀原子,不可能增加铀原子的________数,所以得不到93号元素。
(2)结合材料分析,以下观点正确的是???????? 。
A.面对前人的观点要敢于质疑
B.科学结论的得出要依据客观事实
C.对科学的认识是一个不断修正、完善的过程
21.(2020·衢州)某品牌新能源电动汽车使用磷酸铁锂电池,其反应原理: LiFePO4?放电充电FePO4+Li 。该电池具有容量大、续航能力强的特点。
(1)LiFePO4 , 中铁元素与氧元素的质量比为________。
(2)该电池充电时发生的化学反应属于________(填基本反应类型)。
22.(2020·湖州)由我国自主研发的深海载人潜水器球壳于2019年建造完成并通过验收。球壳用被称为“海洋金属”的钛合金作为制造材料。钛合金不仅强度高而且具有弹性。右图为钛元素在元素周期表中的部分信息。
(1)钛原子的质子数为________。
(2)Ti除了表示钛元素、一个钛原子之外,还能表示________?。
(3)钛元素的化合价为+4价时,其对应的氧化物被认为是现今世界上性能最好的一种白色颜料。它的化学式为________。
23.(2020·金华·丽水)人们为了揭示原子结构的奥秘,经历了漫长的探究过程。1911年物理学家卢瑟福用带正电的α粒子轰击金属箔。实验发现:多数α粒子穿过金属箔后仍保持原来的运动方向,绝少数α粒子发生了较大角度的偏转。
(1)卢瑟福提出了原子的核式结构模型,认为原子的中心有一个很小的________?;
(2)当α粒子轰击金属箔时,图中四条运动轨迹不可能出现的是________(填字母)。
24.(2020·温州)茶是人类健康的饮品之一,联合国将今年5月21日定为首个“国际茶日”。
(1)茶园是一个生态系统,能保持相对稳定,除人的作用外,还与生态系统具有一定的________能力有关。
(2)在泡茶过程中,会闻到茶特有的香气,这是因为分子________。
(3)茶氨酸(C7H14N2O3)是茶树特有的一种氨基酸。茶氨酸中氮元素与氧元素的质量比为 ________。
三、解答题
25.(2021·宁波)“青团”是宁波的一种传统食物。在“青团”制作过程中,需要往糯米粉中添加艾草(或艾草汁)。艾草含有侧柏莲酮芳香油(C10H10O),侧柏莲酮芳香油是一种淡黄色液体,具有香脂香气,所以“青团”具有独特风味。
(1)侧柏莲酮芳香油由________种元素组成。
(2)7.3g侧柏莲桐芳香油中碳元素的质量为________g。
(3)侧柏莲桐芳香油在氧气中完全燃烧的产物是________。
26.(2021·杭州)磁铁矿石(含Fe3O4)是常用的炼铁原料,工业上可通过如下反应:4CO+Fe3O4 高温__ 3Fe+4CO2 , 将其中的Fe3O4转化为Fe。
(1)Fe3O4中铁元素和氧元素的质量比为________。
(2)假设冶炼过程中铁没有损耗,用含有464吨Fe3O4的磁铁矿石可提炼出含铁质量分数为96%的生铁多少吨?
27.(2021·杭州)氮是空气中含量最多的元素,也是构成生物体的必要元素之一但是,空气中游离态的氮不能直接被大多数生物所利用,必须经过变化,并与其他成分形成化合物(如氨或铵盐等),才能被植物利用。如图是自 然界氮循环的示意图请回答:
(1)一株绿色植物的幼苗(如小麦)在生长过程中缺氮其最可能出现的症状是?????。
A.茎秆细小、易倒伏,叶有褐斑??
B.生长矮小,叶色发黄
C.生长缓慢,叶色暗绿带红
D.只开花不结果
(2)工业上常用空气冷冻分离法来获得氮气(即由液态空气分馏来获得氮气)这种方法制氮气的原理是利 用了氮气与氧气哪一物理性质的差异?________。
(3)实验室制备少量氮气的方法很多。例如,可由亚硝酸铵来制取氮气,其反应如下:NH4NO2 Δ__ N2↑+2H2O,该反应是属于________反应(选填“化合”、“分解”、“置换或“复分解”)
(4)空气中的N2转化为NH3 , 的过程中,N元素的化合价由0价转变为________价
(5)有人认为:人类可以通过人工固氮,大量合成含氮化肥并施用于农作物,这将有助于人类粮食增产,但也会造成环境污染。你是否同他的观点并阐述理由。
28.(2021·绍兴)按我国政府要求2021年1月1日起餐饮行业已禁用不可降解的一次性塑料吸管,取而代之的是一些可降解的环保吸管,环保纸吸管的主要成分是纤维素,化学式为(C6H10O5)n,而原来塑料吸管的主要成分是聚丙烯,化学式为(C3H6)n。
(1)纤维素是一种________(选填“有机物”或“无机物”)。
(2)纤维素分子中,氢、氧原子的个数比为 ________?。
(3)计算32.4克纤维素中所含碳元素质量与多少克聚丙烯中所含碳元素质量相同?
29.(2021·嘉兴)氕、氘、氚是氢的三种同位素原子,它们的原子结构模型如图所示,相关信息如下表。试回答:
名称
符号
相对原子质量
氕
H
1
氘
D
2
氚
T
3
(1)超重水有一定的放射性。一个超重水分子由两个氚原子和一个氧原子构成,其化学式可表示为T2O。T2O中T的化合价为________。
(2)重水是由氘和氧组成的化合物,化学式可表示为D2O,重水和普通水化学性质相似。在海水中重水的质量约占0.02%,则100吨海水中所含氘的质量是多少?
(3)原子结构模型中的“ ?”表示的粒子是________。
30.(2021·湖州)人类对未知世界的认知都是在实践和探索中不断地修正和深化的。
(1)原子结构模型的建立是几代科学家通过实验和思维不断地进行修正的。其中卢瑟福基于α粒子轰击金属箔的实验事实,经过思考得出“原子的全部正电荷都集中在________里”这一结论,该结论是对汤姆生关于正电荷均匀分布观点的修正。
(2)“谁控制生物的遗传?”人类对这一命题的认识是不断深化的,直到________双螺旋结构的问世,才标志着对遗传的研究进入到分子水平.
31.(2020·台州)碰碰香是一种常见的室内盆栽植物,因触碰后可散发出令人舒适的香气而得名,其香气具有提神醒脑、驱避蚊虫的作用。
(1)碰碰香受到外力触碰时会释放香味,这种现象属于植物的________性。
(2)在室内其他地方也能闻到碰碰香散发的香味,是因为________。
(3)碰碰香的香味物质中含量最多的是柠檬烯,其化学式为C10H16。计算:
①柠檬烯中碳元素、氢元素的质量比为________。
②柠檬烯中碳元素的质量分数是多少________?(计算结果精确到0.1%)
32.(2020·宁波)覆盆子果实含有丰富的维生素、少量水杨酸以及钙、钾等元素,有“黄金水果”的美誉。其中的水杨酸常温下稳定,加热易分解,微溶于水,其水溶液呈酸性。
(1)覆盆子果实中的钙、钾等元素是以________(填“单质”或“化合物”)的形态存在。
(2)水杨酸(C7H6O3)中碳元素和氧元素的质量比为________。
(3)水杨酸的上述性质中,属于物理性质的是:________。
33.(2020·绍兴)2019年诺贝尔化学奖用地表彰锂离子电池的研发。这种质量轻、可充电、功能强大的电池现在被广泛应用于手机、笔记本电脑和电动汽车等各种产品。
(1)锂电池充电时,电能转化为________能。
(2)碳酸二甲酯(C3H6O3)是锂电池电解液的一种成分,下列关于碳酸二甲酯说法正确的有 ?????。
A.由C,H,O三种元素组成
B.碳元素的质量分数最大
C.相对分子质量是90克
D.分子中C,H,O三种原子的个数比为1:2:1
(3)图为某款锂电池手机在不同温度下的电压随时间变化的图像,请结合图像分析手机夏天比冬天耐用的原因是:________。
34.(2020·嘉兴)随着手机、电脑等移动设备的普及,人们对充电设备的要求越来越高。最近,某品牌氮化镓充电设备以体积小、功率大深受消费者喜爱。
(1)氮化镓(GaN)是充电设备中的核心材料。查阅资料得知:氮化镓中氮元素的化合价与氨气(NH3)中氮元素的化合价相同。由此可知,氮化镓中镓元素的化合价为________。
(2)氮化镓的制取可通过镓与氨气在高温下发生置换反应来实现,其反应的化学方程式为________。
(3)该品牌氮化镓充电器支持“5V 3A”“12V 3A”“20V 3.2A”三个输出档,请分析计算它的最大输出功率。
答案解析部分
一、单选题
1.【答案】 A
【解析】【分析】(1)多种物质反应生成一种物质,该反应为化合反应;
(2)有机物一般指有机化合物,狭义上的有机化合物主要是指由碳元素、氢元素组成,一定是含碳的化合物,但是不包括碳的氧化物和硫化物、碳酸、碳酸盐、氰化物、硫氰化物、氰酸盐、碳化物、碳硼烷、羰基金属、不含M-C键的金属有机配体配合物;
(3)根据示意图确定分子的组成,进而计算出参加反应的物质质量之比;
(4)根据示意图分析反应前后原子的种类是否改变即可。
【解答】A.该反应反应物有两种,生成物只有一种,为化合反应,故A正确;
B.根据示意图可知,乙中不含碳元素,肯定不是有机物,故B错误;
C.甲的化学式为C2H4 , 乙的化学式为H2O,则参加反应的甲和乙的质量之比为:(12×2+1×4):(1×2+16)=28:18,故C错误;
D.反应前后原子的种类都是三种,故D错误。
故选A。
2.【答案】 C
【解析】【分析】(1)碱由金属离子和氢氧根离子构成;
(2)根据硫在空气中燃烧的现象判断;
(3)根据正负化合价代数和为零,确定氧化物b的化学式,并根据它的性质判断;
(4)根据正负化合价代数和为零,确定氧化物d的化学式,并根据它的性质判断。
【解答】A.根据化学式 Na2SO3 可知,亚硫酸钠由金属离子和亚硫酸根构成,则x为盐而不是碱,故A错误;
B.a为硫单质,它在空气中燃烧生成淡蓝色火焰,故B错误;
C.设氧化物的化学式为SxOy,根据正负化合价代数和为零得到:(+4)x+(-2)y=0,解得:x:y=1:2,那么化学式为SO2 , 它有刺激性气味,严重污染空气,故C正确;
D.物质d为酸,其中S元素化合价为+4价,那么应该为H2SO3 , 与氢氧化钠反应,生成Na2SO3和H2O,故D错误。
故选C。
3.【答案】 C
【解析】【分析】根据化合物中元素化合价代数和为0分析。
【解答】 Sr3N2中N的化合价为-3,设Sr元素化合价为x,则3x+(-3)×2=0,解得x=+2;
故选C。
4.【答案】 A
【解析】【分析】根据原子中质子数=电子数分析。
【解答】原子中质子数=电子数,该原子质子数为92,则核外电子数也为92,A正确;
故选A。
5.【答案】 C
【解析】【分析】根据图示中分子构成分析,结合化合物中元素化合价代数和为0、不同种分子性质不同解答。
【解答】 A、 由分子构成可知,两种物质都由两种元素组成 ,不符合题意;
B、 两种物质中碳元素和硫元素化合价都是+4价,不符合题意;
C、 两种物质的分子构成不同,则化学性质不相同 ,符合题意;
D、 分子中原子空间位置不同是因为A原子种类不同 ,不符合题意;
故选C。
6.【答案】 A
【解析】【分析】根据化学变化过程中分子种类一定改变,原子种类一定不变,水的相对分子质量及元素质量比分析。
【解答】A、反应前后原子种类不发生改变,符合题意;
B、反应前后分子种类一定发生改变,不符合题意;
C、 水分子的相对分子质量是18 ,不符合题意;
D、 水中氢元素和氧元素的质量比为1:8,不符合题意;
故选A。
7.【答案】 C
【解析】【分析】化合价是一种元素的一个原子与其他元素的原子化合{即构成化合物}时表现出来的性质。
【解答】由化合物的化合价代数和为零可知,x+(-1)=0;x=+1;
故答案为:C。
8.【答案】 D
【解析】【分析】根据所给碳元素化合价及类别,结合二氧化碳、一氧化碳的性质进行判断分析。
【解答】A、b为+2价碳的氧化物,为CO,c为+4价氧化物,为二氧化碳,一氧化碳与氧气反应可生成二氧化碳,不符合题意;
B、d为碳酸,二氧化碳与水反应生成碳酸,不符合题意;
C、e为碳酸盐,可能溶于水也可能不溶于水,不符合题意;
D、碳燃烧生成二氧化碳,二氧化碳与氢氧化钠等碱溶液反应可生成碳酸盐,所以 a得到e经过两步反应即可实现,符合题意;
故答案为:D。
9.【答案】 D
【解析】【分析】先根据反应前后相同的粒子是未参加反应的粒子,确定出参加反应和生成的微粒,再结合单质到化合物的变化中一定有元素化合价变化及“多变一”的反应为化合反应分析。
【解答】A、划去没有参加反应的粒子,该反应为, 由此可知生成物只一种物质,不符合题意;
B、该反应为一种单质和一种化合物发生的化合反应,一定有元素化合价的变化,不符合题意;
C、参加反应的两种分子个数比为2:1,不符合题意;
D、该反应为两种物质生成一种物质,属于化合反应,符合题意;
故答案为:D。
10.【答案】 D
【解析】【分析】根据图中所给各粒子的构成书写出反应方程式,结合置换反应定义及化学式的配平系数解答。
【解答】A、甲物质为甲烷,由分子构成,其分子由碳原子和氢原子构成,不符合题意;
B、该反应中生成物中没有单质,不属于置换反应,不符合题意;
C、该反应方程式为CH4+2O2=CO2+2H2O,参加反应的分子个数比为1:2,不符合题意;
D、由反应前后质量关系可知,x+y+z=32+200+1=233,符合题意;
故答案为:D。
11.【答案】 C
【解析】【分析】(1)合成纤维、合成塑料和合成橡胶,是三大合成材料;
(2)铜和空气中的氧气、二氧化碳和水反应,生成碱式碳酸铜,也就是铜绿;
(3)计算出银元素的化合价,然后进行比较即可;
(4)根据催化剂的性质判断。
【解答】A.塑料是高分子合成材料,故A正确不合题意;
B.铜螺丝久置在潮湿的空气中会产生铜锈,故B正确不合题意;
C.在溴化银中,银元素的化合价为+1价,在银单质中化合价为0价,因此溴化银分解后,银元素的化合价降低了,故C错误符合题意;
D.催化剂在反应前后性质和质量不变,因此溴和银化合成溴化银前后,氧化铜化学性质不变,故D正确不合题意。
故选C。
12.【答案】 A
【解析】【分析】(1)根据物质乙的分子示意图确定它的化学式;
(2)根据甲分子的示意图确定它的元素组成;
(3)根据丙分子的示意图确定它的原子个数;
(4)根据反应物和生成物的种类和种数确定化学反应种类。
【解答】A.根据乙的示意图可知,乙分子由1个氧原子和2个氢原子构成,那么化学式为:H2O,故A错误符合题意;
B.根据甲的示意图可知,甲物质由氢元素和碳元素组成,故B正确不合题意;
C.根据丙的示意图可知,一个丙分子由2个碳原子、6个氢原子和1个氧原子组成,一共有9个原子,故C正确不合题意;
D.反应物有两种,而生成物只有一种,因此该反应为化合反应,故D正确不合题意。
故选A。
13.【答案】 C
【解析】【分析】1、建立模型的意义:可以帮助人们认识和理解一些不能直接观察到的事物。模型可以是一幅图、一张表格、或一个公式;
2、在难以直接拿研究对象做实验时,有时用模型来做实验,即模仿实验对象制作模型,或者模仿实验的某些条件进行实验,这样的实验叫做模拟实验。
【解答】A、 用力拉板使纸断裂 ,这是模拟向两侧拉的力的作用下地壳的变化的模拟实验,A错误;
B、 向内推书使书隆起 ,这是模拟挤压力下地壳的变形的模拟实验,B错误;
C、地球仪是地球的模型,C正确;
D、 铅笔在篮球和木板上移动 ,这是模拟地球上远去的帆船实验,是模拟实验,D错误。
故选C
14.【答案】 B
【解析】【分析】在化学式中,正负化合价的代数和为零,据此计算。
【解答】在 Ag2S 中,银的化合价为+1价,根据正负化合价代数和为零得到:(+1)×2+x=0,解得:x=-2价,故B正确,而A、C、D错误。
故选B。
15.【答案】 A
【解析】【分析】该题主要考查模型和化学反应的类型;
【解答】由变化示意图可知,该反应中反应物是单质和化合物,生成一种化合物的过程,且单质、化合物化学计量数之比为1:2;故A符合题意;
故答案为:A。
16.【答案】 C
【解析】【分析】根据图像确定该化合物中阴、阳离子的个数之比,然后对四个选项进行判断即可。
【解答】根据图像可知,无论溶液的浓度如何,该化合物的阴、阳离子的个数之比为:2n:2n=1:1;4n:4n=1:1;6n:6n=1:1。在四种物质中,只有NaOH的阴、阳离子的个数之比为1:1,故C正确,而A、B、D错误。
故选C。
二、填空题
17.【答案】 (1)水蒸气
(2)氢气
(3)829 m1+m2=m3
【解析】【分析】(1)根据气体中含有水蒸气分析;
(2)根据质量守恒定律分析;
(3)根据四氧化三铁中氧元素质量为水中氧元素质量,水的质量为氢元素和氧元素质量和分析。
【解答】(1)将气体通过放冷水中的铜管,是降低温度除去气体中的水蒸气;
(2)由反应前元素的种类可知,生成的可燃空气为氢气;
(3)生成水中氧元素质量即为四氧化三铁中氧元素质量,氧元素质量为64232m1=829m1,水的质量为氢元素和氧元素质量和,则 829 m1+m2=m3;
故答案为:(1)水蒸气;(2)氢气;(3) 829 m1+m2=m3。
18.【答案】 (1)弱
(2)-2
(3)中子
【解析】【分析】(1)根据金的活动性比铜弱分析;
(2)根据化合物中元素化合价代数和为0分析;
(3)根据同种元素中不同种原子中子数不同分析。
【解答】(1) 出土的黄金面具仍金光灿灿,而青铜纵目面具已锈迹斑斑,说明铜的发生了缓慢氧化,而金没有,即金的活动性比铜弱;
(2) 二硫化亚铁铜 (CuFeS2),其中铁元素和铜元素均为+2价,根据化合物中元素化合价代数和为0可知,硫元素的化合价为-2价;
(3) 碳-12和碳-14是碳元素的两种同位素原子,它们的主要区别是原子核中的中子数不同;
故答案为:(1)弱;(2)-2;(3)中子。
19.【答案】 (1)复分解反应
(2)ClO2
(3)2KClO2 MnO2__△ 2KCl+3O2↑
【解析】【分析】根据所给氯元素化合价及物质类别确定出对应点的物质,再按要求填空分析。
【解答】(1) A为盐酸,和氢氧化钾反应得到D和水,D为氯化钾,则该反应属于复分解反应;
(2)物质C为+4价氯的氧化物,化学式为 ClO2 ;
(3) E为+5价氯的盐,在一定条件下得到D,则E为氯酸钾,反应方程式为 2KClO2 MnO2__△ 2KCl+3O2↑ ;
故答案为:(1)复分解反应;(2) ClO2 ;(3) 2KClO2 MnO2__△ 2KCl+3O2↑ 。
20.【答案】 (1)质子
(2)A,B,C
【解析】【分析】(1)元素的原子序数等于原子的质子数。根据质量守恒定律可知,用中子轰击铀原子,只可能增加中子数,不可能增加质子数;
(2)根据题目描述的科学发展史进行分析判断。
【解答】(1)费米用中子轰击铀原子,不可能增加铀原子的质子数,所以得不到93号元素。
(2)A.哈恩重复费米的实验后,根据实验的结果对费米的实验提出质疑,可见面对前人的观点要敢于质疑,故A正确;
B.费米知道哈恩的实验结果后,自己再次实验发现原来的结果是错误的,检讨并纠正了错误,这说明科学结论的得出要依据客观事实,故B正确;
C.在科学探究的路上,难免遇到困难,或者得出错误的结论,只要坚持一切以事实为依据的原则,肯定最终能够得到正确结论,故C正确。
故选ABC。
21.【答案】 (1)7:8
(2)分解反应
【解析】【分析】(1)元素的质量之比等于相对原子质量和个数的乘积之比;
(2)一种物质生成两种或多种物质的反应叫分解反应;两种或多种物质生成一种物质的反应叫化合反应。
【解答】(1)根据化学式LiFePO4可知,磷酸铁锂电池中铁元素与氧元素的质量之比:56×1:(16×4)=7:8;
(2)该电池充电时,磷酸铁锂生产磷酸亚铁和锂单质,即一种物质生成两种物质,为分解反应。
?
22.【答案】 (1)22
(2)钛单质
(3)TiO2
【解析】【分析】(1)根据原子中质子数=原子序数分析;
(2)根据金属元素符号表示元素、一个原子和该元素组成的单质分析;
(3)根据化合物化学式书写方法分析。
【解答】(1)原子中质子数=原子序数,钛原子的质子数为22;
(2)钛属于金属元素,钛单质由原子构成,其化学式用元素符号表示,所以钛元素符号除表示钛元素、一个钛原子之外,还能表示钛这种物质;
(3) 钛元素+4价的氧化物化学式为 TiO2 ;
故答案为:(1)22;(2)钛单质;(3) TiO2 。
23.【答案】 (1)原子核
(2)C
【解析】【分析】(1) α粒子带正电荷,原子核也带正电荷,因此二者靠近时会发生排斥。根据图片可知,只有少数靠近原子核中间的α粒子发生了大角度的偏转,即只有少数受到了原子核的排斥力,而大多数都没有受到排斥力,只能说明原子核存在于原子中心;
(2)根据电荷之间的相互作用规律判断。
【解答】(1) 卢瑟福提出了原子的核式结构模型,认为原子的中心有一个很小的原子核;
(2)根据图片可知,原子核带正电荷,而从它上面经过的C也带正电荷,二者之间表现为排斥力,因此C只能向上改变方向,不能向下,故四条运动轨迹不可能出现的是C。
24.【答案】 (1)自动调节
(2)不停地做无规则运动
(3)7:12
【解析】【分析】1、生态系统具有自动调节能力。一般来说,生态系统的成分越 复杂,生物种类 越多,自动调节平衡的能力就越强;
2、扩散现象表明:分子处于不停地无规则运动之中;
3、 ?????根据化学式可以计算出组成物质的各元素的质量之比。化学式中各元素的相对原子质量的和之比即为各元素的质量之比。
【解答】(1) 茶园是一个生态系统,能保持相对稳定,除人的作用外,还与生态系统具有一定的?自动调节能力有关;
(2) 在泡茶过程中,会闻到茶特有的香气?是扩散现象,表明分子在 不停地做无规则运动 ;
(3) 茶氨酸(C7H14N2O3) 中氮元素和氧元素的质量之比为:
2N:3O=(2×14):(3×16)=7:12
故答案为:(1)自动调节? (2) 不停地做无规则运动 ? (3)7:12
三、解答题
25.【答案】 (1)3
(2)6.0
(3)二氧化碳和水(CO2和H2O)
【解析】【分析】(1)在化学式中,一种符号代表一种元素;
(2)元素质量=物质质量×该元素的质量分数;
(3)根据质量守恒定律分析完全燃烧的产物。
【解答】(1)根据化学式 C10H10O 可知,侧柏莲酮芳香油由C、H、O共3种元素组成。
(2)7.3g侧柏莲桐芳香油中碳元素的质量为:7.3g×12×1012×10+1×10+16=6g;
(3)根据化学式C10H10O可知,侧柏莲酮芳香油在氧气中完全燃烧时,碳元素和氧元素组成二氧化碳,氢元素和氧元素组成水,即完全燃烧的产物为二氧化碳和水。
26.【答案】 (1)21:8
(2)解:Fe3O4中含铁元素的质量:m=464t×168/232=336t
生铁的质量=336t÷96%=350t
【解析】【分析】(1)化合物中各元素的质量比等于各元素的相对原子质量与它的原子个数的乘积之比.
(2)铁元素质量守恒 Fe3O4中含铁元素的质量.
【解答】 (1) 铁的相对原子质量为56,氧的相对原子质量为16,所以铁元素跟氧元素的质量比为56×316×4=218.
27.【答案】 (1)B
(2)沸点不同
(3)分解
(4)-3
(5)认同,因为人工固为农田提供了更多的氮肥,有利于人类粮食增产但大量使用合成含氮化肥并施用于农作物,将会导致土壤板结;若土壤中N元素超标,被淋溶后,易导致水体的富营养化污染等一系列环境问题。
不认同,因为人工固氮可以为农田提供更多的氮肥,有利于人类粮食增产,只要我们合理控制化肥的使用量,一般不会造成土壤板结,水体富营养化污染等环境问题。
【解析】【分析】(1)植物的生长需要无机盐,氮肥可以促进叶的生长,磷肥可以促进根的生长,钾肥可以促进果实种子的生长。
(2)空气分离是指低温冷冻原理从空气中分离出其组分(氧、氮和氩、氦等稀有气体)的过程。一般先将空气压缩,并冷至很低温度,或用膨胀方法使空气液化,再进行分离.
(3)分解反应是指由一种物质反应生成两种或两种以上新物质的反应;
(4)化合物中各元素化合价之和等于零;
(5)这题解答可以认同和不认同,只要说出正确解释就可以了.
【解答】(1)缺少氮肥,可以使叶子矮小,故选B;
(2)气体分离根据各气体的沸点不同;
(3)反应为一种物质变成多种物质,是分解反应;
(4)氨气里的氢元素的化合价为+1价,根据原子不带电,氮元素的化合价为-3;
故答案为: (1)B (2) 沸点不同? (3)分解 (4) -3
28.【答案】 (1)有机物
(2)2:1
(3)32.4克纤维素中所含碳元素质量:32.4克×(72n/162n)=14.4克
含碳元素质量相同的聚丙烯为:14.4克/(36n/42n)=16.8克
【解析】【分析】(1)根据含碳化合物为有机物分析;
(2)根据化学式右下角数字为原子个数比分析;
(3)根据元素质量为物质质量×元素质量分数分析。
【解答】(1) 纤维素是一种有机物;
(2)由化学式可知, 纤维素分子中,氢、氧原子的个数比为10:5=2:1;
故答案为:(1)有机物;(2)2:1;(3)16.8克。
29.【答案】 (1)+1
(2)解:重水中氘的质量分数= 2×22×2+16×100%=20%
100t海水中所含氘的质量=100t×0.02%×20%=0.004t=4kg
答:100t海水中所含的质量为4kg。
(3)中子
【解析】【分析】(1)具有相同质子数和不同中子数的原子成为同位素原子,据此分析解答;
(2)在化学式中,正负化合价的代数和为零,据此分析计算;
(3)首先根据化学式计算出重水中氘的质量分数,在用海水的质量×重水的质量分数×氘的质量分数计算出海水中含有氘的质量。
【解答】(1)根据图片可知,三种原子中 的个数不同,根据“同位素原子中子数不同”可知,它表示中子。
(2)在T2O中O元素的化合价为-2价,根据正负化合价代数和为零得到:2x+(-2)=0,解得:x=+1价。
(3)重水中氘的质量分数=? 2×22×2+16×100%=20% ;
100t海水中所含氘的质量=100t×0.02%×20%=0.004t=4kg;
30.【答案】 (1)原子核
(2)DNA
【解析】【分析】(1)根据a粒子散射实验,卢瑟福提出了原子行星模型理论,他认为原子的全部正电荷和几乎全部质量都集中在原子核上,带负电的电子在原子核外绕核做圆周运动,后来的研究表明原子核由带正电的质子与不带电的中子组成。
(2)细胞核中能被碱性染料染成深色的物质叫做染色体,它是由DNA和蛋白质两种物质组成,DNA是主要的遗传物质,它的结构像一个螺旋形的梯子。一条染色体上包含一个DNA分子.一个DNA分子上包含有多个基因,基因是染色体上具有特定遗传信息的DNA片段。
【解答】(1)原子核的体积占原子的体积很小,原子核是由质子和中子构成的,质子带正电,中子不带电。原子核上的正电荷和电子所带的负电荷相等,整个原子对外不显电性,但是看不出原子始终在做无规则运动,是电子绕原子核沿一定轨道运动。 其中卢瑟福基于α粒子轰击金属箔的实验事实,经过思考得出“原子的全部正电荷都集中在原子核里”这一结论,该结论是对汤姆生关于正电荷均匀分布观点的修正。
(2)细胞的控制中心是细胞核,细胞核是遗传信息库,细胞核中有染色体,染色体中有DNA,是遗传物质的载体,DNA上有遗传信息,这些信息就是指导和控制细胞中物质和能量变化的一系列指令,也是生物体建造自己生命大厦,直到DNA双螺旋结构的问世,才标志着对遗传的研究进入到分子水平。
故答案为:(1)原子核 (2)DNA
31.【答案】 (1)应激性(或“感应性”、“感触性”)
(2)分子总是不停地做无规则运动(或“扩散”)
(3)15:2;碳元素的质量分数: 120136 ×100%=88.2%
【解析】【分析】应激性是指生物体能接受外界刺激产生合目的的反应,使生物体能趋利避害和趋吉避凶。应激性与活动性是生物对自然信息的本能反应。布朗运动是指悬浮在液体或气体中的微粒所做的永不停息的无规则运动。元素质量分数指某种元素在物质中所占的质量分数是元素质量与物质质量之比。
【解答】(1) 碰碰香受到外力触碰时会释放香味,这是植物对外界的触碰作出的反应,属于植物的感应性;
(2)在其他地方也能闻到香味,是分子的无规则运动导致的;
(3) 柠檬烯的化学式为C10H16 , 所以碳氢元素的质量比为:12×10:1×16=15:2;其中碳元素的质量分数为12×1012×10+1×16×100%=88.2%
故答案为:(1) 应激性(或“感应性”、“感触性”) ;(2) 分子总是不停地做无规则运动(或“扩散”) ;(3)15:2;88.2%。
32.【答案】 (1)化合物
(2)7:4
(3)水杨酸微溶于水
【解析】【分析】()根据食品中金属元素以化合物形态存在分析;
(2)根据元素质量比为相对原子质量×原子个数之比分析;
(3)根据物理性质为不需要化学变化体现的性质分析。
【解答】(1) 覆盆子果实中的钙、钾等元素是以化合物形态存在;
(2) 水杨酸(C7H6O3)中碳元素和氧元素的质量比为 (12×7): (16×3)=7:4;
(3) 水杨酸常温下稳定,加热易分解,属于化学性质,微溶于水,属于物理性质,其水溶液呈酸性属于化学性质;
故答案为:(1)化合物;(2)7:4;(3) 水杨酸微溶于水 。
33.【答案】 (1)化学
(2)A,D
(3)温度越低,电压下降到放电终止电压时间越短
【解析】【分析】能量转化是指各种能量之间在一定条件下互相转化过程 。用元素符号表示纯净物(单质、化合物)分子的组成及相对分子质量的化学组成式。它能表示物质的一个分子及其成分、组成(分子中各元素原子的数目、分子量和各成分元素的重量比)。
【解答】(1)电池充电时,电能储存在电池内的化学物质中,即化学能;
(2)A、由 碳酸二甲酯的化学式可知,其由C、H、O三种元素组成;故A正确;
B、由化学式可知,氧元素占的质量分数最大;故B错误;
C、相对分子量是比值得出的,没有具体的单位;故C错误;
D、C、H、O三种原子个数之比为 3:6:3=1:2:1; 故D正确;
(3)由乙图可知,温度越低,电池电压下降的越快,冬天温度低,所以手机夏天比冬天耐用;
故答案为:(1)化学;(2)AD;(3) 温度越低,电压下降到放电终止电压时间越短。
34.【答案】 (1)+3
(2)2Ga+2NH3 高温__ 2GaN+3H2
(3)解:P=UI=20V×3.2A=64W
答: 最大输出功率是64W。
【解析】【分析】(1)在化学式中,正负化合价的代数和为零,据此计算出 NH3 中氮元素的化合价,再根据 GaN 计算镓元素的化合价?;
(2)镓和氨气在高温条件下反应,生成氮化镓和氢气,据此写出反应的方程式;
(3)根据P=UI可知,电压越大,电流越大,电功率越大,据此判断并计算即可。
【解答】(1)在NH3 中,根据正好化合价代数和为零得到:x+(+1)×3=0,解得:x=-3价;
在GaN中,得到:y+(-3)=0,解得:y=+3价;
(2) 氮化镓的制取可通过镓与氨气在高温下发生置换反应来实现,其反应的化学方程式为 : 2Ga+2NH3?高温__?2GaN+3H2 ;
(3)比较可知,当处于“20V 3.2A”时,充电器的输出功率最大,即: P=UI=20V×3.2A=64W 。
一、单选题
1.(2021·宁波)如图是物质甲和乙反应生成丙的微观示意图。下列说法正确的是( ???)
A.?该反应属于化合反应
B.?甲、乙、丙都是有机物
C.?该反应中参加反应的甲和乙质量比为1:1
D.?该反应在反应前后原子的种类发生了改变
2.(2021·宁波)含硫元素的同类物质中硫元素的化合价可能不同,不同类物质中硫元素的化合价可能相同,如表所示。下列判断正确的是( ???)
类别
物质
化合价
单质
氧化物
酸
X
0
a
-
-
-
+4
-
b
d
Na2SO3等
+6
-
c
e
f
A.?X表示碱
B.?物质a在空气中燃烧会发出明亮的蓝紫色火焰
C.?物质b是二氧化硫,它是空气污染物之一
D.?物质d和NaOH溶液发生中和反应生成Na2SO4和H2O
3.(2021·温州)氮化锶(Sr3N2)是生产高端荧光粉的主要原料。已知Sr3N2中N的化合价为-3,则Sr的化合价为(??? )
A.?-3?????????????????????????????????????????B.?-2?????????????????????????????????????????C.?+2?????????????????????????????????????????D.?+3
4.(2021·温州)2021年4月,我国科学家首次合成的铀-214,是目前已知质量最小的铀原子。其相对原子质量为214,质子数是92。则铀-214原子的核外电子数为(??? )
A.?92???????????????????????????????????????B.?122???????????????????????????????????????C.?214???????????????????????????????????????D.?306
5.(2021·湖州)二氧化碳和二氧化硫都是由AB2型分子构成的物质,但分子中A原子和B原子的空间位置不同,其模型如右图所示。根据此模型,下列叙述错误的是( ??)
A.?两种物质都由两种元素组成????????????????????????????????B.?两种物质中碳元素和硫元素化合价相同
C.?两种物质的化学性质相同????????????????????????????????????D.?分子中原子空间位置不同是因为A原子种类不同
6.(2021·丽水)相比于普通汽车,氢燃料电池车的排放物只有水,没有其它污染物。如图是氢燃料电池内发生反应的微观示意图,从图中获得的信息正确的是( ???)
A.?反应前后原子种类不变???????????????????????????????????????B.?反应前后分子种类不变
C.?水分子的相对分子质量是18克????????????????????????????D.?水中氢元素和氧元素的质量比为2:1
7.(2020·台州)食盐是生活中重要的调味品,化学式为NaCl,其中氯元素的化合价为-1, 则钠元素的化合价为( )
A.?-2?????????????????????????????????????????B.?-1?????????????????????????????????????????C.?+1?????????????????????????????????????????D.?+2
8.(2020·湖州)“价一类”二维图可以表示元素化合价与物质类别之间的关系,右图中的a、b、c、d、e代表常见的含碳物质,下列说法错误的是(??? )
A.?b和氧气反应生成c?????B.?c和水反应生成d?????C.?e可能难溶于水?????D.?由a得到e至少要经过三步反应
9.(2020·湖州)下图是一定量的B2和AB在一定条件下混合以及混合结果的模型,则(??? )
?
A.?反应得到的生成物有两种????????????????????????????????????B.?反应前后元素化合价不变
C.?参加反应的两种分子个数比为3:2?????????????????????D.?该反应为化合反应
10.(2020·宁波)某化学反应的反应物和生成物的微观示意图及反应前后的质量如下表所示。
下列有关该反应的说法正确的是( ?)
A.?甲物质由碳原子和氢原子直接构成??????????????????????B.?该反应属于置换反应
C.?参加反应的反应物分子个数比为1:1?????????????????????D.?x+y+z=233
11.(2020·宁波)如图是一款变色眼镜,它的镜片内含有溴化银和氧化铜。在强光照射下,溴化银分解成单质溴和银,镜片颜色变深;当光线变暗时,溴和银在氧化铜催化作用下,又立即化合成溴化银,镜片颜色变浅。有关该眼镜的说法错误的是( ?)
A.?塑料是高分子合成材料???????????????????????????????????????B.?铜螺丝久置在潮湿的空气中会产生铜锈
C.?溴化银分解后,银元素的化合价升高??????????????????D.?溴和银化合成溴化银前后,氧化铜化学性质不变
12.(2020·金华·丽水)“宏观一微观一符号”之间建立联系,能帮助我们更好地认识物质的本质。浓度为75%的酒精常用作防疫消毒液,其有效成份是乙醇,如图是工业上在一定条件下制取乙醇的微观示意图。下列叙述中不正确的是( ???)
A.?符号分析:乙的化学式为CO2?????????????????????????????B.?宏观分析:甲物质由2种元素组成
C.?微观分析:一个丙分子由9个原子构成????????????????D.?基本反应类型分析:该反应属于化合反应
13.(2020·金华·丽水)为了认识和理解一些不能直接观察到的或复杂的事物,人们会通过制作模型或模拟实验进行研究。下列属于模型的是( ???)
A.?用力拉板使纸断裂 ??????????????????B.?向内推书使书隆起
C.?地球仪 ???????????????????????????????????????????D.?铅笔在篮球和木板上移动
14.(2020·温州)银器在使用过程中,因为发生化学反应:4Ag+O2+2H2S=2Ag2S+2H2O,产生的Ag2S使银器逐渐失去光泽。已知银的化合价为+1价,则Ag2S中S的化合价为(??? )
A.?+2?????????????????????????????????????????B.?-2?????????????????????????????????????????C.?+1?????????????????????????????????????????D.?-1
15.(2020·绍兴)与图示微观变化相符的化学反应是(??? )
A.?2CO+O2 点燃__ 2CO2????????????????????????????????????????B.?H2+CuO ? H2O+Cu
C.?2H2+O2 点燃__ 2H2O????????????????????????????????????????D.?H2CO3 ? H2O+CO2↑
16.(2020·嘉兴)某化合物在水中能完全电离,将该化合物配制成甲、乙、丙三种不同浓度的水溶液,对溶液中所含阴、阳离子数目进行测定,结果如图所示。由图可判断该化合物可能是( ?)
A.?CaCl2???????????????????????????????B.?Al(NO3)3? ???????????????????????????????C.?NaOH???????????????????????????????D.?H2SO4
二、填空题
17.(2021·温州)1783年,拉瓦锡利用如图装置探究水的组成:往A杯中滴加少量的水,水通过灼热的铁管时发生汽化,水蒸气与灼热的铁反应,生成了一种黑色固体(Fe3O4)和“可燃空气”,将气体通过放在冷水中的铜管,在B装置中收集到纯净的可燃空气。最终,拉瓦锡证明了水是由两种元素组成的。
(1)将气体通过放在冷水中的铜管,目的是除去________。
(2)将B装置收集到的可燃空气在氧气中点燃,生成了水。可燃空气的名称是________。
(3)若该实验中生成的黑色固体质量为m1 , 可燃空气的质量为m2 , 可燃空气完全燃烧生成水的质量为m3 , 如果水是由“氧元素”和“可燃空气元素”组成的,则m1、m2、m3三者应满足的关系是________。
18.(2021·绍兴)? 2021年3月,四川三星堆遗址进行了新一轮考古发掘。至今三星堆已出土了黄金面具、青铜纵目面具等一批珍贵文物,如图。
(1)出土的黄金面具仍金光灿灿,而青铜纵目面具已锈迹斑斑,这说明金的活动性比铜________(选填“强”或“弱”)。
(2)古代制作青铜器的铜来源于铜矿,如黄铜矿。黄铜矿的主要成分为二硫化亚铁铜 (CuFeS2),其中铁元素和铜元素均为+2价,硫元素的化合价为 ________。
(3)应用碳-14测出三星堆遗址距今3000年左右,碳-12和碳-14是碳元素的两种同位素原子,它们的主要区别是原子核中________?数不同。
19.(2021·丽水)“价类图”是以化合价为纵坐标、物质类别为横坐标绘制的图像,它能将散乱的科学知识联系在一起,有助于对科学问题的理解和整体认知。如图是含氯元素的物质的价类图,其中“一”表示物质间的转化关系。请回答;
(1)A和氢氧化钾反应得到D和水,则该反应属于基本反应类型中的化合价________;
(2)物质C的化学式为________;
(3)E在一定条件下得到D的化学方程式为________。
20.(2020·衢州)用高能粒子轰击原子核是研究微观粒子的一种方法。
1934年,意大利科学家费米用中子轰击铀原子(质子数为92,元素符号为U),得到了一种质量增加的原子,他公开宣布发现了93号元素,被科学界认可,从而获得了诺贝尔物理学奖。
1938年,德国科学家哈恩在重复费米的实验后,发现费米实验中得到的是56号钡元素,并用图示模型来定义这一变化。费米知道后,立即重复哈恩的实验,结果证实自己错了,费米坦率地检讨并纠正了错误。
(1)费米用中子轰击铀原子,不可能增加铀原子的________数,所以得不到93号元素。
(2)结合材料分析,以下观点正确的是???????? 。
A.面对前人的观点要敢于质疑
B.科学结论的得出要依据客观事实
C.对科学的认识是一个不断修正、完善的过程
21.(2020·衢州)某品牌新能源电动汽车使用磷酸铁锂电池,其反应原理: LiFePO4?放电充电FePO4+Li 。该电池具有容量大、续航能力强的特点。
(1)LiFePO4 , 中铁元素与氧元素的质量比为________。
(2)该电池充电时发生的化学反应属于________(填基本反应类型)。
22.(2020·湖州)由我国自主研发的深海载人潜水器球壳于2019年建造完成并通过验收。球壳用被称为“海洋金属”的钛合金作为制造材料。钛合金不仅强度高而且具有弹性。右图为钛元素在元素周期表中的部分信息。
(1)钛原子的质子数为________。
(2)Ti除了表示钛元素、一个钛原子之外,还能表示________?。
(3)钛元素的化合价为+4价时,其对应的氧化物被认为是现今世界上性能最好的一种白色颜料。它的化学式为________。
23.(2020·金华·丽水)人们为了揭示原子结构的奥秘,经历了漫长的探究过程。1911年物理学家卢瑟福用带正电的α粒子轰击金属箔。实验发现:多数α粒子穿过金属箔后仍保持原来的运动方向,绝少数α粒子发生了较大角度的偏转。
(1)卢瑟福提出了原子的核式结构模型,认为原子的中心有一个很小的________?;
(2)当α粒子轰击金属箔时,图中四条运动轨迹不可能出现的是________(填字母)。
24.(2020·温州)茶是人类健康的饮品之一,联合国将今年5月21日定为首个“国际茶日”。
(1)茶园是一个生态系统,能保持相对稳定,除人的作用外,还与生态系统具有一定的________能力有关。
(2)在泡茶过程中,会闻到茶特有的香气,这是因为分子________。
(3)茶氨酸(C7H14N2O3)是茶树特有的一种氨基酸。茶氨酸中氮元素与氧元素的质量比为 ________。
三、解答题
25.(2021·宁波)“青团”是宁波的一种传统食物。在“青团”制作过程中,需要往糯米粉中添加艾草(或艾草汁)。艾草含有侧柏莲酮芳香油(C10H10O),侧柏莲酮芳香油是一种淡黄色液体,具有香脂香气,所以“青团”具有独特风味。
(1)侧柏莲酮芳香油由________种元素组成。
(2)7.3g侧柏莲桐芳香油中碳元素的质量为________g。
(3)侧柏莲桐芳香油在氧气中完全燃烧的产物是________。
26.(2021·杭州)磁铁矿石(含Fe3O4)是常用的炼铁原料,工业上可通过如下反应:4CO+Fe3O4 高温__ 3Fe+4CO2 , 将其中的Fe3O4转化为Fe。
(1)Fe3O4中铁元素和氧元素的质量比为________。
(2)假设冶炼过程中铁没有损耗,用含有464吨Fe3O4的磁铁矿石可提炼出含铁质量分数为96%的生铁多少吨?
27.(2021·杭州)氮是空气中含量最多的元素,也是构成生物体的必要元素之一但是,空气中游离态的氮不能直接被大多数生物所利用,必须经过变化,并与其他成分形成化合物(如氨或铵盐等),才能被植物利用。如图是自 然界氮循环的示意图请回答:
(1)一株绿色植物的幼苗(如小麦)在生长过程中缺氮其最可能出现的症状是?????。
A.茎秆细小、易倒伏,叶有褐斑??
B.生长矮小,叶色发黄
C.生长缓慢,叶色暗绿带红
D.只开花不结果
(2)工业上常用空气冷冻分离法来获得氮气(即由液态空气分馏来获得氮气)这种方法制氮气的原理是利 用了氮气与氧气哪一物理性质的差异?________。
(3)实验室制备少量氮气的方法很多。例如,可由亚硝酸铵来制取氮气,其反应如下:NH4NO2 Δ__ N2↑+2H2O,该反应是属于________反应(选填“化合”、“分解”、“置换或“复分解”)
(4)空气中的N2转化为NH3 , 的过程中,N元素的化合价由0价转变为________价
(5)有人认为:人类可以通过人工固氮,大量合成含氮化肥并施用于农作物,这将有助于人类粮食增产,但也会造成环境污染。你是否同他的观点并阐述理由。
28.(2021·绍兴)按我国政府要求2021年1月1日起餐饮行业已禁用不可降解的一次性塑料吸管,取而代之的是一些可降解的环保吸管,环保纸吸管的主要成分是纤维素,化学式为(C6H10O5)n,而原来塑料吸管的主要成分是聚丙烯,化学式为(C3H6)n。
(1)纤维素是一种________(选填“有机物”或“无机物”)。
(2)纤维素分子中,氢、氧原子的个数比为 ________?。
(3)计算32.4克纤维素中所含碳元素质量与多少克聚丙烯中所含碳元素质量相同?
29.(2021·嘉兴)氕、氘、氚是氢的三种同位素原子,它们的原子结构模型如图所示,相关信息如下表。试回答:
名称
符号
相对原子质量
氕
H
1
氘
D
2
氚
T
3
(1)超重水有一定的放射性。一个超重水分子由两个氚原子和一个氧原子构成,其化学式可表示为T2O。T2O中T的化合价为________。
(2)重水是由氘和氧组成的化合物,化学式可表示为D2O,重水和普通水化学性质相似。在海水中重水的质量约占0.02%,则100吨海水中所含氘的质量是多少?
(3)原子结构模型中的“ ?”表示的粒子是________。
30.(2021·湖州)人类对未知世界的认知都是在实践和探索中不断地修正和深化的。
(1)原子结构模型的建立是几代科学家通过实验和思维不断地进行修正的。其中卢瑟福基于α粒子轰击金属箔的实验事实,经过思考得出“原子的全部正电荷都集中在________里”这一结论,该结论是对汤姆生关于正电荷均匀分布观点的修正。
(2)“谁控制生物的遗传?”人类对这一命题的认识是不断深化的,直到________双螺旋结构的问世,才标志着对遗传的研究进入到分子水平.
31.(2020·台州)碰碰香是一种常见的室内盆栽植物,因触碰后可散发出令人舒适的香气而得名,其香气具有提神醒脑、驱避蚊虫的作用。
(1)碰碰香受到外力触碰时会释放香味,这种现象属于植物的________性。
(2)在室内其他地方也能闻到碰碰香散发的香味,是因为________。
(3)碰碰香的香味物质中含量最多的是柠檬烯,其化学式为C10H16。计算:
①柠檬烯中碳元素、氢元素的质量比为________。
②柠檬烯中碳元素的质量分数是多少________?(计算结果精确到0.1%)
32.(2020·宁波)覆盆子果实含有丰富的维生素、少量水杨酸以及钙、钾等元素,有“黄金水果”的美誉。其中的水杨酸常温下稳定,加热易分解,微溶于水,其水溶液呈酸性。
(1)覆盆子果实中的钙、钾等元素是以________(填“单质”或“化合物”)的形态存在。
(2)水杨酸(C7H6O3)中碳元素和氧元素的质量比为________。
(3)水杨酸的上述性质中,属于物理性质的是:________。
33.(2020·绍兴)2019年诺贝尔化学奖用地表彰锂离子电池的研发。这种质量轻、可充电、功能强大的电池现在被广泛应用于手机、笔记本电脑和电动汽车等各种产品。
(1)锂电池充电时,电能转化为________能。
(2)碳酸二甲酯(C3H6O3)是锂电池电解液的一种成分,下列关于碳酸二甲酯说法正确的有 ?????。
A.由C,H,O三种元素组成
B.碳元素的质量分数最大
C.相对分子质量是90克
D.分子中C,H,O三种原子的个数比为1:2:1
(3)图为某款锂电池手机在不同温度下的电压随时间变化的图像,请结合图像分析手机夏天比冬天耐用的原因是:________。
34.(2020·嘉兴)随着手机、电脑等移动设备的普及,人们对充电设备的要求越来越高。最近,某品牌氮化镓充电设备以体积小、功率大深受消费者喜爱。
(1)氮化镓(GaN)是充电设备中的核心材料。查阅资料得知:氮化镓中氮元素的化合价与氨气(NH3)中氮元素的化合价相同。由此可知,氮化镓中镓元素的化合价为________。
(2)氮化镓的制取可通过镓与氨气在高温下发生置换反应来实现,其反应的化学方程式为________。
(3)该品牌氮化镓充电器支持“5V 3A”“12V 3A”“20V 3.2A”三个输出档,请分析计算它的最大输出功率。
答案解析部分
一、单选题
1.【答案】 A
【解析】【分析】(1)多种物质反应生成一种物质,该反应为化合反应;
(2)有机物一般指有机化合物,狭义上的有机化合物主要是指由碳元素、氢元素组成,一定是含碳的化合物,但是不包括碳的氧化物和硫化物、碳酸、碳酸盐、氰化物、硫氰化物、氰酸盐、碳化物、碳硼烷、羰基金属、不含M-C键的金属有机配体配合物;
(3)根据示意图确定分子的组成,进而计算出参加反应的物质质量之比;
(4)根据示意图分析反应前后原子的种类是否改变即可。
【解答】A.该反应反应物有两种,生成物只有一种,为化合反应,故A正确;
B.根据示意图可知,乙中不含碳元素,肯定不是有机物,故B错误;
C.甲的化学式为C2H4 , 乙的化学式为H2O,则参加反应的甲和乙的质量之比为:(12×2+1×4):(1×2+16)=28:18,故C错误;
D.反应前后原子的种类都是三种,故D错误。
故选A。
2.【答案】 C
【解析】【分析】(1)碱由金属离子和氢氧根离子构成;
(2)根据硫在空气中燃烧的现象判断;
(3)根据正负化合价代数和为零,确定氧化物b的化学式,并根据它的性质判断;
(4)根据正负化合价代数和为零,确定氧化物d的化学式,并根据它的性质判断。
【解答】A.根据化学式 Na2SO3 可知,亚硫酸钠由金属离子和亚硫酸根构成,则x为盐而不是碱,故A错误;
B.a为硫单质,它在空气中燃烧生成淡蓝色火焰,故B错误;
C.设氧化物的化学式为SxOy,根据正负化合价代数和为零得到:(+4)x+(-2)y=0,解得:x:y=1:2,那么化学式为SO2 , 它有刺激性气味,严重污染空气,故C正确;
D.物质d为酸,其中S元素化合价为+4价,那么应该为H2SO3 , 与氢氧化钠反应,生成Na2SO3和H2O,故D错误。
故选C。
3.【答案】 C
【解析】【分析】根据化合物中元素化合价代数和为0分析。
【解答】 Sr3N2中N的化合价为-3,设Sr元素化合价为x,则3x+(-3)×2=0,解得x=+2;
故选C。
4.【答案】 A
【解析】【分析】根据原子中质子数=电子数分析。
【解答】原子中质子数=电子数,该原子质子数为92,则核外电子数也为92,A正确;
故选A。
5.【答案】 C
【解析】【分析】根据图示中分子构成分析,结合化合物中元素化合价代数和为0、不同种分子性质不同解答。
【解答】 A、 由分子构成可知,两种物质都由两种元素组成 ,不符合题意;
B、 两种物质中碳元素和硫元素化合价都是+4价,不符合题意;
C、 两种物质的分子构成不同,则化学性质不相同 ,符合题意;
D、 分子中原子空间位置不同是因为A原子种类不同 ,不符合题意;
故选C。
6.【答案】 A
【解析】【分析】根据化学变化过程中分子种类一定改变,原子种类一定不变,水的相对分子质量及元素质量比分析。
【解答】A、反应前后原子种类不发生改变,符合题意;
B、反应前后分子种类一定发生改变,不符合题意;
C、 水分子的相对分子质量是18 ,不符合题意;
D、 水中氢元素和氧元素的质量比为1:8,不符合题意;
故选A。
7.【答案】 C
【解析】【分析】化合价是一种元素的一个原子与其他元素的原子化合{即构成化合物}时表现出来的性质。
【解答】由化合物的化合价代数和为零可知,x+(-1)=0;x=+1;
故答案为:C。
8.【答案】 D
【解析】【分析】根据所给碳元素化合价及类别,结合二氧化碳、一氧化碳的性质进行判断分析。
【解答】A、b为+2价碳的氧化物,为CO,c为+4价氧化物,为二氧化碳,一氧化碳与氧气反应可生成二氧化碳,不符合题意;
B、d为碳酸,二氧化碳与水反应生成碳酸,不符合题意;
C、e为碳酸盐,可能溶于水也可能不溶于水,不符合题意;
D、碳燃烧生成二氧化碳,二氧化碳与氢氧化钠等碱溶液反应可生成碳酸盐,所以 a得到e经过两步反应即可实现,符合题意;
故答案为:D。
9.【答案】 D
【解析】【分析】先根据反应前后相同的粒子是未参加反应的粒子,确定出参加反应和生成的微粒,再结合单质到化合物的变化中一定有元素化合价变化及“多变一”的反应为化合反应分析。
【解答】A、划去没有参加反应的粒子,该反应为, 由此可知生成物只一种物质,不符合题意;
B、该反应为一种单质和一种化合物发生的化合反应,一定有元素化合价的变化,不符合题意;
C、参加反应的两种分子个数比为2:1,不符合题意;
D、该反应为两种物质生成一种物质,属于化合反应,符合题意;
故答案为:D。
10.【答案】 D
【解析】【分析】根据图中所给各粒子的构成书写出反应方程式,结合置换反应定义及化学式的配平系数解答。
【解答】A、甲物质为甲烷,由分子构成,其分子由碳原子和氢原子构成,不符合题意;
B、该反应中生成物中没有单质,不属于置换反应,不符合题意;
C、该反应方程式为CH4+2O2=CO2+2H2O,参加反应的分子个数比为1:2,不符合题意;
D、由反应前后质量关系可知,x+y+z=32+200+1=233,符合题意;
故答案为:D。
11.【答案】 C
【解析】【分析】(1)合成纤维、合成塑料和合成橡胶,是三大合成材料;
(2)铜和空气中的氧气、二氧化碳和水反应,生成碱式碳酸铜,也就是铜绿;
(3)计算出银元素的化合价,然后进行比较即可;
(4)根据催化剂的性质判断。
【解答】A.塑料是高分子合成材料,故A正确不合题意;
B.铜螺丝久置在潮湿的空气中会产生铜锈,故B正确不合题意;
C.在溴化银中,银元素的化合价为+1价,在银单质中化合价为0价,因此溴化银分解后,银元素的化合价降低了,故C错误符合题意;
D.催化剂在反应前后性质和质量不变,因此溴和银化合成溴化银前后,氧化铜化学性质不变,故D正确不合题意。
故选C。
12.【答案】 A
【解析】【分析】(1)根据物质乙的分子示意图确定它的化学式;
(2)根据甲分子的示意图确定它的元素组成;
(3)根据丙分子的示意图确定它的原子个数;
(4)根据反应物和生成物的种类和种数确定化学反应种类。
【解答】A.根据乙的示意图可知,乙分子由1个氧原子和2个氢原子构成,那么化学式为:H2O,故A错误符合题意;
B.根据甲的示意图可知,甲物质由氢元素和碳元素组成,故B正确不合题意;
C.根据丙的示意图可知,一个丙分子由2个碳原子、6个氢原子和1个氧原子组成,一共有9个原子,故C正确不合题意;
D.反应物有两种,而生成物只有一种,因此该反应为化合反应,故D正确不合题意。
故选A。
13.【答案】 C
【解析】【分析】1、建立模型的意义:可以帮助人们认识和理解一些不能直接观察到的事物。模型可以是一幅图、一张表格、或一个公式;
2、在难以直接拿研究对象做实验时,有时用模型来做实验,即模仿实验对象制作模型,或者模仿实验的某些条件进行实验,这样的实验叫做模拟实验。
【解答】A、 用力拉板使纸断裂 ,这是模拟向两侧拉的力的作用下地壳的变化的模拟实验,A错误;
B、 向内推书使书隆起 ,这是模拟挤压力下地壳的变形的模拟实验,B错误;
C、地球仪是地球的模型,C正确;
D、 铅笔在篮球和木板上移动 ,这是模拟地球上远去的帆船实验,是模拟实验,D错误。
故选C
14.【答案】 B
【解析】【分析】在化学式中,正负化合价的代数和为零,据此计算。
【解答】在 Ag2S 中,银的化合价为+1价,根据正负化合价代数和为零得到:(+1)×2+x=0,解得:x=-2价,故B正确,而A、C、D错误。
故选B。
15.【答案】 A
【解析】【分析】该题主要考查模型和化学反应的类型;
【解答】由变化示意图可知,该反应中反应物是单质和化合物,生成一种化合物的过程,且单质、化合物化学计量数之比为1:2;故A符合题意;
故答案为:A。
16.【答案】 C
【解析】【分析】根据图像确定该化合物中阴、阳离子的个数之比,然后对四个选项进行判断即可。
【解答】根据图像可知,无论溶液的浓度如何,该化合物的阴、阳离子的个数之比为:2n:2n=1:1;4n:4n=1:1;6n:6n=1:1。在四种物质中,只有NaOH的阴、阳离子的个数之比为1:1,故C正确,而A、B、D错误。
故选C。
二、填空题
17.【答案】 (1)水蒸气
(2)氢气
(3)829 m1+m2=m3
【解析】【分析】(1)根据气体中含有水蒸气分析;
(2)根据质量守恒定律分析;
(3)根据四氧化三铁中氧元素质量为水中氧元素质量,水的质量为氢元素和氧元素质量和分析。
【解答】(1)将气体通过放冷水中的铜管,是降低温度除去气体中的水蒸气;
(2)由反应前元素的种类可知,生成的可燃空气为氢气;
(3)生成水中氧元素质量即为四氧化三铁中氧元素质量,氧元素质量为64232m1=829m1,水的质量为氢元素和氧元素质量和,则 829 m1+m2=m3;
故答案为:(1)水蒸气;(2)氢气;(3) 829 m1+m2=m3。
18.【答案】 (1)弱
(2)-2
(3)中子
【解析】【分析】(1)根据金的活动性比铜弱分析;
(2)根据化合物中元素化合价代数和为0分析;
(3)根据同种元素中不同种原子中子数不同分析。
【解答】(1) 出土的黄金面具仍金光灿灿,而青铜纵目面具已锈迹斑斑,说明铜的发生了缓慢氧化,而金没有,即金的活动性比铜弱;
(2) 二硫化亚铁铜 (CuFeS2),其中铁元素和铜元素均为+2价,根据化合物中元素化合价代数和为0可知,硫元素的化合价为-2价;
(3) 碳-12和碳-14是碳元素的两种同位素原子,它们的主要区别是原子核中的中子数不同;
故答案为:(1)弱;(2)-2;(3)中子。
19.【答案】 (1)复分解反应
(2)ClO2
(3)2KClO2 MnO2__△ 2KCl+3O2↑
【解析】【分析】根据所给氯元素化合价及物质类别确定出对应点的物质,再按要求填空分析。
【解答】(1) A为盐酸,和氢氧化钾反应得到D和水,D为氯化钾,则该反应属于复分解反应;
(2)物质C为+4价氯的氧化物,化学式为 ClO2 ;
(3) E为+5价氯的盐,在一定条件下得到D,则E为氯酸钾,反应方程式为 2KClO2 MnO2__△ 2KCl+3O2↑ ;
故答案为:(1)复分解反应;(2) ClO2 ;(3) 2KClO2 MnO2__△ 2KCl+3O2↑ 。
20.【答案】 (1)质子
(2)A,B,C
【解析】【分析】(1)元素的原子序数等于原子的质子数。根据质量守恒定律可知,用中子轰击铀原子,只可能增加中子数,不可能增加质子数;
(2)根据题目描述的科学发展史进行分析判断。
【解答】(1)费米用中子轰击铀原子,不可能增加铀原子的质子数,所以得不到93号元素。
(2)A.哈恩重复费米的实验后,根据实验的结果对费米的实验提出质疑,可见面对前人的观点要敢于质疑,故A正确;
B.费米知道哈恩的实验结果后,自己再次实验发现原来的结果是错误的,检讨并纠正了错误,这说明科学结论的得出要依据客观事实,故B正确;
C.在科学探究的路上,难免遇到困难,或者得出错误的结论,只要坚持一切以事实为依据的原则,肯定最终能够得到正确结论,故C正确。
故选ABC。
21.【答案】 (1)7:8
(2)分解反应
【解析】【分析】(1)元素的质量之比等于相对原子质量和个数的乘积之比;
(2)一种物质生成两种或多种物质的反应叫分解反应;两种或多种物质生成一种物质的反应叫化合反应。
【解答】(1)根据化学式LiFePO4可知,磷酸铁锂电池中铁元素与氧元素的质量之比:56×1:(16×4)=7:8;
(2)该电池充电时,磷酸铁锂生产磷酸亚铁和锂单质,即一种物质生成两种物质,为分解反应。
?
22.【答案】 (1)22
(2)钛单质
(3)TiO2
【解析】【分析】(1)根据原子中质子数=原子序数分析;
(2)根据金属元素符号表示元素、一个原子和该元素组成的单质分析;
(3)根据化合物化学式书写方法分析。
【解答】(1)原子中质子数=原子序数,钛原子的质子数为22;
(2)钛属于金属元素,钛单质由原子构成,其化学式用元素符号表示,所以钛元素符号除表示钛元素、一个钛原子之外,还能表示钛这种物质;
(3) 钛元素+4价的氧化物化学式为 TiO2 ;
故答案为:(1)22;(2)钛单质;(3) TiO2 。
23.【答案】 (1)原子核
(2)C
【解析】【分析】(1) α粒子带正电荷,原子核也带正电荷,因此二者靠近时会发生排斥。根据图片可知,只有少数靠近原子核中间的α粒子发生了大角度的偏转,即只有少数受到了原子核的排斥力,而大多数都没有受到排斥力,只能说明原子核存在于原子中心;
(2)根据电荷之间的相互作用规律判断。
【解答】(1) 卢瑟福提出了原子的核式结构模型,认为原子的中心有一个很小的原子核;
(2)根据图片可知,原子核带正电荷,而从它上面经过的C也带正电荷,二者之间表现为排斥力,因此C只能向上改变方向,不能向下,故四条运动轨迹不可能出现的是C。
24.【答案】 (1)自动调节
(2)不停地做无规则运动
(3)7:12
【解析】【分析】1、生态系统具有自动调节能力。一般来说,生态系统的成分越 复杂,生物种类 越多,自动调节平衡的能力就越强;
2、扩散现象表明:分子处于不停地无规则运动之中;
3、 ?????根据化学式可以计算出组成物质的各元素的质量之比。化学式中各元素的相对原子质量的和之比即为各元素的质量之比。
【解答】(1) 茶园是一个生态系统,能保持相对稳定,除人的作用外,还与生态系统具有一定的?自动调节能力有关;
(2) 在泡茶过程中,会闻到茶特有的香气?是扩散现象,表明分子在 不停地做无规则运动 ;
(3) 茶氨酸(C7H14N2O3) 中氮元素和氧元素的质量之比为:
2N:3O=(2×14):(3×16)=7:12
故答案为:(1)自动调节? (2) 不停地做无规则运动 ? (3)7:12
三、解答题
25.【答案】 (1)3
(2)6.0
(3)二氧化碳和水(CO2和H2O)
【解析】【分析】(1)在化学式中,一种符号代表一种元素;
(2)元素质量=物质质量×该元素的质量分数;
(3)根据质量守恒定律分析完全燃烧的产物。
【解答】(1)根据化学式 C10H10O 可知,侧柏莲酮芳香油由C、H、O共3种元素组成。
(2)7.3g侧柏莲桐芳香油中碳元素的质量为:7.3g×12×1012×10+1×10+16=6g;
(3)根据化学式C10H10O可知,侧柏莲酮芳香油在氧气中完全燃烧时,碳元素和氧元素组成二氧化碳,氢元素和氧元素组成水,即完全燃烧的产物为二氧化碳和水。
26.【答案】 (1)21:8
(2)解:Fe3O4中含铁元素的质量:m=464t×168/232=336t
生铁的质量=336t÷96%=350t
【解析】【分析】(1)化合物中各元素的质量比等于各元素的相对原子质量与它的原子个数的乘积之比.
(2)铁元素质量守恒 Fe3O4中含铁元素的质量.
【解答】 (1) 铁的相对原子质量为56,氧的相对原子质量为16,所以铁元素跟氧元素的质量比为56×316×4=218.
27.【答案】 (1)B
(2)沸点不同
(3)分解
(4)-3
(5)认同,因为人工固为农田提供了更多的氮肥,有利于人类粮食增产但大量使用合成含氮化肥并施用于农作物,将会导致土壤板结;若土壤中N元素超标,被淋溶后,易导致水体的富营养化污染等一系列环境问题。
不认同,因为人工固氮可以为农田提供更多的氮肥,有利于人类粮食增产,只要我们合理控制化肥的使用量,一般不会造成土壤板结,水体富营养化污染等环境问题。
【解析】【分析】(1)植物的生长需要无机盐,氮肥可以促进叶的生长,磷肥可以促进根的生长,钾肥可以促进果实种子的生长。
(2)空气分离是指低温冷冻原理从空气中分离出其组分(氧、氮和氩、氦等稀有气体)的过程。一般先将空气压缩,并冷至很低温度,或用膨胀方法使空气液化,再进行分离.
(3)分解反应是指由一种物质反应生成两种或两种以上新物质的反应;
(4)化合物中各元素化合价之和等于零;
(5)这题解答可以认同和不认同,只要说出正确解释就可以了.
【解答】(1)缺少氮肥,可以使叶子矮小,故选B;
(2)气体分离根据各气体的沸点不同;
(3)反应为一种物质变成多种物质,是分解反应;
(4)氨气里的氢元素的化合价为+1价,根据原子不带电,氮元素的化合价为-3;
故答案为: (1)B (2) 沸点不同? (3)分解 (4) -3
28.【答案】 (1)有机物
(2)2:1
(3)32.4克纤维素中所含碳元素质量:32.4克×(72n/162n)=14.4克
含碳元素质量相同的聚丙烯为:14.4克/(36n/42n)=16.8克
【解析】【分析】(1)根据含碳化合物为有机物分析;
(2)根据化学式右下角数字为原子个数比分析;
(3)根据元素质量为物质质量×元素质量分数分析。
【解答】(1) 纤维素是一种有机物;
(2)由化学式可知, 纤维素分子中,氢、氧原子的个数比为10:5=2:1;
故答案为:(1)有机物;(2)2:1;(3)16.8克。
29.【答案】 (1)+1
(2)解:重水中氘的质量分数= 2×22×2+16×100%=20%
100t海水中所含氘的质量=100t×0.02%×20%=0.004t=4kg
答:100t海水中所含的质量为4kg。
(3)中子
【解析】【分析】(1)具有相同质子数和不同中子数的原子成为同位素原子,据此分析解答;
(2)在化学式中,正负化合价的代数和为零,据此分析计算;
(3)首先根据化学式计算出重水中氘的质量分数,在用海水的质量×重水的质量分数×氘的质量分数计算出海水中含有氘的质量。
【解答】(1)根据图片可知,三种原子中 的个数不同,根据“同位素原子中子数不同”可知,它表示中子。
(2)在T2O中O元素的化合价为-2价,根据正负化合价代数和为零得到:2x+(-2)=0,解得:x=+1价。
(3)重水中氘的质量分数=? 2×22×2+16×100%=20% ;
100t海水中所含氘的质量=100t×0.02%×20%=0.004t=4kg;
30.【答案】 (1)原子核
(2)DNA
【解析】【分析】(1)根据a粒子散射实验,卢瑟福提出了原子行星模型理论,他认为原子的全部正电荷和几乎全部质量都集中在原子核上,带负电的电子在原子核外绕核做圆周运动,后来的研究表明原子核由带正电的质子与不带电的中子组成。
(2)细胞核中能被碱性染料染成深色的物质叫做染色体,它是由DNA和蛋白质两种物质组成,DNA是主要的遗传物质,它的结构像一个螺旋形的梯子。一条染色体上包含一个DNA分子.一个DNA分子上包含有多个基因,基因是染色体上具有特定遗传信息的DNA片段。
【解答】(1)原子核的体积占原子的体积很小,原子核是由质子和中子构成的,质子带正电,中子不带电。原子核上的正电荷和电子所带的负电荷相等,整个原子对外不显电性,但是看不出原子始终在做无规则运动,是电子绕原子核沿一定轨道运动。 其中卢瑟福基于α粒子轰击金属箔的实验事实,经过思考得出“原子的全部正电荷都集中在原子核里”这一结论,该结论是对汤姆生关于正电荷均匀分布观点的修正。
(2)细胞的控制中心是细胞核,细胞核是遗传信息库,细胞核中有染色体,染色体中有DNA,是遗传物质的载体,DNA上有遗传信息,这些信息就是指导和控制细胞中物质和能量变化的一系列指令,也是生物体建造自己生命大厦,直到DNA双螺旋结构的问世,才标志着对遗传的研究进入到分子水平。
故答案为:(1)原子核 (2)DNA
31.【答案】 (1)应激性(或“感应性”、“感触性”)
(2)分子总是不停地做无规则运动(或“扩散”)
(3)15:2;碳元素的质量分数: 120136 ×100%=88.2%
【解析】【分析】应激性是指生物体能接受外界刺激产生合目的的反应,使生物体能趋利避害和趋吉避凶。应激性与活动性是生物对自然信息的本能反应。布朗运动是指悬浮在液体或气体中的微粒所做的永不停息的无规则运动。元素质量分数指某种元素在物质中所占的质量分数是元素质量与物质质量之比。
【解答】(1) 碰碰香受到外力触碰时会释放香味,这是植物对外界的触碰作出的反应,属于植物的感应性;
(2)在其他地方也能闻到香味,是分子的无规则运动导致的;
(3) 柠檬烯的化学式为C10H16 , 所以碳氢元素的质量比为:12×10:1×16=15:2;其中碳元素的质量分数为12×1012×10+1×16×100%=88.2%
故答案为:(1) 应激性(或“感应性”、“感触性”) ;(2) 分子总是不停地做无规则运动(或“扩散”) ;(3)15:2;88.2%。
32.【答案】 (1)化合物
(2)7:4
(3)水杨酸微溶于水
【解析】【分析】()根据食品中金属元素以化合物形态存在分析;
(2)根据元素质量比为相对原子质量×原子个数之比分析;
(3)根据物理性质为不需要化学变化体现的性质分析。
【解答】(1) 覆盆子果实中的钙、钾等元素是以化合物形态存在;
(2) 水杨酸(C7H6O3)中碳元素和氧元素的质量比为 (12×7): (16×3)=7:4;
(3) 水杨酸常温下稳定,加热易分解,属于化学性质,微溶于水,属于物理性质,其水溶液呈酸性属于化学性质;
故答案为:(1)化合物;(2)7:4;(3) 水杨酸微溶于水 。
33.【答案】 (1)化学
(2)A,D
(3)温度越低,电压下降到放电终止电压时间越短
【解析】【分析】能量转化是指各种能量之间在一定条件下互相转化过程 。用元素符号表示纯净物(单质、化合物)分子的组成及相对分子质量的化学组成式。它能表示物质的一个分子及其成分、组成(分子中各元素原子的数目、分子量和各成分元素的重量比)。
【解答】(1)电池充电时,电能储存在电池内的化学物质中,即化学能;
(2)A、由 碳酸二甲酯的化学式可知,其由C、H、O三种元素组成;故A正确;
B、由化学式可知,氧元素占的质量分数最大;故B错误;
C、相对分子量是比值得出的,没有具体的单位;故C错误;
D、C、H、O三种原子个数之比为 3:6:3=1:2:1; 故D正确;
(3)由乙图可知,温度越低,电池电压下降的越快,冬天温度低,所以手机夏天比冬天耐用;
故答案为:(1)化学;(2)AD;(3) 温度越低,电压下降到放电终止电压时间越短。
34.【答案】 (1)+3
(2)2Ga+2NH3 高温__ 2GaN+3H2
(3)解:P=UI=20V×3.2A=64W
答: 最大输出功率是64W。
【解析】【分析】(1)在化学式中,正负化合价的代数和为零,据此计算出 NH3 中氮元素的化合价,再根据 GaN 计算镓元素的化合价?;
(2)镓和氨气在高温条件下反应,生成氮化镓和氢气,据此写出反应的方程式;
(3)根据P=UI可知,电压越大,电流越大,电功率越大,据此判断并计算即可。
【解答】(1)在NH3 中,根据正好化合价代数和为零得到:x+(+1)×3=0,解得:x=-3价;
在GaN中,得到:y+(-3)=0,解得:y=+3价;
(2) 氮化镓的制取可通过镓与氨气在高温下发生置换反应来实现,其反应的化学方程式为 : 2Ga+2NH3?高温__?2GaN+3H2 ;
(3)比较可知,当处于“20V 3.2A”时,充电器的输出功率最大,即: P=UI=20V×3.2A=64W 。
同课章节目录
