4.3 蛋白质和核酸 课件 2020-2021学年人教版高二化学选修5(28张PPT)
文档属性
| 名称 | 4.3 蛋白质和核酸 课件 2020-2021学年人教版高二化学选修5(28张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-25 00:00:00 | ||
图片预览





文档简介
化学 · 选修5
第四章 生命中的基础有机化学物质
第三节 蛋白质和核酸
※明确学习目标※
1、知道氨基酸是组成蛋白质的基本结构单位。2、了解氨基酸的组成、结构特点和主要化学性质,理解肽键及多肽的形成。(学习重点)3、了解蛋白质的组成、结构和性质(盐析、变性、水解、颜色反应等)。4、认识蛋白质、酶、核酸等物质与人体健康的关系,体会化学学科在生命科学发展中所起的重要作用。
【资料卡片】生活中的蛋白质
蛋白质属于天然高分子化合物
【资料卡片】我国现代取得的成就
1965年我国科技工作者成功合成了具有生物活性的——结晶牛胰岛素。这是科学史上的一大成就,可以说是科学史上又一“丰碑”。在认识生命现象揭开生命奥秘的伟大历程中,做出了重要贡献。
课本P90“科学视野”
几乎一切生命活动过程都与蛋白质有关,没有蛋白质就没有生命!
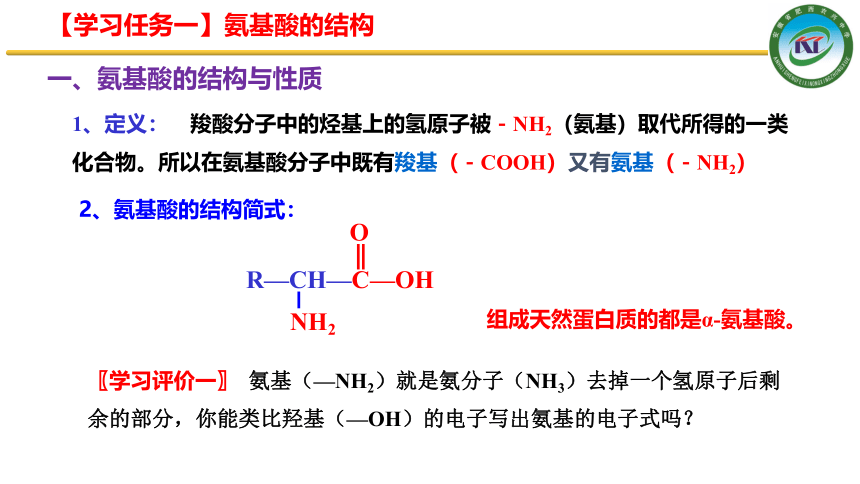
1、定义: 羧酸分子中的烃基上的氢原子被-NH2(氨基)取代所得的一类化合物。所以在氨基酸分子中既有羧基(-COOH)又有氨基(-NH2)
【学习任务一】氨基酸的结构
一、氨基酸的结构与性质
2、氨基酸的结构简式:
组成天然蛋白质的都是α-氨基酸。
R—CH—C—OH
O
NH2
〖学习评价一〗 氨基(—NH2)就是氨分子(NH3)去掉一个氢原子后剩余的部分,你能类比羟基(—OH)的电子写出氨基的电子式吗?
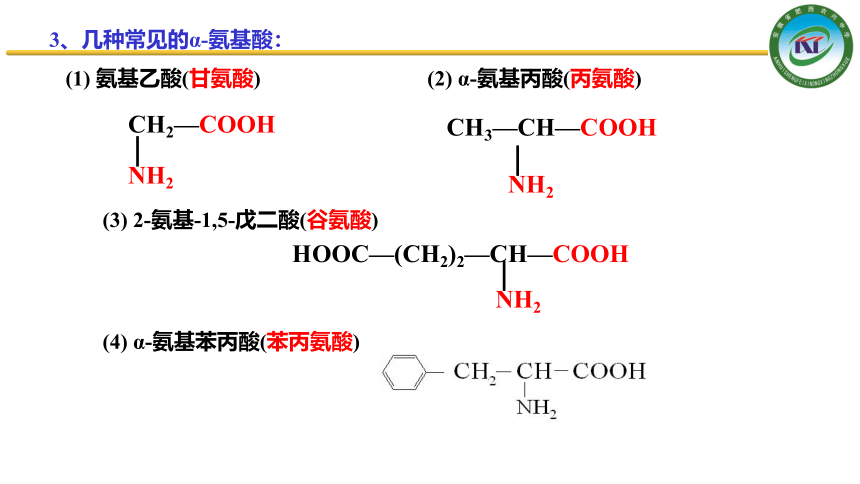
3、几种常见的α-氨基酸:
(1) 氨基乙酸(甘氨酸) (2) α-氨基丙酸(丙氨酸)
CH2—COOH
NH2
CH3—CH—COOH
NH2
(3) 2-氨基-1,5-戊二酸(谷氨酸)
HOOC—(CH2)2—CH—COOH
NH2
(4) α-氨基苯丙酸(苯丙氨酸)
【学习任务二】氨基酸的性质
无色晶体,熔点较高,在200~3000C时熔化分解
一般能溶于水而难溶于乙醇、乙醚,能溶于强酸或者强碱溶液中。
4、氨基酸的物理性质
一、氨基酸的结构与性质
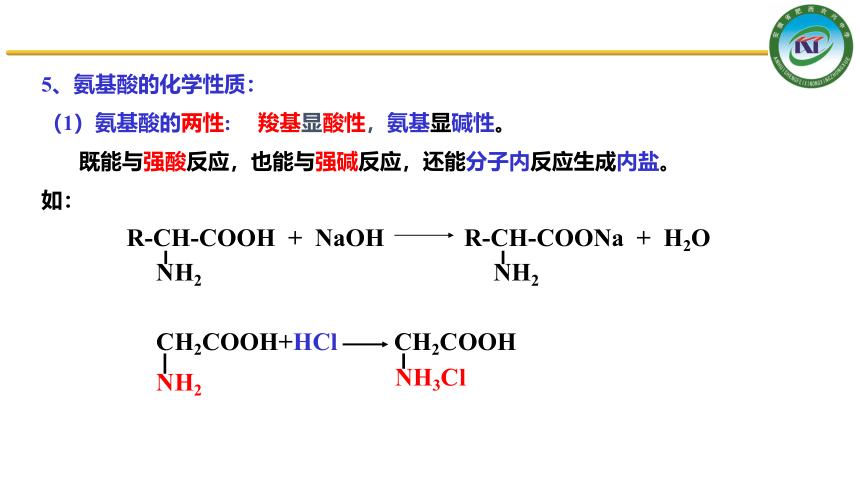
5、氨基酸的化学性质:
(1)氨基酸的两性: 羧基显酸性,氨基显碱性。
既能与强酸反应,也能与强碱反应,还能分子内反应生成内盐。
如:
CH2COOH+HCl CH2COOH
NH2
NH3Cl
R-CH-COOH + NaOH
NH2
R-CH-COONa + H2O
NH2
酶或酸或碱
+ H2O
+
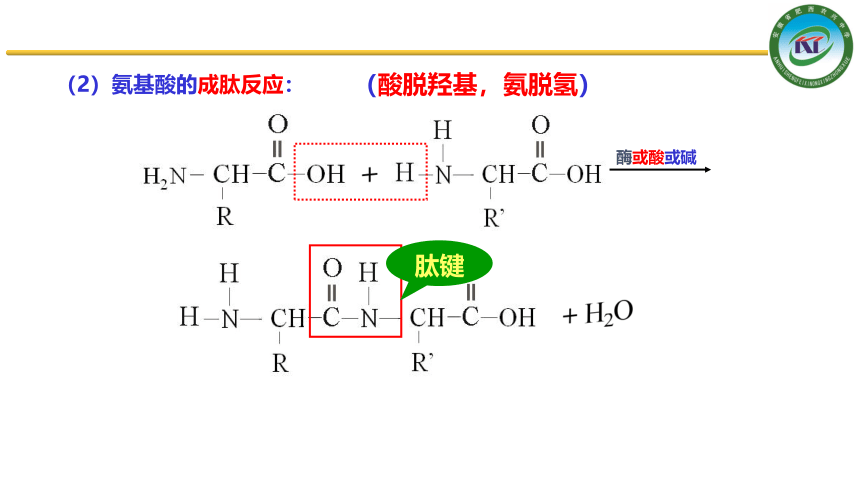
肽键
(2)氨基酸的成肽反应:
(酸脱羟基,氨脱氢)
二肽:两个氨基酸之间脱一分子水得到的产物。
α-氨基酸
脱水缩合
二肽
脱水缩合
多肽
……
蛋白质
多种氨基酸分子按不同的排列顺序以肽键相互结合,可以形成千百万种具有不同的理化性质和生理活性的多肽链。相对分子量在10000以上的,并具有一定空间结构的多肽,称为蛋白质。
〖学习评价二〗分析下图多肽链,属于 肽,形成该化合物的氨基酸有 种,含有肽键的数目是 个。
四
3
4
二、蛋白质的结构与性质
【学习任务三】蛋白质的组成和结构
1、蛋白质的组成和结构
蛋白质的组成
组成元素:
C、H、O、N、S (P)等
组成基本结构单元:
氨基酸
相对分子质量:
几万——几千万,属于天然高分子化合物,
人体内所具有的蛋白质种类达到了10万种以上。
2、蛋白质的结构
各种蛋白质都有其特殊功能和活性,这不仅取决于取决于组成多肽链的氨基酸种类、数目及排列顺序,还与其特定的空间结构密切相关。
任何一种蛋白质分子在天然状态下均具有独特而稳定的结构,这是蛋白质分子结构中最显著的特征:蛋白质分子中含有未缩合的羧基和氨基;天然蛋白质的结构分为:一级结构、二级结构、三级结构、四级结构。
一级结构:蛋白质中各种氨基酸的连接方式和排列顺序,
肽键是一级结构的主键。
蛋白质的一级结构:
二级结构:多肽链卷曲盘旋和折叠的空间结构
蛋白质的二级结构:
三级结构:二级结构的肽链进一步盘曲折叠形成三维结构。
每一个具有三级结构的多肽链叫亚基。
蛋白质的三级结构:
四级结构:亚基的立体排布、亚基间的相互作用与布局
蛋白质的四级结构:
【学习任务四】蛋白质的性质
4、蛋白质的物理性质
溶解性:有些蛋白质(如鸡蛋清)能溶解在水里形成溶液。
5、蛋白质的化学性质
(2)水解:
在酸、碱或酶作用下,生成不同的氨基酸
(1)两性:
含有未缩合的羧基和氨基,与氨基酸的性质相似
二、蛋白质的结构与性质
(3)盐析:
(可逆的物理变化)
向蛋白质溶液中加入某些浓的无机盐溶液后,可使蛋白质凝聚而从溶液中析出。
盐析的应用
采用多次盐析的方法可以分离或提纯蛋白质
5、蛋白质的化学性质
【科学探究一】实验4-2
现象:
向蛋白质溶液中加入(NH4)2SO4溶液时,会使蛋白质从溶液沉淀出来,加水后沉淀又溶解。
【科学探究二】实验4-3
分别取两支试管。加入3mL鸡蛋清溶液,
1.向第一支试管中加入几滴醋酸铅溶液;
2.将第二支试管放在酒精灯上加热。
最后分别向两支试管中加适量的水,振荡观察现象。
现象:
蛋白质均凝结,加入适量清水后,凝结的蛋白质不再溶解。
(不可逆的化学变化)
(4)蛋白质变性:
在某些物理因素或化学因素的影响下,蛋白质的理化性质和生理功能发生改变的现象。
变性因素
物理因素:
加热、加压、搅拌、紫外线照射、超声波等
化学因素:
强酸、强碱、重金属盐、三氯乙酸、乙醇、醛、丙酮等
5、蛋白质的化学性质
阅读课本P90第一、二、三自然段内容,交流如下问题:(1)课本P90“学与问”。 (2)为什么生物实验室用甲醛溶液(福尔马林)保存动物标本?为什么在农业上用波尔多液(由硫酸铜、生石灰和水制成)来消灭病虫害?
思考交流
【科学探究三】实验4-4
用试管取2mL 鸡蛋白溶液;滴加几滴浓硝酸,微热。观察并记录现象。
现象:
鸡蛋白溶液遇浓硝酸加热颜色变黄
总结:
含有苯基的蛋白质均能发生这个反应。如皮肤,指甲等。
(5)颜色反应:
5、蛋白质的化学性质
(6)蛋白质的燃烧
(组成元素C、H、O、N、S、P等)
一般生成CO2、H2O、N2、SO2、P2O5等物质。有烧焦羽毛味。可用于蛋白质的鉴别。
【应用】真假羊毛衫、蚕丝被的鉴别
5、蛋白质的化学性质
蛋白质的用途
(1)食物(人类必须的营养物质)
(2)工业原料
动物的毛、蚕丝 (纺织原料)
动物的皮 (皮革)
动物的骨、皮、蹄 (动物胶)
牛奶中的酪素 (酪素塑料)
【学习任务五】酶与核酸
三、酶
——生物催化剂
1、什么是酶?
一类由细胞产生的,对生物体内的化学反应具有催化作用的有机物,其中绝大多数是蛋白质。
2、酶催化作用具有的特点
(1)条件温和,不需加热。
(2)具有高度的专一性。
(3)具有高效催化作用。
1、一类含磷的生物高分子化合物,相对分子量可达十几万至几百万。
2、核酸在生物体的生长、繁殖、遗传、变异等生命现象中起着决定性的作用。
3、具有酸性
4、分类:
(1)脱氧核糖核酸(DNA):生物遗传信息的载体;还指挥着蛋白质的合成、细胞的分裂和制造新的细胞。
(2)核糖核酸(RNA):根据DNA提供的信息控制体内蛋白质的合成。
四、核酸
——遗传信息的携带者
预习第五章第一节内容。
※ 布置作业 ※
第四章 生命中的基础有机化学物质
第三节 蛋白质和核酸
※明确学习目标※
1、知道氨基酸是组成蛋白质的基本结构单位。2、了解氨基酸的组成、结构特点和主要化学性质,理解肽键及多肽的形成。(学习重点)3、了解蛋白质的组成、结构和性质(盐析、变性、水解、颜色反应等)。4、认识蛋白质、酶、核酸等物质与人体健康的关系,体会化学学科在生命科学发展中所起的重要作用。
【资料卡片】生活中的蛋白质
蛋白质属于天然高分子化合物
【资料卡片】我国现代取得的成就
1965年我国科技工作者成功合成了具有生物活性的——结晶牛胰岛素。这是科学史上的一大成就,可以说是科学史上又一“丰碑”。在认识生命现象揭开生命奥秘的伟大历程中,做出了重要贡献。
课本P90“科学视野”
几乎一切生命活动过程都与蛋白质有关,没有蛋白质就没有生命!
1、定义: 羧酸分子中的烃基上的氢原子被-NH2(氨基)取代所得的一类化合物。所以在氨基酸分子中既有羧基(-COOH)又有氨基(-NH2)
【学习任务一】氨基酸的结构
一、氨基酸的结构与性质
2、氨基酸的结构简式:
组成天然蛋白质的都是α-氨基酸。
R—CH—C—OH
O
NH2
〖学习评价一〗 氨基(—NH2)就是氨分子(NH3)去掉一个氢原子后剩余的部分,你能类比羟基(—OH)的电子写出氨基的电子式吗?
3、几种常见的α-氨基酸:
(1) 氨基乙酸(甘氨酸) (2) α-氨基丙酸(丙氨酸)
CH2—COOH
NH2
CH3—CH—COOH
NH2
(3) 2-氨基-1,5-戊二酸(谷氨酸)
HOOC—(CH2)2—CH—COOH
NH2
(4) α-氨基苯丙酸(苯丙氨酸)
【学习任务二】氨基酸的性质
无色晶体,熔点较高,在200~3000C时熔化分解
一般能溶于水而难溶于乙醇、乙醚,能溶于强酸或者强碱溶液中。
4、氨基酸的物理性质
一、氨基酸的结构与性质
5、氨基酸的化学性质:
(1)氨基酸的两性: 羧基显酸性,氨基显碱性。
既能与强酸反应,也能与强碱反应,还能分子内反应生成内盐。
如:
CH2COOH+HCl CH2COOH
NH2
NH3Cl
R-CH-COOH + NaOH
NH2
R-CH-COONa + H2O
NH2
酶或酸或碱
+ H2O
+
肽键
(2)氨基酸的成肽反应:
(酸脱羟基,氨脱氢)
二肽:两个氨基酸之间脱一分子水得到的产物。
α-氨基酸
脱水缩合
二肽
脱水缩合
多肽
……
蛋白质
多种氨基酸分子按不同的排列顺序以肽键相互结合,可以形成千百万种具有不同的理化性质和生理活性的多肽链。相对分子量在10000以上的,并具有一定空间结构的多肽,称为蛋白质。
〖学习评价二〗分析下图多肽链,属于 肽,形成该化合物的氨基酸有 种,含有肽键的数目是 个。
四
3
4
二、蛋白质的结构与性质
【学习任务三】蛋白质的组成和结构
1、蛋白质的组成和结构
蛋白质的组成
组成元素:
C、H、O、N、S (P)等
组成基本结构单元:
氨基酸
相对分子质量:
几万——几千万,属于天然高分子化合物,
人体内所具有的蛋白质种类达到了10万种以上。
2、蛋白质的结构
各种蛋白质都有其特殊功能和活性,这不仅取决于取决于组成多肽链的氨基酸种类、数目及排列顺序,还与其特定的空间结构密切相关。
任何一种蛋白质分子在天然状态下均具有独特而稳定的结构,这是蛋白质分子结构中最显著的特征:蛋白质分子中含有未缩合的羧基和氨基;天然蛋白质的结构分为:一级结构、二级结构、三级结构、四级结构。
一级结构:蛋白质中各种氨基酸的连接方式和排列顺序,
肽键是一级结构的主键。
蛋白质的一级结构:
二级结构:多肽链卷曲盘旋和折叠的空间结构
蛋白质的二级结构:
三级结构:二级结构的肽链进一步盘曲折叠形成三维结构。
每一个具有三级结构的多肽链叫亚基。
蛋白质的三级结构:
四级结构:亚基的立体排布、亚基间的相互作用与布局
蛋白质的四级结构:
【学习任务四】蛋白质的性质
4、蛋白质的物理性质
溶解性:有些蛋白质(如鸡蛋清)能溶解在水里形成溶液。
5、蛋白质的化学性质
(2)水解:
在酸、碱或酶作用下,生成不同的氨基酸
(1)两性:
含有未缩合的羧基和氨基,与氨基酸的性质相似
二、蛋白质的结构与性质
(3)盐析:
(可逆的物理变化)
向蛋白质溶液中加入某些浓的无机盐溶液后,可使蛋白质凝聚而从溶液中析出。
盐析的应用
采用多次盐析的方法可以分离或提纯蛋白质
5、蛋白质的化学性质
【科学探究一】实验4-2
现象:
向蛋白质溶液中加入(NH4)2SO4溶液时,会使蛋白质从溶液沉淀出来,加水后沉淀又溶解。
【科学探究二】实验4-3
分别取两支试管。加入3mL鸡蛋清溶液,
1.向第一支试管中加入几滴醋酸铅溶液;
2.将第二支试管放在酒精灯上加热。
最后分别向两支试管中加适量的水,振荡观察现象。
现象:
蛋白质均凝结,加入适量清水后,凝结的蛋白质不再溶解。
(不可逆的化学变化)
(4)蛋白质变性:
在某些物理因素或化学因素的影响下,蛋白质的理化性质和生理功能发生改变的现象。
变性因素
物理因素:
加热、加压、搅拌、紫外线照射、超声波等
化学因素:
强酸、强碱、重金属盐、三氯乙酸、乙醇、醛、丙酮等
5、蛋白质的化学性质
阅读课本P90第一、二、三自然段内容,交流如下问题:(1)课本P90“学与问”。 (2)为什么生物实验室用甲醛溶液(福尔马林)保存动物标本?为什么在农业上用波尔多液(由硫酸铜、生石灰和水制成)来消灭病虫害?
思考交流
【科学探究三】实验4-4
用试管取2mL 鸡蛋白溶液;滴加几滴浓硝酸,微热。观察并记录现象。
现象:
鸡蛋白溶液遇浓硝酸加热颜色变黄
总结:
含有苯基的蛋白质均能发生这个反应。如皮肤,指甲等。
(5)颜色反应:
5、蛋白质的化学性质
(6)蛋白质的燃烧
(组成元素C、H、O、N、S、P等)
一般生成CO2、H2O、N2、SO2、P2O5等物质。有烧焦羽毛味。可用于蛋白质的鉴别。
【应用】真假羊毛衫、蚕丝被的鉴别
5、蛋白质的化学性质
蛋白质的用途
(1)食物(人类必须的营养物质)
(2)工业原料
动物的毛、蚕丝 (纺织原料)
动物的皮 (皮革)
动物的骨、皮、蹄 (动物胶)
牛奶中的酪素 (酪素塑料)
【学习任务五】酶与核酸
三、酶
——生物催化剂
1、什么是酶?
一类由细胞产生的,对生物体内的化学反应具有催化作用的有机物,其中绝大多数是蛋白质。
2、酶催化作用具有的特点
(1)条件温和,不需加热。
(2)具有高度的专一性。
(3)具有高效催化作用。
1、一类含磷的生物高分子化合物,相对分子量可达十几万至几百万。
2、核酸在生物体的生长、繁殖、遗传、变异等生命现象中起着决定性的作用。
3、具有酸性
4、分类:
(1)脱氧核糖核酸(DNA):生物遗传信息的载体;还指挥着蛋白质的合成、细胞的分裂和制造新的细胞。
(2)核糖核酸(RNA):根据DNA提供的信息控制体内蛋白质的合成。
四、核酸
——遗传信息的携带者
预习第五章第一节内容。
※ 布置作业 ※
