4.2 糖类 课件 2020-2021学年人教版高二化学选修5(27张PPT)
文档属性
| 名称 | 4.2 糖类 课件 2020-2021学年人教版高二化学选修5(27张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-06-26 00:00:00 | ||
图片预览






文档简介
化学 · 选修5
第四章 生命中的基础有机化学物质
第二节 糖类
※明确学习目标※
1、了解糖类的概念、分类及结构特点,了解分子的手性。2、掌握葡萄糖和果糖的结构特点,能根据葡萄糖的分子结构,推测葡萄糖典型的化学性质并设计实验探究验证。(学习重点)
3、 知道蔗糖、麦芽糖、淀粉、纤维素的存在和主要物理性质。记住蔗糖、麦芽糖、淀粉、纤维素的结构特点和化学性质,并了解它们之间的相互转变和跟烃的衍生物的关系。(学习重点)
【学习任务一】认识糖类的概念和分类
C12H22O11
C6H12O6
(C6H10O5)n
【思考与讨论】如何定义糖类?糖类被称为“碳水化合物”准确吗?
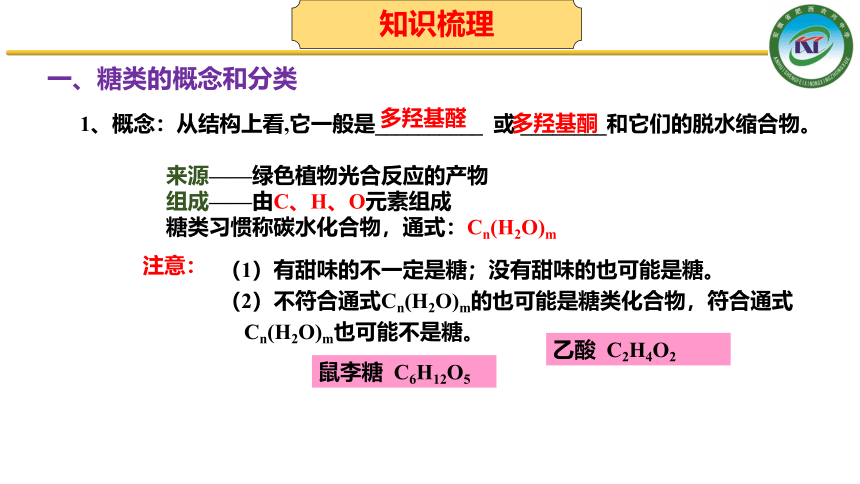
1、概念:从结构上看,它一般是__________ 或 ________和它们的脱水缩合物。
一、糖类的概念和分类
(1)有甜味的不一定是糖;没有甜味的也可能是糖。
(2)不符合通式Cn(H2O)m的也可能是糖类化合物,符合通式Cn(H2O)m也可能不是糖。
注意:
鼠李糖 C6H12O5
乙酸 C2H4O2
多羟基醛
多羟基酮
来源——绿色植物光合反应的产物
组成——由C、H、O元素组成
糖类习惯称碳水化合物,通式:Cn(H2O)m
知识梳理
葡萄糖 C6H12O6
果 糖 C6H12O6
2、分类
蔗 糖 C12H22O11
麦芽糖 C12H22O11
淀 粉 (C6H10O5)n
纤维素 (C6H10O5)n
单糖(不能水解的糖)
低聚糖(1mol水解产生2-10mol单糖)
多糖(1mol水解产生多摩尔单糖)
互为同分异构体
互为同分异构体
n值不同,二者不互为同分异构体
根据生活经验,总结葡萄糖的物理性质
无色晶体,有甜味,易溶于水
稍溶于乙醇,不溶于乙醚
熔点:1460C
【学习任务二】葡萄糖与果糖
〖科学探究〗葡萄糖的结构和性质 (1)分析:葡萄糖的分子式为C6H12O6,其分子的饱和程度如何?结构可能有什么特点? (2)实验探究:完成课本P80“实验4-1”。 现象: 。 结论:葡萄糖分子中具有 (填官能团)的结构。 (3)有如下事实:① 在一定条件下,1mol葡萄糖与乙酸完全酯化,需要消耗乙酸5mol;②葡萄糖可以还原生成直链的己六醇;③ 同一个碳原子不能与两个—OH相连。有这些事实,你能确定葡萄糖的结构简式吗? (4)根据推断出的葡萄糖结构,请你预测葡萄糖应该有哪些化学性质?
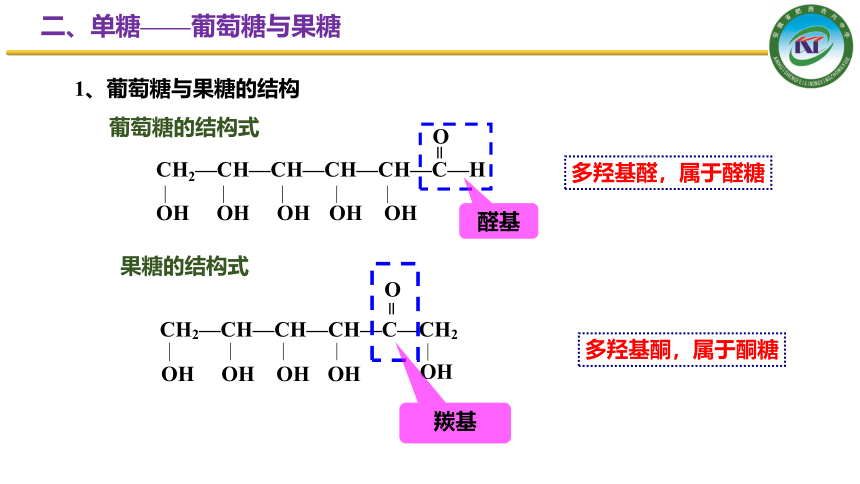
葡萄糖的结构式
O
CH2—CH—CH—CH—CH—C—H
=
OH OH OH
OH OH
醛基
=
O
CH2—CH—CH—CH—C—CH2
OH OH OH
OH
OH
羰基
果糖的结构式
多羟基醛,属于醛糖
多羟基酮,属于酮糖
二、单糖——葡萄糖与果糖
1、葡萄糖与果糖的结构
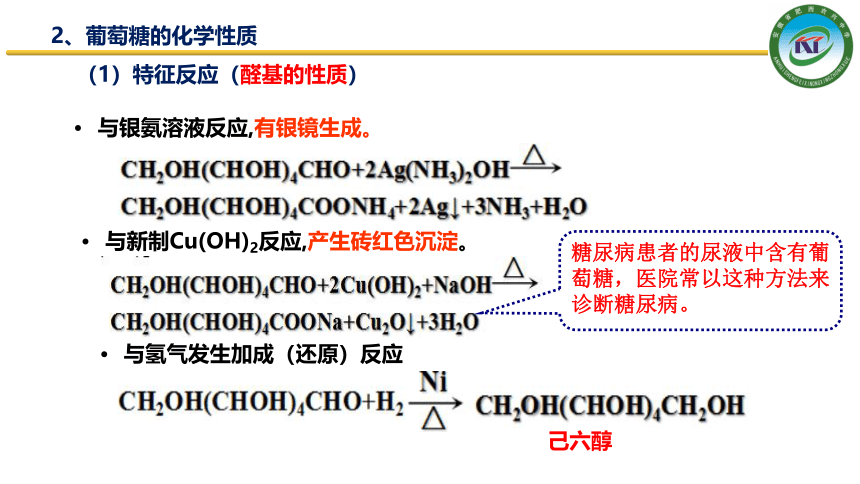
2、葡萄糖的化学性质
(1)特征反应(醛基的性质)
与新制Cu(OH)2反应,产生砖红色沉淀。
与银氨溶液反应,有银镜生成。
与氢气发生加成(还原)反应
己六醇
糖尿病患者的尿液中含有葡萄糖,医院常以这种方法来诊断糖尿病。
5
5
五乙酸葡萄糖酯
+
CHO
(CHOOCCH 3) 4
CH2OOCCH3
H2O
CH3COOH
+
CHO
(CHOH )4
CH2OH
(能与酸发生酯化反应)
(2)酯化反应(有多元醇的性质):
浓H2SO4
(3)氧化反应(与氧气的生理氧化)
葡萄糖是人体内的重要能源物质:
C6H12O6 (s)+ 6O2(g) →6CO2(g) + 6H2O(l) + 2804kJ
(4)发酵成酒精
3、果糖
结构简式:
CH2—CH—CH—CH—C—CH2OH
OH OH OH OH O
分子式:
C6H12O6
多羟基酮
物理性质:纯净的果糖为无色晶体,通常为粘稠性液体,易溶于水、乙醇和乙醚
葡萄糖与果糖互为同分异构体,葡萄糖是一种多羟基醛(醛糖),果糖是一种多羟基酮(酮糖),果糖分子中并无醛基存在,看来似乎不能发生银镜反应,但其实不然,其主要原因是果糖在碱性溶液中可发生反应生成醛基。因此果糖也可以发生银镜反应与斐林反应。
【科学视野】 分子的手性
1、手性碳原子是指与四个各不相同原子或基团相连的碳原子,用C*表示。
2、所有含一个手性碳原子的化合物,都有一对对映异构体。对大多数有机分子而言,分子的手性主要是由分子中的手性碳原子引起的。
你能判断、标出手性碳原子吗?
1、下列有关糖类物质的叙述正确的是( )
A、糖类是具有甜味的物质
B、糖类是具有Cn(H2O)m通式的物质
C、糖类是含有醛基或羰基的物质
D、糖类是多羟基醛或多羟基酮及它们多个分子脱水而形成的高分子物质
D
【学习评价一】
2、下列物质不属于糖类的是 ( ) A.CH2OHCHOHCHOHCHO B.CH2OHCHOHCHOHCH2CHO C.CH2OHCHO D.CH2OH(CHOH)3COCH2OH
C
3、核糖是合成核酸的重要原料,结构简式为:CH2OH(CHOH)3CHO,下列关于核糖叙述正确的是( )
A.与葡萄糖互为同分异构体
B.可以与银氨溶液作用形成银镜
C.可以跟氯化铁溶液发生显色反应
D.可以使紫色石蕊试液变红
B
【学习评价一】
【学习任务三】蔗糖与麦芽糖
阅读课本P82相关内容,了解蔗糖与麦芽糖的存在和主要性质,比较二都的相同点和不同点。
对比实验1:
20%蔗
糖溶液
无明显现象
20%麦芽
糖溶液
产生砖红色沉淀
新制Cu(OH)2
新制Cu(OH)2
课本P82页“科学探究”
三、双糖——蔗糖与麦芽糖
化学性质:
蔗糖:
麦芽糖:
无还原性,是一种非还原性糖
有还原性,是一种还原性糖
C12H22O11
同分异构
对比实验2:
20%蔗
糖溶液
无明显现象
蔗糖 +
稀硫酸
NaOH
中和酸
水解反应:
C6H12O6 + C6H12O6
(葡萄糖) (果糖)
催化剂
C12H22O11 + H2O
(蔗糖)
新制Cu(OH)2
新制Cu(OH)2
产生砖红色沉淀
C12H22O11 + H2O 2 C6H12O6
(麦芽糖) (葡萄糖)
催化剂
蔗糖与麦芽糖的比较
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A} 物质
蔗糖
麦芽糖
分子式
C12H22O11
同分异构
还原性
非还原性糖
(无-CHO)
还原性糖
(有-CHO)
水解情况
水解成一分子葡萄糖,一分子果糖
水解成二分子葡萄糖
分类
二糖
二糖
找找生活中哪些物质含有淀粉,哪些物质含有纤维素?
【学习任务四】淀粉与纤维素
淀粉的存在:植物的种子和块根
大米,约含淀粉80%
小麦,约含淀粉70%
马铃薯,约含淀粉20%
纤维素的存在:纤维素是植物的成分,植物的茎、叶和果皮中都含有纤维素。
棉花含纤维素92%~95%;
亚麻含纤维素约80%;
木材含纤维素约50%。
四、多糖——淀粉与纤维素
1、淀粉、纤维素的结构比较:
(1)多糖具有相同的通式:(C6H10O5)n
(2)其中含有的单糖单元(C6H10O5)的数值n,取值各不相同,只有大致的范围;
(3)当n=几百到几千时,为淀粉;
当n=几千到几万以上时,为纤维素。
(4)淀粉和纤维素不是同分异构体,也不是同系物,都是天然高分子化合物。
2、化学性质
比较:(1)两者均没有还原性
(2)两者在一定条件下都可以发生水解,且最终产物都是葡萄糖。
(C6H10O5)n +nH2O → nC6H12O6
淀粉或纤维素 葡萄糖
催化剂
四、多糖——淀粉与纤维素
(3)淀粉遇碘变蓝色
淀粉水解程度的判断及水解产物的检验 (课本P83“科学探究”。)(1)实验原理: ①淀粉遇碘显蓝色,但不发生银镜反应; ②葡萄糖:遇碘不显蓝色,但可发生银镜反应。(2)实验步骤:
(3)实验现象及结论:
{5940675A-B579-460E-94D1-54222C63F5DA}
现象A
现象B
结论
①
未出现银镜
溶液变蓝色
②
出现银镜
溶液变蓝色
③
出现银镜
溶液不变蓝色
〖总结〗单糖、二糖和多糖关系及与烃的衍生物转化关系:
预习下一节内容。
※ 布置作业 ※
第四章 生命中的基础有机化学物质
第二节 糖类
※明确学习目标※
1、了解糖类的概念、分类及结构特点,了解分子的手性。2、掌握葡萄糖和果糖的结构特点,能根据葡萄糖的分子结构,推测葡萄糖典型的化学性质并设计实验探究验证。(学习重点)
3、 知道蔗糖、麦芽糖、淀粉、纤维素的存在和主要物理性质。记住蔗糖、麦芽糖、淀粉、纤维素的结构特点和化学性质,并了解它们之间的相互转变和跟烃的衍生物的关系。(学习重点)
【学习任务一】认识糖类的概念和分类
C12H22O11
C6H12O6
(C6H10O5)n
【思考与讨论】如何定义糖类?糖类被称为“碳水化合物”准确吗?
1、概念:从结构上看,它一般是__________ 或 ________和它们的脱水缩合物。
一、糖类的概念和分类
(1)有甜味的不一定是糖;没有甜味的也可能是糖。
(2)不符合通式Cn(H2O)m的也可能是糖类化合物,符合通式Cn(H2O)m也可能不是糖。
注意:
鼠李糖 C6H12O5
乙酸 C2H4O2
多羟基醛
多羟基酮
来源——绿色植物光合反应的产物
组成——由C、H、O元素组成
糖类习惯称碳水化合物,通式:Cn(H2O)m
知识梳理
葡萄糖 C6H12O6
果 糖 C6H12O6
2、分类
蔗 糖 C12H22O11
麦芽糖 C12H22O11
淀 粉 (C6H10O5)n
纤维素 (C6H10O5)n
单糖(不能水解的糖)
低聚糖(1mol水解产生2-10mol单糖)
多糖(1mol水解产生多摩尔单糖)
互为同分异构体
互为同分异构体
n值不同,二者不互为同分异构体
根据生活经验,总结葡萄糖的物理性质
无色晶体,有甜味,易溶于水
稍溶于乙醇,不溶于乙醚
熔点:1460C
【学习任务二】葡萄糖与果糖
〖科学探究〗葡萄糖的结构和性质 (1)分析:葡萄糖的分子式为C6H12O6,其分子的饱和程度如何?结构可能有什么特点? (2)实验探究:完成课本P80“实验4-1”。 现象: 。 结论:葡萄糖分子中具有 (填官能团)的结构。 (3)有如下事实:① 在一定条件下,1mol葡萄糖与乙酸完全酯化,需要消耗乙酸5mol;②葡萄糖可以还原生成直链的己六醇;③ 同一个碳原子不能与两个—OH相连。有这些事实,你能确定葡萄糖的结构简式吗? (4)根据推断出的葡萄糖结构,请你预测葡萄糖应该有哪些化学性质?
葡萄糖的结构式
O
CH2—CH—CH—CH—CH—C—H
=
OH OH OH
OH OH
醛基
=
O
CH2—CH—CH—CH—C—CH2
OH OH OH
OH
OH
羰基
果糖的结构式
多羟基醛,属于醛糖
多羟基酮,属于酮糖
二、单糖——葡萄糖与果糖
1、葡萄糖与果糖的结构
2、葡萄糖的化学性质
(1)特征反应(醛基的性质)
与新制Cu(OH)2反应,产生砖红色沉淀。
与银氨溶液反应,有银镜生成。
与氢气发生加成(还原)反应
己六醇
糖尿病患者的尿液中含有葡萄糖,医院常以这种方法来诊断糖尿病。
5
5
五乙酸葡萄糖酯
+
CHO
(CHOOCCH 3) 4
CH2OOCCH3
H2O
CH3COOH
+
CHO
(CHOH )4
CH2OH
(能与酸发生酯化反应)
(2)酯化反应(有多元醇的性质):
浓H2SO4
(3)氧化反应(与氧气的生理氧化)
葡萄糖是人体内的重要能源物质:
C6H12O6 (s)+ 6O2(g) →6CO2(g) + 6H2O(l) + 2804kJ
(4)发酵成酒精
3、果糖
结构简式:
CH2—CH—CH—CH—C—CH2OH
OH OH OH OH O
分子式:
C6H12O6
多羟基酮
物理性质:纯净的果糖为无色晶体,通常为粘稠性液体,易溶于水、乙醇和乙醚
葡萄糖与果糖互为同分异构体,葡萄糖是一种多羟基醛(醛糖),果糖是一种多羟基酮(酮糖),果糖分子中并无醛基存在,看来似乎不能发生银镜反应,但其实不然,其主要原因是果糖在碱性溶液中可发生反应生成醛基。因此果糖也可以发生银镜反应与斐林反应。
【科学视野】 分子的手性
1、手性碳原子是指与四个各不相同原子或基团相连的碳原子,用C*表示。
2、所有含一个手性碳原子的化合物,都有一对对映异构体。对大多数有机分子而言,分子的手性主要是由分子中的手性碳原子引起的。
你能判断、标出手性碳原子吗?
1、下列有关糖类物质的叙述正确的是( )
A、糖类是具有甜味的物质
B、糖类是具有Cn(H2O)m通式的物质
C、糖类是含有醛基或羰基的物质
D、糖类是多羟基醛或多羟基酮及它们多个分子脱水而形成的高分子物质
D
【学习评价一】
2、下列物质不属于糖类的是 ( ) A.CH2OHCHOHCHOHCHO B.CH2OHCHOHCHOHCH2CHO C.CH2OHCHO D.CH2OH(CHOH)3COCH2OH
C
3、核糖是合成核酸的重要原料,结构简式为:CH2OH(CHOH)3CHO,下列关于核糖叙述正确的是( )
A.与葡萄糖互为同分异构体
B.可以与银氨溶液作用形成银镜
C.可以跟氯化铁溶液发生显色反应
D.可以使紫色石蕊试液变红
B
【学习评价一】
【学习任务三】蔗糖与麦芽糖
阅读课本P82相关内容,了解蔗糖与麦芽糖的存在和主要性质,比较二都的相同点和不同点。
对比实验1:
20%蔗
糖溶液
无明显现象
20%麦芽
糖溶液
产生砖红色沉淀
新制Cu(OH)2
新制Cu(OH)2
课本P82页“科学探究”
三、双糖——蔗糖与麦芽糖
化学性质:
蔗糖:
麦芽糖:
无还原性,是一种非还原性糖
有还原性,是一种还原性糖
C12H22O11
同分异构
对比实验2:
20%蔗
糖溶液
无明显现象
蔗糖 +
稀硫酸
NaOH
中和酸
水解反应:
C6H12O6 + C6H12O6
(葡萄糖) (果糖)
催化剂
C12H22O11 + H2O
(蔗糖)
新制Cu(OH)2
新制Cu(OH)2
产生砖红色沉淀
C12H22O11 + H2O 2 C6H12O6
(麦芽糖) (葡萄糖)
催化剂
蔗糖与麦芽糖的比较
{5C22544A-7EE6-4342-B048-85BDC9FD1C3A} 物质
蔗糖
麦芽糖
分子式
C12H22O11
同分异构
还原性
非还原性糖
(无-CHO)
还原性糖
(有-CHO)
水解情况
水解成一分子葡萄糖,一分子果糖
水解成二分子葡萄糖
分类
二糖
二糖
找找生活中哪些物质含有淀粉,哪些物质含有纤维素?
【学习任务四】淀粉与纤维素
淀粉的存在:植物的种子和块根
大米,约含淀粉80%
小麦,约含淀粉70%
马铃薯,约含淀粉20%
纤维素的存在:纤维素是植物的成分,植物的茎、叶和果皮中都含有纤维素。
棉花含纤维素92%~95%;
亚麻含纤维素约80%;
木材含纤维素约50%。
四、多糖——淀粉与纤维素
1、淀粉、纤维素的结构比较:
(1)多糖具有相同的通式:(C6H10O5)n
(2)其中含有的单糖单元(C6H10O5)的数值n,取值各不相同,只有大致的范围;
(3)当n=几百到几千时,为淀粉;
当n=几千到几万以上时,为纤维素。
(4)淀粉和纤维素不是同分异构体,也不是同系物,都是天然高分子化合物。
2、化学性质
比较:(1)两者均没有还原性
(2)两者在一定条件下都可以发生水解,且最终产物都是葡萄糖。
(C6H10O5)n +nH2O → nC6H12O6
淀粉或纤维素 葡萄糖
催化剂
四、多糖——淀粉与纤维素
(3)淀粉遇碘变蓝色
淀粉水解程度的判断及水解产物的检验 (课本P83“科学探究”。)(1)实验原理: ①淀粉遇碘显蓝色,但不发生银镜反应; ②葡萄糖:遇碘不显蓝色,但可发生银镜反应。(2)实验步骤:
(3)实验现象及结论:
{5940675A-B579-460E-94D1-54222C63F5DA}
现象A
现象B
结论
①
未出现银镜
溶液变蓝色
②
出现银镜
溶液变蓝色
③
出现银镜
溶液不变蓝色
〖总结〗单糖、二糖和多糖关系及与烃的衍生物转化关系:
预习下一节内容。
※ 布置作业 ※
