3.3 第2课时 酯 精品课件(人教版选修5)
文档属性
| 名称 | 3.3 第2课时 酯 精品课件(人教版选修5) |

|
|
| 格式 | zip | ||
| 文件大小 | 511.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-04-15 00:00:00 | ||
图片预览







文档简介
(共28张PPT)
第2课时 酯
[读教材·填要点]
一、酯的结构
酯是羧酸分子羧基中的—OH被—OR′取代后的产物,简写成 ,R和R′可以相同,也可以不
同.羧酸酯的官能团是“ ”( ),饱和一元酯的通式 .
RCOOR′
酯基
CnH2nO2
二、酯的性质
酯一般难溶于水,密度比水 ,主要化学性质是易
发生 反应.
1.乙酸乙酯在酸性条件下发生水解反应的化学方程式:
小
水解
2.乙酸乙酯在碱性条件下发生水解反应的化学方程式:
3.乙酸乙酯在不同条件下发生水解的实验探究
试管编号 a b c
实验操作 1 向试管内加入6滴乙酸乙酯,再加入5.5 mL
蒸馏水,振荡均匀 向试管内加入6滴乙酸乙酯,再加入稀硫酸(1∶5)0.5 mL、蒸馏水5 mL,振荡均匀 向试管内加入6滴乙酸乙酯,再加入30%的NaOH溶液0.5 mL、蒸馏水5 mL,振荡均匀
2 将3支试管同时放入70~80℃的水浴里加热约5 min,闻各试管里乙酸乙酯的气味
试管编号 a b c
实验现象
实验结论
乙酸乙酯的
气味很浓
略有乙酸乙
酯的气味
无乙酸乙酯
的气味
乙酸乙酯未
水解
大多数乙酸乙
酯已水解
乙酸乙酯全部
水解
实验时需要注意的问题:
(1)本实验为对比实验,3支试管中反应物的用量、温度、
时间都应相同,否则没有可比性.
(2)乙酸乙酯的沸点为77℃,为了便于控制温度以防止乙
酸乙酯的挥发,加热时要水浴加热且控制温度在70℃~80℃的范围内,实验所用的无机酸最好是稀硫酸.
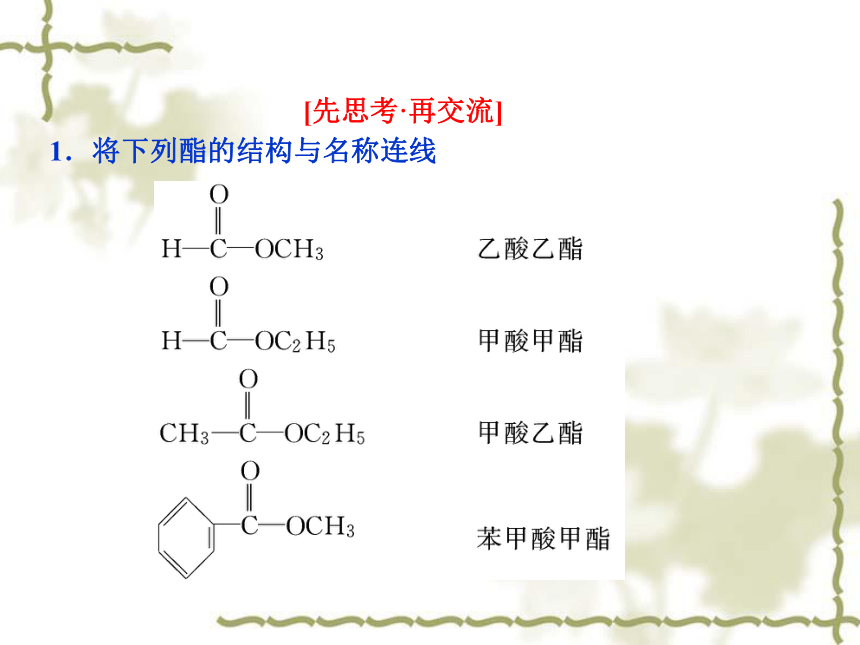
[先思考·再交流]
1.将下列酯的结构与名称连线
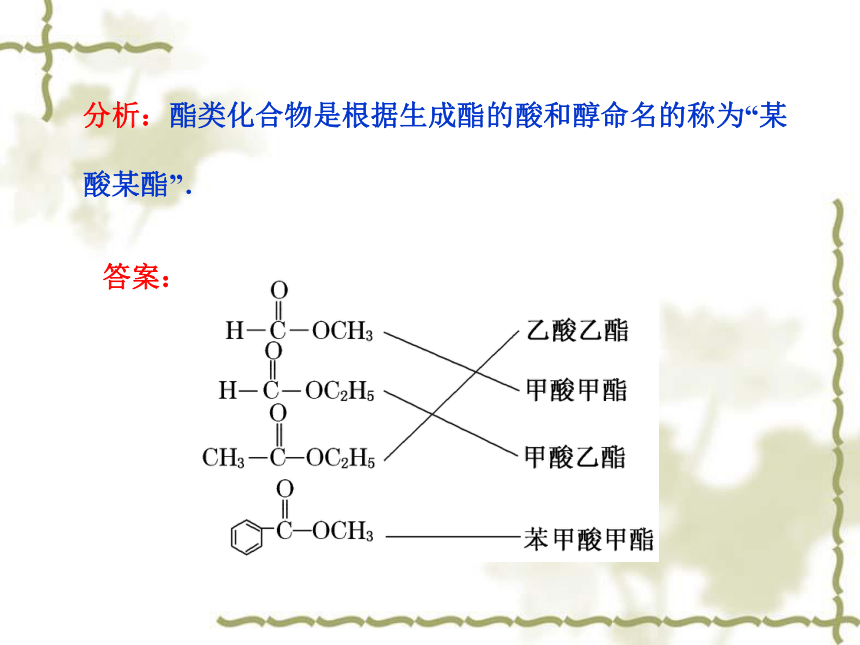
分析:酯类化合物是根据生成酯的酸和醇命名的称为“某酸某酯”.
答案:
2.完成下列表格:
酯化反应和酯的水解反应的比较
酯化反应 酯的水解反应
反应关系 CH3COOH+C2H5OH
CH3COOC2H5+H2O
催化剂
催化剂的作用
加热方法
反应类型
分析:在酯化反应和酯的水解反应中,所用硫酸的浓度是不同的.①在酯化反应中,除利用硫酸的催化性以外,还要利用它的吸水性,以减少酯化反应生成的水,促使可逆反应向酯化的反应方向进行,提高醇和羧酸的转化率(也就是酯的产率),故要选用浓硫酸,且用量较大.②在酯的水解反应中,只需利用硫酸的催化性,故要选用稀硫酸,且用量较小.
酯化反应 酯的水解反应
反应关系 CH3COOH+C2H5OH
CH3COOC2H5+H2O
催化剂 浓H2SO4 稀H2SO4
催化剂的作用 催化剂、吸水剂 催化剂
加热方法 直接加热 水浴加热
反应类型 取代反应 取代反应
答案:
要点一 酯水解的规律 ————————————
1.断键部位,酯化反应形成的键,即是酯水解反应断裂
的键.例如 中,酯基 中的C—O键是酯化反应时形成的键,则水解时C—O键断裂,C原子连接水提供的—OH,O原子连接水提供的—H,分别形成羧基和羟基.
则相应的酸和醇碳原子数目相等,烃基的碳架结构相同,且醇中必有—CH2OH结构.
与醇的相对分子质量相等,则醇比酸多一个碳原子.
能发生银镜反应的有机物除醛类外,还有甲酸、甲酸盐、甲酸某酯及葡萄糖、麦芽糖.
[例] 酯A水解可生成酸X和醇Y,若Y氧化可得酸X,则A不可能是 ( )
.
[答案] C
某有机物X能发生水解反应,水解产物为Y和Z,同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是 ( )
A.乙酸丙酯 B.甲酸乙酯
C.乙酸甲酯 D.乙酸乙酯
解析:相同条件下,相同质量的Y和Z的蒸气所占体积相同,说明Y和Z的相对分子质量相等,酯在酸性条件下水解得到的产物为羧酸和醇,若使二者相对分子质量相等,则醇比羧酸多一个碳原子.
答案: AB
依据有机物的结构简式确定1 mol 该有机物消耗NaOH的物质的量时,要特别注意官能团的连接方式,因不同的连接方式可消耗不同量的NaOH,否则容易造成判断错误.
(1)只有1个—OH连在苯环上时,1 mol 该有机物消耗1
mol NaOH,而—OH连在烃基上时不与NaOH发生反
应.
(2)—X连在烃基上时,1 mol 该有机物消耗1 mol NaOH;
而—X连在苯环上时,1 mol 该有机物能消耗2 mol
NaOH.
(3) (酯基)氧连在烃基上时,1 mol 该有机物
消耗1 mol NaOH,而酯基氧连在苯环上
时消耗2 mol NaOH.
[例] 与足量的NaOH溶液充分反应,消耗的NaOH的物质的量为
( )
A.5 mol B.4 mol
C.3 mol D.2 mol
[解析] 1 mol该分子中有1 mol酚羟基和2 mol酯基,酚羟基消耗1 mol NaOH,酯基水解后生成2 mol酚羟基和2 mol羧基,又消耗4 mol NaOH,共消耗5 mol NaOH,故选A.
[答案] A
第2课时 酯
[读教材·填要点]
一、酯的结构
酯是羧酸分子羧基中的—OH被—OR′取代后的产物,简写成 ,R和R′可以相同,也可以不
同.羧酸酯的官能团是“ ”( ),饱和一元酯的通式 .
RCOOR′
酯基
CnH2nO2
二、酯的性质
酯一般难溶于水,密度比水 ,主要化学性质是易
发生 反应.
1.乙酸乙酯在酸性条件下发生水解反应的化学方程式:
小
水解
2.乙酸乙酯在碱性条件下发生水解反应的化学方程式:
3.乙酸乙酯在不同条件下发生水解的实验探究
试管编号 a b c
实验操作 1 向试管内加入6滴乙酸乙酯,再加入5.5 mL
蒸馏水,振荡均匀 向试管内加入6滴乙酸乙酯,再加入稀硫酸(1∶5)0.5 mL、蒸馏水5 mL,振荡均匀 向试管内加入6滴乙酸乙酯,再加入30%的NaOH溶液0.5 mL、蒸馏水5 mL,振荡均匀
2 将3支试管同时放入70~80℃的水浴里加热约5 min,闻各试管里乙酸乙酯的气味
试管编号 a b c
实验现象
实验结论
乙酸乙酯的
气味很浓
略有乙酸乙
酯的气味
无乙酸乙酯
的气味
乙酸乙酯未
水解
大多数乙酸乙
酯已水解
乙酸乙酯全部
水解
实验时需要注意的问题:
(1)本实验为对比实验,3支试管中反应物的用量、温度、
时间都应相同,否则没有可比性.
(2)乙酸乙酯的沸点为77℃,为了便于控制温度以防止乙
酸乙酯的挥发,加热时要水浴加热且控制温度在70℃~80℃的范围内,实验所用的无机酸最好是稀硫酸.
[先思考·再交流]
1.将下列酯的结构与名称连线
分析:酯类化合物是根据生成酯的酸和醇命名的称为“某酸某酯”.
答案:
2.完成下列表格:
酯化反应和酯的水解反应的比较
酯化反应 酯的水解反应
反应关系 CH3COOH+C2H5OH
CH3COOC2H5+H2O
催化剂
催化剂的作用
加热方法
反应类型
分析:在酯化反应和酯的水解反应中,所用硫酸的浓度是不同的.①在酯化反应中,除利用硫酸的催化性以外,还要利用它的吸水性,以减少酯化反应生成的水,促使可逆反应向酯化的反应方向进行,提高醇和羧酸的转化率(也就是酯的产率),故要选用浓硫酸,且用量较大.②在酯的水解反应中,只需利用硫酸的催化性,故要选用稀硫酸,且用量较小.
酯化反应 酯的水解反应
反应关系 CH3COOH+C2H5OH
CH3COOC2H5+H2O
催化剂 浓H2SO4 稀H2SO4
催化剂的作用 催化剂、吸水剂 催化剂
加热方法 直接加热 水浴加热
反应类型 取代反应 取代反应
答案:
要点一 酯水解的规律 ————————————
1.断键部位,酯化反应形成的键,即是酯水解反应断裂
的键.例如 中,酯基 中的C—O键是酯化反应时形成的键,则水解时C—O键断裂,C原子连接水提供的—OH,O原子连接水提供的—H,分别形成羧基和羟基.
则相应的酸和醇碳原子数目相等,烃基的碳架结构相同,且醇中必有—CH2OH结构.
与醇的相对分子质量相等,则醇比酸多一个碳原子.
能发生银镜反应的有机物除醛类外,还有甲酸、甲酸盐、甲酸某酯及葡萄糖、麦芽糖.
[例] 酯A水解可生成酸X和醇Y,若Y氧化可得酸X,则A不可能是 ( )
.
[答案] C
某有机物X能发生水解反应,水解产物为Y和Z,同温同压下,相同质量的Y和Z的蒸气所占体积相同,化合物X可能是 ( )
A.乙酸丙酯 B.甲酸乙酯
C.乙酸甲酯 D.乙酸乙酯
解析:相同条件下,相同质量的Y和Z的蒸气所占体积相同,说明Y和Z的相对分子质量相等,酯在酸性条件下水解得到的产物为羧酸和醇,若使二者相对分子质量相等,则醇比羧酸多一个碳原子.
答案: AB
依据有机物的结构简式确定1 mol 该有机物消耗NaOH的物质的量时,要特别注意官能团的连接方式,因不同的连接方式可消耗不同量的NaOH,否则容易造成判断错误.
(1)只有1个—OH连在苯环上时,1 mol 该有机物消耗1
mol NaOH,而—OH连在烃基上时不与NaOH发生反
应.
(2)—X连在烃基上时,1 mol 该有机物消耗1 mol NaOH;
而—X连在苯环上时,1 mol 该有机物能消耗2 mol
NaOH.
(3) (酯基)氧连在烃基上时,1 mol 该有机物
消耗1 mol NaOH,而酯基氧连在苯环上
时消耗2 mol NaOH.
[例] 与足量的NaOH溶液充分反应,消耗的NaOH的物质的量为
( )
A.5 mol B.4 mol
C.3 mol D.2 mol
[解析] 1 mol该分子中有1 mol酚羟基和2 mol酯基,酚羟基消耗1 mol NaOH,酯基水解后生成2 mol酚羟基和2 mol羧基,又消耗4 mol NaOH,共消耗5 mol NaOH,故选A.
[答案] A
