化学选修5第三章 烃的含氧衍生物第二节醛
文档属性
| 名称 | 化学选修5第三章 烃的含氧衍生物第二节醛 |

|
|
| 格式 | zip | ||
| 文件大小 | 230.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-04-15 00:00:00 | ||
图片预览







文档简介
(共39张PPT)
化学选修⑤第三章 烃的含氧衍生物
第二节 醛
根据醇类催化氧化反应的原理,
完成下列方程式
醇类发生催化氧化的条件是什么?
1.Ag或Cu作催化剂并加热。
2.羟基所连的碳原子上有氢原子。
2CH3CH2OH+O2
△
Cu
2CH3CHO+2H2O
2CH3CHCH3+O2
OH
△
Cu
2CH3CCH3+2H2O
O
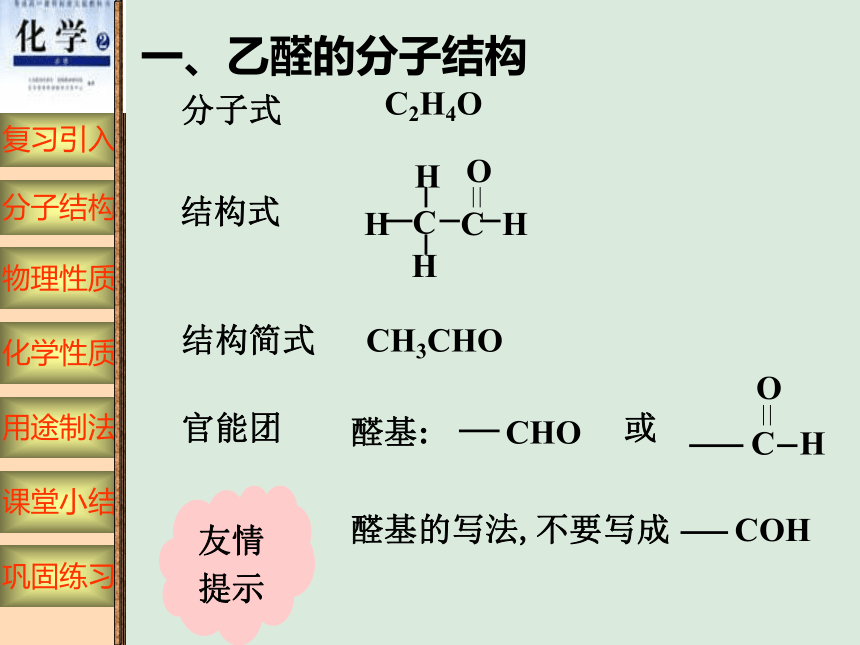
一、乙醛的分子结构
分子式
结构简式 CH3CHO
结构式
H
H
H
H
C
C
O
官能团
醛基:
CHO
或
C
H
O
醛基的写法,不要写成
COH
C2H4O
友情提示
二、乙醛的物理性质
常温下为无色有刺激性气味的液体,
密度比水小,
沸点:20.8℃,
易挥发,易燃烧,
能与水、乙醇、乙醚、氯仿等互溶。
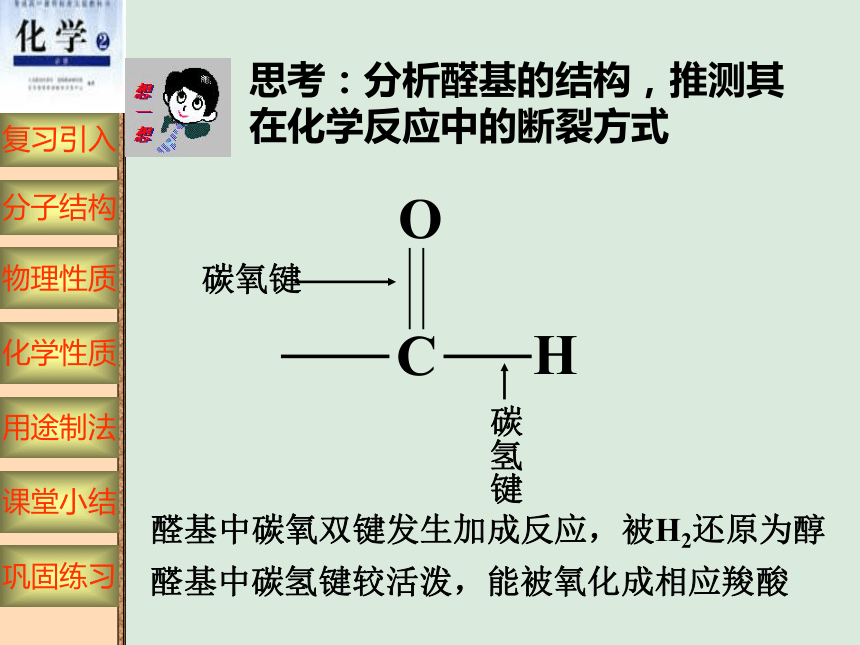
思考:分析醛基的结构,推测其
在化学反应中的断裂方式
C
H
O
碳氧键
碳氢键
醛基中碳氧双键发生加成反应,被H2还原为醇
醛基中碳氢键较活泼,能被氧化成相应羧酸
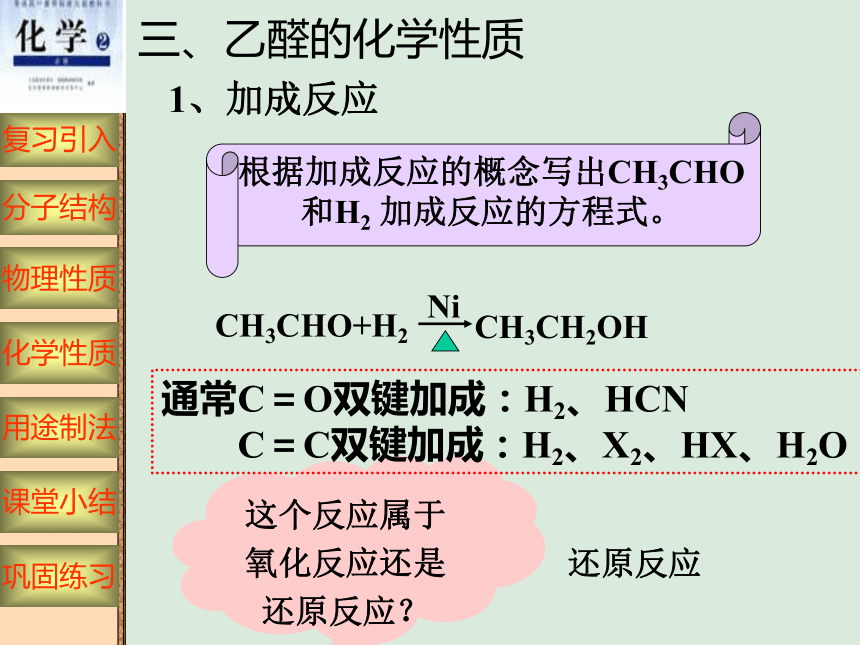
1、加成反应
Ni
CH3CHO+H2
CH3CH2OH
根据加成反应的概念写出CH3CHO
和H2 加成反应的方程式。
这个反应属于氧化反应还是还原反应?
还原反应
三、乙醛的化学性质
通常C=O双键加成:H2、HCN
C=C双键加成:H2、X2、HX、H2O
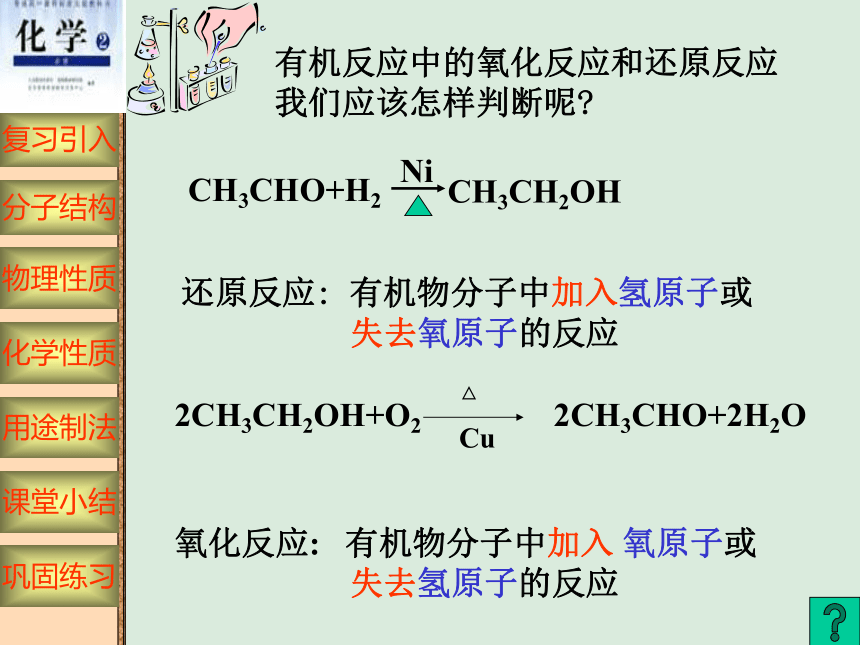
有机反应中的氧化反应和还原反应
我们应该怎样判断呢
2CH3CH2OH+O2
△
Cu
2CH3CHO+2H2O
氧化反应: 有机物分子中加入 氧原子或
失去氢原子的反应
还原反应: 有机物分子中加入氢原子或
失去氧原子的反应
Ni
CH3CHO+H2
CH3CH2OH
回子菜单
2、氧化反应
a. 催化氧化
2CH3CHO+O2
2CH3COOH
催化剂
△
乙醛可以被还原为乙醇,
能否被氧化?
小结:
氧化
乙醛
还原
乙酸
氧化
乙醇
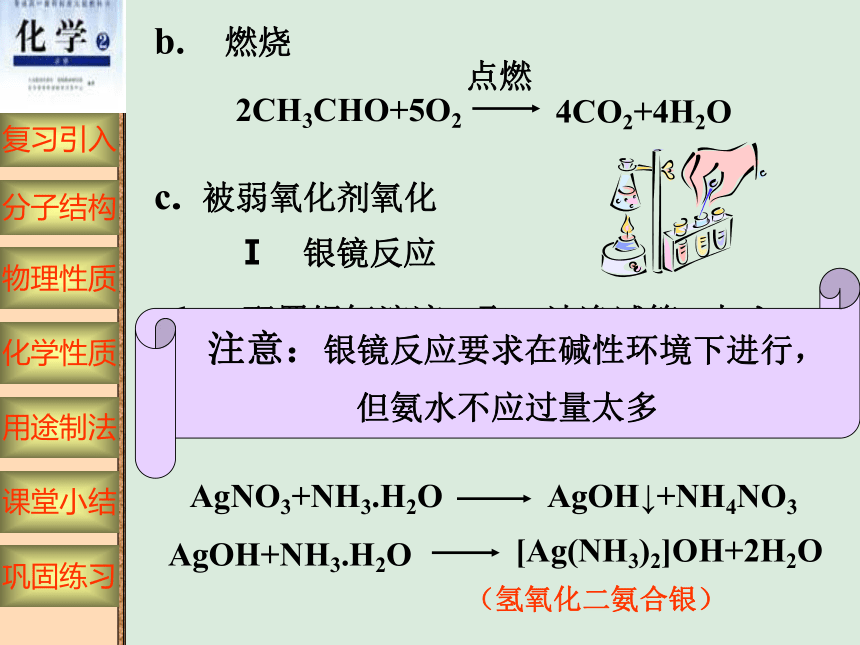
b. 燃烧
2CH3CHO+5O2
4CO2+4H2O
点燃
c. 被弱氧化剂氧化
Ⅰ 银镜反应
AgNO3+NH3.H2O
AgOH↓+NH4NO3
AgOH+NH3.H2O
[Ag(NH3)2]OH+2H2O
1、 配置银氨溶液:取一洁净试管,加入2ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。
注意:银镜反应要求在碱性环境下进行,
但氨水不应过量太多
(氢氧化二氨合银)
CH3CHO+2 Ag(NH3)2OH
水浴
CH3COONH4 +2Ag +3NH3+H2O
氧化剂
还原剂
2、水浴加热形成银镜:在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。
注意:水浴加热时不可振荡和摇动试管
(1)碱性环境下,乙醛被氧化成乙酸后又与 NH3反应生成乙酸铵
(2) 1mol–CHO被氧化,就应有2molAg被还原
(3)必须水浴,不能用酒精灯直接加热;
(4)试管内壁必须洁净(可用洗涤剂和酸以此刷洗);
(5)加热时不可振荡和摇动试管;
(6)须用新配制的银氨溶液,且氨水不能过量(只能加到Ag2O沉淀刚好消失)。
(7)可用稀HNO3清洗试管内壁的银镜
银镜反应有什么应用,
有什么工业价值?
应用: 检验醛基的存在,
测定醛基的数目
工业上用来制瓶胆和镜子
Ⅱ 与新制的氢氧化铜反应
现象:有红色(Cu2O)沉淀生成
(1)配制新制的Cu(OH)2悬浊液:
在试管里加入10%NaOH溶液2mL,滴入2%CuSO4溶液4-6滴,得到新制氢氧化铜。
Cu2++2OH-= Cu(OH)2
(2)乙醛的氧化:
在上述蓝色浊液中加入0.5ml乙醛溶液,加热至沸腾。
CH3CHO + 2Cu(OH)2 +NaOH CH3COONa
+ +3H2O
Cu2O↓
砖红色
注意:氢氧化铜溶液一定要新制
碱NaOH一定要过量
检验醛基的存在
应用:
医学上检验病人是否患糖尿病
能
乙醛能否使溴水或酸性KMnO4溶液褪色?
d. 被酸性KMnO4溶液、酸性K2Cr2O7溶液溴水等强氧化剂氧化
CH3CHO+Br2+H2O → CH3COOH+ 2HBr
5CH3CHO+2KMnO4+3H2SO4 →
5CH3COOH+2MnSO4+K2SO4+3H2O
乙醛有还原性
醛基中碳氧双键能与H2发生加成反应
醛基中碳氢键较活泼,能被氧化成羧基
加成反应
氧化反应
乙 醛
小结:乙醛的化学性质
注意:和C=C双键不同的是,通常情况下, 醛基中的C=O不能和HX、X2、H2O发生加成反应
乙醛
还原(加H)
乙醇
氧化(失H)
氧化(加O)
乙酸
四 乙醛的工业制法
A、乙炔水化法
B、乙烯氧化法
CH CH + H2O CH3-C-H
汞盐
O
2CH2 CH2 + O2 2CH3-C-H
钯盐
O
加压、加热
最简单的醛—甲醛
C
O
H
H
结构式:
分子式:
CH2O
结构简式:
HCHO
【结构特点】甲醛中:醛基, 有2个活泼氢可被氧化
分子结构: C原子以sp2杂化轨道成键。分子为平面形极性分子。
2、甲醛的物理性质
甲醛又叫蚁醛,无色、有刺激性气味的气体,易溶于水和乙醇。35~40%的甲醛水溶液叫做福尔马林。可用于杀菌、消毒。用途非常广泛,是一种主要的有机合成原料,能合成多种有机化合物。
2、甲醛的化学性质
(1)与氢气的加成反应
+H2 CH3OH
△
催化剂
H—C—H
O
(2)氧化反应
HCHO+O2 → CO2+H2O
点燃
2HCHO+O2 → 2HCOOH
催化剂
或:HCHO+O2 →
H—O—C—O— H
O
催化剂
HCHO+ 4 [Ag(NH3)2]OH
4Ag ↓+CO2↑+8NH3+3H2O
加热
写出甲醛发生银镜反应,以及与新制的
氢氧化铜反应的化学方程式
C
O
H
H
HCHO+4Cu(OH)2
2Cu2O↓+CO2↑+5H2O
加热
1mol甲醛最多可以还原得到多少molAg
甲醛与酸性高锰酸钾溶液反应
现象:是酸性高锰酸钾溶液退色。
HCHO HCOOH
KMnO4
加聚反应:
nHCHO → -[-CH2—O-]n
说明:聚甲醛-[-CH2—O-]n--是人造象牙的主要成分。
3、甲醛的用途
(1)甲醛的水溶液是一种良好的杀菌剂。
(2)重要的有机原料,应用于塑料工业(如制酚醛树脂、脲醛塑料—电玉) 、合成纤维工业(如合成维尼纶—聚乙烯醇缩甲醛、氨基树酯) 、皮革工业、医药、染料等。
(3)合成医药上的利尿剂-乌洛托品。
甲醛分子中有醛基发生缩聚反应,得到酚醛树脂(电木)。
(4)在农业上常用质量分数为0.1%~0.5%的甲醛溶液来浸种,给种子消毒。此外,甲醛还是用于制氯霉素、香料、染料的原料。
醛类
C
O
H
H
H
C
C
O
H
H
H
H
C
C
O
H
H
H
C
H
H
甲醛
丙醛
乙醛
C
O
H
R
醛
讨论: 醛的定义
1、醛的定义:
从结构上看,由烃基(或氢原子)跟醛基(-CHO)相连而成的化合物叫醛。
2、醛的分类
3、饱和一元醛的通式:
CnH2n+1CHO 或 CnH2nO
R-CHO
4、醛的同分异构现象
除本身的碳架异构外,醛与酮、烯醇、环醇互为同分异构体
(1)试写出C3H6O的同分异构体
(2)试写出 C5H10O属于醛的同分 异构体
5、化学性质
(1) 和H2加成被还原成醇
(2)氧化反应
a.燃烧
b.催化氧化成羧酸
c.被弱氧化剂氧化
Ⅰ 银镜反应
Ⅱ 与新制的氢氧化铜反应
d.使酸性KMnO4溶液和溴水褪色
醛类应该具备哪些重要的化学性质?
5.醛基的检验
1、怎样检验醛基的存在?
2、哪些有机物中含有—CHO?
醛、HCOOH(甲酸)、HCOOR(甲酸某酯)、葡萄糖、麦芽糖
新制的Cu(OH)2
银镜反应
1.丙酮的分子式C3H6O,结构简式CH3COCH3。酮的通式R1COR2。
酮是羰基直接与两个烃基相连,没有与羰基直接相连的氢原子,所以不能发生氧化反应。
2.丙酮易挥发、易燃烧,可跟水、乙酸及乙醚等以任意比互溶,能溶解多种有机物,是一种重要的有机溶剂。
3.丙酮的化学性质:
CH3COCH3+H2→CH3CHCH3
科学视野
丙酮
1、用化学方法鉴别下列各组物质
(1)溴乙烷 、乙醇 、乙醛
(2)苯、甲苯、乙醇、1-己烯、甲醛、苯酚
反馈练习
2、一定量的某饱和一元醛发生银镜反应,析出银21.6g,等量的此醛完全燃烧时生成CO2 0.89L,则此醛是( )
A、乙醛 B、丙醛
C、丁醛 D、2-甲基丙醛
CD
反馈练习
3、某学生做乙醛的还原实验,取1mol/L的CuSO4溶液2mL和0.4mol/L的NaOH溶液5mL,在一个试管中混合加入40%的乙醛溶液加热至沸腾,无红色沉淀,实验失败的原因是( )
A、乙醛溶液太少 B、氢氧化钠不够用
C、硫酸铜不够用 D、加热时间不够.
4、甲醛、乙醛、丙醛组成的混合物里,氢元素的质量分数是9%,则氧元素的质量分数是( )
A、16% B、37% C、48% D、无法计算
B
例:
B
5、已知柠檬醛的结构简式为:
若要检验出其中的碳碳双键,其方法是什么?
CH3 O
CH3C=CHCH2CH2CH=CHCH
1、足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化;
2、再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳双键能使酸性KMnO4溶液(或溴水)褪色。
6.某有机物的结构简式为CH2=CH-CHO,下列对其化学性质的判断中,不正确的是( )
A.能被银氨溶液氧化
B.能使酸性高锰酸钾溶液褪色
C.1mol该有机物只能与1molBr2发生加成反应
D.1mol该有机物只能与1molH2发生加成反应
D
7. 某有机物加氢反应的还原产物是:CH3CHCH2OH,原有机物是( )
CH3
A.乙醇的同系物 B.丙醇的同分异构体
C.丙醛的同分异构体 D.乙醛的同系物
|
D
9.有乙醛蒸气与乙炔的混合气体aL,当其完全燃烧时, 消耗相同状况下氧气的体积为( )
A.2aL B.2.5aL C.3aL D.条件不足无法计算
10.某有机物的化学式为C5H8O,它能发生银镜反应和加成反应。若将其跟H2加成,所得产物的结构简式可能是 ( )
A.(CH3CH2)2CHOH
B.(CH3)3CCH2OH
C. CH3CH2CH(CH2OH)2
D.CH3(CH2)3CH2OH
RC=O +H-CH2CHO
H
OH
→ R-CH-CH2-CHO
根据上述信息,用乙炔合成1-丁醇。
CH≡CH→CH3CHO→CH3CHCH2CHO
OH
→CH3CH=CHCHO→CH3CH2CH2CH2OH
8.迁移应用
化学选修⑤第三章 烃的含氧衍生物
第二节 醛
根据醇类催化氧化反应的原理,
完成下列方程式
醇类发生催化氧化的条件是什么?
1.Ag或Cu作催化剂并加热。
2.羟基所连的碳原子上有氢原子。
2CH3CH2OH+O2
△
Cu
2CH3CHO+2H2O
2CH3CHCH3+O2
OH
△
Cu
2CH3CCH3+2H2O
O
一、乙醛的分子结构
分子式
结构简式 CH3CHO
结构式
H
H
H
H
C
C
O
官能团
醛基:
CHO
或
C
H
O
醛基的写法,不要写成
COH
C2H4O
友情提示
二、乙醛的物理性质
常温下为无色有刺激性气味的液体,
密度比水小,
沸点:20.8℃,
易挥发,易燃烧,
能与水、乙醇、乙醚、氯仿等互溶。
思考:分析醛基的结构,推测其
在化学反应中的断裂方式
C
H
O
碳氧键
碳氢键
醛基中碳氧双键发生加成反应,被H2还原为醇
醛基中碳氢键较活泼,能被氧化成相应羧酸
1、加成反应
Ni
CH3CHO+H2
CH3CH2OH
根据加成反应的概念写出CH3CHO
和H2 加成反应的方程式。
这个反应属于氧化反应还是还原反应?
还原反应
三、乙醛的化学性质
通常C=O双键加成:H2、HCN
C=C双键加成:H2、X2、HX、H2O
有机反应中的氧化反应和还原反应
我们应该怎样判断呢
2CH3CH2OH+O2
△
Cu
2CH3CHO+2H2O
氧化反应: 有机物分子中加入 氧原子或
失去氢原子的反应
还原反应: 有机物分子中加入氢原子或
失去氧原子的反应
Ni
CH3CHO+H2
CH3CH2OH
回子菜单
2、氧化反应
a. 催化氧化
2CH3CHO+O2
2CH3COOH
催化剂
△
乙醛可以被还原为乙醇,
能否被氧化?
小结:
氧化
乙醛
还原
乙酸
氧化
乙醇
b. 燃烧
2CH3CHO+5O2
4CO2+4H2O
点燃
c. 被弱氧化剂氧化
Ⅰ 银镜反应
AgNO3+NH3.H2O
AgOH↓+NH4NO3
AgOH+NH3.H2O
[Ag(NH3)2]OH+2H2O
1、 配置银氨溶液:取一洁净试管,加入2ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。
注意:银镜反应要求在碱性环境下进行,
但氨水不应过量太多
(氢氧化二氨合银)
CH3CHO+2 Ag(NH3)2OH
水浴
CH3COONH4 +2Ag +3NH3+H2O
氧化剂
还原剂
2、水浴加热形成银镜:在配好的上述银氨溶液中滴入三滴乙醛溶液,然后把试管放在热水浴中静置。
注意:水浴加热时不可振荡和摇动试管
(1)碱性环境下,乙醛被氧化成乙酸后又与 NH3反应生成乙酸铵
(2) 1mol–CHO被氧化,就应有2molAg被还原
(3)必须水浴,不能用酒精灯直接加热;
(4)试管内壁必须洁净(可用洗涤剂和酸以此刷洗);
(5)加热时不可振荡和摇动试管;
(6)须用新配制的银氨溶液,且氨水不能过量(只能加到Ag2O沉淀刚好消失)。
(7)可用稀HNO3清洗试管内壁的银镜
银镜反应有什么应用,
有什么工业价值?
应用: 检验醛基的存在,
测定醛基的数目
工业上用来制瓶胆和镜子
Ⅱ 与新制的氢氧化铜反应
现象:有红色(Cu2O)沉淀生成
(1)配制新制的Cu(OH)2悬浊液:
在试管里加入10%NaOH溶液2mL,滴入2%CuSO4溶液4-6滴,得到新制氢氧化铜。
Cu2++2OH-= Cu(OH)2
(2)乙醛的氧化:
在上述蓝色浊液中加入0.5ml乙醛溶液,加热至沸腾。
CH3CHO + 2Cu(OH)2 +NaOH CH3COONa
+ +3H2O
Cu2O↓
砖红色
注意:氢氧化铜溶液一定要新制
碱NaOH一定要过量
检验醛基的存在
应用:
医学上检验病人是否患糖尿病
能
乙醛能否使溴水或酸性KMnO4溶液褪色?
d. 被酸性KMnO4溶液、酸性K2Cr2O7溶液溴水等强氧化剂氧化
CH3CHO+Br2+H2O → CH3COOH+ 2HBr
5CH3CHO+2KMnO4+3H2SO4 →
5CH3COOH+2MnSO4+K2SO4+3H2O
乙醛有还原性
醛基中碳氧双键能与H2发生加成反应
醛基中碳氢键较活泼,能被氧化成羧基
加成反应
氧化反应
乙 醛
小结:乙醛的化学性质
注意:和C=C双键不同的是,通常情况下, 醛基中的C=O不能和HX、X2、H2O发生加成反应
乙醛
还原(加H)
乙醇
氧化(失H)
氧化(加O)
乙酸
四 乙醛的工业制法
A、乙炔水化法
B、乙烯氧化法
CH CH + H2O CH3-C-H
汞盐
O
2CH2 CH2 + O2 2CH3-C-H
钯盐
O
加压、加热
最简单的醛—甲醛
C
O
H
H
结构式:
分子式:
CH2O
结构简式:
HCHO
【结构特点】甲醛中:醛基, 有2个活泼氢可被氧化
分子结构: C原子以sp2杂化轨道成键。分子为平面形极性分子。
2、甲醛的物理性质
甲醛又叫蚁醛,无色、有刺激性气味的气体,易溶于水和乙醇。35~40%的甲醛水溶液叫做福尔马林。可用于杀菌、消毒。用途非常广泛,是一种主要的有机合成原料,能合成多种有机化合物。
2、甲醛的化学性质
(1)与氢气的加成反应
+H2 CH3OH
△
催化剂
H—C—H
O
(2)氧化反应
HCHO+O2 → CO2+H2O
点燃
2HCHO+O2 → 2HCOOH
催化剂
或:HCHO+O2 →
H—O—C—O— H
O
催化剂
HCHO+ 4 [Ag(NH3)2]OH
4Ag ↓+CO2↑+8NH3+3H2O
加热
写出甲醛发生银镜反应,以及与新制的
氢氧化铜反应的化学方程式
C
O
H
H
HCHO+4Cu(OH)2
2Cu2O↓+CO2↑+5H2O
加热
1mol甲醛最多可以还原得到多少molAg
甲醛与酸性高锰酸钾溶液反应
现象:是酸性高锰酸钾溶液退色。
HCHO HCOOH
KMnO4
加聚反应:
nHCHO → -[-CH2—O-]n
说明:聚甲醛-[-CH2—O-]n--是人造象牙的主要成分。
3、甲醛的用途
(1)甲醛的水溶液是一种良好的杀菌剂。
(2)重要的有机原料,应用于塑料工业(如制酚醛树脂、脲醛塑料—电玉) 、合成纤维工业(如合成维尼纶—聚乙烯醇缩甲醛、氨基树酯) 、皮革工业、医药、染料等。
(3)合成医药上的利尿剂-乌洛托品。
甲醛分子中有醛基发生缩聚反应,得到酚醛树脂(电木)。
(4)在农业上常用质量分数为0.1%~0.5%的甲醛溶液来浸种,给种子消毒。此外,甲醛还是用于制氯霉素、香料、染料的原料。
醛类
C
O
H
H
H
C
C
O
H
H
H
H
C
C
O
H
H
H
C
H
H
甲醛
丙醛
乙醛
C
O
H
R
醛
讨论: 醛的定义
1、醛的定义:
从结构上看,由烃基(或氢原子)跟醛基(-CHO)相连而成的化合物叫醛。
2、醛的分类
3、饱和一元醛的通式:
CnH2n+1CHO 或 CnH2nO
R-CHO
4、醛的同分异构现象
除本身的碳架异构外,醛与酮、烯醇、环醇互为同分异构体
(1)试写出C3H6O的同分异构体
(2)试写出 C5H10O属于醛的同分 异构体
5、化学性质
(1) 和H2加成被还原成醇
(2)氧化反应
a.燃烧
b.催化氧化成羧酸
c.被弱氧化剂氧化
Ⅰ 银镜反应
Ⅱ 与新制的氢氧化铜反应
d.使酸性KMnO4溶液和溴水褪色
醛类应该具备哪些重要的化学性质?
5.醛基的检验
1、怎样检验醛基的存在?
2、哪些有机物中含有—CHO?
醛、HCOOH(甲酸)、HCOOR(甲酸某酯)、葡萄糖、麦芽糖
新制的Cu(OH)2
银镜反应
1.丙酮的分子式C3H6O,结构简式CH3COCH3。酮的通式R1COR2。
酮是羰基直接与两个烃基相连,没有与羰基直接相连的氢原子,所以不能发生氧化反应。
2.丙酮易挥发、易燃烧,可跟水、乙酸及乙醚等以任意比互溶,能溶解多种有机物,是一种重要的有机溶剂。
3.丙酮的化学性质:
CH3COCH3+H2→CH3CHCH3
科学视野
丙酮
1、用化学方法鉴别下列各组物质
(1)溴乙烷 、乙醇 、乙醛
(2)苯、甲苯、乙醇、1-己烯、甲醛、苯酚
反馈练习
2、一定量的某饱和一元醛发生银镜反应,析出银21.6g,等量的此醛完全燃烧时生成CO2 0.89L,则此醛是( )
A、乙醛 B、丙醛
C、丁醛 D、2-甲基丙醛
CD
反馈练习
3、某学生做乙醛的还原实验,取1mol/L的CuSO4溶液2mL和0.4mol/L的NaOH溶液5mL,在一个试管中混合加入40%的乙醛溶液加热至沸腾,无红色沉淀,实验失败的原因是( )
A、乙醛溶液太少 B、氢氧化钠不够用
C、硫酸铜不够用 D、加热时间不够.
4、甲醛、乙醛、丙醛组成的混合物里,氢元素的质量分数是9%,则氧元素的质量分数是( )
A、16% B、37% C、48% D、无法计算
B
例:
B
5、已知柠檬醛的结构简式为:
若要检验出其中的碳碳双键,其方法是什么?
CH3 O
CH3C=CHCH2CH2CH=CHCH
1、足量的银氨溶液(或新制的Cu(OH)2)使醛基氧化;
2、再用酸性KMnO4溶液(或溴水)检验碳碳双键,碳碳双键能使酸性KMnO4溶液(或溴水)褪色。
6.某有机物的结构简式为CH2=CH-CHO,下列对其化学性质的判断中,不正确的是( )
A.能被银氨溶液氧化
B.能使酸性高锰酸钾溶液褪色
C.1mol该有机物只能与1molBr2发生加成反应
D.1mol该有机物只能与1molH2发生加成反应
D
7. 某有机物加氢反应的还原产物是:CH3CHCH2OH,原有机物是( )
CH3
A.乙醇的同系物 B.丙醇的同分异构体
C.丙醛的同分异构体 D.乙醛的同系物
|
D
9.有乙醛蒸气与乙炔的混合气体aL,当其完全燃烧时, 消耗相同状况下氧气的体积为( )
A.2aL B.2.5aL C.3aL D.条件不足无法计算
10.某有机物的化学式为C5H8O,它能发生银镜反应和加成反应。若将其跟H2加成,所得产物的结构简式可能是 ( )
A.(CH3CH2)2CHOH
B.(CH3)3CCH2OH
C. CH3CH2CH(CH2OH)2
D.CH3(CH2)3CH2OH
RC=O +H-CH2CHO
H
OH
→ R-CH-CH2-CHO
根据上述信息,用乙炔合成1-丁醇。
CH≡CH→CH3CHO→CH3CHCH2CHO
OH
→CH3CH=CHCHO→CH3CH2CH2CH2OH
8.迁移应用
