第三节 生物中两种常见的有机物(乙醇)课件
文档属性
| 名称 | 第三节 生物中两种常见的有机物(乙醇)课件 |

|
|
| 格式 | zip | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-04-16 00:00:00 | ||
图片预览










文档简介
(共36张PPT)
借问_____何 处有,
牧童遥指杏花村。
酒家
明月几时有,把____问青天
酒
第三节 饮食中的有机化合物
让我
看一看?
想一想?
气 味 :
无色透明
特殊香味
液体
比水小
跟水以任意比互溶
能够溶解多种无机物和有机物
易挥发
一、乙醇的物理性质
颜 色 :
溶解性:
密 度:
挥发性:
状 态:
思考
乙醇能否作为从溴水中萃取溴的萃取剂?
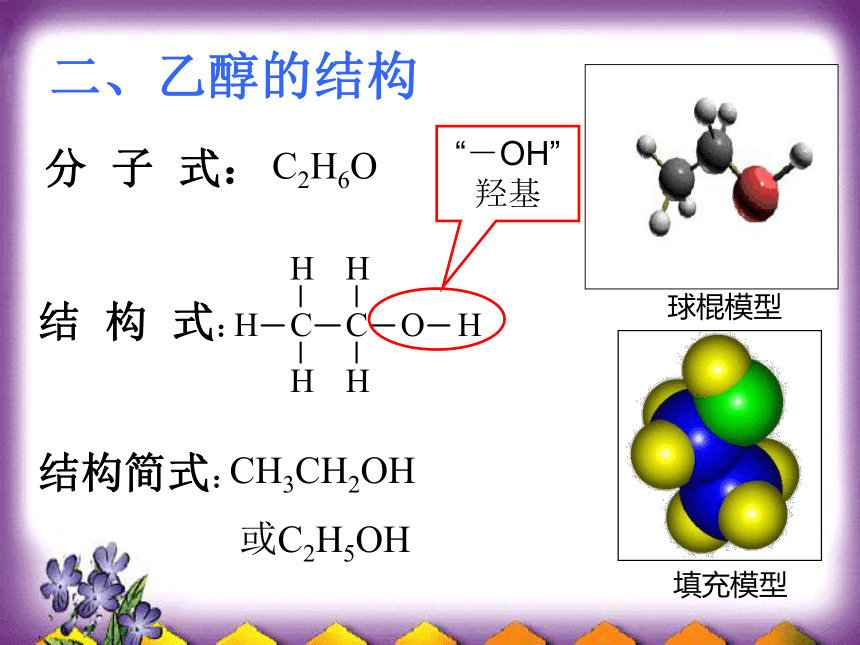
二、乙醇的结构
分 子 式:
结 构 式:
结构简式:
球棍模型
填充模型
CH3CH2OH
或C2H5OH
C2H6O
“-OH”
羟基
三、乙醇的化学性质
实验内容(一) 现 象
向一干燥的试管中加入 约3mL无水乙醇,取一小块(绿豆般大小)金属钠,用滤纸吸干表面的煤油后投入乙醇中,观察并记录实验现象。
钠沉于底部(既而上浮),有无色气泡在钠粒表面生成后逸出液面,最终钠粒消失,液体仍为无色透明
[问题探源]
(1)钠在乙醇中产生的气体是什么气体?
乙醇分子中存在-OH,O-H键容易断裂。在钠的作用下,-OH中的氢被置换出来形成H2。
(2)如果是氢气,那么氢元素是来自哪里?
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
[活学活用]其它活泼金属如钾、钙等也可与乙醇反应,均可产生H2 .
三、乙醇的化学性质
1、乙醇与钠的反应
乙醇与钠反应时的断键位置?
—取代反应
(乙醇钠)
启迪思考:比较乙醇和水分别与钠反应强弱?
现象
浮在水面
熔成小球
四处游动
发出嘶嘶的响声
钠+水
现象
开始时沉在乙醇底部
不熔成小球
四处游动
发出嘶嘶的响声
钠+乙醇
钠与水的
反应剧烈
H—OH C2H5—OH
由于羟基所连的原子或原子团不一样,从而导致羟基氢的活泼性不一样.如: H—OH > C2H5—OH
2CO2 +3H2O
C2H5OH + 3 O2
点燃
现象:产生淡蓝色火焰,同时放出大量热。
三、乙醇的化学性质
2、乙醇的氧化反应(1)— 乙醇燃烧
[知识拓展]
乙醇燃烧产物清洁,无污染,所以乙醇除了用于食品加工业以外另一重要用途就是作燃料使用。
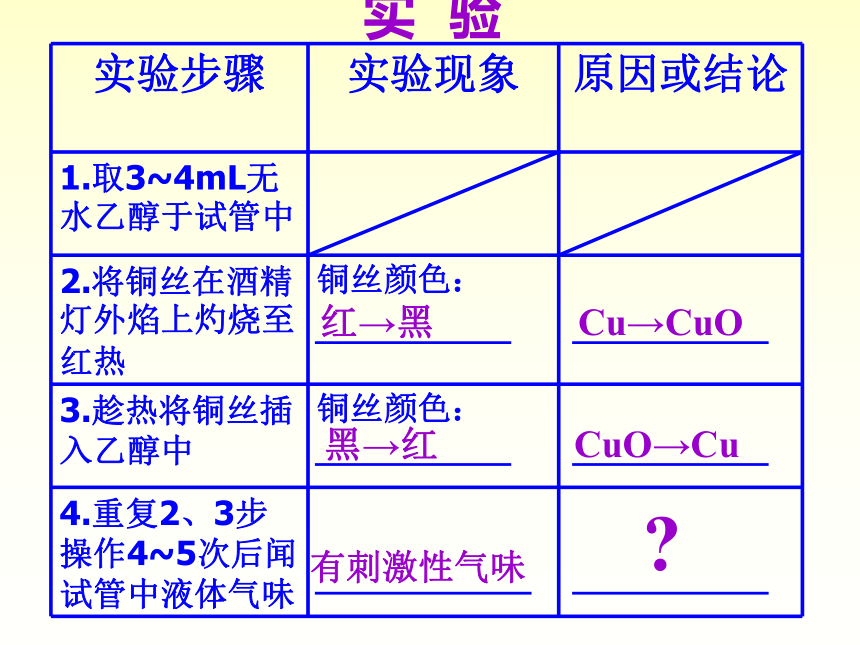
实验步骤 实验现象 原因或结论
1.取3~4mL无水乙醇于试管中
2.将铜丝在酒精灯外焰上灼烧至红热 铜丝颜色:
3.趁热将铜丝插入乙醇中 铜丝颜色:
4.重复2、3步操作4~5次后闻试管中液体气味
实 验
红→黑
黑→红
有刺激性气味
Cu→CuO
CuO→Cu
Cu
2CH3CH2OH+O2 2CH3CHO+2H2O
乙醛
乙醛
2Cu+O2 2CuO
催化剂
乙 醛
b.乙醇的催化氧化
问题思考
1.铜在整个过程中起什么作用?
2.乙醇分子中有哪些化学键断裂?又生成了
哪些化学键?
CuO+ CH3CH2OH Cu+ CH3CHO+ H2O
2
2
2
2
2
2
2
所以,我们可以根据物质的化学性质,按照实际需要,控制反应条件,使化学反应朝着我们所需要的方向进行。
学以致用
四、乙醇的用途
乙 醇
饮 料
化工原料
溶 剂
医 药
燃料
1
2
3
4
5
作燃料 —— 飞机、汽车、火锅、酒精灯等
酒精燃料飞机
酒精火锅
作消毒剂 —— 医用酒精等
消毒剂(75%的乙醇溶液)
工业制取乙酸
制酒精型饮料 —— 啤酒、红酒等
溶剂
饮料
“李白斗酒诗百篇”
世界卫生组织的事故调查显示,大约50%-60%的交通事故与酒后驾驶有关。
交警判断驾驶员是否酒后驾车的方法
CrO3(H+)
Cr2(SO4)3
(橙红色)
(绿色)
去年1月2日到2月3日,东莞市塘厦镇半个月内连续发生4起买假酒导致甲醇(CH3OH)中毒事件,其中3人死亡。卫生防疫部门对中毒者饮用的散装酒进行检验后发现,其中甲醇超标400多倍。随后,有关部门迅速出击,在塘厦镇查获了10多吨散装酒,其中有50多公斤是甲醇超标的,并当众销毁。
散装白酒连夺3命
与水互溶飘清香;
电离水比乙醇强;
钠粒投入放氢气;
氧化成醛铜帮忙。
乙醇性质小结
1.下列有关乙醇的物理性质的应用中不正确的是( )
A. 由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B. 由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的有效成分
C. 由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒
D. 由于乙醇容易挥发,所以才有俗语“酒好不怕巷子深”的说法
3、乙醇分子中不同的化学键如下图:
当乙醇与钠反应时, 键
断裂;当乙醇与氧气反应
(Cu作催化剂)时, 键断裂。
2、1998年山西朔州发生假酒案,假酒中严重超标的有毒成分主要是 ( )
(A)CH3CH2OH (B)CH3OH (C)CH3CHO (D)CH3COOH
B
④ ② ①
③
①
①③
4、把质量为m g的铜丝灼烧变黑,立即趁热放入下列物质中,能使铜丝变红,而且质量仍为m g的是( )
A:稀硫酸
B:酒 精
C:稀硝酸
D:CO
BD
4、能用来检验酒精中是否含有水的试剂是( )
A:CuSO4·5H2O
B:无水硫酸铜
C:浓硫酸
D:金属钠
B
2CrO3(红色)+3C2H5OH+3H2SO4 Cr2(SO4)3(绿色)+3CH3CHO+6H2O被检测的气体的成分是________,上述反应中的氧化剂是______,还原剂是______,转化的电子数是 。
司机是否酒后驾车,可通过对其呼出的气体进行检验而查出,所利用的化学反应如下:
思考
1、取一根光洁的铜丝绕成螺旋状,放在酒精灯
外焰上加热,然后慢慢移向内焰,迅速取出。可能
观察到什么现象?如何解释?写出相关方程式。这
对你了解如何使用酒精灯有什么启示?
2、已知有实验事实:2mol乙醇与足量钠反应生成1mol氢气,从量的角度能否分析产物中的氢原子来自羟基还是乙基?从而得出在此反应中乙醇断裂什么键?
一、乙醇的物理性质:
二、乙醇的结构:
三、乙醇的化学性质:
1、乙醇与活泼金属反应(取代反应)
2C2H5OH+2Na→2C2H5ONa+H2↑
2、乙醇的氧化反应
①燃 烧:
②催化氧化:
四、乙醇的用途:
小结
H—C—C—O—H
︱
︱
︱
︱
H
H
H
H
2CH3CH2OH+O2 2CH3CHO+2H2O
乙醛
Cu
2CO2 +3H2O
C2H5OH + 3 O2
点燃
“酒是陈的香”
3、乙醇的消去反应— 分子内脱水
三、乙醇的化学性质(三)
浓H2SO4
1700C
H C C H CH2=CH2 +H2O
H
H
H
OH
制取乙烯
相邻两个碳上羟基和氢脱去结合成水
教学目标:
1、了解乙醇的物理性质;
2、了解乙醇的结构;
3、掌握乙醇的化学性质和用途。
借问_____何 处有,
牧童遥指杏花村。
酒家
明月几时有,把____问青天
酒
第三节 饮食中的有机化合物
让我
看一看?
想一想?
气 味 :
无色透明
特殊香味
液体
比水小
跟水以任意比互溶
能够溶解多种无机物和有机物
易挥发
一、乙醇的物理性质
颜 色 :
溶解性:
密 度:
挥发性:
状 态:
思考
乙醇能否作为从溴水中萃取溴的萃取剂?
二、乙醇的结构
分 子 式:
结 构 式:
结构简式:
球棍模型
填充模型
CH3CH2OH
或C2H5OH
C2H6O
“-OH”
羟基
三、乙醇的化学性质
实验内容(一) 现 象
向一干燥的试管中加入 约3mL无水乙醇,取一小块(绿豆般大小)金属钠,用滤纸吸干表面的煤油后投入乙醇中,观察并记录实验现象。
钠沉于底部(既而上浮),有无色气泡在钠粒表面生成后逸出液面,最终钠粒消失,液体仍为无色透明
[问题探源]
(1)钠在乙醇中产生的气体是什么气体?
乙醇分子中存在-OH,O-H键容易断裂。在钠的作用下,-OH中的氢被置换出来形成H2。
(2)如果是氢气,那么氢元素是来自哪里?
2CH3CH2OH+2Na→2CH3CH2ONa+H2↑
[活学活用]其它活泼金属如钾、钙等也可与乙醇反应,均可产生H2 .
三、乙醇的化学性质
1、乙醇与钠的反应
乙醇与钠反应时的断键位置?
—取代反应
(乙醇钠)
启迪思考:比较乙醇和水分别与钠反应强弱?
现象
浮在水面
熔成小球
四处游动
发出嘶嘶的响声
钠+水
现象
开始时沉在乙醇底部
不熔成小球
四处游动
发出嘶嘶的响声
钠+乙醇
钠与水的
反应剧烈
H—OH C2H5—OH
由于羟基所连的原子或原子团不一样,从而导致羟基氢的活泼性不一样.如: H—OH > C2H5—OH
2CO2 +3H2O
C2H5OH + 3 O2
点燃
现象:产生淡蓝色火焰,同时放出大量热。
三、乙醇的化学性质
2、乙醇的氧化反应(1)— 乙醇燃烧
[知识拓展]
乙醇燃烧产物清洁,无污染,所以乙醇除了用于食品加工业以外另一重要用途就是作燃料使用。
实验步骤 实验现象 原因或结论
1.取3~4mL无水乙醇于试管中
2.将铜丝在酒精灯外焰上灼烧至红热 铜丝颜色:
3.趁热将铜丝插入乙醇中 铜丝颜色:
4.重复2、3步操作4~5次后闻试管中液体气味
实 验
红→黑
黑→红
有刺激性气味
Cu→CuO
CuO→Cu
Cu
2CH3CH2OH+O2 2CH3CHO+2H2O
乙醛
乙醛
2Cu+O2 2CuO
催化剂
乙 醛
b.乙醇的催化氧化
问题思考
1.铜在整个过程中起什么作用?
2.乙醇分子中有哪些化学键断裂?又生成了
哪些化学键?
CuO+ CH3CH2OH Cu+ CH3CHO+ H2O
2
2
2
2
2
2
2
所以,我们可以根据物质的化学性质,按照实际需要,控制反应条件,使化学反应朝着我们所需要的方向进行。
学以致用
四、乙醇的用途
乙 醇
饮 料
化工原料
溶 剂
医 药
燃料
1
2
3
4
5
作燃料 —— 飞机、汽车、火锅、酒精灯等
酒精燃料飞机
酒精火锅
作消毒剂 —— 医用酒精等
消毒剂(75%的乙醇溶液)
工业制取乙酸
制酒精型饮料 —— 啤酒、红酒等
溶剂
饮料
“李白斗酒诗百篇”
世界卫生组织的事故调查显示,大约50%-60%的交通事故与酒后驾驶有关。
交警判断驾驶员是否酒后驾车的方法
CrO3(H+)
Cr2(SO4)3
(橙红色)
(绿色)
去年1月2日到2月3日,东莞市塘厦镇半个月内连续发生4起买假酒导致甲醇(CH3OH)中毒事件,其中3人死亡。卫生防疫部门对中毒者饮用的散装酒进行检验后发现,其中甲醇超标400多倍。随后,有关部门迅速出击,在塘厦镇查获了10多吨散装酒,其中有50多公斤是甲醇超标的,并当众销毁。
散装白酒连夺3命
与水互溶飘清香;
电离水比乙醇强;
钠粒投入放氢气;
氧化成醛铜帮忙。
乙醇性质小结
1.下列有关乙醇的物理性质的应用中不正确的是( )
A. 由于乙醇的密度比水小,所以乙醇中的水可以通过分液的方法除去
B. 由于乙醇能够溶解很多有机物和无机物,所以可用乙醇提取中草药的有效成分
C. 由于乙醇能够以任意比溶解于水,所以酒厂可以勾兑各种浓度的酒
D. 由于乙醇容易挥发,所以才有俗语“酒好不怕巷子深”的说法
3、乙醇分子中不同的化学键如下图:
当乙醇与钠反应时, 键
断裂;当乙醇与氧气反应
(Cu作催化剂)时, 键断裂。
2、1998年山西朔州发生假酒案,假酒中严重超标的有毒成分主要是 ( )
(A)CH3CH2OH (B)CH3OH (C)CH3CHO (D)CH3COOH
B
④ ② ①
③
①
①③
4、把质量为m g的铜丝灼烧变黑,立即趁热放入下列物质中,能使铜丝变红,而且质量仍为m g的是( )
A:稀硫酸
B:酒 精
C:稀硝酸
D:CO
BD
4、能用来检验酒精中是否含有水的试剂是( )
A:CuSO4·5H2O
B:无水硫酸铜
C:浓硫酸
D:金属钠
B
2CrO3(红色)+3C2H5OH+3H2SO4 Cr2(SO4)3(绿色)+3CH3CHO+6H2O被检测的气体的成分是________,上述反应中的氧化剂是______,还原剂是______,转化的电子数是 。
司机是否酒后驾车,可通过对其呼出的气体进行检验而查出,所利用的化学反应如下:
思考
1、取一根光洁的铜丝绕成螺旋状,放在酒精灯
外焰上加热,然后慢慢移向内焰,迅速取出。可能
观察到什么现象?如何解释?写出相关方程式。这
对你了解如何使用酒精灯有什么启示?
2、已知有实验事实:2mol乙醇与足量钠反应生成1mol氢气,从量的角度能否分析产物中的氢原子来自羟基还是乙基?从而得出在此反应中乙醇断裂什么键?
一、乙醇的物理性质:
二、乙醇的结构:
三、乙醇的化学性质:
1、乙醇与活泼金属反应(取代反应)
2C2H5OH+2Na→2C2H5ONa+H2↑
2、乙醇的氧化反应
①燃 烧:
②催化氧化:
四、乙醇的用途:
小结
H—C—C—O—H
︱
︱
︱
︱
H
H
H
H
2CH3CH2OH+O2 2CH3CHO+2H2O
乙醛
Cu
2CO2 +3H2O
C2H5OH + 3 O2
点燃
“酒是陈的香”
3、乙醇的消去反应— 分子内脱水
三、乙醇的化学性质(三)
浓H2SO4
1700C
H C C H CH2=CH2 +H2O
H
H
H
OH
制取乙烯
相邻两个碳上羟基和氢脱去结合成水
教学目标:
1、了解乙醇的物理性质;
2、了解乙醇的结构;
3、掌握乙醇的化学性质和用途。
