2021年 暑假新初三科学 第5讲 常见的碱(知识讲解+针对练习)(无答案)
文档属性
| 名称 | 2021年 暑假新初三科学 第5讲 常见的碱(知识讲解+针对练习)(无答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 182.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2021-06-30 00:00:00 | ||
图片预览


文档简介
暑假新初三
第5讲
常见的碱
【学习目标】
1.熟悉并掌握质量守恒的含义及应用范围。
2.掌握并熟悉化学方程式的书写规则
3.熟悉并掌握化学方程式的计算方法
一、氢氧化钠
1.氢氧化钠NaOH:俗称
、
。
(1)易潮解,易和空气中的
反应而变质,故应
保存。氢氧化钠固体具有吸水性,所以可以用做某些气体的干燥剂,如
、
。
(2)
于水,放出大量的热。
(3)氢氧化钠的化学性质
①腐蚀性:氢氧化钠能与蛋白质、油脂反应,对皮肤、纸张等有强
性,在使用氢氧化钠溶液时,要注意防止液体溅入眼睛或沾到皮肤上。
①与指示剂反应:
②与酸反应:
③与酸性氧化物反应
④与某些盐反应(CuSO4等):
二、氢氧化钙
1.氢氧化钙Ca(OH)2:俗称
(1)熟石灰能吸收空气中的二氧化碳变成硬的碳酸钙,所以工业用氢氧化钙切砖抹墙
(2)农业上用熟石灰降低土壤酸性,配制农药波尔多液
(3)熟石灰可以用来制造氢氧化钠和漂白粉
2、氢氧化钙的化学性质
①腐蚀性:氢氧化钠能与蛋白质、油脂反应,对皮肤、纸张等有强
性,在使用氢氧化钠溶液时,要注意防止液体溅入眼睛或沾到皮肤上。
①与指示剂反应:
②与酸反应
③与酸性氧化物反应
④与某些盐反应(CuCl2等、碳酸钠溶液):
三.
区分NaOH和Ca(OH)2两种溶液的方法:
方法一:分别通入CO2,变浑浊的是
溶液;
Ca(CH)2+CO2=====
方法二:分别加入Na2CO3溶液,产生白色沉淀的是
溶液。
Ca(OH)2+Na2CO3=====
四、碱的通性
1.碱能与某些非金属氧化物发生反应
2NaOH+CO2=====
+
Ca(OH)2+CO2=====
+
(CO2能使澄清石灰水变浑浊,以此检验CO2)
2NaOH+SO2=====
+
(工业上用碱溶液吸收SO2等有害气体)
由此可知,氢氧化钠和氢氧化钙都应该密封保存,例如存放不严密的NaOH的成分可能有三种(无变质/部分变质/全部变质):
2.碱能与氯化铁、氯化铜溶液等物质反应
3NaOH+FeCl3=====
+
(生成红褐色沉淀)
2NaOH+CuSO4=====
+
(生成蓝色沉淀)
Ca(OH)2+CuCl2=====
+
【随堂练习】
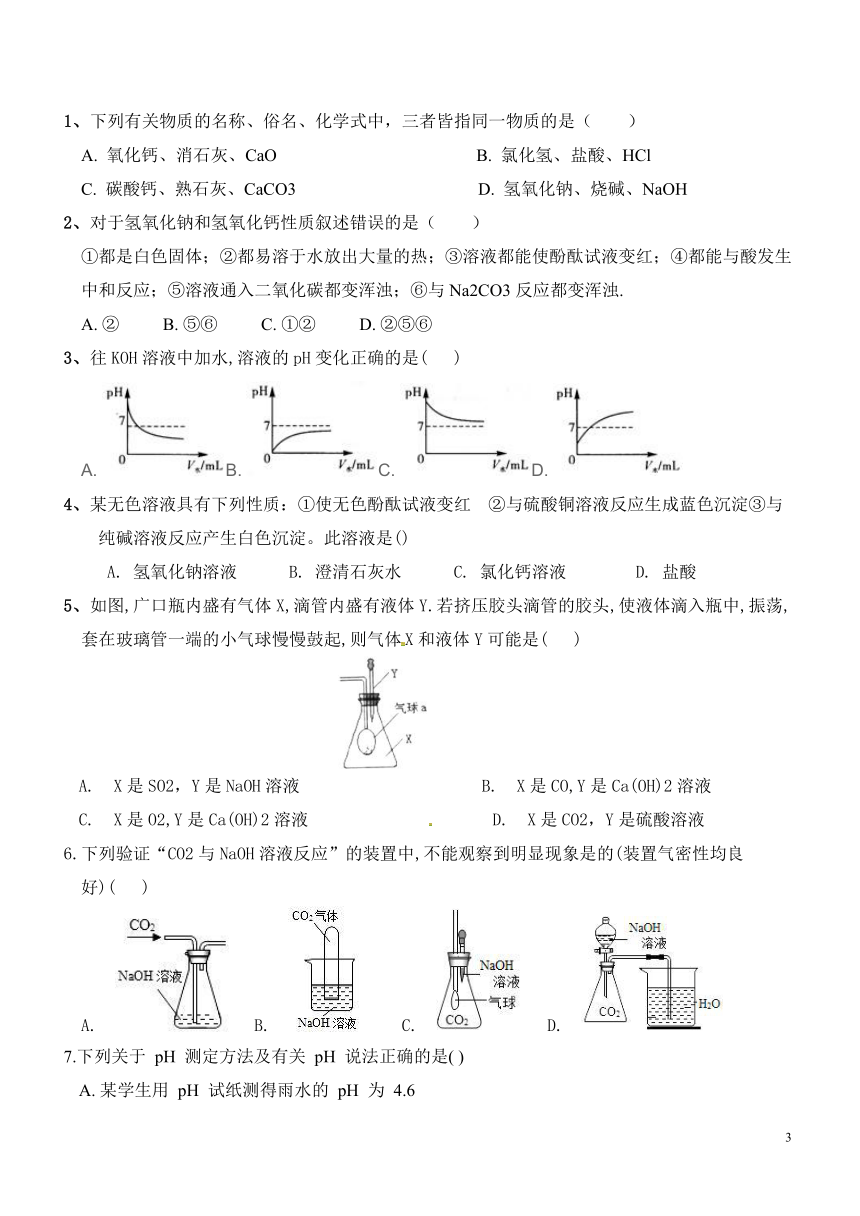
1、下列有关物质的名称、俗名、化学式中,三者皆指同一物质的是( )
A.
氧化钙、消石灰、CaO
B.
氯化氢、盐酸、HCl
C.
碳酸钙、熟石灰、CaCO3
D.
氢氧化钠、烧碱、NaOH
2、对于氢氧化钠和氢氧化钙性质叙述错误的是( )
①都是白色固体;②都易溶于水放出大量的热;③溶液都能使酚酞试液变红;④都能与酸发生中和反应;⑤溶液通入二氧化碳都变浑浊;⑥与Na2CO3反应都变浑浊.
A.
②
B.
⑤⑥
C.
①②
D.
②⑤⑥
3、往KOH溶液中加水,溶液的pH变化正确的是(
)
A.?B.?C.?D.?
4、某无色溶液具有下列性质:①使无色酚酞试液变红?②与硫酸铜溶液反应生成蓝色沉淀③与纯碱溶液反应产生白色沉淀。此溶液是()
A.
氢氧化钠溶液
B.
澄清石灰水
C.
氯化钙溶液
D.
盐酸
5、如图,广口瓶内盛有气体X,滴管内盛有液体Y.若挤压胶头滴管的胶头,使液体滴入瓶中,振荡,套在玻璃管一端的小气球慢慢鼓起,则气体X和液体Y可能是(
)
A.?X是SO2,Y是NaOH溶液
B.?X是CO,Y是Ca(OH)2溶液
C.?X是O2,Y是Ca(OH)2溶液
D.?X是CO2,Y是硫酸溶液
6.下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象是的(装置气密性均良好)(
)
A.?
B.?
C.?
D.?
7.下列关于
pH
测定方法及有关
pH
说法正确的是(
)
A.?某学生用
pH
试纸测得雨水的
pH
为
4.6
B.?当雨水的
pH
小于
5.6
时所降雨水才是酸雨,pH
越大,雨水酸性越强
C.?先将玻璃棒用水清洗干净,后蘸取待测试液滴在
pH
试纸上,测定溶液的
pH
D.?pH
的范围为
0-14
8.为了区别氢氧化钠溶液和澄清石灰水,下列实验方案能达到预期目的的是(?
??)
A.??????????B.??????????C.??????????D.?
9.?取一滤纸条,等间距滴入10滴紫色石蕊溶液,装入玻璃管中,然后从玻璃管的两端同时放入分别蘸有浓氨水和浓盐酸的棉球,并迅速封闭两端管口,很快可观察到管内有白烟产生,待白烟消失后还可观察到如图所示的现象.则下列说法中正确的是( )
A.?氨水和盐酸都属于易挥发性物质?????????????????????????B.?该过程中没有化学反应发生
C.?所有气体分子的运动速率都相同?????????????????????????D.?图示黑点表示石蕊溶液变成了红色
10.下列图像能正确表示对应变化关系的是(???
)
A.?图甲表示水通电分解产生的气体质量m与反应时间t的关系
B.?图乙表示两份完全相同的双氧水在有无Mn02的情况下,产生的02质量m与反应时间t的关系
C.?图丙表示往锌中加入足量的稀H2S04
,
产生的H2质量m与反应时间t的关系
D.?图丁表示往稀盐酸和CuCl2混合液中滴人NaOH溶液,产生的沉淀质量m2与NaOH溶液质量m1的关系
11.通过一个多星期的化学学习,我们认识了许多“奇妙的酸”和“神奇的碱”,请回答下列问题:
(1)如图表示的是一些物质在常温下的近似pH,回答下列问题:
①厨房清洁剂显________性,在少量厨房清洁剂中滴入几滴酚酞,溶液呈________色.
②酸雨的酸性比正常雨水的酸性________(填“强”或“弱”).
③测量苹果汁pH时,先用蒸馏水润湿pH试纸,会使pH偏________(“大”或“小”).
(2)焊接工业上常用稀盐酸清洗铁锈,写出用稀盐酸除铁锈的化学方程式为________,铁制品除锈时________(填“能”或“不能”)长时间浸在酸溶液中.
(3)氢氧化钠固体暴露在空气中容易吸收空气中的水分,表面潮湿并逐渐溶解,这种现象叫做________,该变化是________变化;同时,氢氧化钠固体还能与空气中的二氧化碳反应而变质,请写出变质的化学方程式__
______.
(4)“洁厕灵”用于除污垢,去异味,有效成分为盐酸,“管道通”用于疏通堵塞的管道,其有效成分为氢氧化钠,二者不能混合使用,其原因是_
_______(用化学方程式回答).
(5)胃酸的主要成分是盐酸,胃舒平(主要成分Al(OH)3)常用于治疗胃酸过多症,写出Al(OH)3治疗胃酸过多症时的化学反应方程式____
____.
(6)为除去铁钉上的锈迹,某学生将带锈迹的铁钉放入过量的稀硫酸中,他首先观察到:铁钉表面的锈迹逐渐溶解,溶液由无色逐渐变成________色,这是因为(用化学方程式表示)_____
___;过一会儿,他又观察到铁钉表面________,这是因为_
_______(用化学方程式表示).
(8)盛水的铝壶中常结有一层水垢(主要成分是碳酸钙、氢氧化镁等),可用适量的稀盐酸除去它,写出其中发生的中和反应的化学方程式____
____.
12.某实验小组的四位同学在探究碱的性质时发现氢氧化钠、氢氧化钙等可溶性碱都能使酚酞试液变红。他们想进一步探究:不溶性的氢氧化镁是否也能使酚酞试液变红。为此,他们将适量的氢氧化镁加入到盛有热水的烧杯中搅拌,然后向浑浊的液体中滴加酚酞试液,发现酚酞试液变红,可是过一会儿红色又消失了。四位同学依据所学的化学知识,分别对上述酚酞试液变红、红色又消失的原因作了如下猜想:
小明:可能是个偶然现象。
小东:可能是浑浊液体中的固体氢氧化镁使酚酞试液变红,氢氧化镁沉降后溶液就变无色了。
小花:可能是酚酞试液与空气中的氧气反应,使红色消失;也可能是氢氧化镁溶液与空气中的二氧化碳反应的缘故。
小红:可能是在热水中氢氧化镁的溶解度大,溶液中
OH-
离子较多,使酚酞试液变红;过一会儿温度降低,氢氧化镁的溶解度减小,溶液中
OH-离子变少,酚酞试液又变无色。
(1)对小明猜想“是个偶然现象”,四位同学都认为可以用科学探究的一般方法排除偶然现象。他们的方法是:___
_____。
(2)小花认为小东的猜想不正确,她从碱使酚酞试液变色的原因上给予了否定,小花的理由是________。
(3)四位同学讨论后认为要验证小花的猜想,还需做如下实验,你知道其实验的目的吗?
实验步骤
设计目的
将氢氧化镁加入到热水中搅拌,滴入酚酞试液,并在上方滴一些植物油。
_____
___
(4)对小红的猜想,实验小组的同学设计了多种实验方案进行证明,其中一种如下表。
实验方法
可能观察到的现象
相应结果或结论
取两支试管,分别加入相同质量的氢氧化镁和相同质量的热水振荡,各滴加数滴酚酞试液。一支保持温度不变,另一支自然冷却。
保持温度不变的红色不消失,自然冷却的红色消失。
_____
___
13.小明同学用如下实验装置探究CO2与NaOH溶液能否反应。锥形瓶中的溶液为氢氧化钠溶液或澄清石灰水(均为200mL)。
【查阅资料】
①通常状况下,1体积水能溶解1体积二氧化碳;
②CO2在酸性溶液中溶解性会大大降低,若向溶有CO2的水溶液中加入盐酸,
会将CO2
从水中赶出,观察到溶液中有气泡。
(1)小明向A装置通入的CO2气体体积V应________200mL(填“>”、“<”或“=”)。
(2)A中的溶液是________,B中的溶液是________
,
证明氢氧化钠溶液可以与二氧化碳反应的现象是________。
(3)小红不用B装置,实验后他向锥形瓶A中的溶液中加入盐酸溶液发现有气泡产生,他判断该现象能证明二氧化碳和氢氧化钠溶液反应,你认为他的判断是否正确________。小丽也不用B装置,实验后她向锥形瓶A中的溶液中加入氯化钙溶液,如出现________
,
就能证明二氧化碳和氢氧化钠溶液反应。并写出相关化学方程式____
____。
14.学校某兴趣小组做了氧化铜和盐酸反应的实验,小明为测定反应后混合溶液的成分及含量,想烧杯中分5次共加入200克10%的氢氧化钠溶液,得到沉淀的质量记录如下:
(1)分析实验过程,第一次加入40.0克NaOH,为什么没有生成沉淀?________。
(2)分析实验过程,如果加入90克NaOH,溶液中的溶质是________。
(3)原来混合液中氯化铜的质量为多少克?(写出具体计算过程)
(4)若小明在称量沉淀前,没有将沉淀上吸附的溶质清洗掉就直接干燥,则会造成就计算氯化铜的含量??????
?。
A.?偏高?????????????????????????????????????????B.?偏低?????????????????????????????????????????C.?不变
15.实验室有一份在空气中潮解变质的氢氧化钠样品,质量为1.5g。某实验小组将这份样品完全溶解,配成50g溶液。然后缓慢滴入7.3%的稀盐酸,同时进行搅拌,使二氧化碳全部逸出。滴加过程中,多次测得溶液pH和溶液总质量,部分数据如下表所示:
测量次数
第1次
第6次
第16次
第21次
第26次
滴加的盐酸总质量/g
0
5
15
20
25
溶液总质量/g
50
55
m
69.78
74.78
溶液pH
12.4
12.1
7.0
2.2
2.1
请分析计算:
(1)第________次测量时,溶液中只有一种溶质。
(2)表中m=________。
(3)样品中碳酸钠的质量分数。(计算结果精确到0.1%)
(4)1.5g样品中氢氧化钠固体的质量。
第5讲
常见的碱
【学习目标】
1.熟悉并掌握质量守恒的含义及应用范围。
2.掌握并熟悉化学方程式的书写规则
3.熟悉并掌握化学方程式的计算方法
一、氢氧化钠
1.氢氧化钠NaOH:俗称
、
。
(1)易潮解,易和空气中的
反应而变质,故应
保存。氢氧化钠固体具有吸水性,所以可以用做某些气体的干燥剂,如
、
。
(2)
于水,放出大量的热。
(3)氢氧化钠的化学性质
①腐蚀性:氢氧化钠能与蛋白质、油脂反应,对皮肤、纸张等有强
性,在使用氢氧化钠溶液时,要注意防止液体溅入眼睛或沾到皮肤上。
①与指示剂反应:
②与酸反应:
③与酸性氧化物反应
④与某些盐反应(CuSO4等):
二、氢氧化钙
1.氢氧化钙Ca(OH)2:俗称
(1)熟石灰能吸收空气中的二氧化碳变成硬的碳酸钙,所以工业用氢氧化钙切砖抹墙
(2)农业上用熟石灰降低土壤酸性,配制农药波尔多液
(3)熟石灰可以用来制造氢氧化钠和漂白粉
2、氢氧化钙的化学性质
①腐蚀性:氢氧化钠能与蛋白质、油脂反应,对皮肤、纸张等有强
性,在使用氢氧化钠溶液时,要注意防止液体溅入眼睛或沾到皮肤上。
①与指示剂反应:
②与酸反应
③与酸性氧化物反应
④与某些盐反应(CuCl2等、碳酸钠溶液):
三.
区分NaOH和Ca(OH)2两种溶液的方法:
方法一:分别通入CO2,变浑浊的是
溶液;
Ca(CH)2+CO2=====
方法二:分别加入Na2CO3溶液,产生白色沉淀的是
溶液。
Ca(OH)2+Na2CO3=====
四、碱的通性
1.碱能与某些非金属氧化物发生反应
2NaOH+CO2=====
+
Ca(OH)2+CO2=====
+
(CO2能使澄清石灰水变浑浊,以此检验CO2)
2NaOH+SO2=====
+
(工业上用碱溶液吸收SO2等有害气体)
由此可知,氢氧化钠和氢氧化钙都应该密封保存,例如存放不严密的NaOH的成分可能有三种(无变质/部分变质/全部变质):
2.碱能与氯化铁、氯化铜溶液等物质反应
3NaOH+FeCl3=====
+
(生成红褐色沉淀)
2NaOH+CuSO4=====
+
(生成蓝色沉淀)
Ca(OH)2+CuCl2=====
+
【随堂练习】
1、下列有关物质的名称、俗名、化学式中,三者皆指同一物质的是( )
A.
氧化钙、消石灰、CaO
B.
氯化氢、盐酸、HCl
C.
碳酸钙、熟石灰、CaCO3
D.
氢氧化钠、烧碱、NaOH
2、对于氢氧化钠和氢氧化钙性质叙述错误的是( )
①都是白色固体;②都易溶于水放出大量的热;③溶液都能使酚酞试液变红;④都能与酸发生中和反应;⑤溶液通入二氧化碳都变浑浊;⑥与Na2CO3反应都变浑浊.
A.
②
B.
⑤⑥
C.
①②
D.
②⑤⑥
3、往KOH溶液中加水,溶液的pH变化正确的是(
)
A.?B.?C.?D.?
4、某无色溶液具有下列性质:①使无色酚酞试液变红?②与硫酸铜溶液反应生成蓝色沉淀③与纯碱溶液反应产生白色沉淀。此溶液是()
A.
氢氧化钠溶液
B.
澄清石灰水
C.
氯化钙溶液
D.
盐酸
5、如图,广口瓶内盛有气体X,滴管内盛有液体Y.若挤压胶头滴管的胶头,使液体滴入瓶中,振荡,套在玻璃管一端的小气球慢慢鼓起,则气体X和液体Y可能是(
)
A.?X是SO2,Y是NaOH溶液
B.?X是CO,Y是Ca(OH)2溶液
C.?X是O2,Y是Ca(OH)2溶液
D.?X是CO2,Y是硫酸溶液
6.下列验证“CO2与NaOH溶液反应”的装置中,不能观察到明显现象是的(装置气密性均良好)(
)
A.?
B.?
C.?
D.?
7.下列关于
pH
测定方法及有关
pH
说法正确的是(
)
A.?某学生用
pH
试纸测得雨水的
pH
为
4.6
B.?当雨水的
pH
小于
5.6
时所降雨水才是酸雨,pH
越大,雨水酸性越强
C.?先将玻璃棒用水清洗干净,后蘸取待测试液滴在
pH
试纸上,测定溶液的
pH
D.?pH
的范围为
0-14
8.为了区别氢氧化钠溶液和澄清石灰水,下列实验方案能达到预期目的的是(?
??)
A.??????????B.??????????C.??????????D.?
9.?取一滤纸条,等间距滴入10滴紫色石蕊溶液,装入玻璃管中,然后从玻璃管的两端同时放入分别蘸有浓氨水和浓盐酸的棉球,并迅速封闭两端管口,很快可观察到管内有白烟产生,待白烟消失后还可观察到如图所示的现象.则下列说法中正确的是( )
A.?氨水和盐酸都属于易挥发性物质?????????????????????????B.?该过程中没有化学反应发生
C.?所有气体分子的运动速率都相同?????????????????????????D.?图示黑点表示石蕊溶液变成了红色
10.下列图像能正确表示对应变化关系的是(???
)
A.?图甲表示水通电分解产生的气体质量m与反应时间t的关系
B.?图乙表示两份完全相同的双氧水在有无Mn02的情况下,产生的02质量m与反应时间t的关系
C.?图丙表示往锌中加入足量的稀H2S04
,
产生的H2质量m与反应时间t的关系
D.?图丁表示往稀盐酸和CuCl2混合液中滴人NaOH溶液,产生的沉淀质量m2与NaOH溶液质量m1的关系
11.通过一个多星期的化学学习,我们认识了许多“奇妙的酸”和“神奇的碱”,请回答下列问题:
(1)如图表示的是一些物质在常温下的近似pH,回答下列问题:
①厨房清洁剂显________性,在少量厨房清洁剂中滴入几滴酚酞,溶液呈________色.
②酸雨的酸性比正常雨水的酸性________(填“强”或“弱”).
③测量苹果汁pH时,先用蒸馏水润湿pH试纸,会使pH偏________(“大”或“小”).
(2)焊接工业上常用稀盐酸清洗铁锈,写出用稀盐酸除铁锈的化学方程式为________,铁制品除锈时________(填“能”或“不能”)长时间浸在酸溶液中.
(3)氢氧化钠固体暴露在空气中容易吸收空气中的水分,表面潮湿并逐渐溶解,这种现象叫做________,该变化是________变化;同时,氢氧化钠固体还能与空气中的二氧化碳反应而变质,请写出变质的化学方程式__
______.
(4)“洁厕灵”用于除污垢,去异味,有效成分为盐酸,“管道通”用于疏通堵塞的管道,其有效成分为氢氧化钠,二者不能混合使用,其原因是_
_______(用化学方程式回答).
(5)胃酸的主要成分是盐酸,胃舒平(主要成分Al(OH)3)常用于治疗胃酸过多症,写出Al(OH)3治疗胃酸过多症时的化学反应方程式____
____.
(6)为除去铁钉上的锈迹,某学生将带锈迹的铁钉放入过量的稀硫酸中,他首先观察到:铁钉表面的锈迹逐渐溶解,溶液由无色逐渐变成________色,这是因为(用化学方程式表示)_____
___;过一会儿,他又观察到铁钉表面________,这是因为_
_______(用化学方程式表示).
(8)盛水的铝壶中常结有一层水垢(主要成分是碳酸钙、氢氧化镁等),可用适量的稀盐酸除去它,写出其中发生的中和反应的化学方程式____
____.
12.某实验小组的四位同学在探究碱的性质时发现氢氧化钠、氢氧化钙等可溶性碱都能使酚酞试液变红。他们想进一步探究:不溶性的氢氧化镁是否也能使酚酞试液变红。为此,他们将适量的氢氧化镁加入到盛有热水的烧杯中搅拌,然后向浑浊的液体中滴加酚酞试液,发现酚酞试液变红,可是过一会儿红色又消失了。四位同学依据所学的化学知识,分别对上述酚酞试液变红、红色又消失的原因作了如下猜想:
小明:可能是个偶然现象。
小东:可能是浑浊液体中的固体氢氧化镁使酚酞试液变红,氢氧化镁沉降后溶液就变无色了。
小花:可能是酚酞试液与空气中的氧气反应,使红色消失;也可能是氢氧化镁溶液与空气中的二氧化碳反应的缘故。
小红:可能是在热水中氢氧化镁的溶解度大,溶液中
OH-
离子较多,使酚酞试液变红;过一会儿温度降低,氢氧化镁的溶解度减小,溶液中
OH-离子变少,酚酞试液又变无色。
(1)对小明猜想“是个偶然现象”,四位同学都认为可以用科学探究的一般方法排除偶然现象。他们的方法是:___
_____。
(2)小花认为小东的猜想不正确,她从碱使酚酞试液变色的原因上给予了否定,小花的理由是________。
(3)四位同学讨论后认为要验证小花的猜想,还需做如下实验,你知道其实验的目的吗?
实验步骤
设计目的
将氢氧化镁加入到热水中搅拌,滴入酚酞试液,并在上方滴一些植物油。
_____
___
(4)对小红的猜想,实验小组的同学设计了多种实验方案进行证明,其中一种如下表。
实验方法
可能观察到的现象
相应结果或结论
取两支试管,分别加入相同质量的氢氧化镁和相同质量的热水振荡,各滴加数滴酚酞试液。一支保持温度不变,另一支自然冷却。
保持温度不变的红色不消失,自然冷却的红色消失。
_____
___
13.小明同学用如下实验装置探究CO2与NaOH溶液能否反应。锥形瓶中的溶液为氢氧化钠溶液或澄清石灰水(均为200mL)。
【查阅资料】
①通常状况下,1体积水能溶解1体积二氧化碳;
②CO2在酸性溶液中溶解性会大大降低,若向溶有CO2的水溶液中加入盐酸,
会将CO2
从水中赶出,观察到溶液中有气泡。
(1)小明向A装置通入的CO2气体体积V应________200mL(填“>”、“<”或“=”)。
(2)A中的溶液是________,B中的溶液是________
,
证明氢氧化钠溶液可以与二氧化碳反应的现象是________。
(3)小红不用B装置,实验后他向锥形瓶A中的溶液中加入盐酸溶液发现有气泡产生,他判断该现象能证明二氧化碳和氢氧化钠溶液反应,你认为他的判断是否正确________。小丽也不用B装置,实验后她向锥形瓶A中的溶液中加入氯化钙溶液,如出现________
,
就能证明二氧化碳和氢氧化钠溶液反应。并写出相关化学方程式____
____。
14.学校某兴趣小组做了氧化铜和盐酸反应的实验,小明为测定反应后混合溶液的成分及含量,想烧杯中分5次共加入200克10%的氢氧化钠溶液,得到沉淀的质量记录如下:
(1)分析实验过程,第一次加入40.0克NaOH,为什么没有生成沉淀?________。
(2)分析实验过程,如果加入90克NaOH,溶液中的溶质是________。
(3)原来混合液中氯化铜的质量为多少克?(写出具体计算过程)
(4)若小明在称量沉淀前,没有将沉淀上吸附的溶质清洗掉就直接干燥,则会造成就计算氯化铜的含量??????
?。
A.?偏高?????????????????????????????????????????B.?偏低?????????????????????????????????????????C.?不变
15.实验室有一份在空气中潮解变质的氢氧化钠样品,质量为1.5g。某实验小组将这份样品完全溶解,配成50g溶液。然后缓慢滴入7.3%的稀盐酸,同时进行搅拌,使二氧化碳全部逸出。滴加过程中,多次测得溶液pH和溶液总质量,部分数据如下表所示:
测量次数
第1次
第6次
第16次
第21次
第26次
滴加的盐酸总质量/g
0
5
15
20
25
溶液总质量/g
50
55
m
69.78
74.78
溶液pH
12.4
12.1
7.0
2.2
2.1
请分析计算:
(1)第________次测量时,溶液中只有一种溶质。
(2)表中m=________。
(3)样品中碳酸钠的质量分数。(计算结果精确到0.1%)
(4)1.5g样品中氢氧化钠固体的质量。
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
