天津市天津一中2020-2021学年高一下学期期末考试化学试题 PDF版含答案
文档属性
| 名称 | 天津市天津一中2020-2021学年高一下学期期末考试化学试题 PDF版含答案 |

|
|
| 格式 | |||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2021-07-04 00:00:00 | ||
图片预览


文档简介
天津 一中 2020-20 21-2 高一 年级 化学 学科 期末 质量 调查 试卷
本试 卷分 为第 I 卷( 选择 题) 、第 II 卷( 非选 择题 )两 部分 ,共 100 分, 考试 用时
90 分钟 。第 I 卷 1 至 3 页, 第 II 卷 4 至 5 页。 考生 务必 将答 案涂 写答 题纸 或答 题卡 的规
定位 置上 ,答 在试 卷上 的无 效。
祝各 位考 生考 试顺 利!
第Ⅰ 卷( 共36分)
一、 选择 题(12道 小题 ,每 小题 只有 1 个正 确选 项。 每小 题 3 分,请 将正 确答 案填 涂在
机读 卡上 )
1.水 饺是 中华 传统 美食 。下 列制 作水 饺的 主要 过程 中, 包含 过滤 操作 的是 ( )
A.和 面、 饧面 B.剁 馅、 拌馅 C.擀 皮、 包饺 子 D.煮 熟、 捞饺 子
2.天津市第一中学组建于1947年9月,原名为天津市立中学;1949年3月6日,学校
改名为天津市第一中学。“育人为本,教学为主,全面发展,学有所长”是一中的办学宗
旨。在74年的历史中,天津一中的教育教学成果丰硕。学校培养出一批优秀的学生,其
中化学学科培养的( )获得1995年第27届国际化学奥赛金牌。
A.杨程 B.焦宇辰 C.安金鹏 D.张思睿
3.从石油原料到口罩的生产过程中涉及的下列变化或转化,不属于化学变化的是( )
石油 催化 裂解 得到 丙烯 催化 聚合 生 聚丙 烯熔 融后 喷丝 用环 氧乙 烷与 微生 物
丙烯 成聚 丙烯 压成 熔喷 布 蛋白 质发 生反 应消 毒
A B C D
4.水泥是人类最伟大的发明之一,主要成分为硅酸三钙(3CaO?SiO2)。将其与适量的水反
应,形成相互交联的结构,反应式如下2(3CaO?SiO2)+6H2O=3CaO?2SiO2?
3H2O+3Ca(OH)2 ?H<0。但是,需要避免交联过程热膨胀及产生的水蒸气在建筑结构
中造成空隙。
我国 三峡 大坝 的建 设者 在全 世界 首创 了以 冰代 水的 浇灌 方法 ,有 效解 决了 这一 问题 ,
保证 了大 坝建 筑质 量。 下列 说法 错误 的是 ( )
A.水 泥由 黏土 和石 灰石 等研 磨、 煅烧 制得
B.水 泥生 产过 程中 加入 石膏 ,可 以调 节水 泥的 硬化 速率
C.水 的作 用是 提供 结晶 水以 稳定 交联 结构
D.以 冰代 水的 优点 是减 少了 热膨 胀及 水蒸 气的 产生
5. 天津 市十七 届人 大常 委会 表决 通过 了《 天津 市生 活垃 圾管 理条 例》 ,于 2020 年 12 月
1 日起 施行 。天 津一 中化 学组 老师 从实 验入 手, 带领 学生 们利 用所 学化 学知 识积 极探 索资
源的 有效 使用 、节 约使 用和 循环 使用 ,以 实现 循环 经济 和可 持续 发展 ,从 而实 现废 弃物 的
综合 利用 和保 护环 境。 我们 在实 验室 利用 废旧 电池 的铜 帽( 主要 成分 为 Cu、 Zn)制 备
CuSO4?5H2O 的部 分实 验步 骤如 图:
下列 说法 错误 的是 ( )
A. “溶解 I”中, 为加 快溶 解速 率, 可将 铜帽 粉碎
B.“ 滤液 I” 中, 溶质 的主 要成 分为 ZnSO4
C. “溶解 II”过程 中, 有大 量的 气体 产生
D. “操作 I” 需要 用到 酒精 灯、 玻璃 棒等 仪器
6. 下列 方案 设计 、现 象和 结论 都正 确的 是( )
目的 方案 设计 现象 和结 论
检验 某无 色溶 液 若溶 液变 黄色 且试 管上 部产
取少 量该 溶液 于试 管中 ,加 稀
A 中是 否含 有 NO2 生红 棕色 气体 ,则 该溶 液中
- 盐酸 酸化 ,再 加入 FeCl2溶液 -
含有 NO2
-1
取 5 mL 0.1 mol? L KI 溶液 于
探究 KI 与 FeC l3 试管 中, 加入 1 mL 0.1 若溶 液变 血红 色, 则 KI 与
B -1
反应 的限 度 mol ?L FeCl3溶液 ,充 分反 应 FeCl3的反 应有 一定 限度
后滴 入 5 滴 15%K SC N 溶液
检验 Cu2O 中是 若有 气泡 产生 ,则 说明 样品
C 取样 ,加 入稀 硝酸 ,观 察现 象
否含 有 Cu 中有 Cu
取 2 mL 20%的蔗 糖溶 液于 试
探究 蔗糖 在酸 性 管中 ,加 入适 量稀 H2SO4后水 若没 有生 成砖 红色 沉淀 ,则
D 水溶 液中 的稳 定 浴加 热 5min;再 加入 适量 新 蔗糖 在酸 性水 溶液 中稳 定
性 制 Cu(OH )2并加 热
7.2017年12月20日,在第74次联合国全体会议上,宣布2019年为“国际化学元素
周期表年”。元素W、X、Y和Z在周期表中的相对位置如图所示,其中元素Z位于第四周
期,W、X、Y原子的最外层电子数之和为18。下列说法正确的是( )
A.简 单氢 化物 沸点 : Y>W
B.原 子半 径: Z>Y>X
C.氧 化物 的水 化物 的酸 性: WD.推 测 Z 是半 导体 材料 , Z 与 Y 可形 成化 合物 ZY4
8 . 如 图 是 含 氮 化 合 物 及 单 质 的 “ 类 别 — 价 态 ” 二 维 图 , 结 合 二 维 图 及 氧 化 还 原 反 应 原 理
的基 本规 律, 下列 相关 分析 或预 测错 误的 是( )
A.硝 酸具 有较 强的 氧化 性, 可用 稀硝 酸清 洗 “银镜 实验 ” 后的 试管
B.NO 、NO2和 NH3在一 定条 件下 均能 反应 ,可 用氨 气处 理氮 氧化 物
C.可 加热 NH4NO3和 Ca(O H)2制备 氨气
D.联 氨 (N2H4)可能 被亚 硝酸 (HN O2) 氧化 生成 氢叠 氮酸 HN3
9 . 一 种 具 有 高 能 量 比 的 新 型 干 电 池 示 意 图 如 图 所 示 , 石 墨 电 极 区 发 生 的 电 极 反 应 为 :
- -
MnO2+e + H2O===MnO(OH ) +OH 。该 装置 工作 时, 下列 叙述 正确 的是 ( )
- +
A. Al 电极 区的 电极 反应 式: Al - 3e + 3NH3?H2O ===Al(O H)3↓+ 3NH4
B.石 墨电 极上 的电 势比 Al 电极 上的 低
C.每 消耗 27 g Al ,有 3 mol 电子 通过 溶液 转移 到石 墨电 极上
D.若 采用 “ 食盐 水+ NaOH 溶液 ” 作电 解质 溶液 ,电 极反 应式 相同
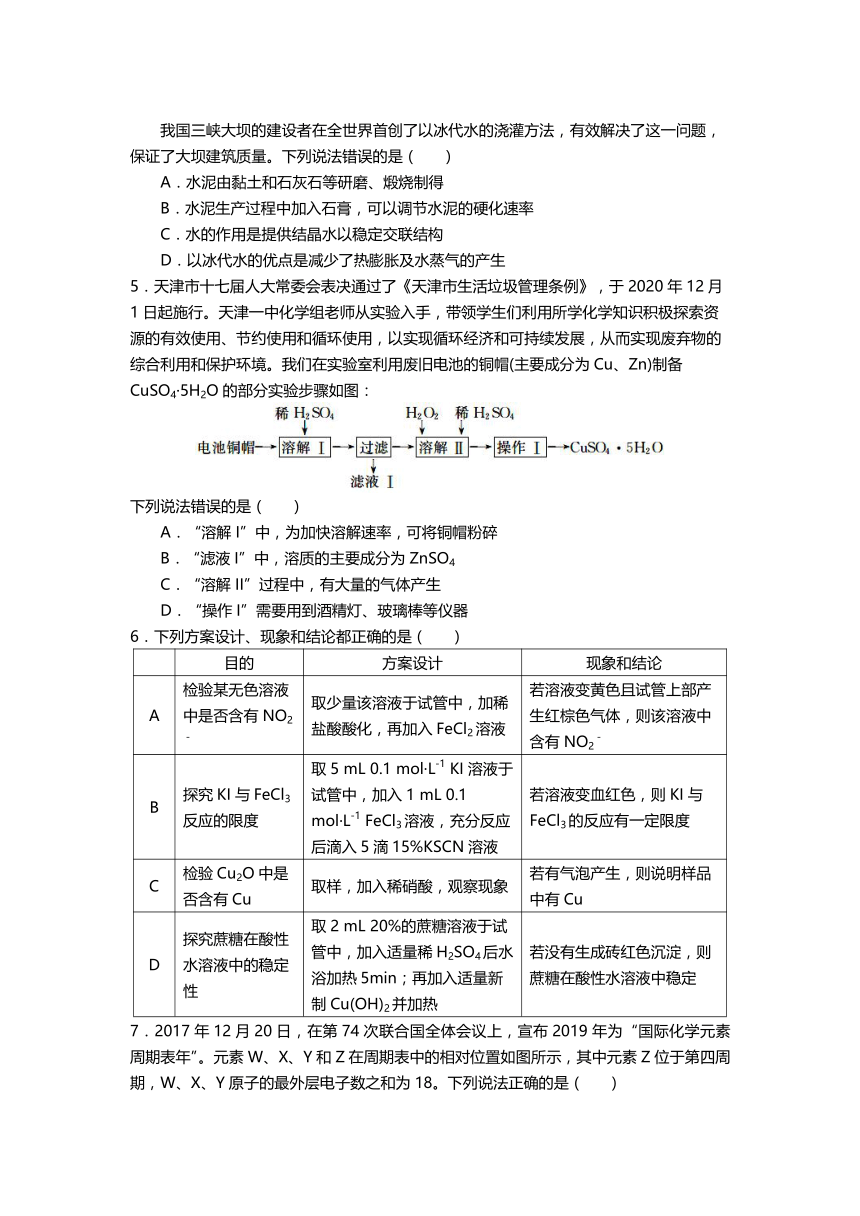
10 . 利 用 NO 、 O2和 Na2CO3溶 液 反 应 制 备 NaNO2的 装 置 如 图 所 示 , 下 列 关 于 该 装 置 的
描述 不正 确的 是( )
A.装 置 A 分液 漏斗 中的 药品 选用 不当 ,应 选用 稀 HNO3
B.实 验过 程中 ,通 过控 制分 液漏 斗的 活塞 控制 气流 速度
C.装 置 C 中发 生反 应的 化学 方程 式为 :2Na2CO3+4NO +O2===4NaNO2+ 2CO2
D.实 验过 程中 ,装 置 C 液面 上方 可能 出现 红棕 色气 体
11. 由一 种阳 离子 与两 种酸 根离 子组 成的 盐称 为混 盐。 混盐 Na4S2O3在酸 性条 件下 可以 产
生 S 。下 列关 于混 盐 Na4S2O3的有 关判 断不 正确 的是 ( )
A.该 混盐 与稀 硫酸 反应 产生 1mol S 时转 移 2NA个电 子
B.该 混盐 在酸 性条 件下 可以 产生 S 的原 因是 发生 了复 分解 反应
C .该 混盐 溶液 中加 入 BaCl2溶液 ,可 以生 成白 色沉 淀
D.该 混盐 中的 硫元 素的 化合 价为 - 2 和+ 4
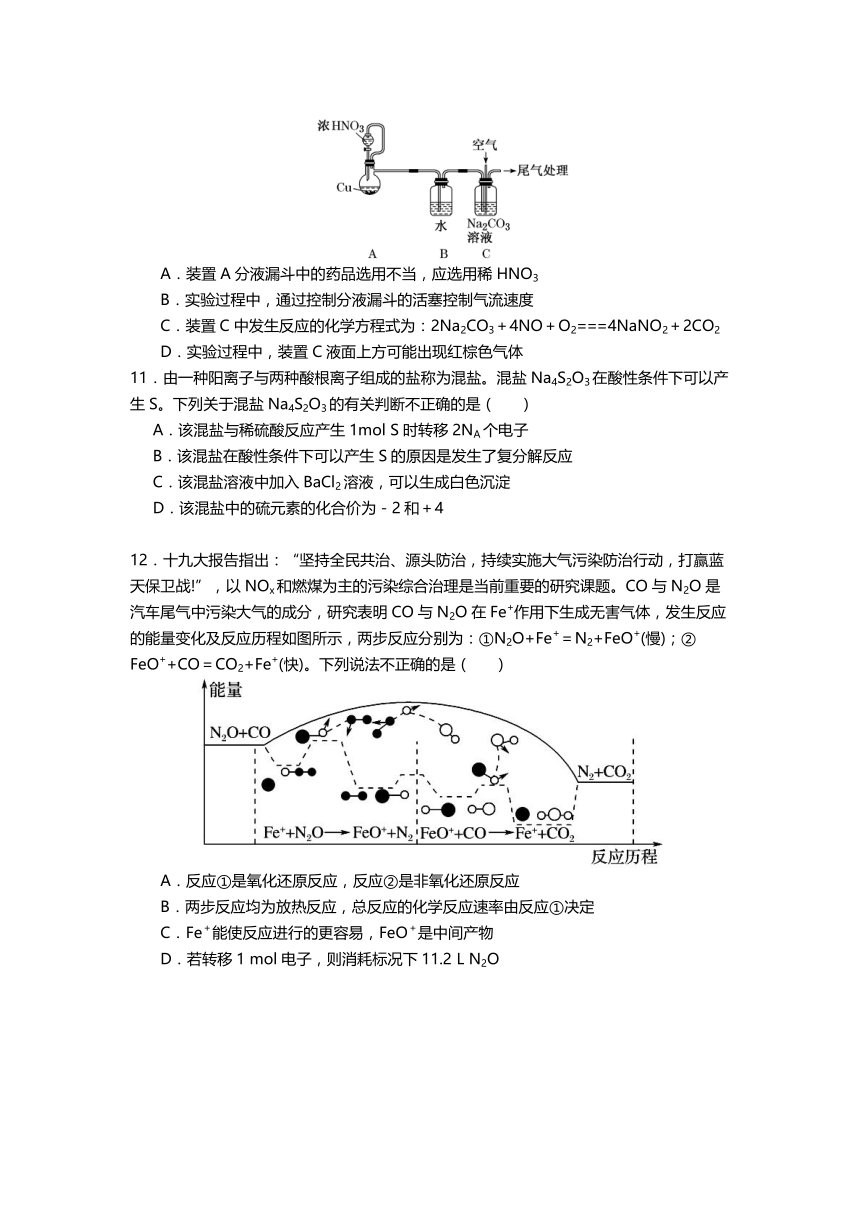
12. 十九 大报 告指 出: “坚持 全民 共治 、源 头防 治, 持续 实施 大气 污染 防治 行动 ,打 赢蓝
天保 卫战 !” ,以 NOx和燃 煤为 主的 污染 综合 治理 是当 前重 要的 研究 课题 。CO 与 N2O 是
+
汽车 尾气 中污 染大 气的 成分 ,研 究表 明 CO 与 N2O 在 Fe 作用 下生 成无 害气 体, 发生 反应
+ +
的能 量变 化及 反应 历程 如图 所示 ,两 步反 应分 别为 :① N2O+Fe = N2+FeO (慢 );②
+ +
FeO +CO = CO2+Fe ( 快) 。下 列说 法不 正确 的是 ( )
A.反 应 ①是氧 化还 原反 应, 反应 ② 是非 氧化 还原 反应
B.两 步反 应均 为放 热反 应, 总反 应的 化学 反应 速率 由反 应① 决定
+ +
C. Fe 能使 反应 进行 的更 容易 ,FeO 是中 间产 物
D.若 转移 1 mol 电子 ,则 消耗 标况 下 11.2 L N2O
第Ⅱ 卷( 共 64 分)
13. (19 分) 现有 下列 短周 期元 素性 质的 有关 数据 :
元素 编号 a b c d e f g h
0.03 0.07 0.07 0.08 0.10 0.14 0.15 0.18
原子 半径 /nm 7 1 5 2 2 3 2 6
最高 化合 价或 最底 + 1 - 1 - 3 + 3 -2 +3 +1 +1
(1)根据元素周期律确定a至h 8种元素在周期表中的位置,将它们的元素编号填入下
表相应的空格内。
Ⅰ Ⅱ Ⅲ Ⅴ
Ⅳ族 Ⅵ族 Ⅶ族 Ⅷ族
族 族 族 族
第一 周期
第二 周期
第三 周期
(2)上述元素形成的常见氢化物中,分子间存在氢键的有(填氢化物的化学
式) 。
(3)氢化铝锂(LiAlH4)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广
泛。在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH)。与氢化铝锂性质相似但
较为温和的还原剂由上述a、d、h三种元素组成,请画出这种还原剂的电子式。
写出该物质受热分解的反应方程
式 。
(4)在元素周期表中,相邻近的元素在结构和性质上有许多相似之处。第二周期的碳、
氮、氧、氟都可以形成氢化物,氧元素的氢化物除H2O外,还有H2O2;碳元素的氢化物
除CH4外,还有C2H6等;与之相似的氮元素的氢化物除NH3外,还有________(填化学
式),其沸点比液氨_______(填“高”或“低”),稳定性比氨_______(填“好”或
“差”),该氢化物与足量盐酸反应的化学方程式为
___________________________________________________。
14.(9分)
?1
(1)①已知:C H ( g ) H O ( g ) C O ( g ) 3H ( g ) H 2 0 6 .2 k J mo l4 ? ??? ? ? ? ? ?2 2
?1
C H ( g ) C O ( g ) 2 C O ( g ) 2 H ( g ) H 2 4 7 .4 k J mo l4 ? ??? ? ? ? ? ?2 2
则C H ( g )4 与H O ( g )2 反应 生成C O ( g )2 和H ( g )2 的热 化学 方程 式为
_____ _____ ____ _____ ____ _____ ____ _____ ____ _____ ____ _____ ____ _____ ____ _____ 。
? ? - - -
(2 )一 定条 件下 ,在 水溶 液中 所含 离子C l 、C lO 、ClO2、C lO3、C lO4各1mol,其
相对 能量 的大 小如 下图 所示 (各离 子在 图中 用氯 元素 的相 应化 合价 表示 ),
- - - ?
则反 应3 C lO (aq )= = = C lO (aq )+ 2 C l (aq ) 1
3 的ΔH=_____ ___k J m o l? 。
(3 )工 业上 可通 过天 然气 跟水 蒸气 反应 制取 H2: CH4(g)+H2O(g) CO( g)+3H2(g),
有关 反应 的能 量变 化如 下图 所示 ,则 该反 应的 ?H=__ _____ ____ _____ __kJ/ mol ( 用含 a、b、
c 的式 子表 示 )。
15. (10 分) 本学 期天 津一 中化 学学 科为 了落 实国 家五 育并 举、 天津 市垃 圾分 类条 列、
着重 培养 学生 的核 心素 养, 在化 学组 各位 老师 的帮 助下 小艾 老师 做了 《废 旧干 电池 的回 收
再利 用》 展示 课, 废弃 物的 综合 利用 既有 利于 节约 资源 ,又 有利 于保 护环 境, 在课 上老 师
带着 学生 们拆 解电 池并 对炭 包中 的物 质设 计实 验并 分离 提纯 、再 利用 。下 面是 实验 室利 用
废弃 旧电 池的 铜帽 (Zn、 Cu 总含 量约 为 99%) 回收 铜并 制备 ZnO 的部 分实 验过 程如 下, 请
同学 们回 答相 关问 题:
(1 )① 铜帽 溶解 时加 入 H2O2的目 的是 _____ _____ ____ _____ ____ _____ ____ _( 用化 学方 程式 表
示) 。
② 铜帽 溶解 后需 将溶 液中 过量 H2O2除去 。除 去 H2O2的简 便方 法是
_____ _____ ____ _____ __。
(2 )为 确定 加入 锌灰 (主要 成分 为 Zn、 ZnO,杂 质为 铁及 其氧 化物 ) 含量 ,实 验中 需测 定
2+ 2+
除去 H2O2后溶 液中 Cu 的含 量。 实验 操作 为: 准确 量取 一定 体积 的含 有 Cu 的溶 液于
带塞 锥形 瓶中 ,加 适量 水稀 释, 调节 pH=3~ 4,加 入过 量 KI,用 Na2S2O3标准 溶液 滴定
至终 点。
2+ - 2- -
上述 过程 中的 离子 方程 式如 下: 2Cu + 4I =2CuI( 白色 )↓+I2、 I2+2S2O3 =2I+
2-
S4O6
① 滴定 选用 的指 示剂 为_____ _____ _ ,滴 定终 点观 察到 的现 象为 ______ _____ ____ __。
2+
② 若滴 定前 溶液 中 H2O2没有 除尽 ,所 测定 的 Cu 的含 量将 会 _____ _____ _( 填“ 偏高 ”
“偏低 ”“ 不变 ” )。
16. (10 分) 海洋 是生 命的 摇篮 ,海 水不 仅是 宝贵 的水 资源 ,而 且蕴 藏着 丰富 的化 学资
源。 从海 水中 提取 淡水 和一 些重 要的 化工 产品 的工 艺流 程如 图所 示。
根据 上述 流程 图回 答下 列问 题:
(1 )写 出反 应① 的化 学反 应方 程式 ______ _____ ____ _____ ____ _____ ____ _____ _。
(2 )工 业上 完成 MgCl2→ Mg 常用 的冶 炼方 法_____ _____ _ 。
(3 )通 入热 空气 或水 蒸气 吹出 Br2,利 用了 溴的 _____ _____ (填序 号 )。
A.氧 化性 B.还 原性 C .挥 发性 D .腐 蚀性
(4 )写 出步 骤 II 反应 的离 子方 程式 _____ _____ ____ _____ ____ _____ ____ _____ ____ _____ ____ _ 。
(5 )从 海水 中获 得淡 水的 主要 方法 有电 渗析 法、 离子 交换 法和 ______ _____ (填一 种 )。
(6 )实 验室 模拟 海水 蒸馏 法制 取淡 水, 蒸馏 过程 中不 可能 用到 的仪 器有 ______ __( 填序
号) 。
A.圆 底烧 瓶 B.容 量瓶 C.直 形冷 凝管 D.接 收器
(7 )离 子交 换法 净化 水的 过程 如图 所示 。下 列说 法正 确的 是_____ _____ (填序 号 )。
A.经 过阳 离子 交换 树脂 后, 水中 阳离 子总 数减 少
2-
B.通 过阴 离子 交换 树脂 后, 水中 只有 SO4 被除 去
C.通 过净 化处 理后 的水 ,导 电性 增强
+ -
D.阴 离子 交换 树脂 填充 段存 在反 应: H +OH =H2O
17 .( 16 分 ) 四 氯 化 锡 (SnC l4) 是 合 成 有 机 锡 化 合 物 的 原 料 , 其 熔 点 为 - 33 ℃ , 沸 点 为
114 ℃ , 在 潮 湿 的 空 气 中 强 烈 水 解 产 生 有 刺 激 性 的 白 色 烟 雾 , 产 物 之 一 为 SnO2。 实 验 室
制 备 四 氯 化 锡 的 操 作 是 : 将 金 属 锡 熔 融 , 然 后 泼 入 冷 水 , 制 成 锡 花 ; 将 干 燥 的 锡 花 加 入 反
应器 中, 再向 反应 器中 缓慢 地通 入干 燥的 氯气 。( 装置 C 中的 试剂 X 未画 出 )
Ⅰ. 图 1 为实 验室 制备 干燥 氯气 的实 验装 置(夹持 装置 已略 )
(1 ) 该装 置 制 备氯 气 选 用的 药 品 为漂 粉 精 固体 [ 主 要成 分 Ca( ClO )2] 和 浓盐 酸 ,A 中 发生 反
应的 化学 方程 式为 _____ _____ ____ _____ ____ _____ ____ _____ _。
(2 )装 置 B 的饱 和食 盐水 能够 除去 Cl2中的 HC l,此 外装 置 B 还有 _____ _____ 作用 。
(3 )试 剂 X 可能 为 ______ ____( 填标 号 )。
A.无 水氯 化钙 B.浓 硫酸
C.五 氧化 二磷 D.碱 石灰
(4 )用 锡花 代替 锡粒 的目 的是 ______ _____ ____ _____ ____ _____ ____ _____ 。
(5 )四 氯化 锡在 潮湿 空气 中水 解的 化学 方程 式为 ______ _____ ____ _____ ____ _____ ___ 。
Ⅱ. 图 2 是蒸 馏 SnCl4的装 置
(6 )该 装置 尚有 两处 不当 之处 ,它 们分 别是
_____ _____ ____ _____ ____ _____ ____ _____ _、_____ _____ ____ _____ ____ _____ ____ _____ ___ 。
(7 )实 验用 的锡 花中 含有 金属 铜。 某同 学设 计下 列实 验测 定锡 花的 纯度 :
第一 步: 称取 7.500 g 锡花 溶于 足量 稀硫 酸中 ,充 分反 应后 过滤 ;
2+ 4+
第二 步: 向滤 液中 加入 过量 Fe2(SO4)3,将 生成 的 Sn 氧化 成 Sn ;
-1 2+
第三 步: 用 0.950 0 mol ?L 的 K2Cr2O7溶液 滴定 生成 的 Fe ,
2+ 2- + 3+ 3+
发生 反应 的方 程式 为 Fe +Cr2O7 +H ―→ Cr + Fe +H2O( 未配 平)
若达 到滴 定终 点时 共消 耗 21.00 mL K2Cr2O7溶液 ,
试计 算锡 花中 锡的 百分 含量 :_____ _____ ( 结果 保留 4 位有 效数 字)。
参考 答案
1 2 3 4 5 6 7 8 9 10 11 12
D B C C C B D C A A A A
13.
(1)
(2 )HF 、 NH3
+ -
(3 )Na [ ] ;2NaBH4 2NaH +2B +3H2↑
(4 )N2H4, 高, 差, N2H4+ 2HC l→ N2H6Cl2。
14.
?1
(1 )C H ( g ) 2 H O ( g ) C O ( g ) 4 H ( g ) ΔH= 1 6 5 k J mo l4 ? ? ? ? ?2 2 2 ? ? ;
(2 )-117
?1
?
(3 )( a +3b-c ) kJ mol
15. Cu +H2O2+H2SO4=CuSO4+ 2H2O ;加 热(至沸 );淀 粉溶 液; 蓝色 褪去 ;偏 高。
16.
(1 )2NaC l +2H2O电解2NaO H + H2↑+ Cl2↑;
(2 )电 解;
(3 )C ;
+ 2— —
(4 )Br2+SO2+2H2O=4H +SO4 +2Br ;
(5 )蒸 馏法 ;
(6 )B;
(7 )D
17.
(1 )Ca( ClO )2+4HC l( 浓 ) =加热= CaC l2+ 2Cl2↑+2H2O;
(2 )安 全瓶 ;
(3 )AC;
(4 )增 大与 氯气 的接 触面 积, 加快 反应 速率 ;
(5 )SnCl4+ 2H2O ===SnO2+ 4HC l;
(6 )温 度计 水银 球位 置不 对, Ⅱ和 Ⅲ之间 缺少 干燥 装置 ;
(7 )94.96 %。
本试 卷分 为第 I 卷( 选择 题) 、第 II 卷( 非选 择题 )两 部分 ,共 100 分, 考试 用时
90 分钟 。第 I 卷 1 至 3 页, 第 II 卷 4 至 5 页。 考生 务必 将答 案涂 写答 题纸 或答 题卡 的规
定位 置上 ,答 在试 卷上 的无 效。
祝各 位考 生考 试顺 利!
第Ⅰ 卷( 共36分)
一、 选择 题(12道 小题 ,每 小题 只有 1 个正 确选 项。 每小 题 3 分,请 将正 确答 案填 涂在
机读 卡上 )
1.水 饺是 中华 传统 美食 。下 列制 作水 饺的 主要 过程 中, 包含 过滤 操作 的是 ( )
A.和 面、 饧面 B.剁 馅、 拌馅 C.擀 皮、 包饺 子 D.煮 熟、 捞饺 子
2.天津市第一中学组建于1947年9月,原名为天津市立中学;1949年3月6日,学校
改名为天津市第一中学。“育人为本,教学为主,全面发展,学有所长”是一中的办学宗
旨。在74年的历史中,天津一中的教育教学成果丰硕。学校培养出一批优秀的学生,其
中化学学科培养的( )获得1995年第27届国际化学奥赛金牌。
A.杨程 B.焦宇辰 C.安金鹏 D.张思睿
3.从石油原料到口罩的生产过程中涉及的下列变化或转化,不属于化学变化的是( )
石油 催化 裂解 得到 丙烯 催化 聚合 生 聚丙 烯熔 融后 喷丝 用环 氧乙 烷与 微生 物
丙烯 成聚 丙烯 压成 熔喷 布 蛋白 质发 生反 应消 毒
A B C D
4.水泥是人类最伟大的发明之一,主要成分为硅酸三钙(3CaO?SiO2)。将其与适量的水反
应,形成相互交联的结构,反应式如下2(3CaO?SiO2)+6H2O=3CaO?2SiO2?
3H2O+3Ca(OH)2 ?H<0。但是,需要避免交联过程热膨胀及产生的水蒸气在建筑结构
中造成空隙。
我国 三峡 大坝 的建 设者 在全 世界 首创 了以 冰代 水的 浇灌 方法 ,有 效解 决了 这一 问题 ,
保证 了大 坝建 筑质 量。 下列 说法 错误 的是 ( )
A.水 泥由 黏土 和石 灰石 等研 磨、 煅烧 制得
B.水 泥生 产过 程中 加入 石膏 ,可 以调 节水 泥的 硬化 速率
C.水 的作 用是 提供 结晶 水以 稳定 交联 结构
D.以 冰代 水的 优点 是减 少了 热膨 胀及 水蒸 气的 产生
5. 天津 市十七 届人 大常 委会 表决 通过 了《 天津 市生 活垃 圾管 理条 例》 ,于 2020 年 12 月
1 日起 施行 。天 津一 中化 学组 老师 从实 验入 手, 带领 学生 们利 用所 学化 学知 识积 极探 索资
源的 有效 使用 、节 约使 用和 循环 使用 ,以 实现 循环 经济 和可 持续 发展 ,从 而实 现废 弃物 的
综合 利用 和保 护环 境。 我们 在实 验室 利用 废旧 电池 的铜 帽( 主要 成分 为 Cu、 Zn)制 备
CuSO4?5H2O 的部 分实 验步 骤如 图:
下列 说法 错误 的是 ( )
A. “溶解 I”中, 为加 快溶 解速 率, 可将 铜帽 粉碎
B.“ 滤液 I” 中, 溶质 的主 要成 分为 ZnSO4
C. “溶解 II”过程 中, 有大 量的 气体 产生
D. “操作 I” 需要 用到 酒精 灯、 玻璃 棒等 仪器
6. 下列 方案 设计 、现 象和 结论 都正 确的 是( )
目的 方案 设计 现象 和结 论
检验 某无 色溶 液 若溶 液变 黄色 且试 管上 部产
取少 量该 溶液 于试 管中 ,加 稀
A 中是 否含 有 NO2 生红 棕色 气体 ,则 该溶 液中
- 盐酸 酸化 ,再 加入 FeCl2溶液 -
含有 NO2
-1
取 5 mL 0.1 mol? L KI 溶液 于
探究 KI 与 FeC l3 试管 中, 加入 1 mL 0.1 若溶 液变 血红 色, 则 KI 与
B -1
反应 的限 度 mol ?L FeCl3溶液 ,充 分反 应 FeCl3的反 应有 一定 限度
后滴 入 5 滴 15%K SC N 溶液
检验 Cu2O 中是 若有 气泡 产生 ,则 说明 样品
C 取样 ,加 入稀 硝酸 ,观 察现 象
否含 有 Cu 中有 Cu
取 2 mL 20%的蔗 糖溶 液于 试
探究 蔗糖 在酸 性 管中 ,加 入适 量稀 H2SO4后水 若没 有生 成砖 红色 沉淀 ,则
D 水溶 液中 的稳 定 浴加 热 5min;再 加入 适量 新 蔗糖 在酸 性水 溶液 中稳 定
性 制 Cu(OH )2并加 热
7.2017年12月20日,在第74次联合国全体会议上,宣布2019年为“国际化学元素
周期表年”。元素W、X、Y和Z在周期表中的相对位置如图所示,其中元素Z位于第四周
期,W、X、Y原子的最外层电子数之和为18。下列说法正确的是( )
A.简 单氢 化物 沸点 : Y>W
B.原 子半 径: Z>Y>X
C.氧 化物 的水 化物 的酸 性: W
8 . 如 图 是 含 氮 化 合 物 及 单 质 的 “ 类 别 — 价 态 ” 二 维 图 , 结 合 二 维 图 及 氧 化 还 原 反 应 原 理
的基 本规 律, 下列 相关 分析 或预 测错 误的 是( )
A.硝 酸具 有较 强的 氧化 性, 可用 稀硝 酸清 洗 “银镜 实验 ” 后的 试管
B.NO 、NO2和 NH3在一 定条 件下 均能 反应 ,可 用氨 气处 理氮 氧化 物
C.可 加热 NH4NO3和 Ca(O H)2制备 氨气
D.联 氨 (N2H4)可能 被亚 硝酸 (HN O2) 氧化 生成 氢叠 氮酸 HN3
9 . 一 种 具 有 高 能 量 比 的 新 型 干 电 池 示 意 图 如 图 所 示 , 石 墨 电 极 区 发 生 的 电 极 反 应 为 :
- -
MnO2+e + H2O===MnO(OH ) +OH 。该 装置 工作 时, 下列 叙述 正确 的是 ( )
- +
A. Al 电极 区的 电极 反应 式: Al - 3e + 3NH3?H2O ===Al(O H)3↓+ 3NH4
B.石 墨电 极上 的电 势比 Al 电极 上的 低
C.每 消耗 27 g Al ,有 3 mol 电子 通过 溶液 转移 到石 墨电 极上
D.若 采用 “ 食盐 水+ NaOH 溶液 ” 作电 解质 溶液 ,电 极反 应式 相同
10 . 利 用 NO 、 O2和 Na2CO3溶 液 反 应 制 备 NaNO2的 装 置 如 图 所 示 , 下 列 关 于 该 装 置 的
描述 不正 确的 是( )
A.装 置 A 分液 漏斗 中的 药品 选用 不当 ,应 选用 稀 HNO3
B.实 验过 程中 ,通 过控 制分 液漏 斗的 活塞 控制 气流 速度
C.装 置 C 中发 生反 应的 化学 方程 式为 :2Na2CO3+4NO +O2===4NaNO2+ 2CO2
D.实 验过 程中 ,装 置 C 液面 上方 可能 出现 红棕 色气 体
11. 由一 种阳 离子 与两 种酸 根离 子组 成的 盐称 为混 盐。 混盐 Na4S2O3在酸 性条 件下 可以 产
生 S 。下 列关 于混 盐 Na4S2O3的有 关判 断不 正确 的是 ( )
A.该 混盐 与稀 硫酸 反应 产生 1mol S 时转 移 2NA个电 子
B.该 混盐 在酸 性条 件下 可以 产生 S 的原 因是 发生 了复 分解 反应
C .该 混盐 溶液 中加 入 BaCl2溶液 ,可 以生 成白 色沉 淀
D.该 混盐 中的 硫元 素的 化合 价为 - 2 和+ 4
12. 十九 大报 告指 出: “坚持 全民 共治 、源 头防 治, 持续 实施 大气 污染 防治 行动 ,打 赢蓝
天保 卫战 !” ,以 NOx和燃 煤为 主的 污染 综合 治理 是当 前重 要的 研究 课题 。CO 与 N2O 是
+
汽车 尾气 中污 染大 气的 成分 ,研 究表 明 CO 与 N2O 在 Fe 作用 下生 成无 害气 体, 发生 反应
+ +
的能 量变 化及 反应 历程 如图 所示 ,两 步反 应分 别为 :① N2O+Fe = N2+FeO (慢 );②
+ +
FeO +CO = CO2+Fe ( 快) 。下 列说 法不 正确 的是 ( )
A.反 应 ①是氧 化还 原反 应, 反应 ② 是非 氧化 还原 反应
B.两 步反 应均 为放 热反 应, 总反 应的 化学 反应 速率 由反 应① 决定
+ +
C. Fe 能使 反应 进行 的更 容易 ,FeO 是中 间产 物
D.若 转移 1 mol 电子 ,则 消耗 标况 下 11.2 L N2O
第Ⅱ 卷( 共 64 分)
13. (19 分) 现有 下列 短周 期元 素性 质的 有关 数据 :
元素 编号 a b c d e f g h
0.03 0.07 0.07 0.08 0.10 0.14 0.15 0.18
原子 半径 /nm 7 1 5 2 2 3 2 6
最高 化合 价或 最底 + 1 - 1 - 3 + 3 -2 +3 +1 +1
(1)根据元素周期律确定a至h 8种元素在周期表中的位置,将它们的元素编号填入下
表相应的空格内。
Ⅰ Ⅱ Ⅲ Ⅴ
Ⅳ族 Ⅵ族 Ⅶ族 Ⅷ族
族 族 族 族
第一 周期
第二 周期
第三 周期
(2)上述元素形成的常见氢化物中,分子间存在氢键的有(填氢化物的化学
式) 。
(3)氢化铝锂(LiAlH4)是一种易燃易爆具有极强还原性的物质,它在有机合成上应用广
泛。在125℃时氢化铝锂分解为氢气、金属铝及氢化锂(LiH)。与氢化铝锂性质相似但
较为温和的还原剂由上述a、d、h三种元素组成,请画出这种还原剂的电子式。
写出该物质受热分解的反应方程
式 。
(4)在元素周期表中,相邻近的元素在结构和性质上有许多相似之处。第二周期的碳、
氮、氧、氟都可以形成氢化物,氧元素的氢化物除H2O外,还有H2O2;碳元素的氢化物
除CH4外,还有C2H6等;与之相似的氮元素的氢化物除NH3外,还有________(填化学
式),其沸点比液氨_______(填“高”或“低”),稳定性比氨_______(填“好”或
“差”),该氢化物与足量盐酸反应的化学方程式为
___________________________________________________。
14.(9分)
?1
(1)①已知:C H ( g ) H O ( g ) C O ( g ) 3H ( g ) H 2 0 6 .2 k J mo l4 ? ??? ? ? ? ? ?2 2
?1
C H ( g ) C O ( g ) 2 C O ( g ) 2 H ( g ) H 2 4 7 .4 k J mo l4 ? ??? ? ? ? ? ?2 2
则C H ( g )4 与H O ( g )2 反应 生成C O ( g )2 和H ( g )2 的热 化学 方程 式为
_____ _____ ____ _____ ____ _____ ____ _____ ____ _____ ____ _____ ____ _____ ____ _____ 。
? ? - - -
(2 )一 定条 件下 ,在 水溶 液中 所含 离子C l 、C lO 、ClO2、C lO3、C lO4各1mol,其
相对 能量 的大 小如 下图 所示 (各离 子在 图中 用氯 元素 的相 应化 合价 表示 ),
- - - ?
则反 应3 C lO (aq )= = = C lO (aq )+ 2 C l (aq ) 1
3 的ΔH=_____ ___k J m o l? 。
(3 )工 业上 可通 过天 然气 跟水 蒸气 反应 制取 H2: CH4(g)+H2O(g) CO( g)+3H2(g),
有关 反应 的能 量变 化如 下图 所示 ,则 该反 应的 ?H=__ _____ ____ _____ __kJ/ mol ( 用含 a、b、
c 的式 子表 示 )。
15. (10 分) 本学 期天 津一 中化 学学 科为 了落 实国 家五 育并 举、 天津 市垃 圾分 类条 列、
着重 培养 学生 的核 心素 养, 在化 学组 各位 老师 的帮 助下 小艾 老师 做了 《废 旧干 电池 的回 收
再利 用》 展示 课, 废弃 物的 综合 利用 既有 利于 节约 资源 ,又 有利 于保 护环 境, 在课 上老 师
带着 学生 们拆 解电 池并 对炭 包中 的物 质设 计实 验并 分离 提纯 、再 利用 。下 面是 实验 室利 用
废弃 旧电 池的 铜帽 (Zn、 Cu 总含 量约 为 99%) 回收 铜并 制备 ZnO 的部 分实 验过 程如 下, 请
同学 们回 答相 关问 题:
(1 )① 铜帽 溶解 时加 入 H2O2的目 的是 _____ _____ ____ _____ ____ _____ ____ _( 用化 学方 程式 表
示) 。
② 铜帽 溶解 后需 将溶 液中 过量 H2O2除去 。除 去 H2O2的简 便方 法是
_____ _____ ____ _____ __。
(2 )为 确定 加入 锌灰 (主要 成分 为 Zn、 ZnO,杂 质为 铁及 其氧 化物 ) 含量 ,实 验中 需测 定
2+ 2+
除去 H2O2后溶 液中 Cu 的含 量。 实验 操作 为: 准确 量取 一定 体积 的含 有 Cu 的溶 液于
带塞 锥形 瓶中 ,加 适量 水稀 释, 调节 pH=3~ 4,加 入过 量 KI,用 Na2S2O3标准 溶液 滴定
至终 点。
2+ - 2- -
上述 过程 中的 离子 方程 式如 下: 2Cu + 4I =2CuI( 白色 )↓+I2、 I2+2S2O3 =2I+
2-
S4O6
① 滴定 选用 的指 示剂 为_____ _____ _ ,滴 定终 点观 察到 的现 象为 ______ _____ ____ __。
2+
② 若滴 定前 溶液 中 H2O2没有 除尽 ,所 测定 的 Cu 的含 量将 会 _____ _____ _( 填“ 偏高 ”
“偏低 ”“ 不变 ” )。
16. (10 分) 海洋 是生 命的 摇篮 ,海 水不 仅是 宝贵 的水 资源 ,而 且蕴 藏着 丰富 的化 学资
源。 从海 水中 提取 淡水 和一 些重 要的 化工 产品 的工 艺流 程如 图所 示。
根据 上述 流程 图回 答下 列问 题:
(1 )写 出反 应① 的化 学反 应方 程式 ______ _____ ____ _____ ____ _____ ____ _____ _。
(2 )工 业上 完成 MgCl2→ Mg 常用 的冶 炼方 法_____ _____ _ 。
(3 )通 入热 空气 或水 蒸气 吹出 Br2,利 用了 溴的 _____ _____ (填序 号 )。
A.氧 化性 B.还 原性 C .挥 发性 D .腐 蚀性
(4 )写 出步 骤 II 反应 的离 子方 程式 _____ _____ ____ _____ ____ _____ ____ _____ ____ _____ ____ _ 。
(5 )从 海水 中获 得淡 水的 主要 方法 有电 渗析 法、 离子 交换 法和 ______ _____ (填一 种 )。
(6 )实 验室 模拟 海水 蒸馏 法制 取淡 水, 蒸馏 过程 中不 可能 用到 的仪 器有 ______ __( 填序
号) 。
A.圆 底烧 瓶 B.容 量瓶 C.直 形冷 凝管 D.接 收器
(7 )离 子交 换法 净化 水的 过程 如图 所示 。下 列说 法正 确的 是_____ _____ (填序 号 )。
A.经 过阳 离子 交换 树脂 后, 水中 阳离 子总 数减 少
2-
B.通 过阴 离子 交换 树脂 后, 水中 只有 SO4 被除 去
C.通 过净 化处 理后 的水 ,导 电性 增强
+ -
D.阴 离子 交换 树脂 填充 段存 在反 应: H +OH =H2O
17 .( 16 分 ) 四 氯 化 锡 (SnC l4) 是 合 成 有 机 锡 化 合 物 的 原 料 , 其 熔 点 为 - 33 ℃ , 沸 点 为
114 ℃ , 在 潮 湿 的 空 气 中 强 烈 水 解 产 生 有 刺 激 性 的 白 色 烟 雾 , 产 物 之 一 为 SnO2。 实 验 室
制 备 四 氯 化 锡 的 操 作 是 : 将 金 属 锡 熔 融 , 然 后 泼 入 冷 水 , 制 成 锡 花 ; 将 干 燥 的 锡 花 加 入 反
应器 中, 再向 反应 器中 缓慢 地通 入干 燥的 氯气 。( 装置 C 中的 试剂 X 未画 出 )
Ⅰ. 图 1 为实 验室 制备 干燥 氯气 的实 验装 置(夹持 装置 已略 )
(1 ) 该装 置 制 备氯 气 选 用的 药 品 为漂 粉 精 固体 [ 主 要成 分 Ca( ClO )2] 和 浓盐 酸 ,A 中 发生 反
应的 化学 方程 式为 _____ _____ ____ _____ ____ _____ ____ _____ _。
(2 )装 置 B 的饱 和食 盐水 能够 除去 Cl2中的 HC l,此 外装 置 B 还有 _____ _____ 作用 。
(3 )试 剂 X 可能 为 ______ ____( 填标 号 )。
A.无 水氯 化钙 B.浓 硫酸
C.五 氧化 二磷 D.碱 石灰
(4 )用 锡花 代替 锡粒 的目 的是 ______ _____ ____ _____ ____ _____ ____ _____ 。
(5 )四 氯化 锡在 潮湿 空气 中水 解的 化学 方程 式为 ______ _____ ____ _____ ____ _____ ___ 。
Ⅱ. 图 2 是蒸 馏 SnCl4的装 置
(6 )该 装置 尚有 两处 不当 之处 ,它 们分 别是
_____ _____ ____ _____ ____ _____ ____ _____ _、_____ _____ ____ _____ ____ _____ ____ _____ ___ 。
(7 )实 验用 的锡 花中 含有 金属 铜。 某同 学设 计下 列实 验测 定锡 花的 纯度 :
第一 步: 称取 7.500 g 锡花 溶于 足量 稀硫 酸中 ,充 分反 应后 过滤 ;
2+ 4+
第二 步: 向滤 液中 加入 过量 Fe2(SO4)3,将 生成 的 Sn 氧化 成 Sn ;
-1 2+
第三 步: 用 0.950 0 mol ?L 的 K2Cr2O7溶液 滴定 生成 的 Fe ,
2+ 2- + 3+ 3+
发生 反应 的方 程式 为 Fe +Cr2O7 +H ―→ Cr + Fe +H2O( 未配 平)
若达 到滴 定终 点时 共消 耗 21.00 mL K2Cr2O7溶液 ,
试计 算锡 花中 锡的 百分 含量 :_____ _____ ( 结果 保留 4 位有 效数 字)。
参考 答案
1 2 3 4 5 6 7 8 9 10 11 12
D B C C C B D C A A A A
13.
(1)
(2 )HF 、 NH3
+ -
(3 )Na [ ] ;2NaBH4 2NaH +2B +3H2↑
(4 )N2H4, 高, 差, N2H4+ 2HC l→ N2H6Cl2。
14.
?1
(1 )C H ( g ) 2 H O ( g ) C O ( g ) 4 H ( g ) ΔH= 1 6 5 k J mo l4 ? ? ? ? ?2 2 2 ? ? ;
(2 )-117
?1
?
(3 )( a +3b-c ) kJ mol
15. Cu +H2O2+H2SO4=CuSO4+ 2H2O ;加 热(至沸 );淀 粉溶 液; 蓝色 褪去 ;偏 高。
16.
(1 )2NaC l +2H2O电解2NaO H + H2↑+ Cl2↑;
(2 )电 解;
(3 )C ;
+ 2— —
(4 )Br2+SO2+2H2O=4H +SO4 +2Br ;
(5 )蒸 馏法 ;
(6 )B;
(7 )D
17.
(1 )Ca( ClO )2+4HC l( 浓 ) =加热= CaC l2+ 2Cl2↑+2H2O;
(2 )安 全瓶 ;
(3 )AC;
(4 )增 大与 氯气 的接 触面 积, 加快 反应 速率 ;
(5 )SnCl4+ 2H2O ===SnO2+ 4HC l;
(6 )温 度计 水银 球位 置不 对, Ⅱ和 Ⅲ之间 缺少 干燥 装置 ;
(7 )94.96 %。
同课章节目录
