乙酸课件
图片预览




文档简介
(共18张PPT)
乙酸是日常生活中的常见物质,我们常用的调味品食醋,其主要成分就是乙酸,因此乙酸又叫醋酸,普通醋含醋酸3%~5%,山西陈醋含醋酸7%。
颜色、状态:
无色液体
气味:
有强烈刺激性气味
沸点:
117.9℃ (低,易挥发)
熔点:
16.6℃
因此,无水乙酸又称为冰醋酸。
溶解性:
易溶于水、乙醇等溶剂
说明:在室温较低时,无水乙酸就会凝结成像冰一样的晶体。
一、乙酸的物理性质
二、分子组成与结构
或 —COOH
C2H4O2
分子式
CH3COOH
结构简式
CH3 —C—OH
O
‖
或
官能团
—C—OH
O
‖
羧基
(—CO2H)
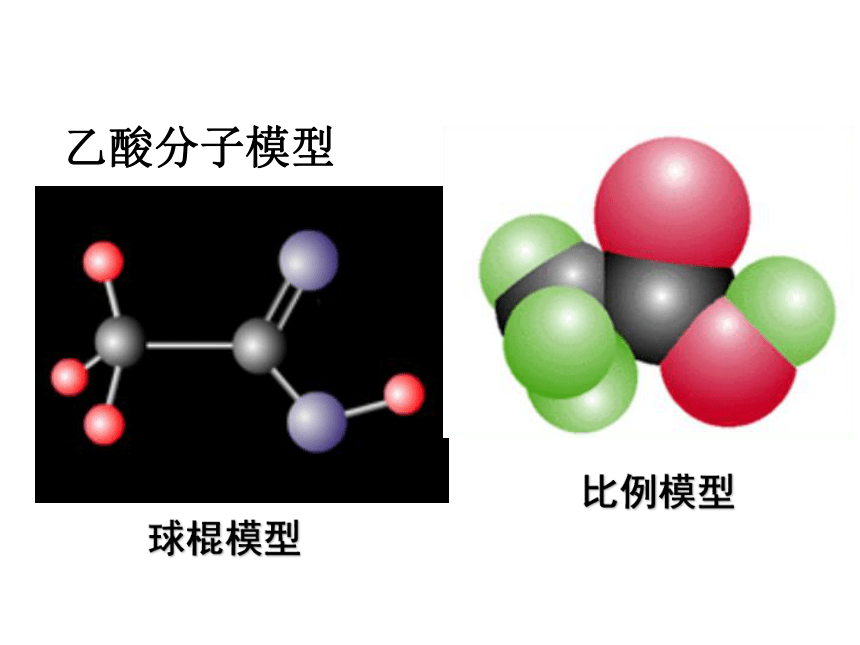
乙酸分子模型
球棍模型
比例模型
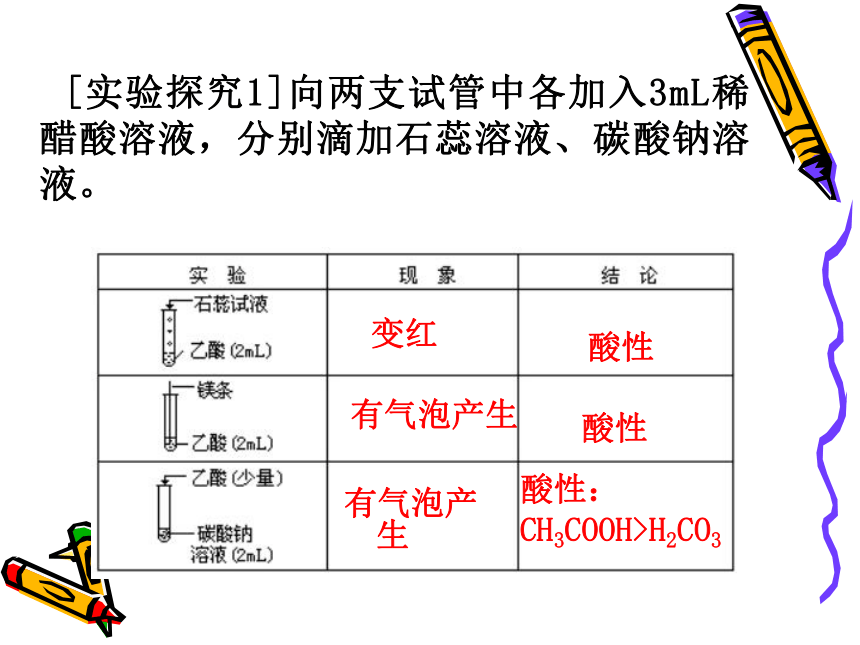
[实验探究1]向两支试管中各加入3mL稀醋酸溶液,分别滴加石蕊溶液、碳酸钠溶液。
变红
有气泡产生
酸性: CH3COOH>H2CO3
有气泡产生
酸性
酸性
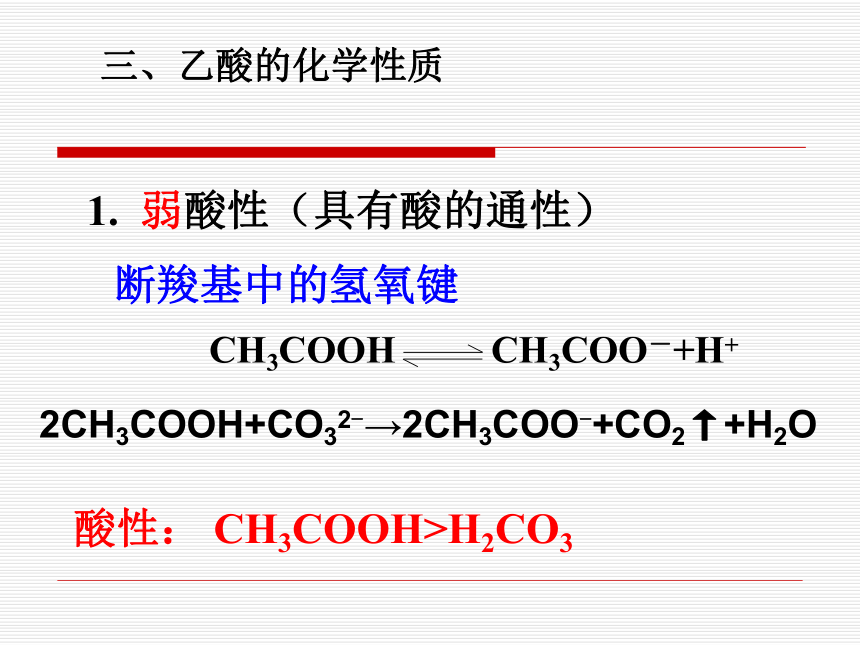
CH3COOH CH3COO-+H+
三、乙酸的化学性质
1. 弱酸性(具有酸的通性)
2CH3COOH+CO32-→2CH3COO-+CO2↑+H2O
断羧基中的氢氧键
酸性: CH3COOH>H2CO3
【实验探究2】在1支大试管中加入两小块碎瓷片、3mL乙醇,然后边摇动边慢慢加入2mL浓硫酸和2mL冰醋酸;连接好装置。用酒精灯缓慢,将产生的蒸气经导管通到饱和碳酸钠溶液的液面上。按教材上的装置(制乙酸乙酯的装置)组装好。注意组装顺序,导管口不能伸入饱和碳酸钠液面下。装有碳酸钠的试管里有什么变化?生成新物质的色、态、味怎样?
实验现象:
实验结论:
饱和碳酸钠溶液的液面上有透明的油状液体产生,并可闻到香味。
在浓硫酸存在、加热的条件下,乙酸和乙醇发生反应,生成无色透明、不溶于水、有香味的油状液体。该油状液体是乙酸乙酯。该反应是可逆反应。
问题:
1.装药品的顺序如何?
2.浓硫酸的作用是什么?
3.得到的反应产物是否纯净?主要杂质有哪些?
4.饱和Na2CO3溶液有什么作用?
5.为什么导管不插入饱和Na2CO3溶液中?
1.浓硫酸应最后加入。
2.催化剂、吸水剂。
3.不纯净。还含乙醇、乙酸。
4.
5.防止倒吸。
a. 溶解乙醇
b. 吸收乙酸
c. 乙酸乙酯的溶解度小,有利于析出。
交流与讨论:
2、酯化反应
CH3COOH + C2H5OH CH3COOC2H5+H2O
定义:酸和醇作用,生成酯和水的反应叫做酯化反应。
乙酸乙酯
探究酯化反应可能的脱水方式
可能一
可能二
酯化反应的历程
实质:酸脱羟基醇脱氢。
方法:同位素示踪法----研究有机反应机理常用的方法
知识延伸:形成酯的酸可以是有机酸也可以是无机含氧酸。
O O
CH3C—OH+H OC2H5 CH3C—OC2H5 + H2O
浓H2SO4
‖
‖
18
18
O
O
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。
教你下厨
小知识:乙酸的用途
乙酸是一种重要的有机化工原料,可用于生产醋酸纤维、合成纤维、喷漆溶剂、香料、燃料、医药和农药等。
O
CH3—C—O—H
酸性
酯化反应
小结:
乙酸发生化学变化时的断键位置:
乙酸是日常生活中的常见物质,我们常用的调味品食醋,其主要成分就是乙酸,因此乙酸又叫醋酸,普通醋含醋酸3%~5%,山西陈醋含醋酸7%。
颜色、状态:
无色液体
气味:
有强烈刺激性气味
沸点:
117.9℃ (低,易挥发)
熔点:
16.6℃
因此,无水乙酸又称为冰醋酸。
溶解性:
易溶于水、乙醇等溶剂
说明:在室温较低时,无水乙酸就会凝结成像冰一样的晶体。
一、乙酸的物理性质
二、分子组成与结构
或 —COOH
C2H4O2
分子式
CH3COOH
结构简式
CH3 —C—OH
O
‖
或
官能团
—C—OH
O
‖
羧基
(—CO2H)
乙酸分子模型
球棍模型
比例模型
[实验探究1]向两支试管中各加入3mL稀醋酸溶液,分别滴加石蕊溶液、碳酸钠溶液。
变红
有气泡产生
酸性: CH3COOH>H2CO3
有气泡产生
酸性
酸性
CH3COOH CH3COO-+H+
三、乙酸的化学性质
1. 弱酸性(具有酸的通性)
2CH3COOH+CO32-→2CH3COO-+CO2↑+H2O
断羧基中的氢氧键
酸性: CH3COOH>H2CO3
【实验探究2】在1支大试管中加入两小块碎瓷片、3mL乙醇,然后边摇动边慢慢加入2mL浓硫酸和2mL冰醋酸;连接好装置。用酒精灯缓慢,将产生的蒸气经导管通到饱和碳酸钠溶液的液面上。按教材上的装置(制乙酸乙酯的装置)组装好。注意组装顺序,导管口不能伸入饱和碳酸钠液面下。装有碳酸钠的试管里有什么变化?生成新物质的色、态、味怎样?
实验现象:
实验结论:
饱和碳酸钠溶液的液面上有透明的油状液体产生,并可闻到香味。
在浓硫酸存在、加热的条件下,乙酸和乙醇发生反应,生成无色透明、不溶于水、有香味的油状液体。该油状液体是乙酸乙酯。该反应是可逆反应。
问题:
1.装药品的顺序如何?
2.浓硫酸的作用是什么?
3.得到的反应产物是否纯净?主要杂质有哪些?
4.饱和Na2CO3溶液有什么作用?
5.为什么导管不插入饱和Na2CO3溶液中?
1.浓硫酸应最后加入。
2.催化剂、吸水剂。
3.不纯净。还含乙醇、乙酸。
4.
5.防止倒吸。
a. 溶解乙醇
b. 吸收乙酸
c. 乙酸乙酯的溶解度小,有利于析出。
交流与讨论:
2、酯化反应
CH3COOH + C2H5OH CH3COOC2H5+H2O
定义:酸和醇作用,生成酯和水的反应叫做酯化反应。
乙酸乙酯
探究酯化反应可能的脱水方式
可能一
可能二
酯化反应的历程
实质:酸脱羟基醇脱氢。
方法:同位素示踪法----研究有机反应机理常用的方法
知识延伸:形成酯的酸可以是有机酸也可以是无机含氧酸。
O O
CH3C—OH+H OC2H5 CH3C—OC2H5 + H2O
浓H2SO4
‖
‖
18
18
O
O
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。
教你下厨
小知识:乙酸的用途
乙酸是一种重要的有机化工原料,可用于生产醋酸纤维、合成纤维、喷漆溶剂、香料、燃料、医药和农药等。
O
CH3—C—O—H
酸性
酯化反应
小结:
乙酸发生化学变化时的断键位置:
