分子的立体结构1[1].3
文档属性
| 名称 | 分子的立体结构1[1].3 |

|
|
| 格式 | zip | ||
| 文件大小 | 76.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2012-04-25 00:00:00 | ||
图片预览





文档简介
(共20张PPT)
第三课时
第二节 分子的立体结构
例题一:下列分子中的中心原子杂化轨道的类型相同的是 ( )
A.CO2与SO2 B.CH4与NH3
C.BeCl2与BF3 D.C2H2与C2H4
例题二:对SO2与CO2说法正确的是( )
A.都是直线形结构
B.中心原子都采取sp杂化轨道
C. S原子和C原子上都没有孤对电子
D. SO2为V形结构, CO2为直线形结构
D
例题三:写出下列分子的路易斯结构式(是用短线表示键合电子,小黑点表示未键合的价电子的结构式)并指出中心原子可能采用的杂化轨道类型,并预测分子的几何构型。 (1)PCl3 (2)BCl3 (3)CS2 (4) C12O
(1) PCl3: SP3 三角锥形
. .
P
CI
CI
解析:
. .
. .
. .
..
..
..
CI
. .
. .
..
CI
. .
..
(2)BCl3 : SP2 平面三角形
B
CI
. .
. .
..
..
Cl
. .
. .
..
(3)CS2 : SP 直线形
C
=
S
=
S
. .
. .
. .
. .
(4) C12O: SP3 V形
O
. .
. .
Cl
. .
. .
..
CI
. .
. .
..
天蓝色
天蓝色
天蓝色
无色
无色
无色
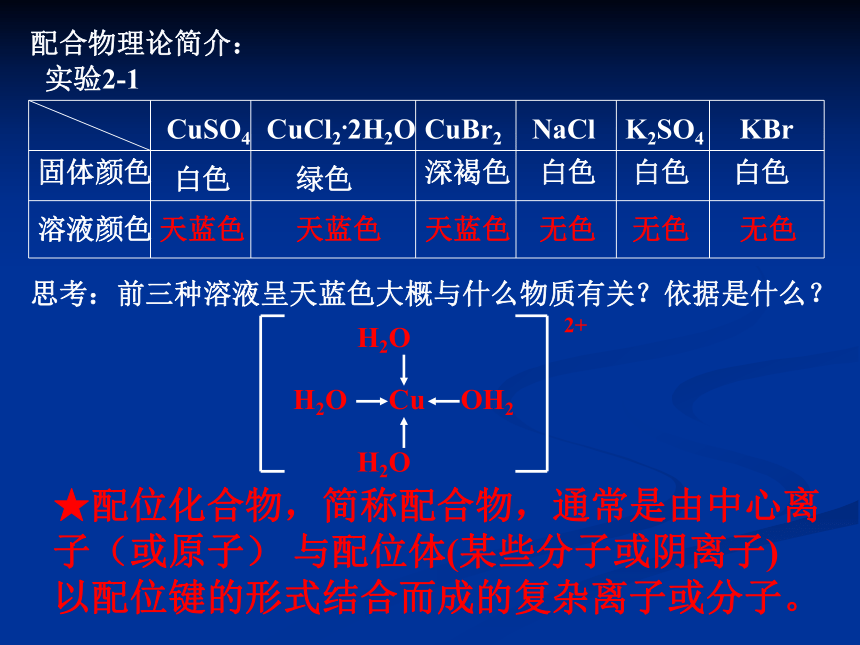
配合物理论简介:
实验2-1
固体颜色
溶液颜色
CuSO4
CuCl2.2H2O
CuBr2
NaCl
K2SO4
KBr
白色
绿色
深褐色
白色
白色
白色
思考:前三种溶液呈天蓝色大概与什么物质有关?依据是什么?
Cu
OH2
H2O
H2O
H2O
2+
★配位化合物,简称配合物,通常是由中心离子(或原子) 与配位体(某些分子或阴离子) 以配位键的形式结合而成的复杂离子或分子。
2+
Cu
NH3
H3N
NH3
NH3
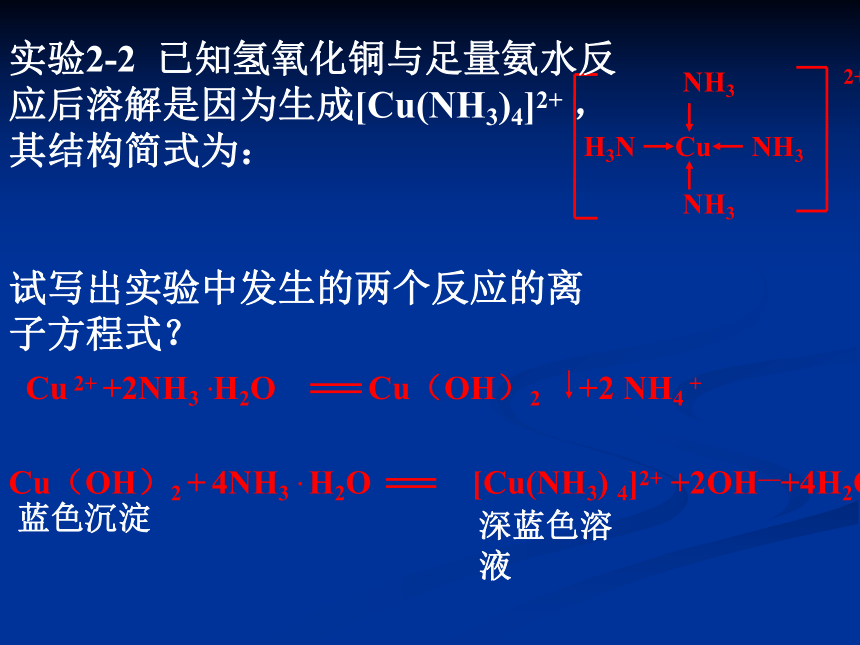
实验2-2 已知氢氧化铜与足量氨水反应后溶解是因为生成[Cu(NH3)4]2+ ,其结构简式为:
试写出实验中发生的两个反应的离子方程式?
Cu 2+ +2NH3 .H2O Cu(OH)2 +2 NH4 +
Cu(OH)2 + 4NH3 . H2O [Cu(NH3) 4]2+ +2OH—+4H2O
蓝色沉淀
深蓝色溶液
实验2-3
Fe 3+ +SCN— [Fe (SCN) ]2+
硫氰酸根
血红色
由于该离子的颜色极似血液,常被用于电影特技和魔术表演。
练习书写:
向硝酸银溶液中逐渐滴加氨水的离子方程式
配合物理论简介
一、配合物的组成
1. 中心离子或原子(也称形成体) 有空轨道
主要是一些过渡金属,如铁、钴、镍、铜、银、金、铂等金 属元素的离子;
或是具有高氧化数的非金属元素,硼,硅、磷等,如Na[BF4] 中的B(Ⅲ)、K2[SiF6]中的Si(Ⅳ)和NH4[PF6]中的P(Ⅴ);
或是不带电荷的中性原子,如[Ni(CO)4], [Fe(CO)5]中的Ni, Fe都是中性原子,
碱金属、碱土金属等可作为螯合物的形成体。
[Cu(NH3)4]SO4中,NH3是配位体,N为配位原子。
2. 配位体和配位原子 有孤对电子
a. 单齿配位体(一个配位体中只有一个配位原子)
含氮配位体 NH3 , NCS - ;含硫配位体 SCN- ;
含卤素配位体 F- , Cl- , Br- , I- ; 含碳配位体 CN- , CO
含氧配位体 H2O, OH- ,羧酸,醇,醚等
b. 多齿配位体(有两个或两个以上的配位原子)
乙二胺 NH2一CH2一CH2一NH2 简写为en,
乙二胺四乙酸根(EDTA)等。
3.配位数
与中心离子直接以配位键结合的配位原子个数。
例:[AlF6]3- 配位数6 、 [Cu(NH3)4]SO4 配位数4 、
[Co(NH3)2(en)2](NO3)3 配位数6
*中心离子的电荷高,对配位体的吸引力较强,有利于形成配位数较高的配合物。
常见的配位数与中心离子的电荷数有如下的关系:
中心离子的电荷:+1 +2 +3 +4
常见的配位数: 2 4(或6) 6(或4) 6(或8)
*中心离子半径越大,其周围可容纳配体就越多,
配位数越大。
[AlF6]3- [AlCl4]- [BF4]- [AgI2]- [AgI4]2-
从这些配离子你看出配位数有什么规律?
4. 配离子的电荷
配离子的电荷等于中心离子电荷与配位体总电荷的代数和。 如 K2[PtCl4]
8.1.2 配位化合物的命名
配位数—配位体名称—合—中心离子(用罗马数字表示氧化数),
用二、三、四等数字表示配位体数。不同配位名称之间用圆点“·”分开。 阴离子次序为:简单离子——复杂离子——有机酸根离子。
中性分子次序为:NH3—H2O—有机分子。
1.配位阴离子配合物--配位阴离子“酸”外界
2.配位阳离子配合物—— “某化某”或“某酸某”
3.中性配合物
K2[SiF6] 六氟合硅(Ⅳ)酸钾
K[PtCl5(NH3)] 五氯·一氨合铂(Ⅳ)酸钾
[Co(NH3)6]Br3 三溴化六氨合钴(Ⅲ)
[Co(NH3)2(en)2](NO3)3 硝酸二氨·二(乙二胺)合钴(Ⅲ)
[PtCl2(NH3)2] 二氯·二氨合铂(Ⅱ)
[Ni(CO)4] 四羰基合镍(0)
配合物的盐与复盐的比较
复盐, 能电离出两种或两种以上阳离子的盐如明矾 KAl(SO4)2·12H2O、光卤石 KCl · MgCl2· 6H2O等,仅在固态时稳定存在,一旦溶于水,几乎全部解离成各组分离子:
KAl(SO4)2·12H2O (溶于水) → K+ +Al3++ 2SO42- +12 H2O
KCl · MgCl2 · 6H2O (溶于水) → K+ +Mg2+ + 3Cl- + 6H2O
配合物盐,是在配合物的溶液或晶体中,十分明确地存在着 含有配位键的、能独立存在的复杂组成的离子:
[Cu(NH3)4]SO4·H2O → [Cu(NH3)4]2+ + SO42- + H2O
形成配合物时性质的改变
1、颜色的改变
Fe3+ + nNCS- == [Fe(NCS)n](n-3)-
2、溶解度的改变:
AgCl + HCl =[AgCl2]- + H+
AgCl + 2NH3 == [Ag(NH3)2]+ + Cl-
Au + HNO3 + 4HCl == H[AuCl4] + NO + 2H2O
3Pt + 4HNO3 + 18HCl = 3H2[PtCl6] + 4NO + 8H2O
例题一:下列分子或离子中都存在着配位键的是 ( )
A.NH3、H2O B.NH4 + 、H3O+
C.N2、HClO D. [Cu(NH3) 4]2+ 、PCI3
B
例题二:下列各种说法中错误的是( )
A、形成配位键的条件是一方有空轨道一方有孤对电子。
B、配位键是一种特殊的共价键。
C、配位化合物中的配体可以是分子也可以是阴离子。
D、共价键的形成条件是成键原子必须有未成对电子。
D
第三课时
第二节 分子的立体结构
例题一:下列分子中的中心原子杂化轨道的类型相同的是 ( )
A.CO2与SO2 B.CH4与NH3
C.BeCl2与BF3 D.C2H2与C2H4
例题二:对SO2与CO2说法正确的是( )
A.都是直线形结构
B.中心原子都采取sp杂化轨道
C. S原子和C原子上都没有孤对电子
D. SO2为V形结构, CO2为直线形结构
D
例题三:写出下列分子的路易斯结构式(是用短线表示键合电子,小黑点表示未键合的价电子的结构式)并指出中心原子可能采用的杂化轨道类型,并预测分子的几何构型。 (1)PCl3 (2)BCl3 (3)CS2 (4) C12O
(1) PCl3: SP3 三角锥形
. .
P
CI
CI
解析:
. .
. .
. .
..
..
..
CI
. .
. .
..
CI
. .
..
(2)BCl3 : SP2 平面三角形
B
CI
. .
. .
..
..
Cl
. .
. .
..
(3)CS2 : SP 直线形
C
=
S
=
S
. .
. .
. .
. .
(4) C12O: SP3 V形
O
. .
. .
Cl
. .
. .
..
CI
. .
. .
..
天蓝色
天蓝色
天蓝色
无色
无色
无色
配合物理论简介:
实验2-1
固体颜色
溶液颜色
CuSO4
CuCl2.2H2O
CuBr2
NaCl
K2SO4
KBr
白色
绿色
深褐色
白色
白色
白色
思考:前三种溶液呈天蓝色大概与什么物质有关?依据是什么?
Cu
OH2
H2O
H2O
H2O
2+
★配位化合物,简称配合物,通常是由中心离子(或原子) 与配位体(某些分子或阴离子) 以配位键的形式结合而成的复杂离子或分子。
2+
Cu
NH3
H3N
NH3
NH3
实验2-2 已知氢氧化铜与足量氨水反应后溶解是因为生成[Cu(NH3)4]2+ ,其结构简式为:
试写出实验中发生的两个反应的离子方程式?
Cu 2+ +2NH3 .H2O Cu(OH)2 +2 NH4 +
Cu(OH)2 + 4NH3 . H2O [Cu(NH3) 4]2+ +2OH—+4H2O
蓝色沉淀
深蓝色溶液
实验2-3
Fe 3+ +SCN— [Fe (SCN) ]2+
硫氰酸根
血红色
由于该离子的颜色极似血液,常被用于电影特技和魔术表演。
练习书写:
向硝酸银溶液中逐渐滴加氨水的离子方程式
配合物理论简介
一、配合物的组成
1. 中心离子或原子(也称形成体) 有空轨道
主要是一些过渡金属,如铁、钴、镍、铜、银、金、铂等金 属元素的离子;
或是具有高氧化数的非金属元素,硼,硅、磷等,如Na[BF4] 中的B(Ⅲ)、K2[SiF6]中的Si(Ⅳ)和NH4[PF6]中的P(Ⅴ);
或是不带电荷的中性原子,如[Ni(CO)4], [Fe(CO)5]中的Ni, Fe都是中性原子,
碱金属、碱土金属等可作为螯合物的形成体。
[Cu(NH3)4]SO4中,NH3是配位体,N为配位原子。
2. 配位体和配位原子 有孤对电子
a. 单齿配位体(一个配位体中只有一个配位原子)
含氮配位体 NH3 , NCS - ;含硫配位体 SCN- ;
含卤素配位体 F- , Cl- , Br- , I- ; 含碳配位体 CN- , CO
含氧配位体 H2O, OH- ,羧酸,醇,醚等
b. 多齿配位体(有两个或两个以上的配位原子)
乙二胺 NH2一CH2一CH2一NH2 简写为en,
乙二胺四乙酸根(EDTA)等。
3.配位数
与中心离子直接以配位键结合的配位原子个数。
例:[AlF6]3- 配位数6 、 [Cu(NH3)4]SO4 配位数4 、
[Co(NH3)2(en)2](NO3)3 配位数6
*中心离子的电荷高,对配位体的吸引力较强,有利于形成配位数较高的配合物。
常见的配位数与中心离子的电荷数有如下的关系:
中心离子的电荷:+1 +2 +3 +4
常见的配位数: 2 4(或6) 6(或4) 6(或8)
*中心离子半径越大,其周围可容纳配体就越多,
配位数越大。
[AlF6]3- [AlCl4]- [BF4]- [AgI2]- [AgI4]2-
从这些配离子你看出配位数有什么规律?
4. 配离子的电荷
配离子的电荷等于中心离子电荷与配位体总电荷的代数和。 如 K2[PtCl4]
8.1.2 配位化合物的命名
配位数—配位体名称—合—中心离子(用罗马数字表示氧化数),
用二、三、四等数字表示配位体数。不同配位名称之间用圆点“·”分开。 阴离子次序为:简单离子——复杂离子——有机酸根离子。
中性分子次序为:NH3—H2O—有机分子。
1.配位阴离子配合物--配位阴离子“酸”外界
2.配位阳离子配合物—— “某化某”或“某酸某”
3.中性配合物
K2[SiF6] 六氟合硅(Ⅳ)酸钾
K[PtCl5(NH3)] 五氯·一氨合铂(Ⅳ)酸钾
[Co(NH3)6]Br3 三溴化六氨合钴(Ⅲ)
[Co(NH3)2(en)2](NO3)3 硝酸二氨·二(乙二胺)合钴(Ⅲ)
[PtCl2(NH3)2] 二氯·二氨合铂(Ⅱ)
[Ni(CO)4] 四羰基合镍(0)
配合物的盐与复盐的比较
复盐, 能电离出两种或两种以上阳离子的盐如明矾 KAl(SO4)2·12H2O、光卤石 KCl · MgCl2· 6H2O等,仅在固态时稳定存在,一旦溶于水,几乎全部解离成各组分离子:
KAl(SO4)2·12H2O (溶于水) → K+ +Al3++ 2SO42- +12 H2O
KCl · MgCl2 · 6H2O (溶于水) → K+ +Mg2+ + 3Cl- + 6H2O
配合物盐,是在配合物的溶液或晶体中,十分明确地存在着 含有配位键的、能独立存在的复杂组成的离子:
[Cu(NH3)4]SO4·H2O → [Cu(NH3)4]2+ + SO42- + H2O
形成配合物时性质的改变
1、颜色的改变
Fe3+ + nNCS- == [Fe(NCS)n](n-3)-
2、溶解度的改变:
AgCl + HCl =[AgCl2]- + H+
AgCl + 2NH3 == [Ag(NH3)2]+ + Cl-
Au + HNO3 + 4HCl == H[AuCl4] + NO + 2H2O
3Pt + 4HNO3 + 18HCl = 3H2[PtCl6] + 4NO + 8H2O
例题一:下列分子或离子中都存在着配位键的是 ( )
A.NH3、H2O B.NH4 + 、H3O+
C.N2、HClO D. [Cu(NH3) 4]2+ 、PCI3
B
例题二:下列各种说法中错误的是( )
A、形成配位键的条件是一方有空轨道一方有孤对电子。
B、配位键是一种特殊的共价键。
C、配位化合物中的配体可以是分子也可以是阴离子。
D、共价键的形成条件是成键原子必须有未成对电子。
D
