2.3.1 氧化还原反应(鲁科版必修1)
图片预览











文档简介
(共46张PPT)
第3节 氧化剂和还原剂
第1课时 氧化还原反应
一、氧化还原反应
1.定义
(1)从是否有氧得失角度来看:__________的反 应是氧化还原反应。
(2)从化合价的变化角度来看:反应前后______ ____________的反应是氧化还原反应。
有得氧失氧
有元素
的化合价变化
(3)从电子的转移(得失与偏移)的角度来看: ___________的反应是氧化还原反应。
2.特征:反应前后________________。
3.本质:___________。
4.电子转移的表示方法
有电子转移
有化合价的变化
有电子转移
(1)双线桥法
表示________________________________的情 况。如CO与Fe2O3的反应表示为:
__________________________
同种元素的原子在反应前后转移电子
(2)单线桥法
在反应物之间用桥的形式表达出不同元素得失 电子的情况。如Zn和Cu2+的反应表示为:
_____________________。
二、相关概念
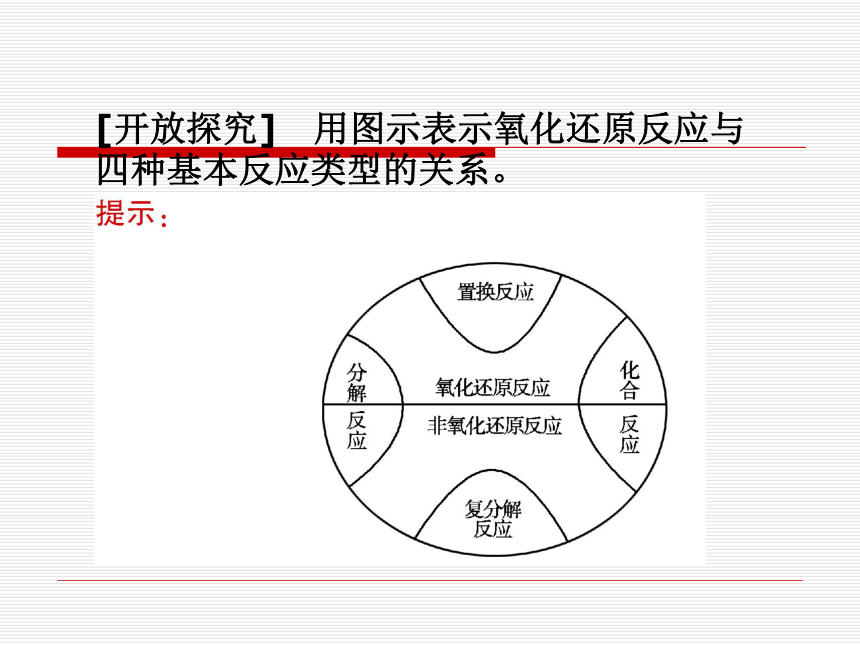
[开放探究] 用图示表示氧化还原反应与四种基本反应类型的关系。
解析: 要判断一个反应是否属于氧化还原反应,就看反应前后是否有元素的化合价发生改变。
答案: C
解析:A项中S元素的化合价保持+6价不变;B项中S元素的化合价由+6降低为+4;C项反应属于复分解反应,S元素的化合价不变;D项中S元素化合价由0升高为+4。
答案:D
3.下列叙述正确的是( )
A.氧化还原反应的本质是化合价发生了变化
B.化合价升高的物质被氧化
C.得到电子的物质被氧化
D.氧化还原反应中,先有氧化后有还原
解析:氧化还原反应的本质是有电子转移;化合价升高的物质失去电子被氧化,B项正确;得到电子的物质化合价降低被还原,而非被氧化;氧化还原反应中,氧化与还原同时相伴发生,没有先后,有氧化必同时有还原。
答案:B
一、氧化还原反应中电子转移的表示方法
步骤:一标变价,二画线桥,三注得失电子数。
1.双线桥法
表明同一元素原子得到或失去电子的情况。
(1)箭头必须由反应物指向生成物,且两端对准同种元素。
(2)在“桥”上标明电子“得到”与“失去”,且得到与失去的电子总数必须相等,电子对的偏移也按得失处理。
(3)电子转移数以a×be-形式表示,a表示发生氧化还原反应的原子个数,b表示每个原子得到或失去的电子数,当a=1或b=1时,要省略。
例如:CuO+COC得到2e-u+C失去2e-O2
(4)箭头方向不代表电子转移的方向,仅表示电子转移前后的变化。
2.单线桥法
表明不同元素原子间得到或失去电子的情况,箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标“得”、“失”字样。
(1)单线桥必须画在反应物中。
(2)箭头指向得电子元素,箭尾指向失电子元素。
(3)不需要写“失去”、“得到”。
(1)对于同一个氧化还原反应,无论是用双线桥法还是用单线桥法表示电子转移情况,其数目是不变的。
(2)反应中,电子转移数目=氧化剂得到电子数目=还原剂失去电子数目,不要误认为电子转移的数目是反应中得、失电子数目的加和。
思路点拨: 解答本题要从以下三点入手:
(1)首先正确标出各元素的化合价。
(2)再依据化合价的变化分析电子转移的方向和数目。
(3)注意要符合客观事实和氧化还原反应规律。
答案: A
规律方法: 同种元素反应规律
(1)歧化反应:相同价态的同种元素反应后一部分化合价升高,另一部分化合价降低的氧化还原反应。
(2)归中反应:不同价态的同种元素发生反应时,高价态降低,低价态升高的氧化还原反应。
说明:例1 D项违背了归中反应规律。
解析: n(Na2SO3)=0.3 L×0.1 mol·L-1=0.03 mol,Na2SO3被氧化为Na2SO4,化合价升高总数为[+6-(+4)]×0.03 mol;设X被还原后的价态为y,则化合价降低总数为(+5-y)×1.5×10-2 mol,由化合价升高总数等于降低总数:(6-4)×0.03=(5-y)×1.5×10-2,y=+1。
答案: C
二、氧化还原反应各概念间的关系
分析判断氧化还原反应中有关概念时,可借助以下口诀帮助解决:
升——失——氧(氧:氧化反应)
降——得——还(还:还原反应)
答案: D
2.(2011·岳阳高一质检)某元素在化学反应中,由化合态变为游离态,则该元素( )
A.一定被氧化
B.一定被还原
C.可能被氧化,也可能被还原
D.化合价降低为0
解析: 化合价既可能升高,如NaCl→Cl2;也可能降低,如Fe2O3→Fe。
答案: C
1.(2011·淮安高一质检)下列反应不属于氧化还原反应的是( )
A.3Cl2+6KOH===5KCl+KClO3+3H2O
B.2NO2+2NaOH===NaNO3+NaNO2+H2O
C.SnCl4+2H2O===SnO2+4HCl
D.2H2S+SO2===3S↓+2H2O
解析: A项中氯元素、B项中氮元素、D项中硫元素的化合价均有变化,C项中各元素的化合价均无变化,故C项不是氧化还原反应。
答案: C
2.(2011·杭州高一质检)下图为反应Fe+CuSO4 ===Cu+FeSO4中电子转移的关系图,则图中的元素甲、乙分别表示( )
A.Fe,S B.Cu,S
C.Fe,O D.Fe,Cu
解析: Fe与CuSO4反应,Fe失电子被氧化,+2价Cu得电子被还原。
答案: D
3.(2009·福建高考)下列类型的反应,一定发生电子转移的是( )
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
答案: C
解析: KClO3中氯为+5价,ClO2中氯为+4价,KClO3为氧化剂,H2C2O4中碳显+3价作还原剂,被氧化,1 mol KClO3得1 mol电子。
答案: D
第3节 氧化剂和还原剂
第1课时 氧化还原反应
一、氧化还原反应
1.定义
(1)从是否有氧得失角度来看:__________的反 应是氧化还原反应。
(2)从化合价的变化角度来看:反应前后______ ____________的反应是氧化还原反应。
有得氧失氧
有元素
的化合价变化
(3)从电子的转移(得失与偏移)的角度来看: ___________的反应是氧化还原反应。
2.特征:反应前后________________。
3.本质:___________。
4.电子转移的表示方法
有电子转移
有化合价的变化
有电子转移
(1)双线桥法
表示________________________________的情 况。如CO与Fe2O3的反应表示为:
__________________________
同种元素的原子在反应前后转移电子
(2)单线桥法
在反应物之间用桥的形式表达出不同元素得失 电子的情况。如Zn和Cu2+的反应表示为:
_____________________。
二、相关概念
[开放探究] 用图示表示氧化还原反应与四种基本反应类型的关系。
解析: 要判断一个反应是否属于氧化还原反应,就看反应前后是否有元素的化合价发生改变。
答案: C
解析:A项中S元素的化合价保持+6价不变;B项中S元素的化合价由+6降低为+4;C项反应属于复分解反应,S元素的化合价不变;D项中S元素化合价由0升高为+4。
答案:D
3.下列叙述正确的是( )
A.氧化还原反应的本质是化合价发生了变化
B.化合价升高的物质被氧化
C.得到电子的物质被氧化
D.氧化还原反应中,先有氧化后有还原
解析:氧化还原反应的本质是有电子转移;化合价升高的物质失去电子被氧化,B项正确;得到电子的物质化合价降低被还原,而非被氧化;氧化还原反应中,氧化与还原同时相伴发生,没有先后,有氧化必同时有还原。
答案:B
一、氧化还原反应中电子转移的表示方法
步骤:一标变价,二画线桥,三注得失电子数。
1.双线桥法
表明同一元素原子得到或失去电子的情况。
(1)箭头必须由反应物指向生成物,且两端对准同种元素。
(2)在“桥”上标明电子“得到”与“失去”,且得到与失去的电子总数必须相等,电子对的偏移也按得失处理。
(3)电子转移数以a×be-形式表示,a表示发生氧化还原反应的原子个数,b表示每个原子得到或失去的电子数,当a=1或b=1时,要省略。
例如:CuO+COC得到2e-u+C失去2e-O2
(4)箭头方向不代表电子转移的方向,仅表示电子转移前后的变化。
2.单线桥法
表明不同元素原子间得到或失去电子的情况,箭头由失电子原子指向得电子原子,线桥上只标电子转移的数目,不标“得”、“失”字样。
(1)单线桥必须画在反应物中。
(2)箭头指向得电子元素,箭尾指向失电子元素。
(3)不需要写“失去”、“得到”。
(1)对于同一个氧化还原反应,无论是用双线桥法还是用单线桥法表示电子转移情况,其数目是不变的。
(2)反应中,电子转移数目=氧化剂得到电子数目=还原剂失去电子数目,不要误认为电子转移的数目是反应中得、失电子数目的加和。
思路点拨: 解答本题要从以下三点入手:
(1)首先正确标出各元素的化合价。
(2)再依据化合价的变化分析电子转移的方向和数目。
(3)注意要符合客观事实和氧化还原反应规律。
答案: A
规律方法: 同种元素反应规律
(1)歧化反应:相同价态的同种元素反应后一部分化合价升高,另一部分化合价降低的氧化还原反应。
(2)归中反应:不同价态的同种元素发生反应时,高价态降低,低价态升高的氧化还原反应。
说明:例1 D项违背了归中反应规律。
解析: n(Na2SO3)=0.3 L×0.1 mol·L-1=0.03 mol,Na2SO3被氧化为Na2SO4,化合价升高总数为[+6-(+4)]×0.03 mol;设X被还原后的价态为y,则化合价降低总数为(+5-y)×1.5×10-2 mol,由化合价升高总数等于降低总数:(6-4)×0.03=(5-y)×1.5×10-2,y=+1。
答案: C
二、氧化还原反应各概念间的关系
分析判断氧化还原反应中有关概念时,可借助以下口诀帮助解决:
升——失——氧(氧:氧化反应)
降——得——还(还:还原反应)
答案: D
2.(2011·岳阳高一质检)某元素在化学反应中,由化合态变为游离态,则该元素( )
A.一定被氧化
B.一定被还原
C.可能被氧化,也可能被还原
D.化合价降低为0
解析: 化合价既可能升高,如NaCl→Cl2;也可能降低,如Fe2O3→Fe。
答案: C
1.(2011·淮安高一质检)下列反应不属于氧化还原反应的是( )
A.3Cl2+6KOH===5KCl+KClO3+3H2O
B.2NO2+2NaOH===NaNO3+NaNO2+H2O
C.SnCl4+2H2O===SnO2+4HCl
D.2H2S+SO2===3S↓+2H2O
解析: A项中氯元素、B项中氮元素、D项中硫元素的化合价均有变化,C项中各元素的化合价均无变化,故C项不是氧化还原反应。
答案: C
2.(2011·杭州高一质检)下图为反应Fe+CuSO4 ===Cu+FeSO4中电子转移的关系图,则图中的元素甲、乙分别表示( )
A.Fe,S B.Cu,S
C.Fe,O D.Fe,Cu
解析: Fe与CuSO4反应,Fe失电子被氧化,+2价Cu得电子被还原。
答案: D
3.(2009·福建高考)下列类型的反应,一定发生电子转移的是( )
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
答案: C
解析: KClO3中氯为+5价,ClO2中氯为+4价,KClO3为氧化剂,H2C2O4中碳显+3价作还原剂,被氧化,1 mol KClO3得1 mol电子。
答案: D
